
диаграмма состояний
.pdf
Диаграммы состояния двойных металлических сплавов
Федеральное агентство по образованию Государственное образовательное учреждение высшего профессионального образования ТОМСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ
В. П. Ротштейн
ДИАГРАММЫ СОСТОЯНИЯ ДВОЙНЫХ МЕТАЛЛИЧЕСКИХ СПЛАВОВ
Методические указания
Томск
2009

2 |
В. П. Ротштейн |
УДК 621.002.3 (075.8) |
Печатается по решению |
ББК 30.3 я73 |
редакционно-издательского совета |
Р 79 |
Томского государственного |
|
педагогического университета |
Р79 Ротштейн, В. П. Диаграммы состояния двойных металлических сплавов : методические указания для студентов ФТП / В. П. Ротштейн ; ГОУ ВПО Томский государственный педагогический университет – Томск : Изд-во ТГПУ, 2009. – 72 с.
Рассмотрены основные понятия теории сплавов: типы твердых фаз, виды металлических сплавов, понятие и метод построения диаграмм состояния, основные типы диаграмм состояния двойных сплавов, правило фаз Гиббса, правило отрезков и правило рычага, ликвация и ее влияние на свойства сплавов, связь между типом диаграммы состояния и свойствами сплава (диаграммы состав – свойства).
Изложена методика выполнения лабораторной работы «Построение и анализ диаграммы состояния висмут–кадмий». В приложениях представлены контрольные вопросы, задания для самостоятельной работы, тестовые задания и диаграммы состояния основных двойных металлических сплавов.
Предназначены для студентов факультета технологии и предпринимательства, изучающих дисциплину «Материаловедение и технологии производства материалов».
Рецензент:
докт. тех. наук, профессор кафедры «Оборудование и технология сварочного производства» ТПУ
Гнюсов С. Ф.
©Томский государственный педагогический университет, 2009
©В. П. Ротштейн, составление, 2009

Диаграммы состояния двойных металлических сплавов |
3 |
Оглавление
1. Введение |
5 |
2. Основные понятия и определения |
6 |
3. Основные фазы в сплавах |
8 |
3.1.Твердые растворы |
8 |
3.2.Химические соединения |
11 |
4. Виды металлических сплавов |
12 |
5. Диаграммы состояния двойных сплавов |
13 |
5.1.Правило фаз Гиббса |
16 |
5.2.Построение диаграмм состояния |
17 |
5.3.Диаграмма состояния сплавов, |
|
образующих механические смеси |
|
чистых компонентов (1-го рода) |
20 |
5.4.Диаграмма состояния сплавов, |
|
образующих неограниченные |
|
твердые растворы (2-го рода) |
23 |
5.5.Правило отрезков и правило рычага |
25 |
5.6.Внутрикристаллитная (дендритная) ликвация |
27 |
5.7.Диаграмма состояния сплавов, |
|
образующих ограниченные твердые |
|
растворы и эвтектику (3-го рода) |
32 |
5.8.Ликвация по плотности |
38 |
5.9.Диаграмма состояния сплавов, |
|
образующих ограниченные твердые |
|
растворы и перитектику |
41 |
5.10. Диаграмма состояния сплавов, |
|
образующих устойчивые химические |
|
соединения (4-го рода) |
44 |
5.11. Диаграмма состояния сплавов |
|
с полиморфными превращениями |
47 |
6. Диаграммы состав – свойства |
49 |
7. Лабораторная работа. |
|
Построение и анализ диаграммы |
|
состояния висмут–кадмий |
50 |
7.1. Цель работы |
50 |
7.2. Материалы, приборы, оборудование |
51 |
7.3. Порядок выполнения работы |
51 |
7.4. Порядок составления отчета |
54 |

4 |
В. П. Ротштейн |
|
8. Литература |
|
54 |
Приложение 1. |
|
|
Диаграмма состояния и микроструктура сплавов Bi-Cd |
55 |
|
Приложение 2. |
|
|
Контрольные вопросы |
|
56 |
Приложение 3. |
|
|
Задания для самостоятельной работы |
57 |
|
Приложение 4. |
|
|
Тестовые задания |
|
63 |
Приложение 5. |
|
|
Диаграммы состояния двойных металлических сплавов |
67 |
|
Литература к Приложениям |
71 |
|

Диаграммы состояния двойных металлических сплавов |
5 |
1. Введение
Чистые металлы из-за низкой прочности применяются, главным образом, в электро- и радиотехнике как проводниковые, электровакуумные и другие материалы. Основными конструкционными материалами являются металлические сплавы.
Свойства сплава зависят от многих факторов, но, в первую очередь, они определяются химическим составом фаз и их количественным соотношением. Эти сведения получают из анализа диаграмм состояния, изучению которых посвящена данная работа.
Диаграммы состояния позволяют представить полную картину формирования равновесной структуры любого сплава. С их помощью можно также:
•оценить оптимальный состав литейных сплавов и оптимальную температуру их заливки в литейную форму
•определить температуру термообработки, например, температуру отжига и температуру закалки сталей
•предсказать микроструктуру сплава в неравновесном состоянии, например, микроструктуру стали после закалки.
Цель работы:
•ознакомиться с видами и строением металлических сплавов.
•ознакомиться с основными типами диаграмм состояния двойных сплавов
•на примере системы Bi-Cd освоить методику построения диаграмм состояния сплавов
•на примере данной диаграммы состояния научиться:
−восстанавливать кривые охлаждения сплава данного состава
−предсказывать фазовые превращения на каждом участке этих кривых
−проверять правильность выводов с помощью правила фаз Гиббса
−определять состояние сплава в двухфазных областях (типы фаз, химический состав и массовую долю каждой фазы)
•на основе диаграмм состав – свойства предсказывать зависимость свойств двойных сплавов от их химического состава.

6 |
В. П. Ротштейн |
2. Основные понятия и определения
Сплав – это вещество, полученное путем сплавления двух или более химических элементов (компонентов). Большинство сплавов состоят из основного металла и небольшого количества добавок или легирующих элементов. Помимо основного метода получения сплавов – сплавления компонентов – существуют другие методы: спекание смесей порошков (порошковая металлургия), высокотемпературная диффузия легирующего элемента в основной металл, плазменное осаждение различных элементов на подложку, электролитическое осаждение покрытий и др.
Металлический сплав – это сплав, содержащий более 50 вес. % металлических элементов. Металлические сплавы имеют кристаллическое строение и металлические свойства. Они обладают более высокими прочностными и эксплуатационными свойствами по сравнению с чистыми металлами. Кроме того свойства металлических сплавов можно изменять с помощью пластической деформации и/или термической обработки значительно сильнее, чем чистых металлов.
Примеры:
латунь: сплав на основе меди: смесь (сплав) меди (Cu) и цинка (Zn) углеродистая сталь: сплав железа (Fe) с углеродом (до ~ 2 вес. % C).
Компоненты – это химические элементы, образующие сплав. Компоненты обозначаются символами химических элементов (Cu, Zn, C) или буквами (A, B, C). В латуни основными компонентами являются Cu и Zn, в сталях – Fe и C. Компонентами металлических сплавов принято считать также устойчивые химические соединения, которые не диссоциируют в исследуемом интервале температур.
Металл или сплав называют системой. Чистый металл является простой однокомпонентной системой, сплав – сложной системой, состоящей из двух и более компонентов.
Двойной сплав содержит два компонента, тройной – три и т. д.
Химический состав сплава определяется концентрацией компонентов в весовых или атомных %.
Весовая концентрация компонента A (вес. %) определяется как
вес компонента А |
|
WA = ∑вес всех компонентов × 100 |
(1) |

Диаграммы состояния двойных металлических сплавов |
7 |
Атомная концентрация компонента A (атом. %) определяется как
число атомов компонента А |
(2) |
ХА = ∑число атомов всех компонентов × 100 |
Между весовой и атомной концентрацией существуют следующие соотношения:
WA |
= |
|
|
|
|
aAXA |
|
|
|
|
|
|
(3) |
|||
|
a |
|
X |
A |
+ a |
X |
B |
|||||||||
|
|
|
|
|
||||||||||||
|
|
|
A |
|
|
|
B |
|
|
|
||||||
WB |
= |
|
|
|
|
aB XB |
|
|
|
|
|
|
(4) |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
a |
X |
|
|
+ a |
X |
|
, |
|||||||||
|
|
A |
B |
|
||||||||||||
|
|
|
A |
|
|
|
B |
|
|
|
||||||
где aA и aB – атомный вес компонентов A и B, соответственно. Фаза – однородная по химическому составу и микрострукту-
ре часть системы (металла или сплава), отделенная от других частей системы границей раздела, при переходе через которую структура и свойства резко меняются. Фазу можно механически выделить из смеси, в которой она находится.
Жидкий металл или сплав также является фазой, а сама система является однофазной. Система (сплав), состоящая из двух типов зерен с различной кристаллической решеткой, или из жидкого металла и кристаллов, является двухфазной системой.
Свойства сплава определяются состоянием сплава и его микроструктурой.
Состояние сплава определяется:
•фазами, присутствующими в сплаве
•составом каждой фазы
•весовой (массовой) долей каждой фазы (в %). Микроструктура определяется характерным размером (нм,
мкм, мм) и морфологией фаз. Под морфологией понимают форму твердых фаз в материале (например, глобулы, диски, столбики) (рис. 1). Самый простой и распространенный метод изучения микроструктуры – оптическая металлография.
Рис. 1.
Морфология фаз в материале.
Источник: http://www.matter.org.uk/ glossary

8 |
В. П. Ротштейн |
3. Основные фазы в сплавах
Рассмотрим двойную металлическую систему А–В. В жидком состоянии обычно существует полная взаимная растворимость компонентов друг в друге. При затвердевании возможны следующие три варианта взаимодействия компонентов А и В:
•атомы А и В сильно отталкивают друг друга; в результате формируется механическая смесь зерен двух чистых металлов, кристаллизующихся порознь, т. е. А + В
•силы взаимодействия (отталкивания и притяжения) между атомами А и В малы; в результате атомы компонента В частично или полностью растворяются в решетке А и наоборот. В этом случае образуются ограниченные или неограниченные твердые растворы, причем в первом случае образуются также механические смеси ограниченных твердых растворов.
• атомы А и В испытывают сильное взаимное притяжение;
вэтом случае могут формироваться химические соединения,
втом числе интерметаллиды (в системах металл–металл). Таким образом, в сплавах могут образовываться следующие
основные фазы: жидкие растворы, твердые растворы, химические соединения. Сплав может быть однофазным (гомогенным) или многофазным (гетерогенным) (не путать с однокомпонентным или многокомпонентным сплавом!).
3.1.Твердые растворы
Вжидком состоянии большинство металлических сплавов, применяемых в технике, представляют собой химически однородные жидкости, т. е. жидкие растворы. При затвердевании
вряде таких сплавах однородность сохраняется, следовательно, сохраняется растворимость компонентов в твердом состоянии.
Твердые растворы – это кристаллические фазы, имеющие решетку основного компонента А (растворителя), в которой размещены атомы другого (или других) компонентов (B и т. д).
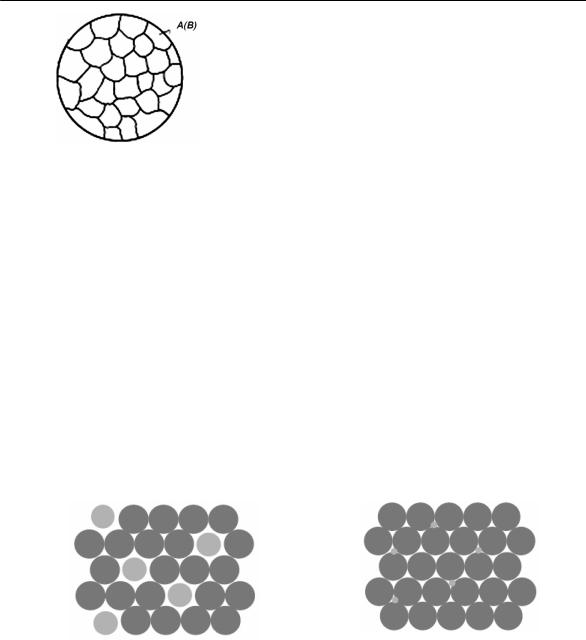
Твердые растворы обозначают греческими буквами, например: α = А(В), где А – растворитель, В – растворяемый компонент. Схематически микроструктура твердого раствора (однофазный сплав) показана на рис. 2.
Диаграммы состояния двойных металлических сплавов |
9 |
Рис. 2.
Схема микроструктуры твердого раствора
Различают твердые растворы замещения и твердые растворы внедрения (рис. 3). При образовании твердого раствора замещения атомы растворенного компонента B статистически случайно занимают узлы решетки растворителя A (рис. 3а). При этом решетка искажается, что приводит к изменению параметра решетки и возникновению напряжений.
Твердые растворы внедрения образуются в том случае, когда атомы растворенного компонента B внедряются в межузельные промежутки растворителя A (рис. 3б). При этом атомы компонента B занимают не любые междоузлия, а только те, которые имеют достаточный свободный объем. В таких пустотах могут разместиться только атомы с очень малыми размерами.
а |
б |
B→ |
|
A→ |
B→ |
|
A→ |
Рис. 3. Двумерная модель твердого раствора замещения (а) и внедрения (б)
Наименьшие размеры имеют атомы неметаллов (водород, азот, углерод, бор); именно они образуют с металлами твердые растворы внедрения. Но и у этих элементов размер атомов превышает размеры междоузлий в решетке металлов, Поэтому при образовании твердого раствора внедрения решетка металла искажается и возникают напряжения. При этом тип решетки не изменяется.
Максимальная концентрация твердого раствора внедрения не может быть высокой: обычно она не превышает 1÷2 вес. %. Таким образом, твердые растворы внедрения являются ограниченными.

10 В. П. Ротштейн
Максимальная концентрация компонента А в решетке В называется пределом растворимости α – твердого раствора. Аналогично вводится предел растворимости β – твердого раствора.
Примерами ограниченных твердых растворов внедрения является феррит и аустенит – основные фазы в железо-углеродистых сплавах (стали и чугуны). Феррит – твердый раствор внедрения углерода в решетку α–железа (ОЦК) (рис. 4а). Предел растворимости углерода в феррите составляет 0.02 вес. %, что соответствует 1 атому углерода на 500 атомов железа. Аустенит – твердый раствор внедрения углерода в решетку γ-железа (ГЦК) (рис. 4б). Предел растворимости углерода в аустените составляет 2.14 вес. %, т. е. в ~ 100 раз больше, чем в феррите.
а |
С |
б |
С |
Рис. 4. |
|
|
|
|
Элементарные ячейки |
|
|
|
|
твердых растворов |
|
|
|
|
внедрения углерода |
|
|
|
|
в ОЦК- и ГЦК-железе: |
|
|
|
|
(а) феррита, |
|
|
|
|
(б) аустенита |
|
|
|
|
Источник: |
|
|
|
|
www.msm.cam.ac.uk/phase- |
|
|
|
|
trans/2003/Lattices/iron.html |
Вотличие от твердых растворов внедрения, которые являются всегда ограниченными, твердые растворы замещения могут быть как ограниченными, так и неограниченными.
Внеограниченных твердых растворах замещения существует
100 %-ная взаимная растворимость компонентов в твердом состоянии, т.е. в решетке друг друга (по аналогии со 100 %-ной растворимостью двух жидкостей, например, воды и этилового спирта).
Вэтом случае, постепенно увеличивая долю компонента В в системе А–В, можно перейти от чистого компонента А к чистому компоненту В, т. е. образуется непрерывный ряд твердых растворов замещения. Примером такой системы является медь – никель (рис. 5).
Неограниченные твердые растворы образуются, если выполняются следующие условия:
•компоненты А и В имеют одинаковый тип решетки (изоморфизм)
