
Vitamins[1]
.pdf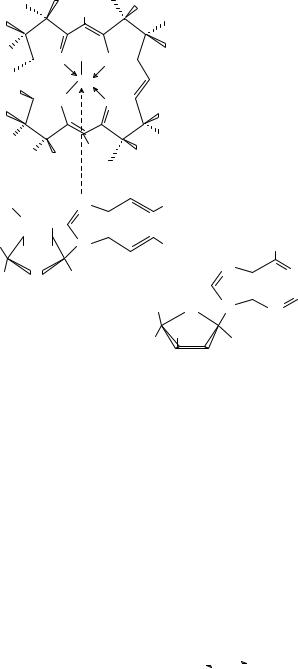
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Окончание табл. 1.3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
Структурная формула, рациональное |
|
|
|
Ферменты |
Переносимые |
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
название и буквенное обозначение |
|
|
|
группы |
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
|
O |
|
|
|
|
|
|
|
|
H |
H3C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
H2N |
|
CCH2CH2 |
|
CH2CONH2 |
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||
|
|
H3C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
H2N |
|
|
|
|
|
|
|
CCH2 |
|
|
|
|
|
|
|
|
|
CH2CH2CONH2 |
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
H3C |
|
|
N R |
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
H3C |
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Co |
|
|
|
|
|
|
|
|
|
|
|
|
|
Реакции |
|||||||||||||||
H2N |
|
O |
|
|
H |
|
|
N |
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
CCH2 |
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
изомериза- |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
O |
|
H |
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
Изомеразы, |
ции, напри- |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
H |
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
HN |
|
|
|
|
|
|
CCH2CH2 CH3 |
CH CH CONH |
|
|
|
|
|
|
метилмало- |
мер изомери- |
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||
|
|
|
|
|
CH2 |
|
O |
|
|
|
2 |
2 |
|
2 |
|
|
|
|
|
|
||||||||||||||||||||||||
CH3 |
|
CH |
|
O |
|
|
|
O- |
|
N |
|
|
|
|
|
|
|
|
CH |
|
|
|
|
|
|
|
|
нил: КоА- |
зация метил- |
|||||||||||||||
|
|
|
P |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O HO |
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
мутаза |
малоновой |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H H |
H N |
|
|
|
|
|
|
|
|
CH3 |
|
|
N |
|
NH2 |
|
кислоты |
||||||||||||
|
HOH C O |
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
в янтарную |
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R = H2C O |
|
|
N |
|
|
N |
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H H |
H |
H |
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
OH |
|
|
|
|
|
|||||
5'-Дезоксиаденозилкобаламин- В |
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
12 |
|
|
|
|
|
|
|
|
|
|
|||
Аденозин-5′-трифосфат (АТФ) и другие нуклеозидтрифосфаты
– гуанозин-5′-трифосфат (ГТФ), уридин-5′-трифосфат (УТФ), тими- дин-5′-трифосфат (ТТФ) и цитидин-5′-трифосфат (ЦТФ) – являются коферментами и переносят фосфатные и нуклеозидные группы на субстраты. Например, в мышцах в значительном количестве присутствует фосфокреатин, образующийся из креатина и АТФ:
|
|
|
|
|
|
|
|
CH3 |
2 |
|
|
|
|
|
|
|
|
|
|
|
CH3 |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
H2N |
|
|
C |
|
N |
|
CH2COO + АТФ |
|
О3Р |
|
NH |
|
|
C |
|
N |
|
CH2COO + AДФ |
|||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
NH |
|
|
|
|
|
|
|
|
NH |
|||||||||||||||||||
|
|
Креатин |
|
|
|
|
Фосфокреатин |
||||||||||||||||||||||||
Вследствие того, что эта реакция обратима, при интенсивной мышечной работе фосфокреатин быстро пополняет расходуемые запасы АТФ, передавая остаток фосфорной кислоты на накапливающийся аденозин-5′-дифосфат (АДФ). Поскольку при использовании
20
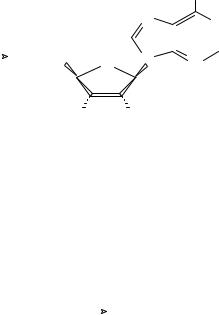
АТФ в ряде реакций образуется аденозин-5′-монофосфат (АМФ), а для регенерации АТФ необходим АДФ, то в местах интенсивного расходования АТФ обычно присутствует фермент аденилаткиназа, катализирующий реакцию образования АДФ из АМФ:
АМФ + АТФ 
 2АДФ
2АДФ
Кроме того, нуклеозидтрифосфаты, обладая макроэргическими связями (связи, при гидролизе которых выделяется большое количество энергии), участвуют в реакциях активации различных метаболитов, а также являются исходными соединениями в биосинтезе нуклеиновых кислот. Метаболиты становятся реакционноспособными (активированными) при присоединении фосфатных или аденозильных остатков. Примером переноса нуклеозидного остатка может служить реакция переноса 5′-аденозильной группы на метионин, в результате которой образуется S-аденозилметионин (активированный метионин):
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
NH2 |
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
СН3 |
Н2О |
|
|
|
|
|
СН3 |
|
|
|
|
N |
2 |
|
|
3 |
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
S + АТФ |
|
+ S |
|
СН |
O |
|
|
N |
N |
+ HPO |
|
|
+ HP |
O |
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
4 |
2 |
|
7 |
||||||||||||
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
+ |
|
CH2 |
+ |
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
H3N |
|
|
|
CH |
H3N |
|
|
|
CH HO |
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
OOC |
|
|
|
|
|
OOC |
|
|
S-Аденозилметионин |
|
|
|
|
|
|
|
|||||||||||||||
Метионин |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
Лигазы катализируют сшивание соединений за счет энергии нуклеозидтрифосфатов, например, в реакции образования аспарагина из аспарагиновой кислоты и иона аммония участвует АТФ:
|
|
3 |
|
|
|||
|
|
|
|
||||
АТФ + -OOCCH2 |
CHCOO-+ NH4+ |
|
-OOCCH2 |
|
CHCONH2 + HP2O7 |
+ АМФ |
|
|
|
||||||
|
+ |
|
|
|
NH+3 |
|
|
NH3 |
|
|
|||||
Аспартат |
|
Аспарагин |
|
||||
Кофермент А является водорастворимым коферментом ацилтрансфераз – ферментов, катализирующих реакции переноса ацильных групп. Сокращенно его обозначают как КоА (СоА) или, если
21
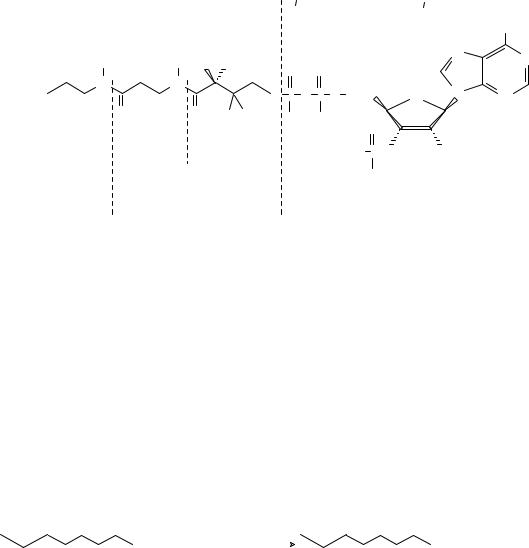
требуется записать химическими символами связанный с ним ацильный остаток, его записывают как КоА-SH.
В организме КоА образуется из пантотеновой кислоты (витамин В3), цистеамина и АТФ.
С химической точки зрения КоА представляет собой эфир пантетеина по γ-гидроксильной группе пантоевой кислоты и 3′-фосфо- аденозин-5′-дифосфата по 5′-дифосфатной группе (рис.1.1).
Пантетеин 3 -фосфоаденозин-5 -дифосфат
|
|
|
|
|
|
|
N |
NH2 |
H |
H |
H OH |
|
|
|
|
N |
|
|
O O |
|
|
|
||||
N |
N |
|
|
|
|
|
|
|
|
|
O P O P O CH2 |
|
O N |
N |
|||
HS |
O |
O H C CH |
|
|||||
|
OH OH |
|
|
|
|
|||
Цистеамин β-Аланин |
3 |
3 |
O |
|
|
|
||
Пантоевая |
|
|
|
|||||
HO P |
O |
OH |
|
|||||
|
|
кислота |
|
|
|
|||
|
|
|
|
|
|
|
|
|
HO
Пантотеновая
кислота
Р и с. 1.1. Строение кофермента А – КоА
Пантетеин состоит из трех компонентов, связанных амидными связями: пантоевой кислоты, β-аланина и цистеамина. Пантотеновая кислота, образованная из пантоевой кислоты и β-аланина, в организме человека играет роль витамина В3.
Кофермент А является акцептором ацильных групп в реакциях окислительного декарбоксилирования α-кетокислот, в ходе которых образуются 6-S-ацилдигидролипоамиды:
HS |
SCOR |
HS |
SH |
|
||||||
|
|
|
CONH~ + KoA-SH |
|
|
|
|
|
CONH~ + KoA-SCOR |
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|||
6-S-Ацилдигидролипоамид |
|
|
|
Дигидролипоамид |
Ацил-КоА |
|||||
Тиоэфиры, какими являются ацил-КоА, представляют собой активированные формы карбоновых кислот. Ацильный остаток ацилКоА легко переносится на другие молекулы.
Например, при взаимодействии ацил-КоА с 3-глицерофосфатом образуются фосфатидные кислоты:
22
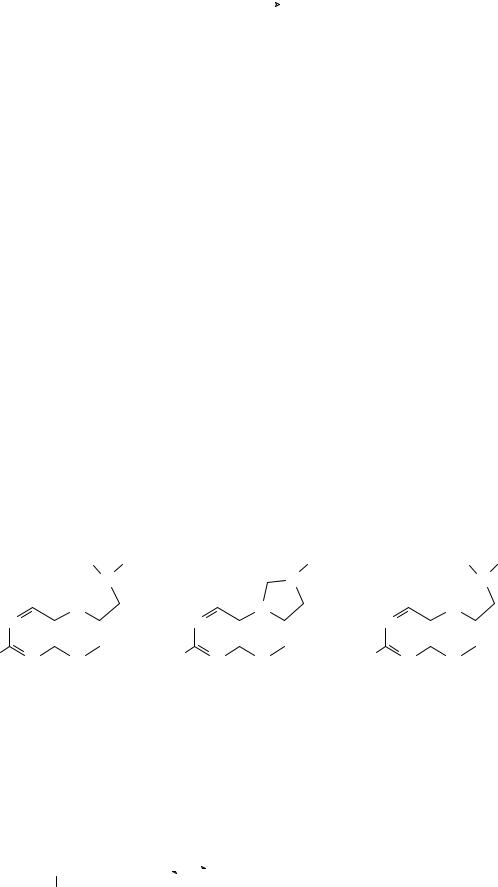
|
|
СН2ОН |
|
|
|
СН2ОСОR |
|
|
|||||
|
|
СНОН 2- + 2KoA-SCOR |
|
|
|
СНОCOR2- + 2KoA-SH |
|
|
|
|
|
||
|
|
|
||||
|
|
СН2ОРО3 |
|
|
|
СН2ОРО3 |
3-Глицерофосфат |
|
Фосфатид |
||||
Тетрагидрофолат (ТГФ) является коферментом, который может переносить С1-остатки в различных степенях окисления. ТГФ образуется из витамина фолиевой кислоты в результате двойного гидрирования птеринового кольца.
С1-фрагменты присоединяются к атомам N5, N10 или к обоим атомам азота в виде мостика. Наиболее важными производными тетрагидрофолата, переносящими С1-фрагменты, являются 10N-формил-ТГФ, 5N,10N-метилен-ТГФ и 5N-метил-ТГФ. Формильное производное ТГФ используется в качестве донора формильных групп, в первую очередь в биосинтезе пуриновых нуклеотидов. Метиленовое производное ТГФ является исходным для образования формильного и метильного производных ТГФ. Метильное производное используется для метилирования главным образом по сульфгидрильным группам метоболитов.
Ниже приведены структурные фрагменты С1-производных ТГФ (R – заместитель, структура которого одинакова в ТГФ и фолиевой кислоте, см. табл. 1.1 и 1.3):
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
|
|
|
|
|
H R |
||||
|
|
|
|
|
|
C R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
H |
|
|
|
N |
|
|
|
|
|
|
|
|
N |
|
|
|
|
H C |
|
|
N |
|||
|
|
OH |
|
|
|
|
10 |
|
|
OH |
|
|
10 |
|
|
OH |
3 |
|
10 |
||||||||||
|
|
|
|
|
|
|
9 |
|
|
|
|
|
9 |
|
|
|
|
|
9 |
||||||||||
N2 |
|
|
|
|
N |
N2 |
|
|
|
N |
N2 |
|
|
|
N |
||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
1 |
|
5 |
6 |
|
|
1 |
|
5 |
6 |
|
|
1 |
|
5 |
6 |
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
3 |
4 |
|
8 |
|
7 |
|
|
3 |
4 |
|
8 |
7 |
|
|
3 |
4 |
|
8 |
7 |
|
|
||||||||
H2N |
|
|
|
|
H2N |
|
|
|
H2N |
|
|
|
|||||||||||||||||
N N |
|
|
|
|
N N |
|
|
|
N N |
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
H |
|||||||
10N-формил-ТГФ |
5N,10N-метилен-ТГФ |
5N-метил-ТГФ |
|||||||||||||||||||||||||||
Главным процессом, в результате которого ТГФ «заряжается» одноуглеродным фрагментом, является его реакция с серином с образованием 5N,10N-метилен-ТГФ, катализируемая ферментом гидроксиметилтрансферазой:
HOCH CHCOO- |
+ ТГФ |
|
5N,10N-СН -ТГФ |
+ CH COO- |
+ H O |
||||
|
|||||||||
|
|||||||||
2 |
|
|
2 |
|
|
|
2 |
2 |
|
|
NH3+ |
|
5N,10N-метилен-ТГФ |
|
|
NH3+ |
|
||
|
|
|
|||||||
Серин |
|
Глицин |
|
||||||
23

5N,10N-Метилен-ТГФ далее может окисляться, образуя 10N- формил-ТГФ, или восстанавливаться, образуя 5N-метил-ТГФ:
5N,10N-СН2-ТГФ + НАДФ+ + Н2О  10N-СНО-ТГФ + НАДФН + Н+
10N-СНО-ТГФ + НАДФН + Н+
5N,10N-СН2-ТГФ + НАДФН + Н+ 
 5N-СН3-ТГФ + НАДФ+
5N-СН3-ТГФ + НАДФ+
В качестве примера переноса метильной группы рассмотрим реакцию, в которой главным образом расходуется 5N-метил-ТГФ (синтез метионина из гомоцистеина):
|
|
|
|
|
H |
R |
|
|
|
|
|
|
|
|
|
|
H |
R |
|||||||||||||
|
|
|
|
H C N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H N |
|
|
CH3 |
||||||||
|
|
OH 3 |
|
|
SH |
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
S |
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
N |
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
N |
|
|
CH2 |
||||||||||
N |
|
+ |
|
|
|
|
N |
|
+ |
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
H2N N N |
|
|
|
|
|
|
+ |
|
H2N |
|
|
|
|
|
|
|
|
|
2 + |
||||||||||||
|
|
CH |
|
NH3 |
N N |
|
|
CH |
|
NH |
|||||||||||||||||||||
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
COO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
||||||
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
COO |
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
5N-метил-ТГФ |
Гомоцистеин |
|
|
|
|
ТГФ |
Метионин |
||||||||||||||||||||||||
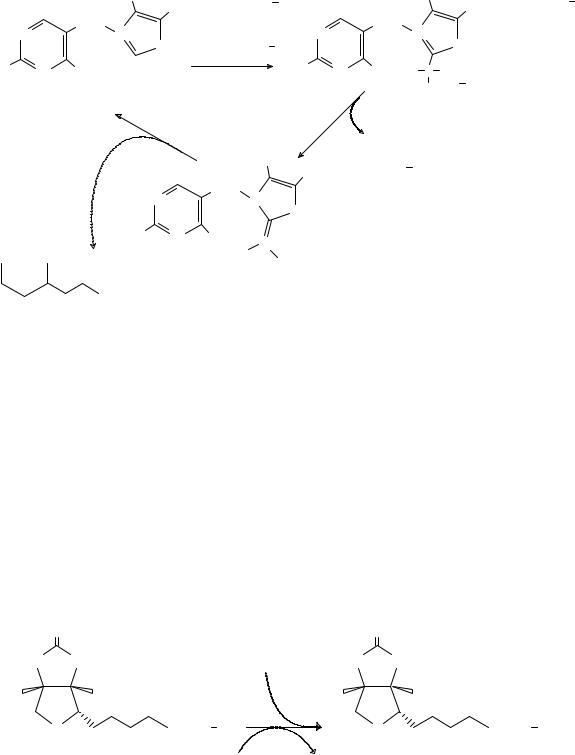
Тиаминпирофосфат (ТПФ) активирует альдегиды и кетоны и переносит их в виде гидроксиалкильных групп на другую молекулу. Этот способ переноса важен, например, в транскетолазной реакции. Гидроксиалкильные остатки участвуют также в декарбоксилировании кетокислот. Они либо высвобождаются в виде альдегидов, либо переносятся на липоамидные остатки, как в случае дегидрогеназ 2-кето- кислот. Ниже приведена схема реакций 2-кетокислот с участием ТПФ в качестве кофермента (рис.1.2).
Молекула ТПФ имеет подвижный атом водорода в положении 2 тиазольного кольца, благодаря чему легко присоединяется к карбонильным соединениям, образуя «заряженные» формы ТПФ.
Пиридоксальфосфат – наиболее важный кофермент в метаболизме аминокислот. Его роль при трансаминировании была подробно рассмотрена авторами ранее (Смирнов, В.А. Аминокислоты и полипептиды: учеб. пособ. Ч. I/ В.А. Смирнов, Ю.Н. Климочкин. – Самара.
Самар. гос. техн. ун-т, 2007. С. 31-33).
24
|
|
|
CH3 |
|
|
О3 |
|
|
|
|
CH3 |
CH CH OP |
О |
3 |
|
|
|
СН |
|
CH CH OP |
|
СН |
|
|
|||||||
N |
|
+ |
|
2 2 |
2 |
6 |
|
|
+ |
2 2 2 |
|
6 |
|||
|
2 |
N |
|
|
|
N |
|
|
2 |
N |
|
|
|
||
H C |
|
NH |
|
S |
+RCOCOO |
|
NH |
|
S |
|
|
|
|||
N |
|
|
|
|
H3C |
N |
|
R C OH |
|
|
|
||||
3 |
2 |
|
|
|
|
|
|
2 |
|
|
|
||||
|
|
ТПФ |
|
|
|
|
|
|
|
|
|
COO |
|
|
|
|
|
|
|
|
|
|
|
"Заряженная форма ТПФ" |
|
||||||
|
|
|
|
+Липоамид + Н+ |
|
|
|||||||||
|
|
|
|
|
CO2 |
|
|
|
|
|
|||||
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
О |
3 |
|
|
|
|
|
|
|
|
|
|
|
|
CH CH OP |
|
|
|
|
||||
|
|
|
|
N |
СН2 |
|
2 |
2 |
2 |
|
6 |
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|||
|
|
|
H3C |
|
NH |
|
S |
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
||
HS |
SCOR |
|
2 |
R |
C OH |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|||||
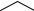 CONH~
CONH~
6-S-Ацилдигидролипоамид
Ри с. 1.2. Взаимодействие ТПФ с 2-кетокислотами
иперенос ацильной группы на липоамид
Пиридоксальфосфат принимает участие и в других реакциях аминокислот, таких, как декарбоксилирование и дегидратирование. Представленная здесь альдегидная форма в свободном виде не встречается. В отсутствие субстрата альдегидная группа связана с аминогруппой лизинового остатка фермента в виде альдимина.
Биотин реагирует с гидрокарбонатом (НСО3-) в присутствии АТФ с образованием биотин-N-кар6оксилата:
|
O |
HOCOO- |
|
O |
NСОО- |
|
HN |
NH |
HN |
|
|||
H |
H |
|
|
H |
|
H |
|
S |
CONH R |
|
|
S |
CONH R |
|
Биотин |
АТФ |
АДФ |
Биотин-N-карбоксилат |
||
Эта активированная форма диоксида углерода может быть перенесена на другую молекулу. Примерами биотинзависимых реакций являются образование оксалоацетата из пирувата и синтез малонилКоА из ацетил-КоА. Примерами биотинзависимых реакций являются реакции карбоксилирования пирувата с образованием оксалоацетата,
25
ацетил-КоА с образованием малонил-КоА, пропионил-КоА с образованием метилмалонил-КоА:
СН3СОСОО‾ + НСО3‾ + АТФ → ‾ООССН2СОСОО‾ + АДФ + Н2РО4‾
СН3СО-КоА + НСО3‾ + АТФ → ‾ООССН2СО-КоА + АДФ + Н2РО4‾
СН3СН2СО-КоА + НСО3‾ + АТФ → ‾ООССН(СН3)СО-КоА + АДФ + Н2РО4‾
С помощью первой из рассматриваемых реакций осуществляется непрерывное пополнение щавелевоуксусной кислоты, необходимой для работы цикла Кребса. Вторая реакция – важнейший этап в биосинтезе жирных кислот. Третья реакция обеспечивает утилизацию пропионовой кислоты, образующейся при β-окислении жирных кислот с разветвленным углероднымскелетом или нечетным числом атомов углерода.
5′-Дезоксиаденозилкобаламин (коферментная форма витамина В12) принимает участие в реакции изомеризации метилмалонил-КоА в сукцинил-КоА, биосинтезе метионина из гомоцистеина, восстановлении рибонуклеотидов бактериями до дезоксирибонуклеотидов.
1.1.3. БИОЛОГИЧЕСКАЯ РОЛЬ ВИТАМИНОВ И КОФЕРМЕНТОВ
Возникновение в организме дефицита того или иного витамина вызывает развитие соответствующей болезни витаминной недостаточности. Различают две основные степени такой недостаточности – авитаминоз и гиповитаминоз. Авитаминоз характеризуется глубоким дефицитом данного витамина в организме и развернутой клинической картиной его недостаточности (болезни – цинга, рахит, бери-бери, пеллагра, злокачественная анемия и др.). К гиповитаминозам относят состояния умеренного дефицита со стёртыми неспецифическими проявлениями (потеря аппетита, усталость, раздражительность) и отдельными симптомами (кровоточивость десен, гнойничковые заболевания кожи и т.д.). Наряду с дефицитом одного какого-либо витамина на практике более часто встречаются полигипо– и полиавитаминозы, при которых организм испытывает недостаток несколькихвитаминов.
Прием ряда витаминов в дозах, существенно превышающих физиологическую потребность, может давать нежелательные эффекты, а
26
в ряде случаев привести к серьезным патологическим расстройствам (гипервитаминоз). Особенно в этом отношении опасны витамины D и А. Водорастворимые витамины гипервитаминоз не вызывают, их избыток просто выводится из организма.
Потребность человека в витаминах находится в зависимости от таких факторов, как возраст, состояние здоровья, климатическая зона, условия труда, питания и др.
Препараты витаминов широко используют не только при гипо– или авитаминозах, но и в терапии сердечно-сосудистых, нервных, кожных, глазных, желудочно-кишечных заболеваний, при лучевой болезни, после операций и т.д.
Источником промышленного получения витаминов служит растительное и животное сырье, а также микроорганизмы. Чрезвычайно перспективны синтетические методы получения витаминов. Они разработаны для витаминов С, А, Е, D, K3, В1, В2, B3, B6, B15, U, РР и др. Преимущества этих методов заключаются в сравнительно невысокой стоимости исходного сырья и высоких выходах конечных продуктов.
Ряд сложных по химической структуре витаминов, например кобаламины, менахиноны, выделяют как побочный продукт при микробиологическом синтезе антибиотиков.
В табл. 1.4 приведены данные по основным функциям витаминов, их суточнойпотребностидлявзрослого человекаипищевымисточникам.
Таблица 1.4
Основные функции витаминов, их потребность и пищевые источники
|
|
Суточная |
|
|
Вита- |
Функция в организме |
потребность |
Пищевые |
|
мин |
для взросло- |
источники |
||
|
|
го человека, |
|
|
|
|
мг |
|
|
|
Водорастворимые витамины |
|
||
|
|
|
|
|
|
|
|
Зерновые, |
|
В1 |
Образование кофермента ТПФ |
1,5 |
дрожжи, |
|
|
|
|
свинина |
|
В2 |
Образование коферментов ФМН |
1,8 |
Молоко, |
|
и ФАД |
яйца |
|||
|
|
|||
27
Продолжение табл. 1.4
|
|
Суточная |
|
|
|
|
потребность |
Пищевые |
|
Витамин |
Функция в организме |
для взросло- |
источники |
|
|
|
го человека, |
|
|
|
|
мг |
|
|
|
Образование кофермента А и просте- |
|
Во многих |
|
В3 |
тической группы ацилпереносящего |
7,0 |
пищевых |
|
|
белка (АПБ) |
|
продуктах |
|
|
Образование кофермента пиридок- |
|
Мясо, ово- |
|
В6 |
2,0 |
щи, зерно- |
||
сальфосфата |
||||
|
|
вые |
||
|
|
|
||
|
1. Образование кофермента 5′- |
|
Кишечная |
|
|
|
микрофло- |
||
|
дезокси-аденозилкобаламина. |
|
||
В12 |
0,002 |
ра, мясо, пе- |
||
2. Участие в восстановлении рибо- |
||||
|
|
чень, яйца, |
||
|
нуклеотидов бактериями |
|
||
|
|
молоко |
||
|
|
|
||
|
|
|
Свежая |
|
Вс |
Образование кофермента ТГФ |
0,2 |
зелень, ово- |
|
|
|
|
щи, печень |
|
|
1. Участие в процессах синтеза кол- |
|
|
|
С |
лагена, катехоламинов, желчных ки- |
60 |
Фрукты, |
|
слот и деградации тирозина. |
овощи |
|||
|
|
|||
|
2. Антиоксидант |
|
|
|
Н |
Кофермент карбоксилаз |
0,1 |
Дрожжи, |
|
орехи, бобы |
||||
|
|
|
||
|
Образование коферментов НАД+ и |
|
Мясо, ово- |
|
РР |
НАДФ+ |
20 |
щи, фрукты, |
|
|
|
|
дрожжи |
|
|
Водорастворимые витамины |
|
||
|
|
|
|
|
U |
Участие в метилировании биогенных |
50 |
Капуста, |
|
аминов |
мясо, бобы |
|||
|
|
|||
Липоевая |
Кофермент мультиферментных де- |
|
|
|
кислота |
10 |
Печень |
||
гидрогеназ (ПДГ, ОДГ и др.) |
||||
и ее амид |
|
|
|
|
|
Жирорастворимые витамины |
|
||
|
|
|
|
|
|
1. Участие в процессах роста и диф- |
|
|
|
|
ференциации эпиталиальных и кост- |
|
|
|
А1 |
ных тканей. |
1,0 |
Фрукты, |
|
2. Увеличение проницаемости мем- |
овощи |
|||
|
|
|||
|
бран для углеводов. |
|
|
|
|
3. Стимуляция образования спермы |
|
|
|
28
Окончание табл. 1.4
|
|
Суточная |
|
|
|
|
потребность |
Пищевые |
|
Витамин |
Функция в организме |
для взросло- |
||
источники |
||||
|
|
го человека, |
|
|
|
|
мг |
|
|
|
Простетическая группа светочувст- |
|
Молоко, |
|
А2 |
|
желток яйца, |
||
вительного белка родопсина |
|
|||
|
1,0 |
печень |
||
|
|
|||
|
|
|
||
А3 |
Участие в процессе дифференциа- |
Рыбий жир |
||
|
||||
ции клеток (в 10 раз активнее А1) |
|
|||
|
|
|
||
D2 |
Образование гормона кальцитриола, |
0,01 |
Рыбий жир, |
|
поддерживающего в организме по- |
||||
|
|
молоко, жел- |
||
|
стоянство концентрации ионов Са2+ |
|
||
D3 |
Для птиц |
|||
и фосфата |
ток |
|||
|
|
|
||
|
|
|
Раститель- |
|
Е |
Антиоксидант |
15 |
ные масла, |
|
печень, яйца, |
||||
|
|
|
||
|
|
|
зерновые |
|
К1 |
Коферменты в реакциях γ- |
|
Кишечная |
|
карбоксилирования остатков глута- |
|
|||
|
|
микрофлора, |
||
К2 |
0,3 |
|||
миновой кислоты в предшественни- |
||||
овощи, |
||||
|
ке протромбина и в других факторах |
|
||
К3 |
|
печень |
||
свёртывания крови |
|
За последние годы возрос интерес к витаминам и так называемой «здоровой пище». Получили широкое распространение биологически активные добавки (БАДы), содержащие витамины.
В производство пищевых продуктов все шире внедряется обогащение их витаминными препаратами. В связи с этим актуальной является разработка научно обоснованных норм по содержанию витаминов в пищевых продуктах, БАДах и лекарственных препаратах. Все витамины применяют в медицинской практике как лекарственныесредства.
Основной специфической функцией водорастворимых витаминов в организме является образование коферментов. Из жирорастворимых витаминов лишь витамины К и А2 осуществляют коферментную функцию, а остальные участвуют не в ферментативных реакциях, а в различных физиологических процессах.
29
