
Лабораторная диагностика нарушений гемостаза
.pdf
Обеспечение диагностики нарушений гемостаза в КДЛ
Скрининговые тесты на АПС разработаны на основе модифицированного теста АЧТВ, который проводится с и без АПС, или на основе ПВ со змеиным ядом.
Тест резистентности фактора Va к АПС на основе модифицированного АЧТВ
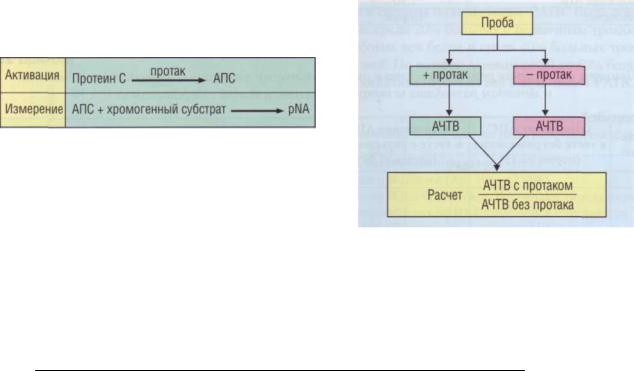
Добавление АПС в норме вызывает удлинение АЧТВ за счет инактивации факторовVa и Villa в плазме. Поэтому в тесте сравнивается время выпадения сгустка в тесте АЧТВ с добавлением и без добавления АПС и рассчитывается отношение (рис. 114). Референтные значения теста зависят от используемых реактивов и приборов. Тем не менее, несмотря на разные методы и приборную базу, обычно добавление АПС к плазме приводит, по крайней мере, к 2-кратному удлинению АЧТВ (табл. 27).
Недостаточное удлинение АЧТВ(патологический результат, свидетельствующий о РАПС) наблюдается у пациентов с факторомV Лейден, волчаночным антикоагулянтом, при беременности, увеличенном содержании фактора VIII и при-
еме оральных контрацептивов. Этот тест имеет специфичность для выявления фактораV Лейден примерно 80%, неполная специфичность связана с влиянием на результат других факторов, в частности с подавлением активности фактораVIIIa. На результаты теста оказывают влияние прием непрямых антикоагулянтов и введение гепарина.
Тест полезен для выявления пациентов с высоким риском тромбоэмболической болезни.
Тест для диагностики фактора V Лейден
Мутация гена фактора V (фактор Лейден) оценивается как наиболее распространенная причина РАПС. Эту патологию можно выявить при проведении теста на РАПС с плазмой пациента, разбавленной 1:5 плазмой с дефицитом ф.V. Этот тест обладает высокой специфичностью и чувствительностью на выявление фактораV Лейден
(табл. 28).
Тест на РАПС проводится также с использованием змеиного яда, обозначаемого как протак (Ргоtac), специфически активирующего протеин С. При внесении активатора протеина С в смесь нор-
Таблица 27
Примеры резистентности к активированному протеину С
Таблица 28
Примеры определения резистентности к активированному протеину С методом без разведения и методом разведения испытуемой плазмы плазмой с дефицитом ф. V
Обеспечение диагностики нарушений гемостаза в КДЛ
мальной и дефицитной по ф.V плазмы время свертывания в тесте АЧТВ удлиняется примерно в 2 раза. Если имеется РАПС, удлинение АЧТВ выражено в малой степени.
Определение протеина С
Для определения протеина С разработано несколько методов: иммунохимический метод, метод с хромогенным субстратом и коагуляционный вариант. Для функциональных методов используется специфический активатор протеина С из яда змеи щитомордника, обозначаемый как протак.
Определение протеина С с использованием хромогенного субстрата
Определение основано на активации протеина С активатором протак с последующим определением (кинетическим методом или методом конечной точки) изменения оптической плотности пробы из-за образования паранитроанилина (рис. 113). Этот метод прост, специфичен, легко автоматизируется. Так как протеин С - витамин- К-зависимый гликопротеин, то при лечении непрямыми антикоагулянтами (антагонистами витамина К) появляются PIVKA-формы протеина С, которые не обладают антикоагулянтной активностью, но определяются методами с хромогенными субстратами. Поэтому у больных, принимающих непрямые антикоагулянты, могут быть завышенными результаты определения протеина С хромогенными методами.
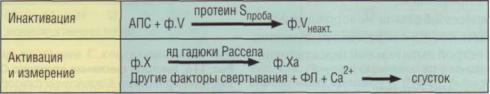
разцах исследуемой плазмы активируется протаком. Для контроля тест проводится с и без протака (рис. 114). Активированный протеин С вызывает протеолиз и соответственно инактивацию факторов Va и VIIIa в плазме (рис. 115). Последнее сопровождается удлинением времени свертывания в тесте АЧТВ, по которому оценивается активность протеина С в плазме пациента. Если фактор Va нечувствителен к активному протеину С, то АЧТВ не удлиняется в присутствии активатора протеина С. Рассчитывают отношение АЧТВ с протаком/АЧТВ без протака, величина которого определяется в конкретной лаборатории, так как тест зависит от использованных приборов и реактивов. Тем не менее этот коэффициент близок к 1 практически у всех больных с фактором Лейден и с дефицитом протеина С и существенно выше 1 в случаях без дефицита активности протеина С и при дисфункции протеина S. Метод легко автоматизируется.
Коагуляционный метод оценивает активность протеина С, фиксирующегося карбоксилированной частью на фосфолипидах. PIVKA-фор- мы не функционируют в этой системе, и тест не дает ложных результатов у пациентов, принимающих непрямые антикоагулянты или имеющих дефицит витамина К.
Исказить результаты теста могут такие факторы, как наличие мутации ф.V Лейден, присутствие в плазме волчаночного антикоагулянта,
Рис. 113. Принцип определения протеина С с использо-
ванием хромогенного субстрата, АПС - активированный протеин С
Определение протеина С коагуляционным методом
Пробы пациентов сопоставляются с дефицитной по протеину С плазмой, которую получают методом иммуносорбции. Протеин С в об-
Рис. 114. Принцип скрининга на резистентность к активированному протеину С (РАПС). Активатор протеина С из змеиного яда (протак), добавленный к пробе, в норме существенно удлиняет АЧТВ, Если же имеет место РАПС, то удлинения АЧТВ в присутствии протака не происходит
Обеспечение диагностики нарушений гемостаза в КДЛ

Рис. 115.Принцип определения протеина С коагуляционным методом. АПС - активированный протеин С, ФЛ фосфолипиды
терапия гепарином. Для получения достоверных результатов очень важно качество используемой протеин-С-дефицитной плазмы.
У некоторых пациентов, принимающих непрямые антикоагулянты, выявляются чрезвычайно низкие цифры содержания протеина. ЭтиС результаты могут быть связаны не только с - ис тинным дефицитом протеина С, но и с развитием резистентности фактора Va к АПС.
Определение протеина С иммунохимическим методом
Иммунохимическое определение протеина С применяется реже, чем функциональные методы. Это объясняется тем, что данный способ выявляет
только классическое снижение концентрации протеина С и не определяет его функциональную неполноценность. Методическим обеспечением этого определения чаще всего служат автоматизированный турбидиметрический метод или
ELISA-тест.
Оценка результатов
В норме активность протеина С у взрослых составляет 70-140%.
Небольшое повышение протеина С отмечается во время беременности, а уменьшение - в послеродовом и послеоперационном периодах.
Снижение содержания (активности) протеина С наблюдается при:
•врожденном (наследственном) дефиците или аномалиях протеина С;
•геморрагической болезни новорожденных;
•заболеваниях печени с нарушением функции;
•синдроме острой дыхательной недостаточно сти;
•менингококковом сепсисе;
•ДВС-синдроме;
•гемодиализе;
•лечении L-аспарагиназой;
•лечении пероральными (непрямыми) антико агулянтами (дефицит витамина К). Отдельные результаты могут колебаться в
зависимости от используемых методов и тест--на боров, тем более что многие из них разработаны до того, как стала известна мутация гена фактора V Лейден. В общем случае разведение пробы может минимизировать влияние фактораV Лейден в коагуляционных тестах.
В некоторых случаях при лечении больных с дефицитом протеина С непрямыми антикоагулянтами у них могут возникнуть некрозы кожи в результате рикошетных тромбозов. Если антикоагулянты назначаются в высокой дозе без поддержки гепарином, то возникает состояние, при котором протеин С очень быстро снижается(время его полужизни в системе циркуляции 4-6 ч). В то же время витамин-К-зависимые факторы свертывания, в том числе протромбин, остаются еще в пределах нормы (у них период полужизни 16-20 ч) (рис. 116).
Рис. 116. Быстрое снижение протеина С, превышающее уменьшение витамин-К-зависимых факторов свертывания, может быть причиной возникновения тромботического - со стояния (рикошетные тромбозы) при начале лечения высокими дозами непрямых антикоагулянтов
Обеспечение диагностики нарушений гемостаза в КДЛ
Эта ситуация может усугубляться тем, что непря- |
ф.VIII и волчаночный антикоагулянт могут су- |
мые антикоагулянты начинают назначать в слу- |
щественно влиять на результаты теста, а именно: |
чае развития тромбозов или угрожающей ситуа- |
с этими факторами часто проводят дифференци- |
ции по тромбообразованию (при воспалении, ин- |
альную диагностику, определяя протеин S. На |
фекциях, лихорадке), когда система прокоагулян- |
результаты влияют качество дефицитной плазмы |
тов активирована. Быстрое снижение протеина С |
и препаратов АПС, а также состав фосфолипи- |
провоцирует в этом случае массивное тромбооб- |
дов, поэтому значения теста зависят от конкрет- |
разование, проявляющееся вплоть до некрозов |
ного производителя. Так как коагуляционный |
кожи. Непосредственно в период лечения непря- |
метод подвержен действию многих интерфериру- |
мыми антикоагулянтами (кумаринами) определе- |
ющих факторов и не стандартизован, то предпо- |
ние протеина С затруднено. Определять его сле- |
читают использовать иммунохимический метод |
дует до начала лечения кумаринами. |
для определения протеина S. |
Определение протеина S
Протеин S - витамин-К-зависимый белок, который является кофактором АПС. Эта функция положена в основу всех известных коммерческих тест-систем определения протеина S. Описаны случаи как функционального, так и количественного дефицита протеина S. При проведении тестов важно помнить, что протеин S присутствует в плазме частично в свободном состоянии, частично в комплексе с С4-связывающим протеином (С4-СП), но активна только свободная форма протеина S.
Определение протеина S коагуляционным методом
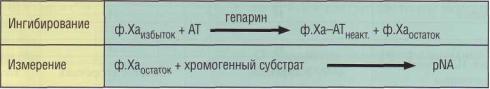
Для определения протеина S необходимо использовать тест-систему, содержащую очищенный активный протеин С, его субстрат - фактор Va и дефицитную по протеину S плазму. После инкубации исследуемой плазмы с тест-системой определяют время свертывания, выполняя тест АЧТВ или индуцируя активацию змеиным ядом,
2+
фосфолипидами и Са (рис. 117). Удлинение времени свертывания пропорционально активности протеина S. Специфичность метода относительная, так как фактор V Лейден, высокий уровень
Определение протеина S иммунохимическим методом
Иммунохимический метод достаточно широко распространен. Первая генерация тест-набо- ров определяла «общий протеин S», включая свободную форму и форму протеинаS, связанную с белком С4-СП. Наборы последних генераций позволяют определять «свободный протеин S» прямо без предварительной обработки. Чаще всего используют турбидиметрический метод с полистироловыми частицами или метод ELISA. Недостатком иммунохимического метода является то, что он выявляет протеолитически неактивные формы протеина S, которые иногда появляются в плазме.
Оценка результатов Уменьшение содержания (активности) проте-
ина S наблюдается при:
•врожденном (наследственном) дефиците;
•врожденном (наследственном) уменьшении свободной фракции протеина S;
•заболеваниях печени с нарушением синтети ческой функции;
•нефротическом синдроме;
•ДВС-синдроме;
Рис. 117. Принцип определения протеина S коагуляционным методом
|
Обеспечение диагностики нарушений гемостаза в КДЛ |
|||
• |
системной красной волчанке; |
Небольшое снижение AT наблюдается в середи- |
||
• |
лечении L-аспарагиназой; |
не менструального цикла, в пред- и послеродо- |
||
• |
лечении пероральными (непрямыми) антико |
вом периоде, при токсикозах второй половины |
||
|
агулянтами; |
беременности, в послеоперационном периоде. |
||
• |
приеме эстрогенов (пероральных контрацеп |
Эти сдвиги более выражены у пациентов с груп- |
||
|
тивов); |
пой крови А (II), а также у пожилых. |
||
• |
беременности, в послеродовом периоде; |
|
Снижение содержания (активности) А Т от- |
|
• наличии аутоантител к протеинуS. |
мечается при: |
|||
Относительный дефицит протеина S наблю |
• |
врожденном (наследственном) дефиците или |
||
дается при повышении С4-СП. С4-СП - белок |
|
аномалии AT (снижение активности или чув |
||
острой фазы, его количество повышается в |
|
ствительности к гепарину); |
||
плазме крови при воспалении, аутоиммунных |
• |
заболеваниях печени (опухоли, цирроз, алко |
||
реакциях, беременности, у женщин, принима |
|
гольный гепатит); |
||
ющих стероидные контрацептивы. С4-СП оп |
• |
нефротическом синдроме (протеинурия свы |
||
ределяют методом иммунотурбидиметрии или |
|
ше 5 г/л); |
||
ELISA. |
• |
карциноме легких; |
||
|
|
• |
ДВС-синдроме; |
|
Определение антитромбина |
• множественных травмах, тяжелых родах, по |
|||
|
здних гестозах; |
|||
|
В клинико-диагностических лабораториях |
• |
приеме эстрогенов (пероральных контрацеп |
|
AT определяют иммунохимическими методами |
|
тивов), кортикостероидов; |
||
(ELISA, турбидиметрия, нефелометрия), тестами |
• |
лечении L-аспарагиназой; |
||
с хромогенными субстратами или коагуляцион- |
• многие протеазы, включая гранулоцитарную |
|||
ными методами. |
|
эластазу, могут вызывать деградацию AT. |
||
|
Методом с хромогенным субстратом AT оп- |
|
Тест может применяться для мониторинга |
|
ределяется через фактор Ха или Па при насы- |
лечения гепарином. Длительная гепаринотера- |
|||
щающей концентрации гепарина. Принцип оп- |
пия может приводить к снижению активности |
|||
ределения AT представлен на рис. 118. При вы- |
AT в плазме. Лечение высокими дозами гепари- |
|||
боре предпочтение отдают методу с использо- |
на, особенно нефракционированным гепарином, |
|||
ванием ф.Ха, так как он более стабилен и под- |
приводит к транзиторному снижению AT по ме- |
|||
вержен меньшим влияниям со стороны интер- |
ханизму потребления (рис. 119), особенно у боль- |
|||
ных с тяжелой патологией, в критических слу- |
||||
ферирующих воздействий, чем тромбин (фак- |
||||
чаях, при ДВС-синдроме, сепсисе, злокачествен- |
||||
тор На). |
||||
ных опухолях. |
||||
|
Нормальный уровень активности AT в плаз- |
|||
|
|
Увеличение содержания (активности) А Т от- |
||
ме взрослых колеблется в диапазоне75-125%, |
|
|||
мечается во время менструации, а также при: |
||||
этот диапазон практически одинаков при исполь- |
||||
• |
остром вирусном гепатите; |
|||
зовании разных тест-наборов. Дефицит AT - се- |
||||
• |
холестазе; |
|||
рьезный фактор риска развития венозных тром- |
||||
бозов. |
• |
приеме анаболических стероидов; |
||
• |
лечении пероральными (непрямыми) антико |
|||
|
У новорожденных уровень AT составляет |
|||
около 50% и достигает уровня взрослых к 6 мес. |
агулянтами. |
|
Рис. 118. Принцип определения антитромбина (AT) хромогенным методом

Обеспечение диагностики нарушений гемостаза в КДЛ
|
волчаночным антикоагулянтом и антифосфоли- |
|
|
пидным синдромом. В некоторых случаях при ко- |
|
|
агулологических признаках волчаночного антико- |
|
|
агулянта не находят иммунологических признаков |
|
|
антифосфолипидного синдрома, в свою очередь |
|
|
антифосфолипидный синдром не всегда сопровож- |
|
|
дается коагулологическими признаками волчаноч- |
|
|
ного антикоагулянта. |
|
|
Антифосфолипидный синдром, сопровождаю- |
|
|
щийся волчаночным антикоагулянтом, выявляют |
|
|
комбинацией фосфолипид-зависимых коагуляци- |
|
|
онных и иммунохимических методов, причем на- |
|
Рис. 119. Снижение уровня AT в плазме в период активно- |
дежная диагностика обеспечивается только комп- |
|
лексным использованием группы тестов. Как пра- |
||
го лечения нефракционированным гепарином |
||
вило, волчаночныи антикоагулянт распознается по |
||
|
||
|
удлинению фосфолипид-зависимых коагуляцион- |
|
Лабораторная диагностика |
ных тестов. Волчаночныи антикоагулянт являет- |
|
антифосфолипидного синдрома и |
ся неспецифическим ингибитором. При подозре- |
|
волчаночного антикоагулянта (см. также |
нии на волчаночныи антикоагулянт необходимо |
|
«Тромбозы. Волчаночныи антикоагулянт») |
начинать лабораторные анализы со екрининговых |
|
При антифосфолипидном синдроме в крови |
тестов и теста смешивания. В табл. 29 представле- |
|
циркулируют антитела против фосфолипидов или |
ны данные екрининговых тестов при врожденном |
|
фосфолипид-связанных белков. При этом синдро- |
дефиците факторов VIII и IX, при наличии специ- |
|
ме возникает лабораторный феномен, при кото- |
фического ингибитора и волчаночном антикоагу- |
|
ром происходит удлинение времени свертывания |
лянте. Важно помнить, что не все реактивы для |
|
крови в тестах, выполняемых на фосфолипидах |
проведения АЧТВ одинаково чувствительны к |
|
(АЧТВ, ПВ). Этот феномен впервые был описан у |
волчаночному антикоагулянту. Для анализа АЧТВ |
|
пациентов с системной красной волчанкой и по- |
при подозрении на волчаночныи антикоагулянт |
|
этому получил названиеволчаночного антикоагу- |
необходимо применять реактивы, содержащие ка- |
|
лянта. Клинически, однако, при антифосфолипид- |
олин, но не эллаговую кислоту. |
|
ном синдроме и волчаночном антикоагулянте нет |
Выявление волчаночных антикоагулянтов |
|
геморрагических проявлений, но есть выраженная |
проводят последовательно: сначала в екринин- |
|
тенденция к патологически усиленному тромбооб- |
говых методах, а затем в подтверждающих. На |
|
разованию. Нельзя ставить знак равенства между |
рис. 120 представлен алгоритм выявления вол- |
|
|
Таблица 29 |
Изменения екрининговых тестов при врожденном дефиците факторов VIII и IX, наличии специфического ингибитора и волчаночном антикоагулянте
Обеспечение диагностики нарушений гемостаза в КДЛ
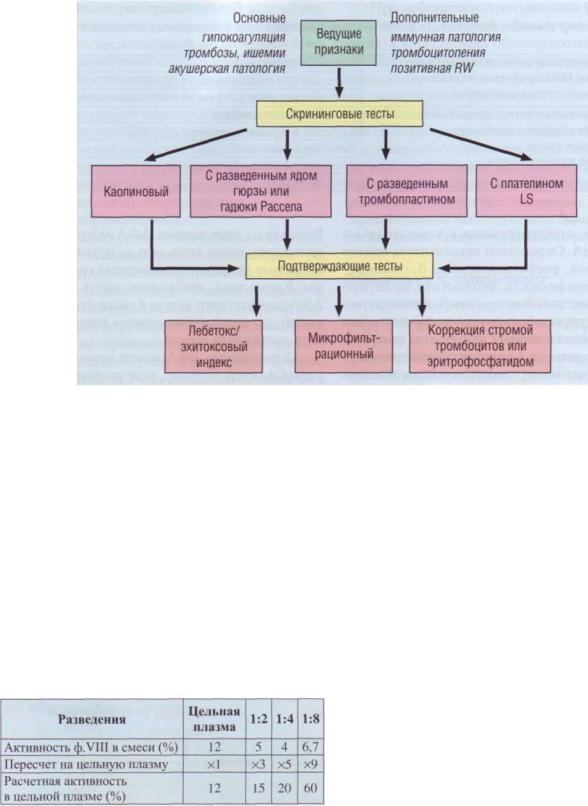
Рис. 120. Алгоритм выявления волчаночных антикоагулянтов
чаночного антикоагулянта (Баркаган З.С., Мо- |
щие тесты, например тест нейтрализации на тром- |
мот А.П., 1999). |
боцитах. Проводится определение АЧТВ и активно- |
Еще одним подтверждающим тестом для опре- |
сти факторов внутреннего пути плазмы больного до |
деления волчаночного антикоагулянта является тест |
и после инкубации с тромбоцитами здорового до- |
разведения. В серии последовательных разведений |
нора или эритрофосфатидом. При наличии волча- |
анализируемой плазмы буфером активность фак- |
ночного антикоагулянта АЧТВ сокращается, а ак- |
торов свертывания крови, определяемая коагуля- |
тивность факторов возрастает за счет связывания |
ционным методом, относительно возрастает при |
части антифосфолипидных антител на тромбоцитах |
наличии волчаночного антикоагулянта (табл. 30). |
здорового человека. В группу подтверждающих вне- |
|
сены также индексы, основанные на сравнении ре- |
Таблица 30 |
зультатов фосфолипид-зависимьгх и фосфолипид-не- |
Эффект разведения на активность факторов |
зависимых тестов (лебетокс/эхитоксовый индекс). |
свертывания в присутствии волчаночного |
Для уточнения диагноза антифосфолипидно- |
антикоагулянта |
го синдрома необходимо провести определение |
|
кардиолипиновых антител с использованием ме- |
|
тода ELISA. В табл. 31 представлен перечень ан- |
|
тифосфолипидных антител, которые выявляют- |
|
ся ИФА и коагуляционным методом. |
|
Определение антифосфолипидных |
|
антител (АФА) |
Для подтверждения диагноза волчаночного ан- |
АФА, выявляемые твердофазным ИФА, пред- |
тикоагулянта необходимо провести подтверждаю- |
ставляют собой различные комбинации иммуно- |

Обеспечение диагностики нарушений гемостаза в КДЛ
Таблица 31
Спектр антифосфолипидных антител, присутствующих в сыворотке больных А ФС
глобулинов, принадлежащих |
к классам IgG и |
Результаты определения АФА могут считаться |
IgM, реже IgA. Определяют аутоантитела против |
положительными лишь при их повышении в2 и |
|
кардиолипина, фосфатидилсерина, β2-гликопро- |
более раза по сравнению с верхней границей нор- |
|
теина I. Специфичность диагностики по антите- |
мы. Кроме того, необходимо иметь в виду, что |
|
лам различна: антитела против β2-гликопротеи-на |
АФА присутствуют всегда в сыворотке здоровых |
|
I демонстрируют большую |
специфичность, чем |
людей, но они заблокированы гистонами и их |
антитела к кардиолипину или другим фосфоли- |
титр достаточно низкий. |
|
пидам. Лабораторный диагноз антифосфолипид- |
Определению АФА может мешать ревмато- |
|
ного синдрома можно ставить только в том слу- |
идный фактор, поэтому, если на фоне клиничес- |
|
чае, если содержание диагностических аутоанти- |
ких признаков заболевания иммунохимические |
|
тел в сыворотке крови, выявленных иммунофер- |
тесты на АФА дают отрицательный результат, то |
|
ментным методом, подтверждает патологию по- |
необходимо провести коагулянтные тесты на на- |
|
вторно с интервалом, по крайней мере, в 6 недель. |
личие волчаночного антикоагулянта. |
|
Тесты АЛЯ исслелования фибринолитической системы
Основным функциональным ферментом фибринолиза является плазмин. При лизисе фибринового сгустка плазминоген и его активаторы фиксируются на фибрине, где идет активное расщепление субстрата, тогда как в плазме фибринолиз
слабо выражен, плазмин блокирован а-антиплаз-
2
мином.
Спонтанный эуглобулиновый лизис
Спонтанный эуглобулиновый лизис - традиционный метод оценки фибринолиза. В кислой среде при низкой температуре происходит осаждение эуглобулиновой фракции белков плазмы, содержащей фибриноген, факторы свертывания, плазминоген и его активаторы (рис. 121). Ингибиторы фибринолиза выпадают в осадок в незначительном количестве (около 2%). После растворения эуглобулиновой фракции и образования фиб-
ринового сгустка определяют время его лизиса, что отражает фибринолитическую активность плазмы.
Укорочение времени лизиса эуглобулинов (ак-
тивация фибринолиза) отмечается при:
•уменьшении концентрации фибриногена - гипо- и дисфибриногенемия;
•увеличении содержания плазминогена и его ак тиваторов - панкреатит, панкреонекроз, мета-
Рис. 121. Компоненты фибринолитической системы, которые определяют результаты метода«спонтанный эуглобулиновый лизис»

Обеспечение диагностики нарушений гемостаза в КДЛ
стазирующии рак предстательной железы, легкого, |
|
При добавлении стрептокиназы (бактериаль- |
|||||
яичников, метастазы |
меланомы, операции |
на |
ный препарат, который используется как тромбо- |
||||
легких, предстательной, |
поджелудочной железе, |
литик) к разведенному образцу исследуемой плаз- |
|||||
гиперкатехоламинемия (стресс, тиреотоксикоз, |
мы образуется плазминоген-стрептокиназный ком- |
||||||
гипертонический |
криз, |
введение |
адреналина), |
плекс, который обладает ферментативной актив- |
|||
шок, патология |
беременности, терминальные |
и |
ностью и способен расщеплять хромогенный суб- |
||||
другие состояния, сопровождающиеся |
развитием |
страт (рис. 122). Ферментативная активность ком- |
|||||
ДВС-синдрома, цирроз, рак, метастатическое |
плекса плазминоген-стрептокиназа не подавляет- |
||||||
поражение печени (снижение ан-типлазминовой и |
ся α2-макроглобулином и α2-антиплазмином. Тес- |
||||||
антиактиваторной функции). Увеличение времени |
ты, в которых сначала переводили плазминоген в |
||||||
лизиса эуглобулинов (угнетение фибринолиза) |
плазмин, а затем пытались определить активность |
||||||
отмечается при: |
|
|
|
|
плазмина, не получились надежными, так как сво- |
||
• |
гиперфибриногенемии; |
|
|
бодный плазмин мгновенно инактивируется α2-ан- |
|||
• |
врожденной а-, гипоили дисплазминогенемии; |
|
типлазмином, присутствующим в пробе. |
||||
• дефиците плазминогена и его активаторов - ре |
|
|
|
||||
|
цидивирующие венозные тромбозы, системные |
|
Определение α2-антиплазмина |
||||
|
васкулиты, сепсис, нефротический синдром, ги- |
|
|||||
|
|
|
α2 -антиплазмин - самый быстрый «реактив- |
||||
|
покоагуляционная стадия ДВС-синдрома, цир |
|
|
||||
|
роз печени (нарушение синтеза плазминогена). |
|
ный» ингибитор плазмина, он не позволяет при- |
||||
|
Тест может применяться при фибринолитичес- |
|
сутствовать плазмину в крови в свободном виде. |
||||
кой терапии для контроля эффективности лечения. |
α2 -антиплазмин, помимо плазмина, ингибирует |
||||||
Метод требует учета исходного содержания |
активаторы плазминогена - урокиназу (u-РА) и тка- |
||||||
плазме фибриногена, так как при снижении фиб- |
невой активатор (t-PA). Дефицит α2-антиплазмина |
||||||
риногена время лизиса укорачивается, что трак- |
встречается относительно редко, но если возникает, |
||||||
туется ошибочно как гиперфибринолиз. При ги- |
то это сопровождается тяжелым геморрагическим |
||||||
перфибриногенемии время лизиса удлиняется. |
синдромом, проявляющимся диапедезными крово- |
||||||
Поэтому при отклонениях содержания фибрино- |
течениями. Основной причиной кровотечений яв- |
||||||
гена в плазме, а также неполноценной полимери- |
ляется присутствие свободного плазмина, который |
||||||
зации фибрина и гепаринемии возможно получе- |
разрушает все тромбы и деградирует фибриноген. |
||||||
ние ошибочных результатов. В связи с ориентиро- |
|
Определение α2-антиплазмина вместе с опре- |
|||||
вочным характером и недостаточной специфично- |
делением ингибитора тканевого активатора плаз- |
||||||
стью в последнее время вместо теста спонтанного |
миногена типа 1 (PAI-1), XIII фактора можно рас- |
||||||
лизиса эуглобулинового сгустка начали использо- |
сматривать как тесты 2-го уровня, которые необ- |
||||||
вать определение отдельных факторов фибрино- |
ходимо выполнять, если скрининговые тесты (ПВ, |
||||||
лиза, в первую очередь плазминогена. |
|
|
АЧТВ, ТВ и определение функции тромбоцитов) |
||||
|
|
|
|
|
|
нормальны, а больной страдает кровотечениями. |
|
Определение плазминогена |
|
|
|
Уменьшение содержания (активности) α2-ан- |
|||
|
|
типлазмина наблюдается при: |
|||||
|
Дефицит плазминогена - один из потенциаль- |
||||||
|
• |
врожденном (наследственном) дефиците; |
|||||
ных факторов риска тромбоза, хотя клинически |
• |
заболеваниях печени (нарушается синтез α2-ан- |
|||||
это подтверждается не всегда. |
|
|
|
типлазмина); |
|||
Рис. 122. Принцип определения плазминогена хромогенным методом. СК - стрептокиназа
Обеспечение диагностики нарушений гемостаза в КДЛ
• |
ДВС-синдроме; |
ется как один из тестов профиля(панели) оценки |
• |
лейкозах; |
тромбофилии. У больных с кровотечениями не- |
• |
нефротическом синдроме; |
ясного генеза с нормальными скрининговыми |
• |
интенсивной тромболитической терапии, ко |
тестами дефицит PAI-1 может быть причиной па- |
|
торая может вызвать потребление α2-анти- |
тологии. Истинный дефицит выявляется относи- |
|
плазмина. |
тельно редко, но сопровождается тяжелыми кро- |
|
После экстракорпорального кровообраще- |
вотечениями. |
ния с использованием АИК может наблюдаться |
Повышение PAI-1 встречается достаточно ча- |
|
истощение α2-антиплазмина, что приводит к ги- |
сто, так как PAI-1 - белок острой фазы. Это име- |
|
перфибринолизу, сочетающемуся с истощением |
ет клиническое значение, так как является при- |
|
фибриногена, деградацией плазмином плазмен- |
чиной рецидивирующего венозного тромбоза и |
|
ных белков (в том числе факторов гемостаза), |
отмечается часто у мужчин в преклонном возрас- |
|
разрушением тромбоцитов и кровотечениями. |
те. PAI-1 повышается при: |
|
|
Принцип определения α2-антиплазмина подо- |
инфекционных и воспалительных процессах; |
бен технологиям определения других ингибито- |
послеоперационном периоде; |
|
ров (рис. 123). Так как происходит быстрая инак- |
злокачественных опухолях; |
|
тивация плазмина α2-антиплазмином, то стадия |
ожирении; |
|
ингибирования и стадия измерения стартуют |
гипертриглицеридемии; |
|
практически одновременно (что позволяет повы- |
лечении дексаметазоном. |
|
сить специфичность метода при сниженной актив- |
У больных с инфарктом миокарда персисти- |
|
ности ингибитора в плазме). |
рующий подъем PAI-1 рассматривается как не- |
|
|
|
благоприятный прогностический признак. |
Опрелеление ингибитора активатора |
Определение PAI-1 состоит из нескольких |
|
этапов. На первом этапе необходимо инактиви- |
||
плазминогена типа 1 (PAI-1) |
ровать ингибиторы плазмина - α2-антиплазмин и |
|
|
PAI-1 в качестве основного ингибитора уро- |
α2-макроглобулин. Затем используется общий |
киназы (u-РА) и тканевого активатора (t-PA) иг- |
принцип определения остаточной активности до- |
|
рает важную роль в контроле за активностью |
бавленного в избытке фактора, который должен |
фибринолиза. Определение PAI-1 часто включа- |
подавляться исследуемым ингибитором (рис. 124). |
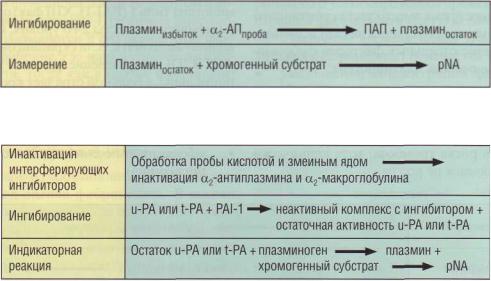
Рис. 123. Принцип определения α2-антиплазмина хромогенным методом. ПАП - комплекс плазмин-антиплазмин
Рис. 124. Принцип определения ингибитора тканевого активатора плазминогена типа 1 (РАМ) хромогенным методом. u-PA - урокиназа, t-PA - тканевой активатор
