
- •13.1.1 Полипептид, иэт, цв. Реакции
- •13.2.1 Декарбоксилирование пвк
- •13.3 Фад – химические свойства
- •13.4 Роль желчи в процессе пищеварения и всасывания жиров
- •13.5.1 Нуклеопротеиды, гидролиз
- •14.1.1 Биосинтез мочевины
- •14.2.1 Рнк
- •14.3 Гормоны, роль в регуляции глюкозы
- •14.4 Над и надф
- •14.5.1 Синтез полипептидов
- •14.5.2 Активация по Курциусу:
13.1.1 Полипептид, иэт, цв. Реакции
Полипептид – высокомолекулярное соединение, представляющее собой цепочку аминокислотных остатков, соединенных пептидной связью. В 1888 году химик Данилевский предположил, что белки – это полипептиды, линейные молекулы, которые образуются в результате действия карбоксильной группы одной аминокислоты с амино-группой другой аминокислоты с отщеплением воды и образуется дипептид.Образуется амидная связь (для белков пептидная), эти пептидные связи разделены только одним углеродным атомом. На основании биуретовой реакции Данилевский сделал такой вывод, что пептидная связь в белковых молекулах имеет специфическое строение. Вследствие кетоенольной таутомерии она на половину двойная, на половину одинарная.
Белки можно обнаружить с помощью двух типов реакций: цветные и осаждения. При взаимодействии белка с некоторыми реактивами образуются окрашенные продукты реакции, обусловленные в молекуле белка определенной аминокислоты и пептидной химической связи. При денатурации белки утрачивают свою биологическую активность. Одним из важнейших признаков белка является его изоэлектрическая точка, т.е. такое значение pH, при котором белок находится в виде нейтральных молекул. Белки в этом состоянии наименее устойчивы и легко выпадают в осадок.
Цветные реакции на белки и аминокислоты
1. Биуретовая реакция на пептидную связь (не менее двух). Фиолетовое окрашивание.
 2.
Нингидриновая реакция на аминокислоты
характерна для аминогрупп, находяшихся
в α-положении. При нагревании
розово-фиолетовое окрашивание.
2.
Нингидриновая реакция на аминокислоты
характерна для аминогрупп, находяшихся
в α-положении. При нагревании
розово-фиолетовое окрашивание.

3. Ксантопротеиновая реакция открывает ароматические аминокислоты: триптофан, фениламин, тирозин и др. Желтый, оранжевый цвет.

4. Реакция Милона на тирозин. Кирпично-красный осадок при нагревании.

5. Реакция Фоля указывает на присутствие в белке цистеина и цистина, содержащих слабосвязанную серу. Черный осадок сульфида свинца.

6. Реакция Адамкевича обусловлена наличием в белке наличием триптофана. Красно-фиолетовое окрашивание.

7.
Реакция Сакагучи
обусловлена присутствием в белке
аргинина. В результате реакции аргинин
с α-нафтолом образуется продукт
конденсации окисленного аргинина
α-нафтолом. Гипобромид играет роль
окислителя. Красное окрашивание.
8. Реакция Паули обусловлена присутствием гистидина или тирозина в белке, которые, реагируя с диазобензосульфокислотой, образуют краситель красного цвета.
9. Нитропруссидная реакция обусловлена присутствием в белке серусодержащих аминокислот, которые при кипячении со щелочью разрушаются до сернистого натрия. Нитропруссид натрия [NaFe3+(CN)5NO] при взаимодействии с сернистым натрием превращается в соединение, окрашенное в красный цвет.
13.2.1 Декарбоксилирование пвк
Анаэробное декарбоксилирование пировиноградной кислоты





Пировиноградная
кислота
 Триаминопирофосфат
Триаминопирофосфат

Активный перуват
Аэробное декарбоксилирование пировиноградной кислоты

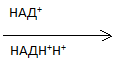


Декарбоксилазный-дегидрогеназный комплекс, это система состоит из 3 ферментов и 5 коферментов.
Ликоливая
кислота легко восстанавливается с
образованием гидроликоливой кислоты


Ацетилгидроликолевая кислота

![]()
![]()
![]()
ФАДН2 + НАД+ → ФАД + НАДФ + Н+
Ацетилгидроликолевая кислота взаимодействует с коэнзимом-А, происходит перенос ацетильной группы на коэнзим-А. Дегидроликолевая кислота взаимодействует с ФАД. ФАД взаимодействует с НАД.
Продуктом аэробного декарбоксилирования является ацетикоэнзим-А. Ацетикоэнзим-А расходуется для синтеза аминокислот, жирных кислот, углеводов (глюконеогенез). Пировиноградная кислота и ацетикоэнзим-А – главные метаболиты клетки.
