
- •Конденсированные двухкомпонентные системы.
- •I. По растворимости в твердом состоянии:
- •II. По образованию химического соединения:
- •Диаграмма состояния неизоморфноплавящихся веществ.
- •Построение диаграмм плавкости.
- •Диаграммы состояния неизоморфноплавящихся веществ с обазованием устойчивого химического соеднения.
- •Диаграммы состояния изоморфноплавящихся веществ.
- •Правило рычага.
- •Построение Диаграмм состояния изоморфноплавящихся веществ.
Построение диаграмм плавкости.
Диаграммы плавкости строят экспериментально по кривым охлаждения. Мы уже рассматривали кривые охлаждения чистых веществ – воды. Кривые охлаждения двухкомпонентной смеси будут несколько отличаться от кривых охлаждения чистых веществ.
Рассмотрим кривую охлаждения
двухкомпонентной смеси
![]() .
Возьмем смесь, состоящую из 20% висмута
и 80% кадмия.
.
Возьмем смесь, состоящую из 20% висмута
и 80% кадмия.
Смесь расплавляем и начинаем охлаждать.

По прямой (1-2) идет охлаждение расплава.
точка 2 – начало кристаллизации одного из компонентов, которого больше по отношению к эвтектике (Cd).
Так как при этом выделяется теплота кристаллизации (т.е. система как бы сама себя разогревает), то скорость охлаждения упадет, на графике это отображается изменением угла наклона кривой охлаждения.
точка 3 –
начинается кристаллизация
второговещества ![]() ,
или это называется кристаллизацией
эвтектической смеси.
,
или это называется кристаллизацией
эвтектической смеси.
точка 4 – характеризует исчезновение последней капли расплава.
Линия 4-5 характеризует охлаждение кристаллов до температуры окружающей среды.
Точка 6: по правилу фаз Гиббса С=К-Ф+1=2-1+1=2
Можно изменять два параметра:
а) температуру;
б) состав смеси.
Точка 7: С=2-2+1=1 (можно менять только температуру)
На отрезке 3-4, точка 8: С= 2-3 +1 =0 (ничего менять нельзя)
Система условно нонвариантна (безвариантна).
Только чистое вещество кристаллизуется в точке, т.е. при одной температуре. Смесь веществ всегда кристаллизуется в интервале температур.
Одновременная кристаллизация расплава при одном и том же составе и при одной температуре характерна для эвтектической смеси.
Для построения диаграмм плавкостиполучают набор кривых охлаждения смесей разного состава.
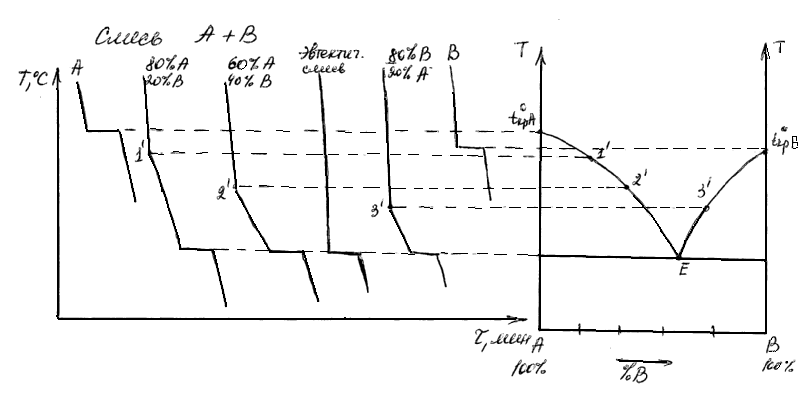
Все точки изломов 1΄, 2΄, 3΄ и горизонтальные участки наносят на диаграмму и получают диаграмму плавкости системы.
Данный метод построения диаграмм называется термическим анализом и относится к физико–химическим методам анализа.
Диаграммы состояния неизоморфноплавящихся веществ с обазованием устойчивого химического соеднения.

К типу таких составов относятся системы магний–олово [Mg–Sn], система [H2O–LiClO3], образующая 2 или 3 типа кристаллогидратов.
В системе магний–олово образуется
соединение Mg2Sn(![]() ),
которое имеет свою собственную температуру
плавления намного выше, чем температуры
плавления чистых магния и олова (точка
С).
),
которое имеет свою собственную температуру
плавления намного выше, чем температуры
плавления чистых магния и олова (точка
С).
Образование химического соединения является причиной возникновения на диаграмме плавкости двух точек эвтектики Е1и Е2.
Точка Е1 соответствует эвтектическому составу, образованному из компонента А и химического соединения.
Точка Е2 соответствует эвтектическому составу, образованному из компонента В и химического соединения.
Линия ликвидуса Е1СЕ2– это линия равновесного моновариантного существования расплава и кристаллов образовавшегося химического соединения.
Точка С – температура плавления химического соединения.
ПОСТРОЕНИЕ ДИАГРАММ.
Такие диаграммы получают также с помощью кривых охлаждения.

По кривым охлаждения строят диаграмму плавкости, нанося все точки изгибов и горизонтальных участков.
Расплав химического соединения состава АВ имеет кривую охлаждения чистого вещества с одним горизонтальным участком (температура плавления или кристаллизации АВ), (точка С).
Однако, состав расплава химического соединения АВ, заключенного между Е1и Е2 имеет некоторые особенности (кривые 2 и 3).
В точках 2΄ и 3΄ образуются кристаллы АВ и кристаллизуется эвтектика (горизонтальные участки на этих кривых).
Т. 1 С=2-2+1=1
Т. Т![]() С=1-2+1=0
С=1-2+1=0
Т. Т![]() С=1-2+1=0
С=1-2+1=0
Т. Е С=2-3+1=0
