
- •Учреждение образования
- •Введение
- •Условные обозначения
- •1. Основные технологические показатели и их расчет
- •1.1. Способы выражения концентраций и составов газообразных, жидких и твердых растворов и их смесей
- •1.2. Показатели химико-технологического процесса
- •1.3. Примеры расчетов
- •Решение.
- •1.4. Задания
- •2. Материальный баланс химико-технологических процессов
- •2.1. Стехиометрический материальный баланс
- •2.2. Примеры составления стехиометрических балансов
- •2.3. Практический материальный баланс
- •Материальный баланс процесса получения фосфора из апатитовой руды
- •1 330 Кг
- •Часовой материальный баланс окисления аммиака
- •Материальный баланс производства сн3он
- •Материальный баланс производства сульфида натрия
- •Материальный баланс процесса кристаллизации СuSо4 5н2о
- •Материальный баланс процесса получения негашеной извести
- •2.5. Задания
- •3. Тепловой баланс химико-технологических процессов
- •3.1. Примеры расчета тепловых балансов
- •Тепловой баланс процесса газификации твердого топлива
- •3.2. Задания
- •Молярные массы некоторых элементов и веществ
- •Удельная теплоемкость с [кДж/(кг к)] газов и паров
- •Удельная теплоемкость с [кДж/(кг к)] жидкостей и водных растворов
- •Основные термодинамические константы некоторых неорганических веществ в стандартных условиях
- •Литература
- •Содержание
- •Общая химическая технология
- •220050. Минск, Свердлова, 13а.
- •220050. Минск, Свердлова, 13.
О
Кокс, (9,5%)1 330 Кг
Печь Шлак, 9 000
кг (64,5%) Фосфор, 1 000
кг 17,2
% СО2, 3 668
кг (26,3%) Апатит,
10 250 кг (73,5%) Песок 2 370
кг (17%) Ферро-фосфор, 282
кг (2
%)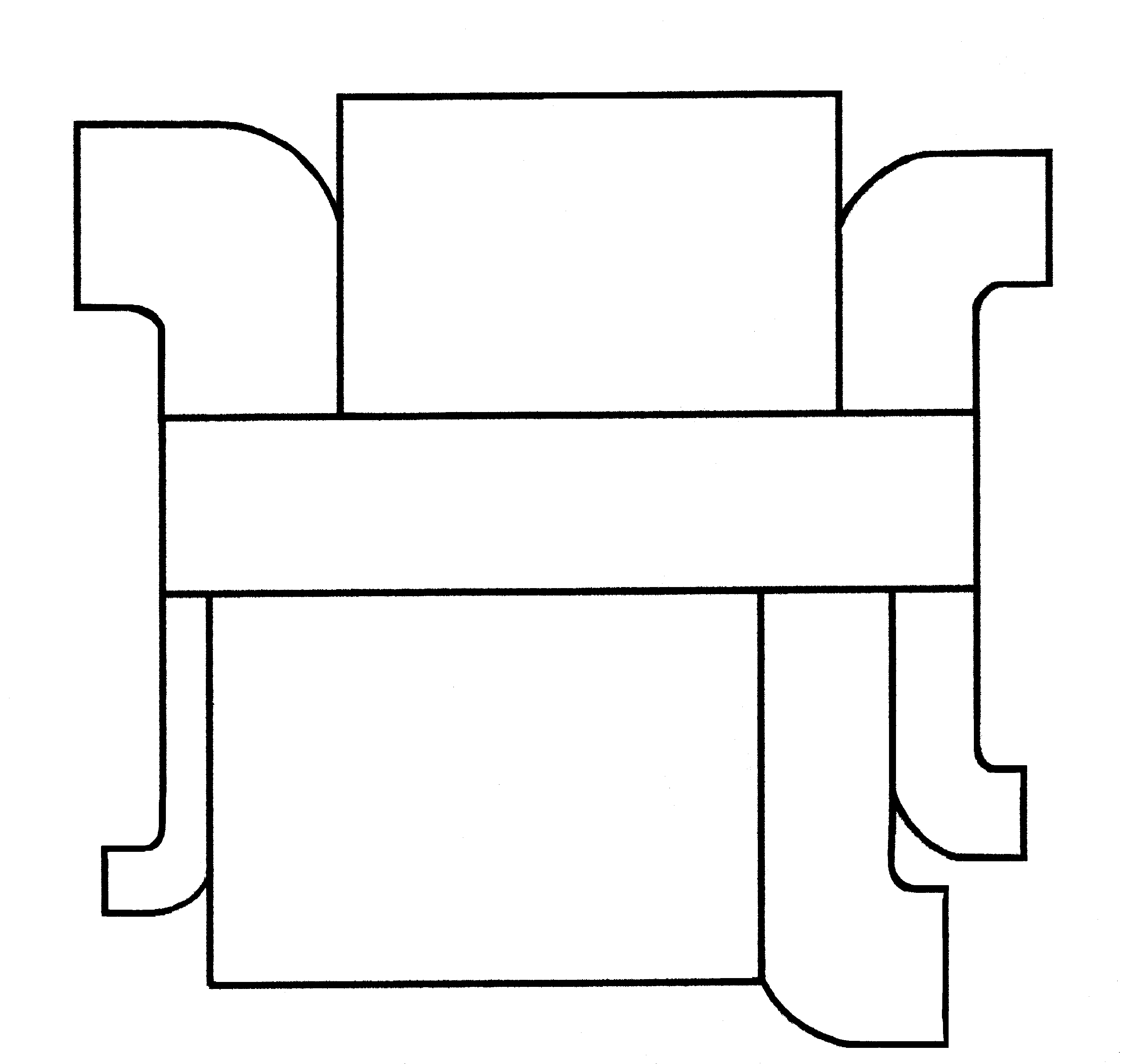
Рис. 1. Поточная диаграмма материального баланса процесса получения
фосфора из апатитовой руды
Ширина потоков на диаграмме Санкея пропорциональная массам материалов (или теплотам в случае теплового баланса), участвующих в процессе.
2.4. Примеры расчета материальных балансов технологических процессов
Пример 1. Составить часовой материальный баланс процесса окисления аммиака, необходимого для получения 100 000 т/год HNO3, если цех работает 355 дней в году, селективность окисления аммиака в оксид азота (II) 97%, концентрация аммиака в аммиачно-воздушной смеси 11,5 об. %. Молярная масса, г/моль или кг/кмоль: О2 – 32; N2 – 28, NН3 – 17, HNO3 – 63, NО – 30, Н2О – 18.
Решение.
При получении азотной кислоты протекают следующие реакции:
1-я стадия
основная 4NН3 + 5О2 = 4NО + 6Н2О; (36)
параллельная 4NН3 + 3О2 = 2N2 + 6Н2О; (37)
2-я стадия
2NО + О2 = 2NО2;
3-я стадия
2NО2 + Н2О + 0,5О2 = 2HNO3.
Суммарной реакции получения азотной кислоты соответствует следующее стехиометрическое уравнение:
NН3 + 2О2 = HNO3 + Н2О.
С учетом степени превращения аммиака в оксид азота (II) для получения 100 000 т/г. HNO3 необходимо
![]() =
(100 000 · 17) / (63 · 0,97) = 27 819 т/г.
=
(100 000 · 17) / (63 · 0,97) = 27 819 т/г.
или
27 819 / 355 · 24 = 3 265 кг/ч.
![]() =
(3260
· 22,4 · 1 000) / 17 = 4 302 м3/ч.
=
(3260
· 22,4 · 1 000) / 17 = 4 302 м3/ч.
Вместе с аммиаком подается воздуха
Vвозд = (4 302 · (100 – 11,5)) / 11,5 = 33 108 м3.
Так как для технических расчетов принимается, что содержание кислорода в воздухе составляет 21 об. %, азота – 79 об. %, то их объемный и массовый расходы составляют:
![]() =
33 108 · 0,21 = 6 953 м3/ч;
=
33 108 · 0,21 = 6 953 м3/ч;
![]() =
6 953 · 32 / 22,4 =
9 933 кг/ч;
=
6 953 · 32 / 22,4 =
9 933 кг/ч;
![]() =
33 108 – 6 953 = 26 155 м3/ч;
=
33 108 – 6 953 = 26 155 м3/ч;
![]() =
26 155 · 28 / 22,4 = 32 694 кг/ч.
=
26 155 · 28 / 22,4 = 32 694 кг/ч.
С учетом селективности процесса образуется NО:
VNО = 4 302 · 0,97 = 4 173 м3/ч;
mNO = 4173 30 / 22,4 = 5 589 кг/ч.
В результате протекания реакции (37) образуется N2:
(4 302 – 4 173) / 2 = 65 м3/ч
или
65 · 28 / 22,4 = 81 кг/ч.
Объем и масса Н2О, образующейся по реакции (36), составляют:
![]() =
4 173 · 6 / 4 = 6 260 м3/ч;
=
4 173 · 6 / 4 = 6 260 м3/ч;
![]() =
6 260 · 18 / 22,4 = 5 030 кг/ч;
=
6 260 · 18 / 22,4 = 5 030 кг/ч;
по реакции (37)
![]() =
65 · 6 / 2 = 195м3/ч;
=
65 · 6 / 2 = 195м3/ч;
![]() =
195 · 18 / 22,4 = 157 кг/ч.
=
195 · 18 / 22,4 = 157 кг/ч.
Суммарная масса воды составляет
![]() ∑=
5 030 + 157 =
5 187 кг/ч.
∑=
5 030 + 157 =
5 187 кг/ч.
Расходуется кислорода по реакции (36)
![]() =
4 173 · 5 / 4 = 5 216 м3/ч;
=
4 173 · 5 / 4 = 5 216 м3/ч;
по реакции (37)
![]() =
65 · 3 / 2 = 98 м3/ч.
=
65 · 3 / 2 = 98 м3/ч.
Объем и масса непрореагировавшего кислорода составят:
![]() =
6 960 – 5 216 – 98 = 1 639 м3;
=
6 960 – 5 216 – 98 = 1 639 м3;
![]() =
1 655 · 32 / 22,4 = 2 341 кг.
=
1 655 · 32 / 22,4 = 2 341 кг.
Образуется газ состава:
м3 об. %
NО 4 173 10,8
N2 65 + 26 155 = 26 220 68,1
О2 6 953 – (5 216 + 98) = 1 639 4,2
Н2О 195 + 6 260 = 6 455 16,9
Результаты расчетов сведены в табл. 4.
Таблица 4
