
- •Учреждение образования
- •Введение
- •Условные обозначения
- •1. Основные технологические показатели и их расчет
- •1.1. Способы выражения концентраций и составов газообразных, жидких и твердых растворов и их смесей
- •1.2. Показатели химико-технологического процесса
- •1.3. Примеры расчетов
- •Решение.
- •1.4. Задания
- •2. Материальный баланс химико-технологических процессов
- •2.1. Стехиометрический материальный баланс
- •2.2. Примеры составления стехиометрических балансов
- •2.3. Практический материальный баланс
- •Материальный баланс процесса получения фосфора из апатитовой руды
- •1 330 Кг
- •Часовой материальный баланс окисления аммиака
- •Материальный баланс производства сн3он
- •Материальный баланс производства сульфида натрия
- •Материальный баланс процесса кристаллизации СuSо4 5н2о
- •Материальный баланс процесса получения негашеной извести
- •2.5. Задания
- •3. Тепловой баланс химико-технологических процессов
- •3.1. Примеры расчета тепловых балансов
- •Тепловой баланс процесса газификации твердого топлива
- •3.2. Задания
- •Молярные массы некоторых элементов и веществ
- •Удельная теплоемкость с [кДж/(кг к)] газов и паров
- •Удельная теплоемкость с [кДж/(кг к)] жидкостей и водных растворов
- •Основные термодинамические константы некоторых неорганических веществ в стандартных условиях
- •Литература
- •Содержание
- •Общая химическая технология
- •220050. Минск, Свердлова, 13а.
- •220050. Минск, Свердлова, 13.
Условные обозначения
А, В, …R, S – исходные вещества и продукты реакции;
а, b, … r, s – коэффициенты в стехиометрических уравнениях;
Рк – расходный коэффициент, т/т, кг/т, м3/т;
С – концентрация, моль/л, кмоль/м3;
срм – молярная теплоемкость, Дж/(моль К);
ср – удельная теплоемкость, кДж/(кг К), кДж/(м3 К);
![]()
средняя
молярная теплоемкость, Дж/(моль
К);
средняя
молярная теплоемкость, Дж/(моль
К);
П – производительность, кг/ч, т/сут;
I – интенсивность, кг/(ч м3), м3/(ч м3), т/(сут м2);
F поверхность теплообмена, м2;
G – массовый расход, кг/ч, т/ч;
k коэффициент теплопередачи, Дж/(м2 К);
m – масса, кг;
n – химическое количество вещества, моль, кмоль;
М – молекулярная масса;
Q – тепловой эффект реакции, количество тепла, Дж, кДж;
Р – давление, Па, кПа;
Т – температура, С, К;
V – объем, л, м3;
х – степень превращения;
z число эквивалентов;
плотность, г/л, кг/м3;
α – выход продукта;
τ продолжительность, мин, ч;
ω – массовая доля;
N – молярная доля.
1. Основные технологические показатели и их расчет
1.1. Способы выражения концентраций и составов газообразных, жидких и твердых растворов и их смесей
Исходными реагентами, а также конечными продуктами могут быть вещества, находящиеся в твердом, жидком и газообразном состояниях. На практике используют различные способы выражения концентраций и составов, а также переход от одних единиц, характеризующих состав, к другим.
Для газообразных веществ масса их смеси определяется по формуле
![]() (1)
(1)
где 22,4 – объем (л или м3), который занимает 1 моль (кмоль) газа при нормальных условиях (Т = 273 K, Р = 101,3 кПа); V1, V2, …, Vi объемы газообразных компонентов, л или м3; М1, М2, …, Мi молярные массы газообразных компонентов, г/моль или кг/кмоль.
Средняя молярная масса газовой смеси (при аддитавности ее свойств) равна
Мсмеси = (V1 М1 + V2 М2 + … + Vi Мi) / (V1 + V2 + … + Vi). (2)
Концентрацию компонентов газовых смесей выражают чаще всего в объемных долях (Vi / Vсмеси) или объемных процентах (Vi 100 / Vсмеси). Объемная доля численно совпадает с молярной долей данного компонента.
Зависимость между давлением P, объемом V и температурой Т(K) вещества в газообразном состоянии определяется уравнением состояния газа (уравнением Менделеева – Клапейрона)
PV = nRT = (m / M) RT, (3)
где n – химическое количество газа; М – молярная масса газа; R – универсальная газовая постоянная, равная 8,314 Дж/(моль · K).
Если газ находится при одних условиях (Р, Т) и необходимо определить его объем при других условиях (Р1, Т1) или массу, то используют следующие формулы:
1) для расчета объема
![]() ;
(4)
;
(4)
2) для расчета массы
![]() (5)
(5)
где Vн.у. – объем газа, приведенный к нормальным условиям; V – объем газа при заданных условиях.
Раствор – однородная система переменного состава, содержащая два и большее число компонентов. Компонент, взятый в избытке и в том же агрегатном состоянии, что и сам раствор, принято считать растворителем, а компонент, взятый в недостатке, – растворенным веществом.
В жидком состоянии реагенты и продукты чаще всего находятся в виде растворов.
Для растворов необходимо знать их количественный состав, который может выражаться следующими способами:
массовая доля растворенного вещества А ((А));
молярная концентрация С(А), моль/л.
молярная концентрация эквивалента С(1/z(А)), моль-экв/л.
молярная доля растворенного вещества N(А).
Массовая доля растворенного вещества (А) – это величина, равная отношению массы вещества mА к массе раствора mр-ра.
(А) = mА / mр-ра, (6)
где mр-ра = mА + mрастворителя.
Массовую долю выражают в долях единицы или в процентах.
Молярная концентрация равна отношению химического количества растворенного вещества (n(А), моль) к объему раствора (V, л).
С(А) = n(А) / V. (7)
Химическое количество вещества выражается соотношением
n(А) = m(А) / М(А), (8)
где m(А) – масса вещества А, г, кг; М(А) – молярная масса вещества А, г/моль, кг/кмоль.
Если известна масса m и плотность раствора, то его объем V рассчитывается по формуле
V = mр-ра / . (9)
Молярная концентрация эквивалента (нормальная концентрация) С(1/z(А)) равна отношению химического количества вещества эквивалента (nэкв(А), моль) к объему раствора (V, л).
С(1/z(А)) = nэкв(А) / V. (10)
Химическое количество вещества эквивалента выражается соотношением
nэкв(А) = m(А) / М(1/z(А)). (11)
Молярная доля растворенного вещества N(А) это величина, равная отношению химического количества растворенного вещества к общему числу моль всех веществ в растворе.
N(А) = n(А) / ni. (12)
Молярная доля выражается в долях единицы или в процентах (моль %).
Расчеты при разбавлении и смешении двух растворов удобно производить с помощью так называемого правила креста, наглядное представление о котором дает приведенная ниже схема:
С1 (С С2)
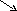

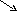
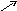 С
С
С2 (С1 С)
В точке С пересечения прямых записывают содержание вещества в смешанном растворе С (%). Содержание веществ в исходных смешиваемых растворах С1 и С2 (%) указывают с левой стороны креста, причем С1 > С2. Разность С1 С соответствует количеству массовых частей С2%-ного раствора, необходимого для смешения с С С2 частями С1%-ного разбавляемого раствора. При разбавлении раствора водой С2 = 0.
В химической промышленности широкое распространение получили процессы с использованием твердых веществ. Их состав чаще всего выражается:
в массовых долях (mi / mсмеси) или массовых процентах (m i · 100 / m смеси);
в молярных долях (рассчитывается по формуле (12)).
