
- •Введение
- •Содержание отчета
- •Лабораторная работа № 1 Карбонизация аммиачно-солевого раствора
- •Литература.
- •Лабораторная работа № 2 Никелирование металлов
- •Литература.
- •Лабораторная работа № 3 Сухая перегонка древесины
- •Цель работы
- •Литература
- •Лабораторная работа № 4 Поликонденсация дихлорэтана и тетрасулфида натрия
- •Теоретические сведения
- •Литература.
- •Лабораторная работа № 5. Поликонденсация фенола с формальдегидом.
- •Теоретические сведения.
- •5.4 Методика выполнения работы.
- •5.5 Методика обработки экспериментальных данных
- •Литература.
- •Лабораторная работа» № 6 Ионообменное умягчение воды
- •Контрольные вопросы
- •Литература
- •Лабораторная работа» № 7 Определение влажности материалов
- •Литература
Министерство образования и науки Украины
Восточноукраинский национальный университет им. В.Даля
Рубежанский филиал
Химико-технологический факультет
Кафедра технологии высокомолекулярных соединений
ОБЩАЯ ХИМИЧЕСКАЯ ТЕХНОЛОГИЯ
Методические указания к лабораторным работам
2002
Общая химическая технология. Методические указания к лабораторным работам для студентов специальностей:
8.091601 - «Химическая технология органических веществ»
7.091605 – «Химическая технология высокомолекулярных соединений»
8.090220 - «Оборудование химических производств и предприятий строительных материалов»
Составитель Беляев П.Г. – Рубежное: РФ ВНУ им. В.Даля
2002.- 42с.
В методических указаниях приводятся описания 7 лабораторных работ по курсу «Общая химическая технология», которые включают гомогенные и гетерогенные, каталитические и некаталитические, высокотемпературные, электрохимические процессы, а также процессы анализа и подготовки сырья.
Предназначены для студентов дневной и заочной форм обучения.
Одобрено кафедрой ТВМС
Протокол № 7 , « 14 » 03 2002 р.
Зав. кафедрой ТВМС Ю.П. Кудюков
Одобрено методическим советом РФ ВНУ
Протокол № 10 , « 20 » 06 2002р.
Председатель методического совета_____________А.С. Тимошин
Введение
Целью лабораторного практикума по курсу «Общая химическая технология» является закрепление теоретических знаний, знакомство с экспериментальными методами исследования химических процессов, выработка навыков обработки результатов экспериментов и расчета показателей эффективности процессов.
Перед выполнением работы студенты знакомятся с теоретическими сведениями по теме лабораторной работы, схемой экспериментальной установки и методикой выполнения лабораторной работы, правилами техники безопасности при работе на установке.
После беседы с преподавателем по этим вопросам студенты допускаются к работе на установке, выполняют экспериментальную часть работы, проводят обработку полученных результатов, рассчитывают необходимые показатели процесса и оформляют отчет.
Содержание отчета
Цель работы.
Теоретические сведения по теме работы.
Схема экспериментальной установки.
Методика выполнения работы.
Полученные результаты и их обработка. Расчет основных показателей процесса.
Титульный лист отчета по лабораторной работе оформляется по форме в соответствии с приложением А.
Выполненная и оформленная работа защищается на следующем занятии или в часы консультаций. На защите студенты должны показать знание теоретических вопросов по теме лабораторной работы и практического ее выполнения. Контрольные вопросы приводятся в конце описания каждой лабораторной работы.
Количество выполняемых работ зависит от специальности и формы обучения студентов и определяется рабочей учебной программой дисциплины.
Лабораторная работа № 1 Карбонизация аммиачно-солевого раствора
Цель работы
Ознакомление с процессом карбонизации, определение выхода гидрокарбоната натрия на лабораторной установке.
Теоретические сведения
К содовым
продуктам, в больших количествах
вырабатываемых химической промышленностью,
относятся кристаллическая сода (карбонат
натрия)
![]() ,
пищевая сода (гидрокарбонат натрия)
,
пищевая сода (гидрокарбонат натрия)![]() ,
кристаллическая сода
,
кристаллическая сода![]() ,
тяжелая сода
,
тяжелая сода![]() ,
каустическая сода (едкий натр)
,
каустическая сода (едкий натр)![]() .
.
Наиболее важным содовым продуктом является кальцинированная сода. Единственным промышленным способом производства соды в настоящее время является аммиачный способ, практические основы которого были разработаны в конце XIX века бельгийским инженером Сольве, а теория процесса русским ученым П.П.Федотьевым и другими.
Аммиачный способ производства соды включает следующие стадии.
Раствор поваренной соли насыщается аммиаком (аммонизация), а затем углекислым газом (карбонизация). При этом выпадает осадок гидрокарбоната натрия.
![]() . (1.1)
. (1.1)
Осадок гидрокарбоната натрия отфильтровывается и прокаливается (кальцинация).
![]() .
(1.2)
.
(1.2)
При этом
образуется конечный продукт
![]() (кальцинированная сода) и углекислый
газ, который возвращается на стадию
карбонизации.
(кальцинированная сода) и углекислый
газ, который возвращается на стадию
карбонизации.
Свежий углекислый газ получается обжигом известняка.
![]() .
(1.3)
.
(1.3)
Полученная при обжиге известь гасится водой.
![]() .
(1.4)
.
(1.4)
Известковое молоко используется для регенерации аммиака из маточного раствора после фильтрации гидрокарбоната натрия (дистилляция).
![]() .
(1.5)
.
(1.5)
Полученный аммиак направляется на аммонизацию солевого раствора. Раствор хлорида кальция является отходом.
Основной стадией аммиачно-содового производства является стадия карбонизации, описываемая суммарным уравнением (1.1). В свою очередь эта реакция протекает в несколько стадий.
Стадия монокарбонизации.
![]() .
(1.6)
.
(1.6)
Стадия бикарбонизации.
![]() .
(1.7)
.
(1.7)
Обменное разложение.
![]() .
(1.8)
.
(1.8)
Реакция (1.8)
является обратимой. гетерогенной
реакцией. Ее равновесие и равновесный
выход осадка гидрокарбоната натрия
определяются условиями растворимости
в четырехкомпонентной системе
![]() ,
которая была изучена П.П.Федотьевым.
Выход гидрокарбоната натрия (или степень
превращения
,
которая была изучена П.П.Федотьевым.
Выход гидрокарбоната натрия (или степень
превращения![]() в осадок
в осадок![]() )
зависит от температуры и концентрации
)
зависит от температуры и концентрации![]() и
и![]() в растворе. Наивысший равновесный выход
в растворе. Наивысший равновесный выход![]() достигается при температуре 32оС
и равен 84%.
достигается при температуре 32оС
и равен 84%.
В промышленных условиях основной технологический показатель (степень использования хлорида натрия) колеблется в пределах 65 - 75 %. Повысить его можно увеличением концентрации хлорида натрия в исходном рассоле, степени насыщения его аммиаком, повышением давления и содержания углекислого газа в газе, подаваемом на карбонизацию, а также снижением температуры в конце процесса карбонизации.
Схема экспериментальной установки
Экспериментальная установка для карбонизации аммиачно-солевого раствора (рис. 1.1) состоит из узлов получения воздуха и углекислого газа,
приготовления воздушно-аммиачной смеси, абсорбции углекислого газа аммонизированным рассолом. Воздух воздуходувкой подается через буферную склянку (1) и ротаметр (3), измеряющий его расход, в смеситель (7). Туда же подается углекислый газ из баллона через буферную склянку (4) и ротаметр (6). Для обеспечения равномерной подачи газов к линиям подачи газов присоединены маностаты (гидрозатворы) (2) и (5). Газовая смесь из смесителя через ротаметр (8) и трехходовой кран (11) подается в абсорбер (9), заполненный аммонизированным рассолом. Выходящий из абсорбера газ перед выбросом в атмосферу пропускается через поглотительную склянку (11), заполненную раствором соляной кислоты.
Методика выполнения работы.
Приготавливается
50 см3аммонизированного рассола,
содержащего 240 – 250 г/дм3![]() и 85 – 95 г/дм3
и 85 – 95 г/дм3![]() .
Раствор анализируется на содержание
аммиака и заливается в абсорбер
(9). Трехходовой кран
.
Раствор анализируется на содержание
аммиака и заливается в абсорбер
(9). Трехходовой кран
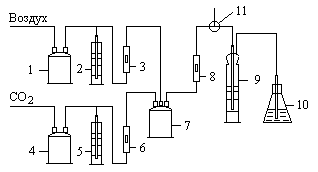
Рис. 1.1 Схема экспериментальной установки для карбонизации аммиачно-солевого раствора
1, 4 – буферные склянки, 2, 5 – гидравлические затворы, 3, 6, 8 – ротаметры, 7 – смеситель, 9 – абсорбер, 10 – поглотительная склянка, 11 – кран трехходовой.
открывается на выход в атмосферу, включается подача воздуха и с помощью
ротаметра (3) устанавливается его расход. Из баллона подается углекислый газ и с помощью ротаметра (6) устанавливается его расход. Трехходовой кран (11) переключается на подачу газовой смеси в абсорбер (9), с помощью ротаметра (8) устанавливается ее расход.
Процесс карбонизации продолжается в течение 1 – 1,5 часов. По окончании карбонизации осадок гидрокарбоната отфильтровывается на воронке Бюхнера при помощи вакуумного насоса. Осадок гидрокарбоната промывается насыщенным раствором гидрокарбоната натрия, сушится при температуре 40 – 50оС и взвешивается.
Маточный раствор после фильтрации осадка гидрокарбоната натрия анализируется на содержание свободного и полусвязанного аммиака. Анализ проводится аналогично анализу исходного раствора на содержание аммиака.
Для анализа отбирается проба раствора объемом 2 см3в коническую колбу, добавляется 10 см3дистиллированной воды и 1 – 2 капли метилового оранжевого, после чего титруется 1н раствором соляной кислоты до перехода желтой окраски в розовую. При титровании свободный и полусвязанный аммиак нейтрализуется кислотой:
![]() ,
(1.9)
,
(1.9)
![]() ,
(1.10)
,
(1.10)
![]() .
(1.11)
.
(1.11)
Методика обработки экспериментальных данных
Выход гидрокарбоната натрия определяется по формуле:
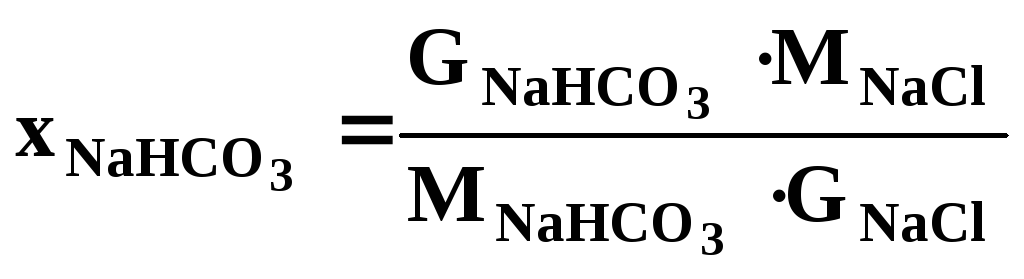 ,
(1.12)
,
(1.12)
где
![]() масса
сухого осадка гидрокарбоната натрия
(г),
масса
сухого осадка гидрокарбоната натрия
(г),
![]() масса
хлорида натрия в растворе, введенном в
абсорбер (г),
масса
хлорида натрия в растворе, введенном в
абсорбер (г),
![]() молекулярная
масса гидрокарбоната натрия (г/моль),
молекулярная
масса гидрокарбоната натрия (г/моль),
![]() молекулярная
масса хлорида натрия (г/моль).
молекулярная
масса хлорида натрия (г/моль).
Содержание свободного и полусвязанного аммиака определяется по формуле:
![]() ,
(1.13)
,
(1.13)
где
![]() содержание
свободного и полусвязанного аммиака в
анализируемом растворе (г/дм3),
содержание
свободного и полусвязанного аммиака в
анализируемом растворе (г/дм3),
![]() объем 1н раствора соляной кислоты,
израсходованной на титрование (см3),
объем 1н раствора соляной кислоты,
израсходованной на титрование (см3),
![]() объем
пробы анализируемого раствора (см3),
объем
пробы анализируемого раствора (см3),
![]() масса
аммиака, соответствующего 1см31н
раствора соляной кислоты.
масса
аммиака, соответствующего 1см31н
раствора соляной кислоты.
Степень использования аммиака определяется по формуле:
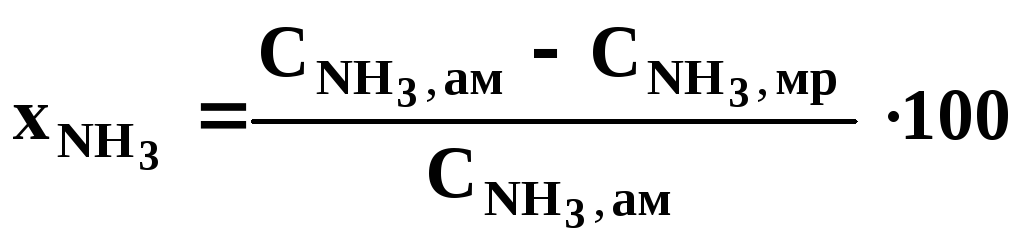 ,
(1.14)
,
(1.14)
где
![]() степень
использования аммиака (%),
степень
использования аммиака (%),
![]() содержание
свободного аммиака в исходном
аммонизированном растворе (г/дм3),
содержание
свободного аммиака в исходном
аммонизированном растворе (г/дм3),
![]() содержание
свободного и полусвязанного аммиака в
маточном растворе.
содержание
свободного и полусвязанного аммиака в
маточном растворе.
Техника безопасности
Приготовление аммонизированного раствора следует проводить в вытяжном шкафу.
Не открывать самостоятельно баллон с углекислым газом. Для выполнения этой операции пригласить лаборанта или преподавателя.
Не перекрывать (не пережимать) трубку, ведущую от газовой линии в гидрозатвор (во избежание чрезмерного повышения давления и возможного при этом разрыва стеклянных сосудов).
Контрольные вопросы
Из каких основных стадий складывается аммиачный способ производства соды? Составить уравнения соответствующих реакций.
Дать характеристику стадии карбонизации как основной стадии аммиачно-содового производства.
От каких факторов зависит состояние равновесия процесса карбонизации и равновесная степень превращения хлорида натрия в гидрокарбонат натрия.
От каких факторов зависит скорость процесса карбонизации?
