
Фармация, 2 курс, лекции биохимии / 24
.docЭнергией для такого переноса служит электрохимический градиент ионов Na+, вследствие чего этот процесс существенно зависит также от активности Na+ -
21
насоса, выносящего Na+ из клетки. Инсулин влияет также и на синтез белков, стимулируя активность рибосомального аппарата. Ниже представлена схема отражающая влияние инсулина на метаболизм в клетке:

Интеграция процессов клеточного метаболизма
Высшая форма регуляции - интеграция регуляторных систем клеточного метаболизма на уровне органов. Одной из наиболее важных и сложных проблем является выяснение взаимосвязи, взаимоподчинённости и взаимодействия разных регуляторных сигналов и регуляторных механизмов при реализации биологического эффекта. Поскольку многие нейромедиаторы и гормоны вызывают изменение концентрации ионов Са2+ и циклических нуклеотидов (важнейших внутриклеточных регуляторов), интегрирование эффектов многих внеклеточных регуляторов осуществляется на уровне взаимодействия Са-зависимых и цАМФ или цГМФ-зависимых процессов. Нередко вызывает недоумение тот факт, что десятки гормонов и гормоноподобных веществ действуют на клетку одним и тем же способом путем повышения концентрации циклического нуклеотида, однако каждый из
22
этих гормонов сохраняет свое "лицо", имеет свои, только ему присущие биологические эффекты. Это можно объяснить тем, что разные гормоны направляются по "разным адресам" - в те ткани, где есть соответствующие рецепторы. Часто гормон действует сразу на несколько тканей. Примером такого гормона является АКТГ:

Ответ ткани на регуляторный сигнал определяется набором генов и белков, функционирующих в данных клетках. Это позволяет организму с помощью одного специфического регулятора контролировать самые разнообразные химические процессы. Избирательность действия специфических регуляторов на те или иные клетки полностью определяется наличием в клетках соответствующих рецепторов, сопряженных с метаболическими особенностями ткани.
Регуляция и интеграция на уровне клетки
Регуляция и интеграция метаболических процессов в клетке осуществляется на уровне ферментов. Регуляторами ферментов являются:
субстраты и продукты реакции, коферменты и кофакторы, активаторы и ингибиторы, аллостеричеокие эффекторы, меняющиеся условия среды (рН, температура). Повышение концентрации субстрата не всегда приводит к росту ферментативной активности, а продукт не всегда ингибирует фермент (например, фосфофруктокиназа может тормозиться субстратами: А ТФ и фруктозо-I, 6-дифосфатом). Кофакторы и коферменты не обладают высокой специфичностью в отношении ферментов, изменение их концентрации в биологической системе может привести к изменению активности целой группы ферментов. Появление ферментов, обладающих олигомерной структурой,
23
значительно расширило возможности их регуляции. Еще более совершенным с каталитической и с регуляторной точки зрения является объединение разных ферментов, участвующих в реакции одной цепи метаболизма, в общий сложный олигомерный комплекс. Такие комплексы могут состоять из десятка ферментов, каждый из которых обладает четвертичной структурой (например, синтетаза жирных кислот, пируватдегидрогеназный комплекс).
Скорость метаболических процессов, происходящих в клетке, зависит от концентрации веществ, потребляющихся и накапливающихся в данной цепи реакций, а также от концентрации веществ, участвующих в других метаболических процессах. Интеграция на уровне отдельных метаболических систем осуществляется путем положительной или отрицательной обратной связи. Интегрирующая роль отводится ацетил-КоА:

Определенный пул НАДН2, уровень АТФ регулируют фосфофруктокиназу, пируваткиназу, цитрат дегидрогеназу - являются мощными регуляторами гликогенолиза, цикла Кребса.
24
При рассмотрении регуляторных путей, контролирующих биологические циклы, обращает на себя внимание, что регуляция в основном направлена на необратимые реакции (однако важность необратимых реакций в одном и том же биохимическом цикле может быть различна). Последовательная цепь реакций не будет протекать, пока не начнет функционировать фермент, стоящий в начале цепи. Затем превращения будут протекать со скоростью, которая определяется активностью самого медленного фермента в цепи реакций. Ферменты, запускающие метаболический путь, а также ферменты, лимитирующие скорость его протекания, принято называть ключевыми. Регуляторное воздействие, направленное на определенный метаболический цикл, опосредованно может изменять активность других циклов, а следовательно, и функциональную значимость других регуляторов, контролирующих эти циклы.
В клетке ферменты и субстраты могут быть разделены мембраной и тогда любой фактор, оказывающий влияние на проницаемость мембран, может служить регулятором ферментативного процесса. В механизмах клеточной интеграции большое значение имеют механизмы митохондриально-цитоплазматической интеграции, т.е. функционирование челночных механизмов:

25

26

Другим примером является усиление значения пентозного шунта при патологии. Так при инфаркте миокарда, когда основные пути аэробного энергообеспечения тормозятся, происходит переключение обмена на гликолиз и пентозный путь. НАДФН2, необходимый для энергообеспечения сердечной мышцы, поставляется из пентозного цикла, т.е. энергообеспечение проводящей системы миокарда зависит от него.
Хорошим примером интеграции метаболических путей в клетке является для клеток почек двойной цикл Кребса (цикл мочевины и цикл трикарбоновых кислот). Слайд демонстрирует взаимосвязь двух циклов Кребса:
27

Из цикла Кребса в цикл мочевины поступают: АТФ, аспартат, CО2, из цикла мочевины в цикл Кребса - фумарат.
Системы интегративных связей многоуровневы, часто дублированы, что имеет большое значение при патологии (в случае нарушения - возможно переключение на другие уровни, за счет которых будет осуществляться нарушенная функция).
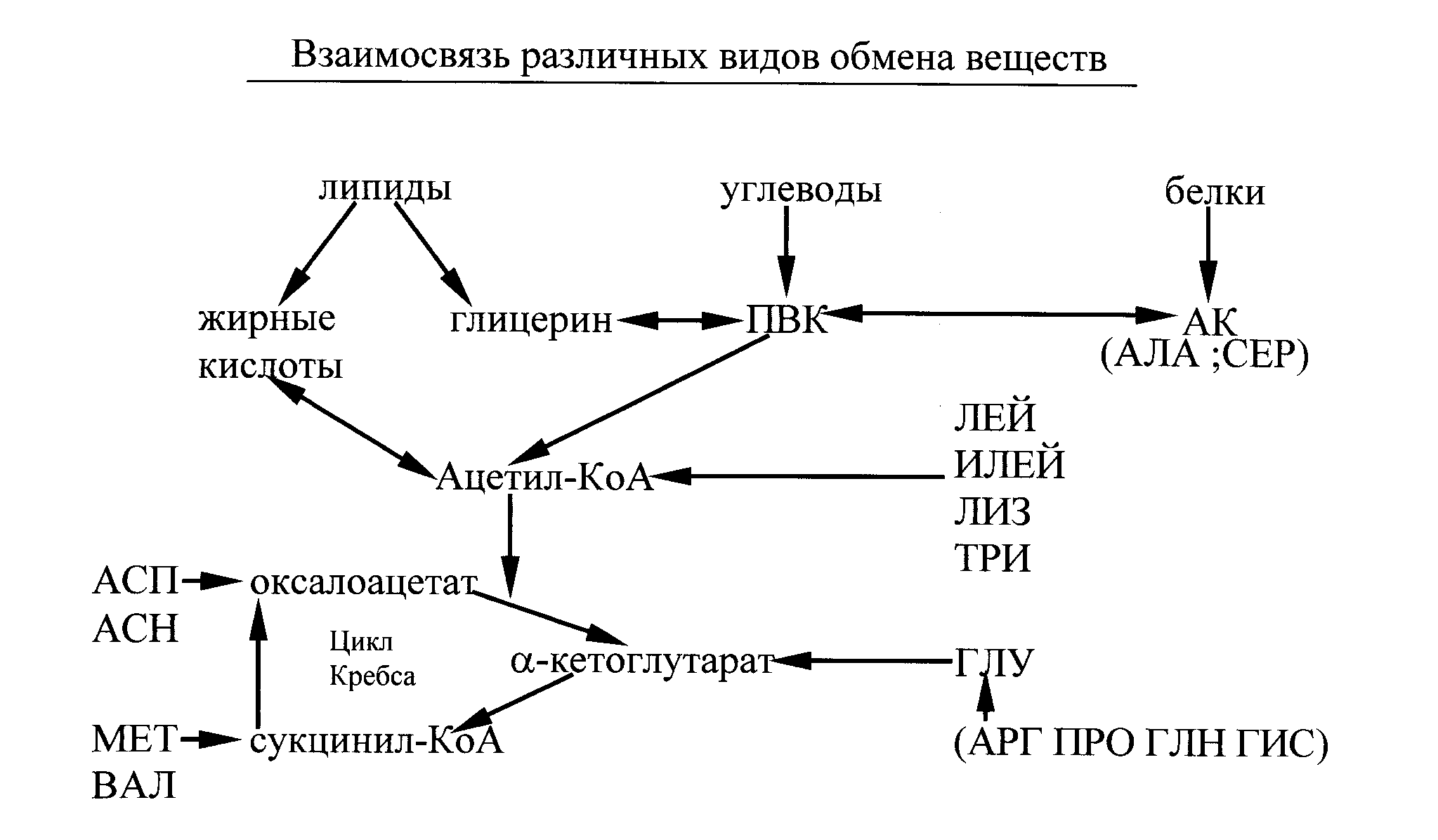
Взаимосвязь различных видов обмена веществ
В организме при различных патологиях, при питании однообразной пищей, когда наблюдается недостаток белков или углеводов, или жиров, происходит возмещение того или иного вещества за счет распада и синтеза имеющихся веществ. Ниже представлены схемы демонстрирующие переход одних веществ в другие:

29

30
ЗАКЛЮЧЕНИЕ
Реакции, идущие в клетках и в организме, должны быть скоординированы с помощью регуляторных механизмов. Эти механизмы, как мы видели, весьма разнообразны.
Регуляция метаболизма на клеточном и субклеточном уровнях осуществляется прежде всего путем регуляции синтеза и каталитической активности ферментов. К таким регуляторным механизмам относится: подавление синтеза ферментов конечным продуктом метаболического пути, индукция синтеза одного или более ферментов субстратами, модуляция активности уже присутствующих молекул ферментов. Большое значение имеет такая регуляция скорости метаболитов в клетку, и здесь ведущая роль за биологическими мембранами, окружающими протоплазму, и находящимися в ней ядром, митохондриями, лизосомами и другими субклеточными органеллами. Важнейшим средством, с помощью которого осуществляется регуляция обмена веществ в живых организмах, являются гормоны. Особая
31
роль в механизме действия гормонов принадлежит циклическим нуклеотидам (цАМФ и цГМФ).
У животных и человека гормональная регуляция обмена веществ тесно связана с координирующей деятельностью нервной системы.
Таким образом, можно выделить следующие уровни регуляции:
- регуляцию на уровне мембраны;
- регуляцию с участием циклических нуклеотидов;
- регуляцию количества фермента;
- регуляцию ферментативной активности;
- регуляцию с участием гормонов и нервной системы.
