
- •3 Алкены а. И. Кузнецов
- •3. Алкены
- •1. Получение
- •Б. Дегидратация спиртов
- •В. Дебромирование вицинальных дибромидов
- •2. Електрофильное присоединение (ае)
- •2.1. Присоединение галогеноводородов (гидрогалогенирование)
- •2.2. Гидратация
- •2.3 Присоединение спиртов
- •2.4. Галогенирование
- •3. Радикальное присоединение
- •4. Аллильное галогенирование
- •5. Метатезис
- •6. Окисление алкенов
- •6.1. Эпоксидирование
- •Упр.8. Какие продукты образуются в результате эпоксидирования с последующим кислотным гидролизом (а) цис-2-бутена и (б) транс-2-бутена.
- •6.2. Гидроксилирование
- •6.3. Озонолиз алкенов
- •6.4. Окисление алкенов в жестких условиях
- •6.5. Окисление этилена в ацетальдегид
- •6.6. Хлорокисление этилена
- •6.7. Окислительный аммонолиз
- •7. Гидроформилирование алкенов (Оксосинтез)
- •8. Присоединение карбенов и карбеноидов
- •8.1. Строение карбенов
- •9. Полимеризация алкенов
- •Полиакрилонитрил разлагается раньше, чем плавится. Он растворим в n,n-диметилформамиде, что позволяет изготовлять из него волокна Радикальной полимеризацией получают политетрафторэтилен (тефлон):
- •Тетрафторэтилен тефлон (плавится при 327оС)
- •Г. Координационная полимеризация
- •Синдиотактический изотактический
6.4. Окисление алкенов в жестких условиях
Окисление алкенов перманганатом калия в щелочной среде при нагревании (жесткие условия) приводит к разрушению их углеродного скелета по месту двойной связи. При этом в зависимости от числа алкильных групп, связанных с винильным фрагментом, могут быть получены две карбоновые кислоты, кислота и кетон или два кетона:
 (61)
(61)
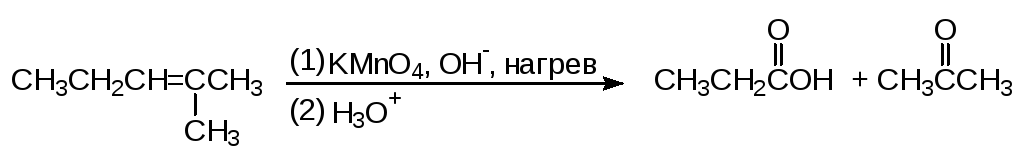 (62)
(62)
Упр.11. Какой продукт образуются при окислении циклогексена (а) разбавленным раствором перманганата калия на холоде и (б) концентрированным раствором перманганата калия с последующим подкислением.
Упр.12.Какие продукты образуются из 1,2-диметилциклогексена при его (а) каталитическом гидрировании, (б) окислении разбавленным раствором перманганата калия на холоде, (в) озонировании с последующим восстановительным расщеплением.
6.5. Окисление этилена в ацетальдегид
Окисление этилена кислородом воздуха в присутствии хлоридов палладия (II) и меди (II) приводит к образованию ацетальдегида (Вакер-процесс):
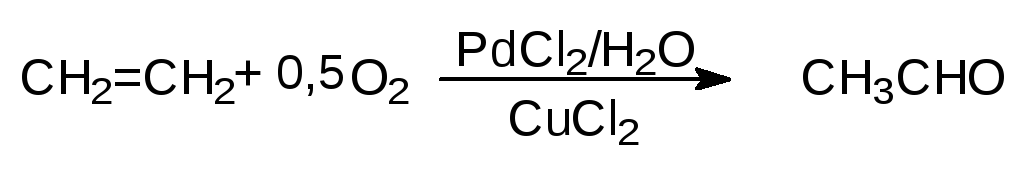 (63)
(63)
этаналь (ацетальдегид)
6.6. Хлорокисление этилена
Винилхлорид получают хлорокислением этилена:
![]() (64)
(64)
6.7. Окислительный аммонолиз
Окисление углеводородов кислородом воздуха в присутствии аммиака приводит к превращению метильной группы в цианогруппу. Такое окисление называется окислительным аммонолизом. Окислительным аммонолизом пропилена получают акрилонитрил.
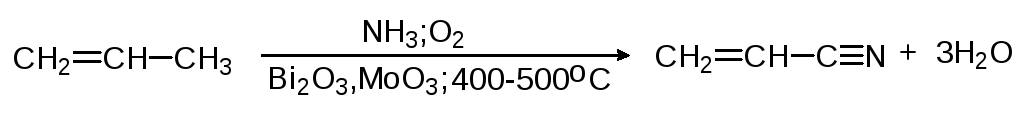 (65)
(65)
акрилонитрил
Окислительным аммонолизом метана получают синильную кислоту:
 (66)
(66)
7. Гидроформилирование алкенов (Оксосинтез)
При температуре от 30 до 250 оС и давлении 100-400 атм. в присутствии дикобальтоктакарбонила алкены присоединяют водород и монооксид углерода с образованием альдегидов. Обычно получается смесь изомеров:
![]() (67)
(67)
![]()
Механизм:
1. Отщепление лиганда
![]()
2. Присоединение этилена

3. Внедрение этилена

4. Присоединение лиганда
![]()
5. Внедрение СО
![]()
6. Окислительное присоединение водорода
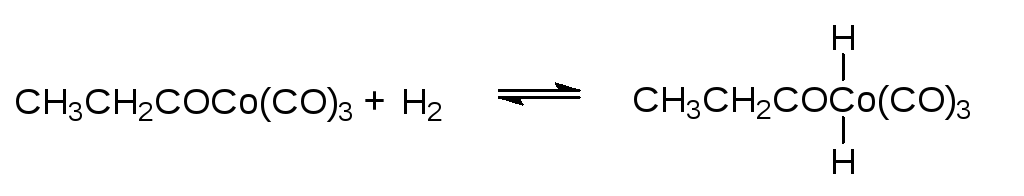
7. Восстановительное отщепление пропаналя
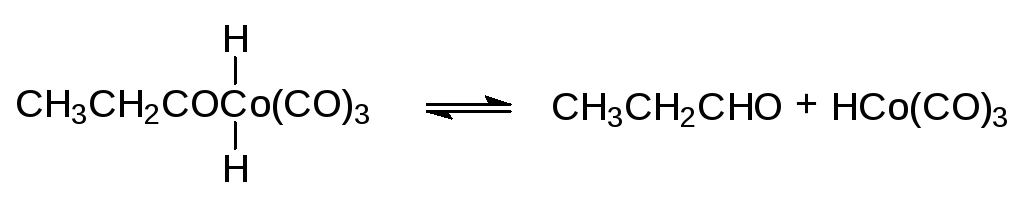
и т. д.
8. Присоединение карбенов и карбеноидов
Последние годы большое внимание в органической химии уделяется соединениям двухвалентного углерода – карбенам. Большинство из карбенов неустойчивы и сразу же после их образования реагируют с другими соединениями.
8.1. Строение карбенов
Незамещенный
карбен :СН2,
называемый также метиленом, может
находиться в синглетной или триплетной
форме. В синглетной форме карбена два
несвязывающих электрона со спаренными
спинами находятся на одной орбитали, в
то время как в триплетной форме два
неспаренных электрона с параллельными
спинами находятся на двух орбиталях
одинаковой энергии. Различные электронные
конфигурации синглетных и триплетных
карбенов находят отражение как в
различной геометрии этих частиц, так и
в различной химической активности.
Двухвалентный атом углерода синглетного
карбена находится в sp2-гибридном
состоянии, оба электрона расположены
на sp2-гибpиднoй
орбитали (ВЗМО), а р-орбиталь (НСМО) -
свободна. Триплетный карбен характеризуется
sp-гибридизацией двухвалентного углерода;
при этом два неспаренных электрона
располагаются на двух р-орбиталях, т. е.
триплетный карбен является бирадикалом.
Угол Н-С-Н для синглетного метилена,
согласно спектральным данным, равен
102-1050
, а для триплетного метилена этот угол
увеличивается до 135![]() 140o.
Это соответствует более высокой
стабильности триплетного метилена.
Согласно данным квантовомеханических
расчетов триплетный метилен действительно
на 10 ккал/моль стабильнее синглетного
метилена.
140o.
Это соответствует более высокой
стабильности триплетного метилена.
Согласно данным квантовомеханических
расчетов триплетный метилен действительно
на 10 ккал/моль стабильнее синглетного
метилена.

Заместители, однако, вызывают изменение относительной стабильности этих двух форм карбенов. Для диалкилкарбенов триплетная форма также стабильнее синглетной, но для дигалокарбенов :CHal2, и других карбенов с заместителями, содержащими неподеленную пару электронов, основным состоянием является синглетное. Валентный угол С1-С-С1 для дихлоркарбена, равный 106o, хорошо согласуется с синглетной формой. Более высокая стабильность синглетной формы дигалокарбенов по сравнению с триплетной, по-видимому, обусловлена ее стабилизацией за счет неподеленной пары электронов гетероатома

Такая стабилизация триплетной формы дигалокарбенов невозможна. Согласно данным квантовомеханического расчета, энергия синглет - триплетного перехода для дихлоркарбена составляет 13,5 Ккал/моль.
А. Дихлоркарбен
Для
генерирования дигалокарбенов разработаны
методы, основанные на реакции
![]() -элиминирования
галогеноводорода из тригалогенометанов
под действием сильных оснований. Этот
метод исторически был первым, с помощью
которого в качестве интермедиата был
генерирован первый из карбенов -
дихлоркарбен (Дж. Хайн
1950 г.).
При взаимодействии с сильными основаниями
из хлороформа (рКа хлороформа составляет
~16), бромоформа (рКа = 9)
и других тригалогенометанов образуется
анион который стабилизируется за счет
отщепления галогенид-иона с образованием
дигалокарбена.
Действием на хлороформ сильных оснований
получают дихлоркарбен:
-элиминирования
галогеноводорода из тригалогенометанов
под действием сильных оснований. Этот
метод исторически был первым, с помощью
которого в качестве интермедиата был
генерирован первый из карбенов -
дихлоркарбен (Дж. Хайн
1950 г.).
При взаимодействии с сильными основаниями
из хлороформа (рКа хлороформа составляет
~16), бромоформа (рКа = 9)
и других тригалогенометанов образуется
анион который стабилизируется за счет
отщепления галогенид-иона с образованием
дигалокарбена.
Действием на хлороформ сильных оснований
получают дихлоркарбен:
![]() (68)
(68)
дихлоркарбен
В качестве основания можно использовать также литийорганические соединения в индифферентной апротонной среде. Тогда ниже -100 0С можно зафиксировать образование трихлорметиллития в качестве интермедиата.

С помощью таких сильных оснований, как RLi, можно генерировать карбены из 1,1-дигалогенпроизводных

В последние годы для генерирования дигалокарбенов вместо н-бутиллития широко используют в качестве основания бис(триметилсилил)амид натрия.

При этом выделяется химически инертный силазан [бис(триметилсилил)амид]. Бис(триметилсилил)амид натрия, в отличие от н-бутиллития, можно выделять в инертной атмосфере в сухом виде. На практике чаще используют его эфирные растворы, которые можно хранить при комнатной температуре в течение длительного времени.
Дихлоркарбен может быть также генерирован при термическом декарбоксилировании сухого трихлорацетата натрия:

Один из самых доступных современных методов генерирования дихлоркарбена из хлороформа под действием гидроксида натрия в условиях межфазного катализа будет подробно рассмотрен позднее.
Дихлоркарбен присоединяется к алкенам, давая дихлорциклопропаны. Присоедине-ние происходит стереоспецифично - конфигурация исходного алкена сохраняется и в продукте реакции - циклопропане:
 (69)
(69)
транс-2-бутентранс-1,2-диметил-3,3-
дихлорциклопропан
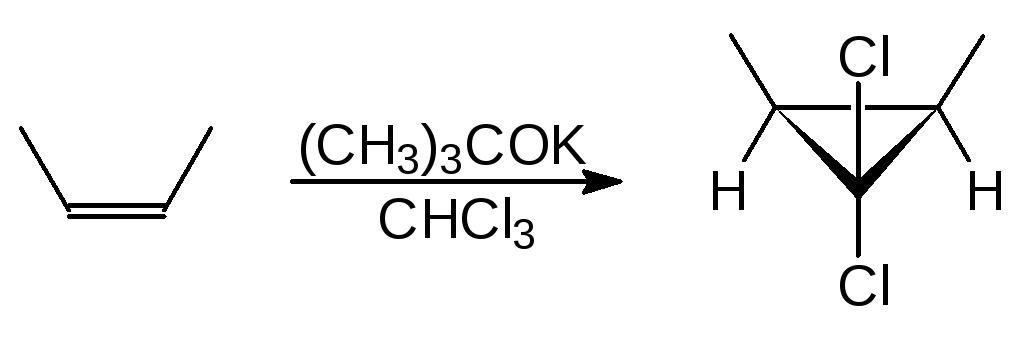 (70)
(70)
цис-2-бутенцис-1,2-диметил-3,3-
дихлорциклопропан
 (71)
(71)
7,7-дихлорбицикло[4.1.0]гептан
При восстановлении 1,1-дигалогенциклопропанов под действием лития в mpem-бутиловом спирте, цинка в уксусной кислоте или натрия в жидком аммиаке оба атома галогена замещаются на водород. Это один из общих методов получения производных циклопропана.
 (72)
(72)
бицикло[4.1.0]гептан
Упр. 11. Завершите реакции:
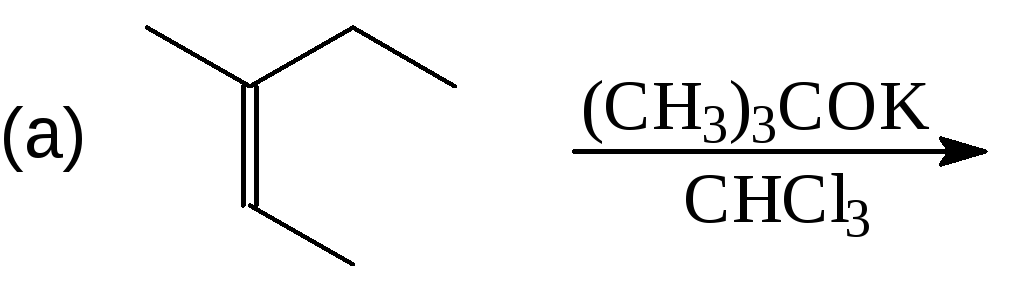

(Z)-3-метил-2-пентен метиленциклогексан
Ответ

Б. Метилен
Метилен может быть получен разложением диазометана. Диазометан представляет собой относительно неустойчивое вещество, разлагающееся при облучении на азот и метилен.
 (73)
(73)
диазометан
Метилен :СН2 при фотолизе диазометана образуется в менее стабильной синглетной форме. Синглетный метилен в условиях реакции в результате столкновений с молекулами диазометана или азота быстро теряет энергию и превращается в более стабильный триплетный метилен.
Для синглетного карбена характерно синхронное присоединение к двойной связи алкена с полным сохранением геометрии при двойной связи (реакция [2+1]-циклоприсоединения). Присоединение синглетной формы карбена по двойной связи происходит, таким образом, строго стереоспецифично.
В. Реакция Симмонса-Смита
Эффективный и экспериментально очень простой способ превращения алкенов в производные циклопропана основан на реакции алкенов с иодистым метиленом и сплавом цинка и меди. Эта реакция была открыта в 1958 г. Симмонсом и Смитом и сразу же завоевала широкую популярность в синтезе производных циклопропана. Активной частицей в этой реакции является не карбен :СН2, а карбеноид - иодид иодметилцинка IZnCH2I, образующийся при взаимодействии иодистого метилена и цинк-медной пары.
![]() (74)
(74)
дииодметан иодометилцинкиодид
(реактив Симмонса-Смита)
 (75)
(75)
Реакция проходит по следующему механизму:

Реакция Симмонса-Смита представляет собой очень удобный метод превращения алкенов в циклопропаны.
Упр. 12. Завершите реакции:


Ответ
 (76)
(76)
метиленциклопентан спиро[2.4]гептан
 (77)
(77)
стирол циклопропилбензол
