
Справочник витаминов
.pdf
41
ХИМИЧЕСКОЕ СТРОЕНИЕ И СВОЙСТВА ВИТАМИНА Е
В20-е годы XX в. Г. Эванс сумел излечить бесплодие у содержащихся на синтетической диете крыс, добавляя им в корм листья салата. Активное соединение, способствующее развитию эмбриона, было выделено также из масел зародышей пшеницы и других семян. Оно получило название токоферол (от греч. tokos — потомство, phero — несу).
В1938 г. токоферол, или витамин Е, был синтезирован химическим путем. Однако между природным и синтетическим витамином Е существуют различия, что отражено в их классификации. Натуральные формы токоферола обозначаются как
RRR-а-токоферолы (R обозначает конфигурацию метильной группы) и имеют единственный сте-реоизомер. Синтетические формы называются all-rac-a-токоферолы и являются рацемической смесью из 8 стереоизомеров, из которых 7 не найдено в природе. Основной биологически активной формой является RRR-a-токоферол:
Свободная ОН-группа обуславливает свойства витамина Е как антиоксиданта.
Кроме токоферолов к группе витамина Е относятся альфа- , бета- , гамма- и 8-токотриенолы — аналоги соответствующих токоферолов, которые отличаются от последних наличием двойных связей в боковой цепи.
Токоферолы — прозрачные, светло-желтые, вязкие масла, хорошо растворимые в большинстве органических растворителей.
Медленно окисляются на воздухе, разрушаются под действием УФ-лучей.
МЕТАБОЛИЗМ ТОКОФЕРОЛА
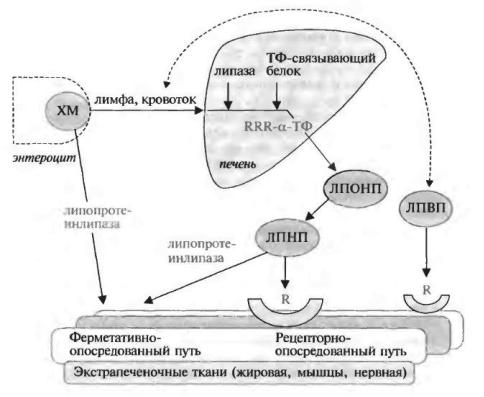
Витамин Е поступает в желудочно-кишечный тракт в составе масел, гидролиз которых липазой и эстеразой приводит к высвобождению витамина. Затем он всасывается и в составе хиломик-ронов поступает в лимфатическую систему и кровяное русло. В печени витамин связывается с токоферолсвязывающими белками, причем наибольшим сродством обладает RRR-a-
токоферол. Другие токоферолы выделяются из печени с желчными кислотами. Эти белки «экспортируют» витамин в кровь в составе ЛПОНП. В плазме крови происходит обмен токоферолом между Л ПОН П и другими липопротеинами крови. Обмен между фракциями липопротеинов (особенно между ЛПНП и ЛПВП) и эритроцитами обеспечивает равновесие концентраций токоферола в крови.
42
Витамин поступает в экстрапеченочные ткани в составе ЛПНП, которые захватываются соответствующими рецепторами.
Кроме такого рецепторно-опосрепованного механизма имеется и другой, зависящий от активности липопротеин-липазы:
фермент высвобождает токоферол из хиломикронов и ЛПОНП, после чего витамин поступает в ткани путем пассивной диффузии. Благодаря пассивной диффузии через клеточную мембрану концентрация RRR-a-токоферола увеличивается во всех тканях организма, особенно в мозге. Структурная организация фосфолипидов в клеточных мембранах способна узнавать хиральную форму RRR-a-токоферола, благодаря чему витамин задерживается в мембране, где и выполняет свою функцию (синтетические токоферолы в составе мембраны обеспечивают меньшую ее защиту от оксидативного стресса).
Не всосавшиеся в кишечнике токоферолы выводятся с калом. Продукты метаболизма витамина — токофери новая кислота и ее водорастворимые глюкурониды — выводятся с мочой.
БИОХИМИЧЕСКИЕ ФУНКЦИИ ТОКОФЕРОЛА
Биохимические функции токоферола многообразны:
|
Витамин Е является универсальным протектором клеточных мембран от окислительного повреждения. Он занимает |
|||||
|
такое |
положение в мембране, |
которое |
препятствует |
контакту кислорода с ненасыщенными липидами |
мембран |
|
(образование гидрофобных комплексов). Это защищает биомембраны от их перекисной деструкции. Антиоксидантные |
|||||
|
свойства токоферола обусловлены также способностью подвижного гидроксила хроманового ядра его молекулы |
|||||
|
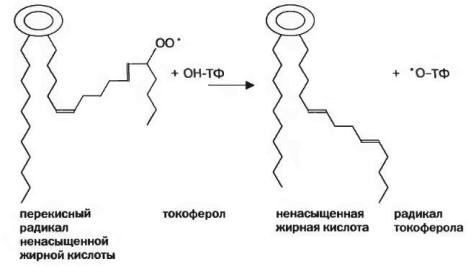
непосредственно взаимодействовать со свободными радиказами кислорода (О2*, НО* НО*), свободными радикалами |
|||||
|
ненасыщенных жирных кислот (RO*, RO2*) и перекисями жирных кислот. Мембраностабилизируюшее действие |
|||||
|
витамина проявляется и в его свойстве предохранять от окисления SH-группы мембранных белков. Его |
|||||
|
антиоксидантное действие заключается также в способности защищать от окисления двойные связи в молекулах |
|||||
|
каротина и витамина А. Витамин Е (совместно с аскорбатом) способствует включению селена в состав активного |
|||||
|
центра |
глутатионпероксидазы, |
тем |
самым он |
активизирует ферментативную антиоксидантную |
защиту |
43
(глутатионпероксидаза |
обезвреживает |
гидропероксиды |
липидов). |
Токоферол является не только антиоксидантом, но и актигипоксантом, что объясняется его способностью стабилизировать митохондриальную мембрану и экономить потребление кислорода клетками. Следует отметить, что из всех клеточных орга-нелл митохондрии наиболее чувствительны к повреждению, так как в них содержится больше всего легко окисляющихся ненасыщенных липидов. Вследствие мембраностабилизируюшего эффекта витамина Е в митохондриях увеличивается сопряженность окислительного фосфорилирования, образование АТФ и креатинфосфата.
Важно также отметить, что витамин контролирует биосинтез убихинона — компонента дыхательной цепи и главного антиоксиданта митохондрий.
Токоферол контролирует синтез нуклеиновых кислот (на уровне транскрипции), а также гема, микросомных иитохромов и других гемсодержаших белков.
Витамин Е обладает способностью угнетать активность фос-фолипазы А2 лизосом, разрушающей фосфолипиды мембран. Повреждение мембран лизосом приводит к выходу в цитозоль протеолитических ферментов, которые и повреждают клетку.
Витамин Е является эффективным иммуномодулятором, способствующим укреплению иммунозащитных сил организма.
ГИПОВИТАМИНОЗ ТОКОФЕРОЛА
Недостаточность токоферола — весьма распространенное явление, особенно у людей, проживающих на загрязненных радионуклидами территориях, а также подвергающихся воздействию химических токсикантов. Глубокий гиповитаминоз встречается редко — преимущественно у недоношенных детей (проявляется гемолитической анемией).
При Е-витаминной недостаточности наблюдается частичный гемолиз эритроцитов, в них снижается активность ферментов антиок-сидантной защиты. Повышение проницаемости мембран всех клеток и субклеточных структур, накопление в них продуктов ПОЛ — главное проявление гиповитаминоза. Именно этим обстоятельством объясняется разнообразие симптомов недостаточности токоферола — от мышечной дистрофии и бесплодия вплоть до некроза печени и размягчения участков мозга, особенно мозжечка. Увеличение активности выходящих из поврежденных тканей ферментов в сыворотке крови (креатинфосфокиназы, аланинаминотрансферазы и других) и увеличение содержания в ней продуктов ПОЛ наблюдается уже на ранних стадиях Е-гиповитаминоза.
44
Дефицит витамина Е в организме сопровождается снижением содержания иммуноглобулинов Е. После его введения нормализуется численность Т- и В-лимфоцитов в периферической крови и восстанавливается функциональная активность Т-
клеток.
ГИПЕРВИТАМИНОЗ ТОКОФЕРОЛА
Витамин нетоксичен при значительных (10—20-кратных к суточной потребности) и длительных превышениях его дозировки, что обусловлено ограничением способности специфических токоферолсвязывающих белков печени включать витамин в состав ЛПОНП. Его избыток выводится из организма с желчью. В некоторых случаях длительный прием мегадоз токоферола (более 1 г в сутки) может привести к гипертриглицеридемии и повышению кровяного давления.
ВРОЖДЁННЫЕ НАРУШЕНИЯ ОБМЕНА ТОКОФЕРОЛА
Акантоцитоз (шиловидные эритроциты). При этой патологии в плазме крови отсутствуют хиломикроны, ЛПНП и ЛПОНП вследствие нарушения в печени больных синтеза одного из структурных белков этих липопротеинов. Так как витамин Е транспортируется в крови в составе хиломикронов и ЛПНП, то отсутствие последних приводит к нарушению всасывания токоферола и поступления его в ткани. Клинически это проявляется в резком снижении гемолитической устойчивости эритроцитов и акантоцитозе, пигментном ретините, мышечной слабости и атаксической нейропатии. Лечение сводится к ограничению потребления жиров и дополнительному введению водорастворимых форм жирорастворимых витаминов
(например, то-коферолполиэтиленгликоль сукцинат).
Врожденная дисэритропоэтическая анемия типа II При этом заболевании увеличивается расход витамина Е на процесс стабилизации и защиты от перекисной деструкции дефектных эритроцитарных мембран.
Врожденные мышечные дистрофии. В некоторых случаях дистрофия мышц обуславливается врожденным нарушением процесса поступления или обмена в них токоферола.
ОЦЕНКА ОБЕСПЕЧЕННОСТИ ОРГАНИЗМА ВИТАМИНОМ Е
Основным методом является определение концентрации витамина Е в крови. Однако при гипер-бета-липопротеинемиях, в
том числе и возрастных, содержание токоферола в крови не отражает уровня обеспеченности им тканей организма (ЛПНП
— одна из транспортных форм витамина).
Наиболее доступны клинической лаборатории функциональные тесты, позволяющие оценить глубину Е-витаминной недостаточности. Основными являются тесты на перскисную или гемолитическую устойчивость эритроцитов, определение суточной экскреции креатина (мышцы при Е-гиповитаминозе плохо «удерживают» креатин) и содержание продуктов ПОЛ в крови и эритроцитах.
СУТОЧНАЯ ПОТРЕБНОСТЬ И ПИЩЕВЫЕ ИСТОЧНИКИ ТОКОФЕРОЛА
Основной источник токоферола — растительные масла, однако только свежие, получаемые методом холодного прессования.
Поскольку растительное масло обычно экстрагируют из семян при высокой температуре, затем подвергают очистке,
дезодорированию и рафинированию, в нем значительно уменьшается содержание токоферола. Более того, избыток растительных масел в рационе усиливает недостаточность витамина Е в организме, так как он расходуется на интенсифицированный потреблением ненасыщенных жирных кислот масел процесс ПОЛ.

45
Лучшим пищевым источником витамина Е являются орехи, семечки, гречневая крупа, проросшие ростки пшеницы. Он содержится в листьях салата и капусты. Из продуктов животного происхождения более всего токоферола в сливочном масле,
сале, мясе, желтке яиц. В молоке этого витамина мало.
Суточная потребность — 10 мг. Однако токоферол быстро расходуется в организме, особенно в условиях стимулированного ПОЛ, что имеет место при многих заболеваниях. Окислительной деструкции витамина Е препятствует витамин С. Это обусловлено присутствием в молекуле последнего фенольной группы — донора водорода, который способен «гасить» свободный радикал токоферола. Тем самым витамин С экономит фонд витамина Е. С целью усиления антиоксидант-ного эффекта токоферола его следует назначать с аскорбиновой кислотой.
Продукты, богатые витамином Е
ВИТАМИН Д (КАЛЬЦИФЕРОЛ), ХИМИЧЕСКОЕ СТРОЕНИЕ И СВОЙСТВА
В 1936 г. А. Виндаусом из рыбьего жира был выделен препарат, излечивающий рахит. Он был назван витамином Д3, так как ранее А. Гессом и М. Вейнштоком из растительных масел был выделен эргостерин, получивший название витамин Д1, При воздействии на витамин Д1 УФ-лучей образовывалось излечивающее рахит соединение — витамин Д2, эргокалциферол
(кальциферол означает несущий кальций). В растениях при УФ-облучении синтезируются и другие витамеры эргостерина
(Д4-7).
Наиболее важным из группы витаминов Д является витамин Д3 — холекальциферол. Холекальциферол образуется в качестве промежуточного продукта при биосинтезе холестсрола (из 7-дегидрохолестерола) в клетках кожи человека под влиянием УФ-лучей.
МЕТАБОЛИЗМ ВИТАМИНА Д
Витамины группы Д всасываются подобно витамину А. В печени витамины подвергаются гидроксилированию микросомной системой оксигеназ по С-25 (из витамина Д3 образуется 25 (ОН) -Д3 т. е. 25-гидроксихолекальциферол), и затем переносятся током крови с помощью специфического транспортного белка в почки. В почках осуществляется вторая реакция гидроксилирования по С-1 с помощью митохондриальных оксигеназ (образуется 1,25 (ОН) 2-Д3, т. е. 1,25-
дигидроксихолекальциферол, или кальцитриол). Эта реакция активируется паратиреоидным гормоном, секретируемым паращито-видной железой, когда уровень кальция в крови снижается. Если уровень кальция адекватен физиологической потребности организма, вторичное гидроксилирование происходит по С-24 (вместо С-1), при этом образуется неактивный метаболит 1,24 (ОН) 2-Д3. В реакциях гидроксилирования принимает участие витамин С.

46
Витамин Д3 накапливается в жировой ткани. Выводится главным образом с калом в неизмененном или окисленном виде, а
также в виде конъюгатов.
БИОХИМИЧЕСКИЕ ФУНКЦИИ КАЛЬЦИФЕРОЛА
Витамин Д3 можно рассматривать как про-гормон, так как он превращается в 1,25 (ОН) 2-Д3 действующий аналогично стероидным гормонам. Так, проникая в клетки-мишени, он связывается с белковыми рецепторами, которые мигрируют в ядро клетки. В энтероцитах этот гормон-рецепторный комплекс стимулирует транскрипцию иРНК, несущую информацию на синтез белка-переносчика ионов кальция. Вероятно, витамин отвечает также за синтез Са2±АТФ-азы в разных клетках.
Вкишечнике всасывание кальция осуществляется как путем облегченной диффузии (с участием кальцийсвязывающего белка), так и путем активного транспорта (с помощью Са2±АТФ-азы). Одновременно ускоряется и всасывание фосфора.
Вкостной ткани 1,25 (ОН) 2-Д3 стимулирует процесс деминерализации (синергично с паратирином).
Впочках активация витамином 1,25 (ОН) 2-Д3 кальциевой АТФ-азы мембран почечных канальцев приводи к увеличениию реабсорбции ионов кальция; возрастает и реабсорбция фосфатов.
Кальцитриол принимает участие в регуляции роста и дифференцировке клеток костного мозга. Он обладает антиоксидантным и антиканцерогенным действием.
ГИПОВИТАМИНОЗ ВИТАМИНА Д
Недостаток витамина Д у детей приводит к заболеванию рахитом. Основные проявления этого заболевания сводятся к симптоматике недостаточности кальция. Прежде всего страдает остеогенез: отмечается деформация скелета конечностей
(искривление их в результате размягчения — остеомаляции), черепа (позднее заращение родничков), грудной клетки
(появление своеобразных «четок» на костно-хрящевой границе ребер), задерживается прорезывание зубов. Развивается гипотония мышц (увеличенный живот), возрастает нервно-мышечная возбудимость (у младенца выявляется симптом облысения затылочка из-за частого вращения головкой), возможно появление судорог. У взрослого недостаточность кальция в организме приводит к кариесу и остеомаляции; у пожилых — к развитию остеопороза (снижение плотности костной ткани вследствие нарушения остеосинтеза). Разрушение неорганического матрикса объясняется усиленным «вымыванием» кальция из костной ткани и нарушением реабсорбции кальция в почечных канальцах при дефиците витамина Д.
На схеме ниже показано угнетение (пунктирная стрелка) всасывания, снижение поступления кальция в кость и уменьшение экскреции кальция при недостатке витамина Д. Одновременно в ответ на гипокальциемию секретируется паратирин и увеличивается (сплошная стрелка) поступление кальция из кости в кровяное русло (вторичный гиперпаратиреоидизм).

47
ВРОЖДЕННЫЕ НАРУШЕНИЯ ОБМЕНА КАЛЬЦИФЕРОЛА
Семейный гипофосфатемический витамин-Д-резистентный рахит.
Клиническое течение этой формы рахита весьма вариабельно: от некоторой задержки роста ребенка до развития симптомов тяжелого рахита. Изменения скелета обычно проявляются на 1—2-м году жизни, типична утиная походка, однако мышечная гипотония отсутствует. Задержка роста и утолщение костей при этом заболевании приводят к формированию приземистого,
псевдоатлетического телосложения.
Основным биохимическим симптомом является гипофосфатемия в результате снижения реабсорбции неорганического фосфата в почечных канальцах. Фосфор теряется с мочой. Нарушается также всасывание фосфора (нередко и кальция) в
тонком кишечнике. Избирательный дефект реабсорбции фосфата в почечных канальцах связан не с нарушением образования гормонально активной формы витамина Д, а с генетически обусловленным повреждением структуры белков, участвующих в этом процессе.
Лечение: назначение высоких доз витамина Д и фосфатов.
Врожденный псевдодефинитный витамин-Д-зависимый рахит.
Клиническая картина подобна проявлениям «классического» рахита. В крови снижено содержание кальция, иногда — фосфора, резко повышена активность щелочной фосфатазы в крови (повышение активности этого фермента является диагностическим показателем). Характерны гипераминоацидурия и вторичный гиперпаратиреоидизм.
Главным метаболическим дефектом является нарушение образования в почках 1,25-дигидроксихолекальциферола
(кальцитриола), вследствие чего нарушается всасывание кальция в тонком кишечнике. Развивающаяся гипокальциемия ведет к вторичному гиперпаратиреоидизму.
Лечение: парентеральное введение 1,25 (ОН) 2-Д3, либо постоянное назначение высоких (1000-кратно превышающих физиологические) доз холекальциферола.
ГИПЕРВИТАМИНОЗ ВИТАМИНА Д
Избыточный прием витамина Д приводит к интоксикации и сопровождается выраженной деминерализацией костей — вплоть до их переломов. Содержание кальция в крови повышается. Это приводит к кальцификации мягких тканей, особенно склонны к этому процессу почки (образуются камни и развивается почечная недостаточность).
48
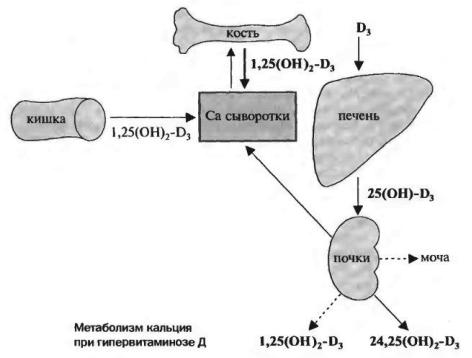
Повышение уровня кальция (и фосфора) в крови объясняется следующим образом:
1.резорбцией костной ткани (сплошная стрелка);
2.увеличением интенсивности всасывания кальция и фосфора в кишечнике и
3.увеличением их реабсорбции в почках (т. е. угнетением экскреции с мочой — пунктир).
Внормальных условиях повышение содержания кальция в крови будет приводить к образованию неактивного 24,25 (ОН) 2-
Д3, который не вызывает резорбцию («рассасывание») кости, однако при гипер-витаминозс Д этот механизм становится неэффективным.
Интересно, что пигментация кожи (загар) является защитным фактором, предохраняющим от избыточного образования витамина Д при УФ-облучении кожи. Однако у светлокожих жителей северных стран, испытывающих недостаток солнечной инсоляции, витамин-Д-дефицитные состояния, как правило, не развиваются, так как их диета включает рыбий жир.
СУТОЧНАЯ ПОТРЕБНОСТЬ В ВИТАМИНЕ Д И ЕГО ИСТОЧНИКИ
Оценка обеспеченности организма витамином Д
Обеспеченность организма витамином Д оценивается на основании определения активных форм витамина Д в крови и тканях методом радиоконкурентного анализа; содержания кальция, фосфора и активности щелочной фос-фатазы в сыворотке крови; уровня экскреции с мочой фосфатов. Применяются также нагрузочные пробы с приемом фиксированных доз кальция при парентеральном введении с последующим определением содержания кальция в крови и его экскреции с мочой.
Потребность и источники
Витамин Д3 содержится исключительно в животной пище. Особенно богат им рыбий жир. Содержится он в печени, желтке яиц. В растительных маслах и молоке присутствует витамин Д2. Много его в дрожжах. Биологически он менее активен.

49
Суточная потребность для детей колеблется от 10 до 25 мкг (500— 1000 ME), у взрослых она меньше.
Продукты богатые витамином Д
ВИТАМИН К (АНТИГЕМОРРАГИЧЕСКИЙ ВИТАМИН), ХИМИЧЕСКОЕ СТРОЕНИЕ И СВОЙСТВА
За открытие витамина К Э. Дойзи и X. Дам в 1943 г. получили Нобелевскую премию.
Витамин К — это две группы хинонов с боковыми изопреноильными цепями: витамин К, (филлохиноны) и витамин К2 (менахиноны). Филлохиноны открыты в растениях, а менахиноны имеются также и у животных. Они различаются строением и количеством изопреновых единиц в боковой цепи.
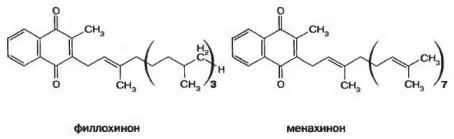 Оба витамина не растворяются в воде, но хорошо растворимы в органических растворителях; они разрушаются при нагревании в щелочной среде и на свету.
Оба витамина не растворяются в воде, но хорошо растворимы в органических растворителях; они разрушаются при нагревании в щелочной среде и на свету.
Синтезированы аналоги витамина К — менадион (витамин К3, лишенный боковой цепи) и его водорастворимый аналог викасол, последний широко применяется в медицинской практике.
МЕТАБОЛИЗМ И БИОХИМИЧЕСКИЕ ФУНКЦИИ ВИТАМИНА K
Метаболизм витамина К
Витамин К всасывается аналогично всем жирорастворимым витаминам, т. е. включается вначале в состав мицелл, а затем — хиломикронов. В плазме крови он связывается с альбуминами. Накапливается в печени, селезенке и сердце. В тканях образуется активная форма витамина — менахинон-4 (содержит четыре изопреноидные единицы). Конечные продукты обмена витамина выделяются с мочой.
Биохимические функции витамина К
Единственная известная биологическая роль витамина К заключается в том, что он является коферментом у-глута-
маткарбоксилазы, карбоксилирующей глутаминовую кислоту с образованием у-карбоксиглутаминовой кислоты. Фермент удалось очистить до гомогенного состояния (белковая цепь содержит 758 аминокислот с преобладанием гидрофобных) и
определить его структурный ген (он включает 15 экзонов).

50
При взаимодействии восстановленной формы витамина К-Н2 с у-глутаматкарбоксилазой в присутствии кислорода образуется сильное основание (алкоксид), способное отнять от у-С атома глутамино-вой кислоты водород, на место которого присоединяется СО2, при этом образуется у-карбоксиглутаминовая кислота. В холе реакции появляются коротко живущие и высоко токсичные промежуточные соединения (свободные радикалы витамина К), которые превращаются в нетоксичный эпоксид витамина К в присутствии тута мата. Эпоксил витамина К снова восстанавливается в витамин К-Н2 с помощью ферментов редуктаз. Следовательно, при дефиците глутаминовой кислоты в клетке затрудняется обезвреживание токсичных свободных радикалов витамина К.
у-карбоксиглутаминовая кислота является Са+*-связывающей аминокислотой, которая необходима для функционирования кальцийсвя-швающих белков. К таковым относятся:
факторы свертывающей системы крови — IX, VII, X и протромбин;
регуляторные белки (протеин С и протеин S), нуждающиеся в у-карбоксиглутаминовой кислоте для Са-
индуцированного взаимодействия с поверхностью клеточной мембраны;
белки минерализации костной ткани (костный у-карбоксиглута-миновый протеин и другие); поскольку при дефекте синтеза костного у-карбоксиглутаминового белка кальцифицируются артерии и хряши; возможно, что его функцией является также контроль за внекостной кальцификацией;
витамин-К-зависимый белок Gas 6, активирующий рост глад-комышечных клеток; витамин-К-зависимый сократительный белок хвостика сперматозоида;
некоторые нейротоксины (например, содержащиеся в яде улитки).
Общей особенностью всех витамин-К-зависимых белков является формирование белковой сеточки, образованной гамма-
карбоксилутаминовой кислотой, связанной с кальцием. Такая сеть впервые была описана для протромбина. Протромбин в присутствии Са++ связывается с биомембраной, что является необходимым условием для реализации процесса свертывания крови.
Витамин-К-зависимые белки синтезируются в эндоплазматическом ретикулуме в виде белков-предшественников,
содержащих сигнальный участок и «участок узнавания» для гамма-карбоксилирования. После отщепления сигнального пептида белок с помощью «участка узнавания» связывается с витамин-К-зависимой карбоксилазой, локализирующейся в мембранах эндоплазматического ретикулума. В результате этого связывания у-карбоксиглутаматкарбоксилаза переходит из неактивного состояния в активное и начинает осуществлять каталитическое превращение остатка глутаминовой кислоты в у-
карбоксиглутаминовую кислоту в витамин-К-зависимом пробелке.
