
- •Основные стадии гетерогенного каталитической процесса
- •Состав и пористая структура твёрдых катализаторов
- •Пористая структура твёрдых катализаторов
- •Теплопроводность катализатора
- •Механическая прочность катализатора
- •Продолжительность работы катализатора
- •Взаимодействие катализатора и реакционной среды
- •Истинное отравление катализатора
- •Термическое воздействие на катализатор
- •Технология производства катализатора
- •Формовка катализаторов и носителей
- •Порошкообразные массы
- •Таблетирование
- •Основные способы производства катализатора Осажденные катализаторы
- •Растворение
- •Осаждение
- •Фильтрование
- •Промывка осадка
- •Сушка осадка
- •Прокаливание
- •Формование
- •Катализаторы получаемые методом пропитки
- •Метод окунания
- •Пропитка расплавом
- •Катализаторы, получаемые механическим смешением компонентов (смешанные катализаторы)
- •Измельчение
- •Формовка
- •Термическая обработка
- •Плавление и скелетные контактные массы
Лекция №1 (20 фев. 2023)
Катализ - физическое явление изменения скорости химической реакции под влиянием веществ, нагреваемых катализатором.
С помощью каталитических реакций получают около 30% всей промышленной продукции и более 70% всей химической продукции.
Различают положительный и отрицательный катализ. В 1-ом случае катализатор ускоряет реакцию, во 2-ом - скорость реакции уменьшается и процесс наз. ингибированием, а вещество, применяемое для ингибирования, - ингибитор.
Различают по наличию различных реагирующих фаз: гомогенный (все вещества в одной фазе) и гетерогенный (в качестве катализатора обычно выступает твердое вещество, другая фаза - жидкая или газообразная).
Сущность каталитического действия:
Катализатор вступает в реакцию с исходными веществами и направляет хим. реакцию по другому реакционному пути (механизму).

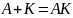

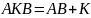
 , где
, где
 – уравнение
Аррениуса;
– уравнение
Аррениуса;
 – константа скорости (увеличивается
при снижении
– константа скорости (увеличивается
при снижении
 );
– энергия активации хим. реакции,
кДж/моль;
);
– энергия активации хим. реакции,
кДж/моль;
 – предэкспоненциальный множитель
(отражает количество соударений между
частицами);
– предэкспоненциальный множитель
(отражает количество соударений между
частицами);
 – температура, К;
– температура, К;

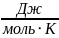 .
.
КАТАЛИЗАТОР ПОНИЖАЕТ ЭНЕРГИЮ АКТИВАЦИИ.
Л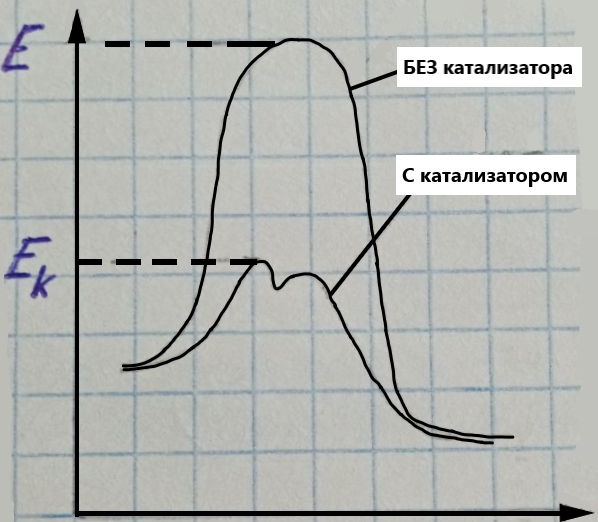 екция
№2 (1
мар. 2023)
екция
№2 (1
мар. 2023)
Скорость реакции выражает количество вещества, вступившего в реакцию в единицу времени. Количество вещества выражается в молях.
1 моль
— количество вещества, содержащее число
Авогадро ( )
структурных формульных единиц — реальных
частиц, таких как атомы, молекулы, ионы.
)
структурных формульных единиц — реальных
частиц, таких как атомы, молекулы, ионы.
Скорость
гетерогенной реакции:
 ,
где
,
где
 – поверхность
контакта
(площадь, на кот. происходит вся
гетерогенная реакция). В случае
каталитической реакции эта поверхность
постоянна.
– поверхность
контакта
(площадь, на кот. происходит вся
гетерогенная реакция). В случае
каталитической реакции эта поверхность
постоянна.
Чем больше поверхность, тем выше скорость реакции.
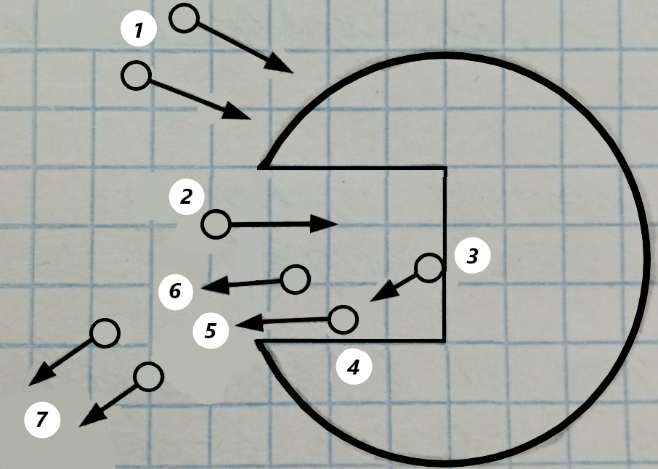
Основные стадии гетерогенного каталитической процесса
Гетерогенно-каталитический процесс включает в себя ряд физических и химических стадий:
1) Диффузия частиц реагирующих веществ к внешней поверхности зёрен (гранул) катализатора (внешняя диффузия);
2) Диффузия частиц реагирующих веществ внутри пор к внутренней поверхности катализатора;
3) Активированная (химическая) адсорбция одного или нескольких реагентов на внутренней поверхности катализатора;
4) Перегруппировка атомов с образованием поверхностных соединений (комплекса) продукт-катализатор (химическая реакция с образованием продукта реакции, адсорбированного на поверхности);
5) Десорбция частиц продукта реакции с внутренней поверхности катализатора;
6) Диффузия частиц продукта реакции внутри пор катализатора и внешней поверхности частиц;
7) Диффузия частиц продукта реакции от внешних поверхностей катализатора в ядро потока.
Каждая из стадий протекает со своей скоростью, не равной скорости других стадий. Общая скорость всего процесса определяется (равна) скорости наиболее медленной стадии процесса. Сама эта стадия наз. лимитирующей.
Области протекания гетерогенно-каталитического процесса:
1) Внешнедиффузионная обл. – 1 или 7 стадия явл. наиболее медленными.
2) Внутридиффузионная обл. – лимитирующие стадии 2 и 6.
3) Кинетическая обл. – лимитирующая стадия 3, 4 или 5.
В кинетической обл. процессы протекают в основном на малоактивных катализаторах мелкого зернения с крупными порами. Во внешнедиффузионной обл. протекают процессы на высокоактивных катализаторах, обеспечивающих быструю реакцию и достаточный выход продукта за короткое время.
Во внутридиффузионной обл. скорость процесса можно регулировать величиной среднего размера пор, увеличение кот. приводит в первом приближении к росту скорости процесса.
Кроме основных областей протекания иногда используют переходные области. Протекание процесса в переходной обл. соответствует оптимальной скорости. В этой области протекают многие промышленные гетерогенные процессы.
Состав и пористая структура твёрдых катализаторов
Промышленные катализаторы в большинстве своём не явл. индивидуальными чистыми в-вами, а представл. собой смеси нескольких компонентов.
1) Активный компонент – вещество, ускоряющее реакцию. Его содержание составляет от 1 до 30% по массе.
2) Носитель.
1] Создаёт развитию поверхность (и внешнюю, и внутреннюю);
2] Повышает механическую прочность катализатора;
3] Снижает стоимость катализатора (путем его разбавления) (напр. SiO2, Al2O3, природные материалы и т.д.).
3) Промотор – вещество, способствующее интенсификации активного компонента (увеличивает активность катализатора).
По своему действию делятся на:
1] структурные;
2] химические (энергетические).
Л екция
№3 (6
мар. 2023)
екция
№3 (6
мар. 2023)
В общем случае процедура введения в состав катализатора промотора и использование его в каталитической реакции наз. промотированием.
Структурный промотор обеспечивает стабильное структурное состояние катализатора, при котором увеличивается количество активных центров, участвующих в каталитической реакции.
При структурном промотировании скорость единичного взаимодействия на одном активном центре не изменяется, а общая скорость реакции увеличивается за счёт увеличения количества активных центров.
При химическом промотировании концентрация активных центров практически не изменяется, но скорость каждого единичного взаимодействия возрастает.
Имеют место случаи комбинированного промотирования – и структурные, и химические.
