
- •5) Почему давление насыщенного пара зависит от формы поверхности жидкости?
- •6) Почему в случае смачивания капилляров жидкость в нем поднимается, а при не смачивании, наоборот, опускается?
- •7) Какие параметры используют для количественной характеристики адгезии и смачивания?
- •13) Что понимается под адсорбцией, абсорбцией, адсорбентом, адсорбатом, адсорбтивом?
- •14) В чём принципиальное отличие адсорбции на твёрдых поверхностях от адсорбции на поверхности жидкости?
- •15) Какие величины используют для количественного описания адсорбции? Дайте определение этих величин и покажите как их можно вычислить в общем виде?
- •16) Как можно рассчитать гиббсовскую адсорбцию по изотерме поверхностного натяжения.
- •17) Как можно определить параметры молекул пав ( и ).
- •18) У какой горячей или холодной воды на границе с воздухом больше поверхностное натяжение, и почему?
- •19) Какая жидкость лучше смачивает гидрофобную поверхность вода или бензол? Ответ аргументировать.
- •20) Почему процесс диспергирования твердых веществ легче происходит в присутствии пав?
- •21) Какие самопроизвольные процессы, протекающие в поверхностном слое, обусловлены уменьшением площади поверхности раздела фаз? Перечислите их и дайте характеристику.
- •22) Охарактеризуйте самопроизвольные процессы, протекающие в поверхностном слое, которые приводят к уменьшению поверхностного натяжения на границе раздела фаз?
- •2 9) Изобразите основные типы изотерм полимолекулярной адсорбции и опишите взаимодействие адсорбент-адсорбат для разных типов изотерм бэт.
- •30) Что понимается под поверхностной активностью? Как ее можно определить?
- •31) Каким процессом является адсорбция, экзотермическим или эндотермическим? Как на ее величину будет влиять повышение температуры и почему?
- •32) Назовите основные виды зависимости адсорбционного равновесия. Что понимается под состоянием адсорбционного равновесия?
- •3 4) Как осуществляется расчёт удельной поверхности адсорбента методом бэт?
- •35) В чем принципиальное отличие адсорбции из растворов электролитов от молекулярной адсорбции?
- •36) Как влияет собственный радиус иона на его способность к адсорбции?
- •37) Какие адсорбенты называют ионитами?
- •38) Дайте определение и назовите объекты исследования коллоидной химии.
- •39) Охарактеризуйте значение коллоидной химии для развития промышленности и охраны окружающей среды.
- •40) Основные признаки дисперсных систем – гетерофазность и дисперсность, какой из них является более универсальным? Почему?
- •41) Какие количественные характеристики дисперсности Вы знаете? Дайте их характеристику.
- •42) Перечислите основные признаки, положенные в основу классификации дисперсных систем.
- •43) Как будут ориентированы молекулы пав на границах раздела фаз: масло – вода и вода – воздух?
- •44) Почему в эмпирическом уравнении Шишковского константа «в» одинакова для всех соединений одного гомологического ряда?
- •45) Если из водного раствора нужно адсорбировать органические вещества, то какой следует выбрать адсорбент полярный или неполярный?
- •46) Для получения абсолютного спирта, то есть извлечения из спирта примесей воды какой следует выбрать адсорбент (полярный или неполярный)?
- •47) Изобразите каплю воды на гидрофобной поверхности и укажите краевой угол смачивания?
- •48) Каким определением поверхностного натяжения пользуются при выводе уравнения Лапласа?
- •49) Приведите вывод уравнения Лапласа и дайте его анализ.
- •50) В чем выражаются особенности адсорбции пав на твердой поверхности?
- •51) Какая поверхность будет лучше смачиваться водой: стекла или фторопласта?
- •52) Изобразите рисунки, которые необходимы для вывода уравнений для расчета работы когезии и адгезии. Каким определением поверхностного натяжения при этом нужно пользоваться?
- •53) Чем обусловлено броуновское движение частиц дисперсной фазы в жидкой или газообразной среде?
- •54) От каких факторов зависит интенсивность движения частиц дисперсной фазы в дисперсионной среде?
- •56) Что понимается под диффузией и от каких факторов зависит скорость диффузии? Каков физический смысл коэффициента диффузии?
- •58) Как можно увеличить скорость седиментации коллоидных частиц?
- •59) Что понимается под седиментационно-диффузионным равновесием? Каков физический смысл гипсометрической высоты (h)?
- •60) Какой заряд (положительный или отрицательный) в соответствии с правилом Кена приобретает поверхность волокон смоченной водой фильтровальной бумаги?
- •61) Составьте задачу, для решения которой нужно использовать правило Панета-Фаянса.
- •67) Почему электрофорез и электроосмос называют электрокинетическими явлениями 1-го рода, а потенциал протекания и потенциал седиментации явление 2-го рода?
- •68) Почему лиофильные системы обладают агрегативной устойчивостью и как можно разрушить лиофильную систему?
- •69) Почему лиофобные дисперсные системы являются термодинамически неустойчивыми? Перечислите факторы, которые обеспечивают агрегативную устойчивость лиофобных систем.
- •72) Какие закономерности наблюдаются при коагуляции золей смесью электролитов?
- •73) Какова природа сил притяжения в соответствии с теорией длфо? Изобразите график, иллюстрирующий зависимость этих сил от расстояния между частицами.
- •79) Как влияют на величину электрокинетического потенциала индифферентные электролиты? Какое состояние системы называется изоэлектрическим?
- •80) Что представляет собой релаксационный эффект, электрофоретическое торможение и поверхностная проводимость? Когда их нужно учитывать при расчете величины электрокинетического потенциала?
- •81) Что понимается под устойчивостью дисперсной системы? Назовите виды устойчивости и дайте их характеристику.
- •82) Что такое расклинивающее давление и каковы причины его возникновения? Назовите составляющие расклинивающего давления.
- •83) Что такое осмос? Каковы особенности осмотического давления в коллоидных растворах?
- •84) Чем обусловлено светорассеяние в дисперсных системах и истинных растворах? Какими параметрами количественно характеризуют рассеяние света в системе?
- •85) Что называется оптической плотностью и что она характеризует?
- •86) Каковы особенности рассеяния света для малых и больших частиц дисперсной фазы?
- •87) Что выражают диаграммы Ми?
- •88) Какую зависимость выражает закону Бугера-Ламберта-Бера?
- •89) Особенности адсорбции поверхностно-активных веществ и в чем заключается различие между гиббсовскими и ленгмюровскими адсорбционными слоями.
- •90) К каким системам молекулярно-дисперсным, гомогенным, коллоидно-дисперсным или лиофильным применимы понятия фаза и гетерогенность?
- •91) Как называются дисперсные системы при наличии или отсутствии в них взаимодействия между частицами дисперсной фазы?
- •92) Что представляет собой работа, затрачиваемая на обратимый разрыв тела и отнесенная к единице площади сечения?
- •94) В чем заключается инверсия смачивания и какое практическое значение она имеет?
- •95) Что такое обменная адсорбция? в чем заключается ее практическое значение? Объясните на примерах действие катионитов и анионитов.
- •96) Где находится практическое применение коллоидные поверхностно-активные вещества? в чем заключается механизм их моющего действия?
- •97) Чем отличаются коллоидные пав от истинно растворимых? Что называется критической концентрацией мицеллообразования ккм?
- •98) Какие существуют методы определения ккм? в чем заключается суть этих методов? Что общего между ними?
- •99) Что понимают под явлением солюбилизации? Чем оно обусловлено и каково практическое значение этого явления?
- •100) Можно ли очистить раствор коллоидного пав от ионов электролита с помощью диализа?
2 9) Изобразите основные типы изотерм полимолекулярной адсорбции и опишите взаимодействие адсорбент-адсорбат для разных типов изотерм бэт.
 рисунки+
типа I
взаимодействие адсорбент – адсорбат
сильнее взаимодействия адсорбат
–адсорбат, а в случае изотерм типа II
взаимодействие адсорбат –адсорбат
сильнее взаимодействия адсорбент –
адсорбат.. Изотермы типа III и IV для них
характерна конечная адсорбция при
приближении давления пара к давлению
насыщенного пара
рисунки+
типа I
взаимодействие адсорбент – адсорбат
сильнее взаимодействия адсорбат
–адсорбат, а в случае изотерм типа II
взаимодействие адсорбат –адсорбат
сильнее взаимодействия адсорбент –
адсорбат.. Изотермы типа III и IV для них
характерна конечная адсорбция при
приближении давления пара к давлению
насыщенного пара
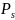 .
Изотермы типа I и II характерны для
адсорбции на не пористом адсорбенте, а
типа III и IV – на пористом твердом теле.
Изотерма типа III (ступенчатая) отражает
послойное заполнение поверхности
молекулами адсорбата.
.
Изотермы типа I и II характерны для
адсорбции на не пористом адсорбенте, а
типа III и IV – на пористом твердом теле.
Изотерма типа III (ступенчатая) отражает
послойное заполнение поверхности
молекулами адсорбата.
30) Что понимается под поверхностной активностью? Как ее можно определить?
Поверхностная
активность характеризует природу
растворённого в-ва и определяет знак
гиббсовской адсорбции,чем сильнее
уменьшается поверхностное натяжение
с ростом концетрации, тем выше поерхностная
активность в-ва. Это сила, удерживающая
в-ва на поверхности, рассчитанная на
единицу гиббсовской адсорбции.( )
)
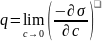 .
.
31) Каким процессом является адсорбция, экзотермическим или эндотермическим? Как на ее величину будет влиять повышение температуры и почему?
Процесс адсорбции протекает самопроизвольно, поэтому он сопровождается убылью энергии Гиббса (∆G < 0). Энтропия системы при адсорбции также уменьшается (∆S < 0), так как беспорядочно двигающиеся молекулы закрепляются в поверхностном слое. Адсорбция – это процесс экзотермический (∆Н < 0). Выделяющееся при адсорбции тепло, называется теплотой адсорбции. Процесс адсорбции всегда протекает до состояния адсорбционного равновесия, при котором скорость процесса адсорбции (Vад.) становится равной скорости процесса десорбции (Vдес.). повышение температуры будет уменьшать величину адсорбции
32) Назовите основные виды зависимости адсорбционного равновесия. Что понимается под состоянием адсорбционного равновесия?
Адсорбционное равновесие – скорость адсорбции равна скорости десорбции. В этом состоянии количество адсорбированных молекул остается постоянным сколь угодно долго, если неизменны внешние условия.
Основными видами зависимости адсорбции являются:
- Изотерма - выражает зависимость количества адсорбированного вещества от равновесного давления (или концентрации) при постоянстве температуры А = ƒ(Р)Т или А = ƒ(С)Т.
- Изобара - выражает зависимость количества адсорбированного вещества от температуры при постоянстве давления А = ƒ(Т)Р.
- Изопикна - выражает зависимость количества адсорбированного вещества от температуры при постоянном значении концентрации А = ƒ(Т)С.
- Изостера - выражает зависимость равновесного давления (или концентрации) от температуры при постоянстве количества адсорбированного вещества Р = ƒ(Т)А или С = ƒ(Т)А.
33) Каковы основные положения теории полимолекулярной адсорбции БЭТ? Приведите уравнения изотермы БЭТ, дайте его анализ и в чем заключаются ограничения этой теории?
Б рунауэр,
Эммет, Теллер Адсорбция многослойна,
на поверхности адсорбента имеется
определенное число активных центров,
адсорбция обусловлена физическими
силами, действующими между адсорбентом
и адсорбатом, каждая молекула первого
слоя представляет собой активный центр
для дальнейшей адсорбции, что приводит
к образованию второго, третьего и т.д.
При этом построение последующих слоев
возможно при незаполненном первом слое,
Первый слой адсорбата образуется в
результате действия сил Ван-дерВаальса
между адсорбентом и адсорбатом, а
последующие в результате конденсации
пара, Взаимодействие соседних
адсорбированных молекул в первом и
последующих слоях отсутствует. уравнение
изотермы полимолекулярной адсорбции
паров – уравнение БЭТ
рунауэр,
Эммет, Теллер Адсорбция многослойна,
на поверхности адсорбента имеется
определенное число активных центров,
адсорбция обусловлена физическими
силами, действующими между адсорбентом
и адсорбатом, каждая молекула первого
слоя представляет собой активный центр
для дальнейшей адсорбции, что приводит
к образованию второго, третьего и т.д.
При этом построение последующих слоев
возможно при незаполненном первом слое,
Первый слой адсорбата образуется в
результате действия сил Ван-дерВаальса
между адсорбентом и адсорбатом, а
последующие в результате конденсации
пара, Взаимодействие соседних
адсорбированных молекул в первом и
последующих слоях отсутствует. уравнение
изотермы полимолекулярной адсорбции
паров – уравнение БЭТ
 .
где А – количество
адсорбированного пара при равновесном
давлении (Р) в окружающей среде; Рs –
давление насыщенных паров;
– количество пара, адсорбированного в
виде насыщенного монослоя; С – постоянная,
характеризующая энергию взаимодействия
в адсорбционном слое. Основные типы
изотерм при полимолекулярной адсорбции
.
где А – количество
адсорбированного пара при равновесном
давлении (Р) в окружающей среде; Рs –
давление насыщенных паров;
– количество пара, адсорбированного в
виде насыщенного монослоя; С – постоянная,
характеризующая энергию взаимодействия
в адсорбционном слое. Основные типы
изотерм при полимолекулярной адсорбции и
уравнение БЭТ переходит в уравнение
Ленгмюра
и
уравнение БЭТ переходит в уравнение
Ленгмюра
 При Р → 0
уравнение БЭТ переходит в изотерму
Генри
При Р → 0
уравнение БЭТ переходит в изотерму
Генри
 .
Ограничения
теории БЭТ
Теория не учитывает энергетической
неоднородности поверхности, Относительное
давление должно быть 0,05 <
.
Ограничения
теории БЭТ
Теория не учитывает энергетической
неоднородности поверхности, Относительное
давление должно быть 0,05 <
 <
0,3, Теорию используют только для описания
адсорбции паров; она неприменима к
адсорбции газов, Теория предполагает
постоянство общей площади для каждого
слоя, однако на самом деле площадь
уменьшается по мере увеличения числа
слоев, Теория предполагает постоянство
площади, приходящейся на одну молекулу
в поверхностном слое, и не учитывает
возможных изменений агрегатного
состояния поверхностного слоя.
<
0,3, Теорию используют только для описания
адсорбции паров; она неприменима к
адсорбции газов, Теория предполагает
постоянство общей площади для каждого
слоя, однако на самом деле площадь
уменьшается по мере увеличения числа
слоев, Теория предполагает постоянство
площади, приходящейся на одну молекулу
в поверхностном слое, и не учитывает
возможных изменений агрегатного
состояния поверхностного слоя.
