
3 курс / Фармакология / Диссертация_Ромодановский_Д_П_Разработка_требований_для_оценки_фармакокинетики
.pdf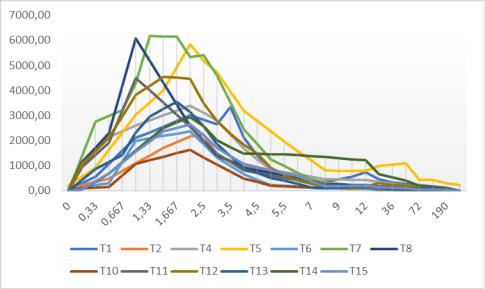
Таблица 217.
Усредненные фармакокинетические параметры УДХК.
№ |
Cmax T, нг/мл |
Cmax R, нг/мл |
AUC0-t T, нг*ч/мл |
AUC0-t R, нг*ч/мл |
tmax T, ч |
tmax R, ч |
|
|
|
|
|
|
|
1 |
4771,56 |
4778,64 |
21507,24 |
21256,77 |
2,60 |
2,50 |
|
|
|
|
|
|
|
2 |
2388,33 |
2512,22 |
8311,94 |
8677,78 |
2,28 |
2,25 |
|
|
|
|
|
|
|
3 |
7,99* |
10,01* |
20,67* |
25,44* |
1,25 |
1,14 |
|
|
|
|
|
|
|
4 |
3657,00 |
3632,08 |
26106,82 |
24404,01 |
2,21 |
1,88 |
|
|
|
|
|
|
|
5 |
6631,04 |
6299,75 |
139279,96 |
125343,44 |
2,23 |
2,17 |
|
|
|
|
|
|
|
6 |
2617,78 |
2628,89 |
7333,19 |
7714,86 |
1,94 |
2,11 |
|
|
|
|
|
|
|
7 |
8021,42 |
8975,42 |
21830,07 |
25414,55 |
1,58 |
1,71 |
|
|
|
|
|
|
|
8 |
6259,62 |
5805,55 |
20544,50 |
21071,04 |
1,08 |
1,21 |
|
|
|
|
|
|
|
9 |
20,57* |
23,47* |
82,35* |
81,11* |
2,26 |
2,59 |
|
|
|
|
|
|
|
10 |
2278,81 |
2181,58 |
8807,12 |
9281,27 |
2,06 |
2,00 |
|
|
|
|
|
|
|
11 |
4712,82 |
4994,96 |
13056,34 |
13552,84 |
1,23 |
1,06 |
|
|
|
|
|
|
|
12 |
6266,62 |
6882,17 |
18027,07 |
18807,35 |
2,04 |
1,91 |
|
|
|
|
|
|
|
13 |
4497,10 |
4413,43 |
11632,13 |
10483,17 |
1,99 |
1,93 |
|
|
|
|
|
|
|
14 |
3760,44 |
4783,27 |
48671,05 |
56564,83 |
2,31 |
1,95 |
|
|
|
|
|
|
|
15 |
3383,85 |
4351,19 |
15203,65 |
16929,08 |
2,18 |
1,86 |
|
|
|
|
|
|
|
Mean |
4557,41 |
4787,63 |
27716,24 |
27653,92 |
1,95 |
1,88 |
|
|
|
|
|
|
|
SD |
1795,23 |
1905,81 |
35221,20 |
31964,94 |
0,45 |
0,45 |
|
|
|
|
|
|
|
Примечание: Cmax – максимальная концентрация в крови; AUC0-t – площадь под кривой «концентрация время» в интервале времени от 0 до момента t отбора последней пробы крови; tmax – время достижения максимальной концентрации; T – исследуемый препарат; R – референтный препарат; Mean – среднее арифметическое; SD – стандартное отклонение; * - значения не учитывались при расчете среднего и стандартного отклонения, т.к. размерность выражена в мкмоль/л.
Рисунок 54.
Усредненные фармакокинетические профили УДХК.
а
301
б
Примечание: а) фармакокинетические профили исследуемых препаратов; б) фармакокинетические профили препаратов сравнения; Т1-Т15 и Р1-Р15 – нумерация исследований биоэквивалентности, вошедших в анализ (за исключением исследований 3 и 9, в которых концентрация измерялась в мкмоль/л).
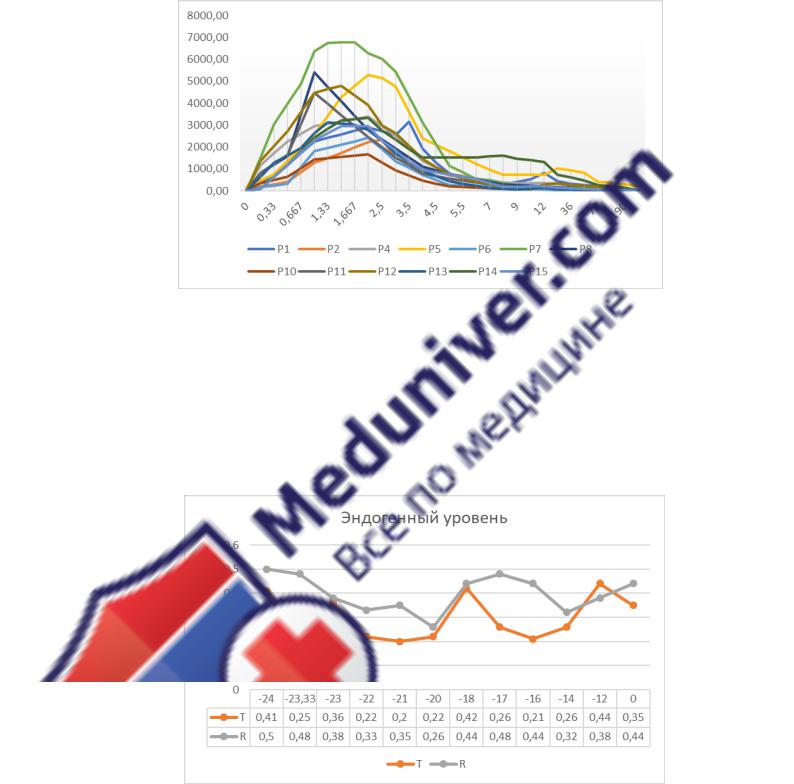
В рамках одного из исследований была изучена эндогенная концентрация УДХК на ограниченной выборке - 4 субъекта в течение 24 до приема исследуемых препаратов. Результаты продемонстрировали колебание концентрации в диапазоне 0,2-0,5 мкмоль/л (см. рисунок 55).
Рисунок 55.
Профиль эндогенной концентрации УДХК (мкмоль/л).
Примечание: T - профили исследуемых препаратов; R - профили препаратов сравнения;
Результаты исследования позволяют судить о том, что tmax для УДХК находиться в районе
1,5-2,5 часов, средние значения Cmax находились на уровне 4700 (±1800) нг/мл.
Аналитическую методику определения УДХК следует планировать с учетом ожидаемой максимальной концентрации и имеющегося оборудования, например, НПКО менее 235 (±90) нг/
мл. В проведенных исследованиях НПКО варьировал от 20 нг/мл до 250 нг/мл (0,25 мкг/мл), т.е.
302
правило «НПКО менее 5% от Cmax» было соблюдено в большинстве исследований.
Период полувыведения УДХК согласно инструкции референтного препарата составляет около 3,5-5,8 дней; по данным анализа исследований биоэквивалентности t1/2 варьировал от 1 до
30 часов (в среднем 12,49±11,48 часов), концентрация УДХК снижалась к эндогенному уровню спустя 72 часа, однако в некоторых исследованиях требовалось большее количество времени.
Поэтому при выборе точек забора образцов крови для ФК анализа можно ограничиться длительностью 72 часов. Более частый отбор образцов крови следует планировать в диапазоне времени достижения Сmах около 1,5-2,5 часов. Период отмывки с учетом длительности периода полувыведения - 7 дней.
При выборе точек забора образцов крови для ФК анализа УДХК следует учитывать наличие эндогенной концентрации. По данным анализа, в большинстве случаев концентрации УДХК до приема исследуемых препаратов значительно варьировали (от 20 нг/ до 350 нг/мл), что,
скорее всего, связано с особенностями проведения клинического исследования и биоаналитической методики определения аналитов (см. таблицу 218).
|
|
|
|
|
Таблица 218 |
|
Средние значения эндогенной концентрации УДХК. |
|
|||
№ |
Аналитический метод |
НПКО |
Врем. Точки |
Эндогенная |
Эндогенная |
|
|
|
|
концентрация, T |
концентрация, |
|
|
|
|
(SD) |
R (SD) |
1 |
ВЭЖХ МС/МС |
120 нг/мл |
0 |
51,920 (176,220) |
89,81 (254,480) |
|
|
|
|
нг/мл |
нг/мл |
2 |
ВЭЖХ МС |
0,25 мкг/мл |
0 |
Менее НПКО |
Менее НПКО |
|
|
|
|
|
|
3 |
ГХ ДИП |
0,2 мкмоль/л |
0 |
Менее НПКО |
Менее НПКО |
|
|
|
|
|
|
4 |
ВЭЖХ МС |
0,1 мкг/мл |
-12; 0 |
0,102 (0,019) мкг/мл |
0,099 (0,014) |
|
|
|
|
|
мкг/мл |
5 |
ВЭЖХ МС |
0,05 мкг/мл |
0 |
0,212 (0,131) мкг/мл |
0,174 (0,100) |
|
|
|
|
|
мкг/мл |
6 |
ВЭЖХ МС |
0,01 мкг/мл |
0 |
Менее НПКО |
Менее НПКО |
|
|
|
|
|
|
7 |
ВЭЖХ МС |
50 нг/мл |
-1,5; -1; 0 |
Менее НПКО (во |
Менее НПКО |
|
|
|
|
всех точках отбора) |
(во всех точках |
|
|
|
|
|
отбора) |
8 |
ВЭЖХ МС |
100 нг/мл |
-12; 0 |
24,400 (1,103) нг/мл |
44,755 (3,245) |
|
|
|
|
|
нг/мл |
9 |
ВЭЖХ УФ |
0,71 мкмоль/л |
-24; -20; -18; - |
0,430 (0,039) |
0,426 (0,043) |
|
|
|
16; 0 |
мкмоль/л |
мкмоль/л |
10 |
ГХ МС |
30 нг/мл |
0 |
48,390 (38,060) |
44,120 (32,660) |
|
|
|
|
нг/мл |
нг/мл |
11 |
ВЭЖХ МС |
100 нг/мл |
-12; 0 |
14,950 (10,733) |
18,325 (5,451) |
|
|
|
|
нг/мл |
нг/мл |
12 |
ВЭЖХ МС |
20 нг/мл |
0 |
Менее НПКО |
18,927 (65,135) |
|
|
|
|
|
нг/мл |
13 |
ВЭЖХ МС |
100 нг/мл |
-1,5; -1; 0 |
Менее НПКО |
Менее НПКО |
|
|
|
|
|
|
14 |
ВЭЖХ МС/МС |
50 нг/мл |
-24; -12; 0 |
106,967 (51,202) |
105,669 (50,999) |
|
|
|
|
нг/мл |
нг/мл |
15 |
ВЭЖХ МС/МС |
50 нг/мл |
-24; -12; 0 |
75,641 (28,631) |
77,828 (17,022) |
|
|
|
|
нг/мл |
нг/мл |
Примечание: ВЭЖХ МС - высокоэффективная жидкостная хроматография с масс-спектрометрической детекцией; ВЭЖХ МС/МС – высокоэффективная жидкостная хроматография с тандемной массспектрометрической детекцией; ВЭЖХ УФ - высокоэффективная жидкостная хроматография с
303

ультрафиолетовой детекцией; ГХ МС - газовая хроматография с масс-спектрометрической детекцией; ГХ ДИП – газовая хроматография с ионно-плазменной детекцией; НПКО – нижний предел количественного определения; SD
–стандартное отклонение.
Вбольшинстве исследований средние эндогенные концентрации были ниже НПКО
аналитического метода или незначительно превышали НПКО, но не превышали 5% от средней
Cmax. (см. таблицу 219).
Таблица 219. Доля средних эндогенных концентраций УДХК от средних значений Cmax.
№ |
Эндогенная |
Эндогенная |
Cmax, Т |
Сmax, R |
Cmax/ЭК, Т |
Cmax/ЭК, R |
|
концентрация, T |
концентрация, |
|
|
% |
% |
|
(SD) |
R (SD) |
|
|
|
|
1 |
51,920 (176,220) |
89,81 (254,480) |
4771,56 нг/мл |
4778,64 |
1,09 |
1,88 |
|
нг/мл |
нг/мл |
|
нг/мл |
|
|
2 |
Менее НПКО |
Менее НПКО |
2,388 мкг/мл |
2,512 |
<10,47 |
<9,95 |
|
|
|
|
мкг/мл |
|
|
3 |
Менее НПКО |
Менее НПКО |
7,99 мкмоль/л |
10,01 |
<2,5 |
<2 |
|
|
|
|
мкмоль/л |
|
|
4 |
0,102 (0,019) мкг/мл |
0,099 (0,014) |
3,657 мкг/мл |
3,632 |
2,79 |
2,73 |
|
|
мкг/мл |
|
мкг/мл |
|
|
5 |
0,212 (0,131) мкг/мл |
0,174 (0,100) |
6,631 мкг/мл |
6,300 |
3,20 |
2,76 |
|
|
мкг/мл |
|
мкг/мл |
|
|
6 |
Менее НПКО |
Менее НПКО |
2,62 мкг/мл |
2,63 мкг/мл |
<0,38 |
<0,38 |
|
|
|
|
|
|
|
7 |
Менее НПКО (во |
Менее НПКО (во |
8021,42 нг/мл |
8975,42 |
<0,62 |
<0,56 |
|
всех точках отбора) |
всех точках |
|
нг/мл |
|
|
|
|
отбора) |
|
|
|
|
8 |
24,400 (1,103) нг/мл |
44,755 (3,245) |
6259,62 нг/мл |
5805,55 |
0,39 |
0,77 |
|
|
нг/мл |
|
нг/мл |
|
|
9 |
0,430 (0,039) |
0,426 (0,043) |
20,57 |
23,47 |
2,09 |
1,82 |
|
мкмоль/л |
мкмоль/л |
мкмоль/л |
мкмоль/л |
|
|
10 |
48,390 (38,060) нг/мл |
44,120 (32,660) |
2278,81 нг/мл |
2181,58 |
2,12 |
2,02 |
|
|
нг/мл |
|
нг/мл |
|
|
11 |
14,950 (10,733) нг/мл |
18,325 (5,451) |
4712,82 нг/мл |
4994,96 |
0,32 |
0,37 |
|
|
нг/мл |
|
нг/мл |
|
|
12 |
Менее НПКО |
18,927 (65,135) |
6266,62 нг/мл |
6882,17 |
<0,32 |
0,28 |
|
|
нг/мл |
|
нг/мл |
|
|
13 |
Менее НПКО |
Менее НПКО |
4497,10 нг/мл |
4413,43 |
<2,22 |
<2,27 |
|
|
|
|
нг/мл |
|
|
14 |
106,967 (51,202) |
105,669 (50,999) |
3760,44 нг/мл |
4783,27 |
2,84 |
2,21 |
|
нг/мл |
нг/мл |
|
нг/мл |
|
|
15 |
75,641 (28,631) нг/мл |
77,828 (17,022) |
3383,85 нг/мл |
4351,19 |
2,24 |
1,79 |
|
|
нг/мл |
|
нг/мл |
|
|
Mean |
|
|
|
|
2,24 |
2,12 |
|
|
|
|
|
|
|
SD |
|
|
|
|
2,50 |
2,33 |
|
|
|
|
|||
|
|
|
|
|
|
|
Примечание: Cmax – максимальная концентрация в крови; НПКО – нижний предел количественного определения; SD
– стандартное отклонение; T – исследуемый препарат; R – референтный препарат.
Результаты анализа внутрииндивидуальной вариабельности УДХК из исследований БЭ со стандартным простым перекрестным дизайном 2х2х2 представлены в таблице 220, и
демонстрируют, что в 4 исследованиях из 13 была обнаружена высокая вариабельность хотя бы одного из ФК параметров AUC0-t Cmax.
304
Таблица 220.
Коэффициенты внутрииндивидуальной вариабельности УДХК.
№ |
|
|
|
|
|
|
CVintra AUC0-t, % |
CVintra Cmax, % |
|
|
|
1 |
12,39 |
15,05 |
|
|
|
2 |
16,43 |
24,58 |
|
|
|
3 |
38,81* |
32,99* |
|
|
|
4 |
21,44 |
18,38 |
|
|
|
5 |
30,18* |
16,53 |
|
|
|
6 |
28,24 |
19,72 |
|
|
|
7 |
14,01 |
21,77 |
|
|
|
8 |
21,23 |
18,95 |
|
|
|
9 |
20,28 |
31,26* |
|
|
|
10 |
16,42 |
11,27 |
|
|
|
11 |
19,56 |
15,90 |
|
|
|
12 |
17,60 |
28,06 |
|
|
|
13 |
23,25 |
31,85* |
|
|
|
CVpooled, % |
22,14 (23,02) |
23,11 (24,03) |
(верхняя граница ДИ)
Примечание: AUC0-t – площадь под кривой «концентрация время» в интервале времени от 0 до момента t отбора последней пробы крови; Cmax – максимальная концентрация в крови; CVintra – коэффициент внутрииндивидуальной вариабельности; CVpooled - усредненное («пулированное») значение коэффициента внутрииндивидуальной вариабельности; ДИ – доверительный интервал; НД – нет данных (метаболит не определялся); * - значения, превышающие 30%.
Полученные значения коэффициентов внутрииндивидуальной вариабельности УДХК были «пулированы». «Результаты «пулирования» данных 13 исследований показали, что значения CVpooled Cmax и AUC0-t не превышают 30% (23%; верхняя граница 80% доверительного интервала 24%, и 21%; верхняя граница 80% доверительного интервала 23%, соответственно).
В двух исследованиях с неполным повторным дизайном (2х2х3), в которых участвовало
36 субъектов, были получены высокие значения внутрииндивидуальной вариабельности исследуемого и референтного препарата (см. таблицу 221).
Таблица 221. Коэффициенты внутрииндивидуальной вариабельности исследуемого и референтного
препаратов УДХК.
№ |
Исследуемый |
Референтный |
||
|
|
|
|
|
|
CVintra AUC0-t, % |
CVintra Cmax, % |
CVintra AUC0-t, % |
CVintra Cmax, % |
|
|
|
|
|
14 |
22,31 |
31,92 |
25,71 |
32,83 |
|
|
|
|
|
15 |
28,99 |
39,60 |
37,83 |
31,64 |
|
|
|
|
|
CVpooled, % |
25,83 (28,04) |
35,91 (39,08) |
32,23 (35,04) |
32,23 (35,04) |
(верхняя граница ДИ)
Примечание: AUC0-t – площадь под кривой «концентрация время» в интервале времени от 0 до момента t отбора последней пробы крови; Cmax – максимальная концентрация в крови; CVintra – коэффициент внутрииндивидуальной вариабельности.
Таким образом, получены противоречивые данные в отношении внутрииндивидуальной вариабельности ФК параметров УДХК. В 6 из 15 исследований была показано высокая внутрииндивидуальная вариабельность. Поэтому препараты УДХК можно отнести к препаратам
305

с «умеренной» высокой внутрииндивидуальной вариабельностью (высокая вариабельность продемонстрирована в 40% исследований) [98] и включить в Перечень лекарственных средств с высокой внутрииндивидуальной вариабельностью ФК параметров (см. Приложение №3). При планировании расчета размера выборки в исследования БЭ следует ориентироваться на значения вариабельности около 25-38%.
Также были рассчитаны коэффициенты внутрииндивидуальной вариабельности УДХК для отдельных популяций субъектов мужского и женского пола (см. таблицу 222). Всего в исследованиях УДХК в статический анализ были включены данные от 365 субъектов, из которых 197 было мужского пола и соответственно 168 женского.
В10 из 13 исследований стандартного дизайна (2х2х2) участвовали субъекты обоего пола,
в3 исследованиях, соответственно участвовали субъекты только одного пола. В 10 исследованиях УДХК участвовало 155 субъектов мужского пола и в 150 женского. Высокие значения CVintra фармакокинетических параметров Cmax и AUC0-t (более 30 %), были получены в 2 исследованиях у мужчин и 2 у женщин.
Таблица 222. Данные о внутрииндивидуальной вариабельности УДХК у мужчин и женщин.
|
М |
Ж |
|
М |
|
Ж |
Ж/М |
Ж/М |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Cmax, % |
|
AUC0-t, % |
Cmax, % |
|
AUC0-t, % |
Cmax |
AUC0-t |
|
|
|
|
|
|
|
|
|
|
|
1 |
19 |
5 |
14,03 |
|
11,70 |
18,71 |
|
17,99 |
1,33 |
1,54 |
|
|
|
|
|
|
|
|
|
|
|
4 |
17 |
7 |
21,78 |
|
24,86 |
5,85 |
|
13,27 |
0,27 |
0,53 |
|
|
|
|
|
|
|
|
|
|
|
6 |
5 |
13 |
28,82 |
|
15,83 |
16,51 |
|
28,95 |
0,57 |
1,83 |
|
|
|
|
|
|
|
|
|
|
|
7 |
7 |
17 |
32,47* |
|
17,16 |
17,20 |
|
13,63 |
0,53 |
0,79 |
|
|
|
|
|
|
|
|
|
|
|
8 |
13 |
11 |
16,74 |
|
13,72 |
20,19 |
|
28,78 |
1,21 |
2,10 |
|
|
|
|
|
|
|
|
|
|
|
9 |
9 |
14 |
13,56 |
|
23,52 |
40,39* |
|
17,15 |
2,98 |
0,73 |
|
|
|
|
|
|
|
|
|
|
|
10 |
12 |
6 |
12,89 |
|
15,80 |
8,27 |
|
19,14 |
0,64 |
1,21 |
|
|
|
|
|
|
|
|
|
|
|
11 |
11 |
13 |
13,97 |
|
16,15 |
16,97 |
|
21,79 |
1,21 |
1,35 |
|
|
|
|
|
|
|
|
|
|
|
12 |
10 |
14 |
32,37* |
|
17,57 |
26,37 |
|
15,84 |
0,81 |
0,90 |
|
|
|
|
|
|
|
|
|
|
|
13 |
14 |
16 |
20,99 |
|
19,53 |
38,79* |
|
27,34 |
1,85 |
1,40 |
|
|
|
|
|
|
|
|
|
|
|
СРЗНАЧ |
|
|
20,76 |
|
17,58 |
20,92 |
|
20,39 |
1,14** |
1,24** |
СРГЕОМ |
|
|
19,50 |
|
17,18 |
18,03 |
|
19,61 |
|
|
МАКС |
|
|
32,47 |
|
24,86 |
40,39 |
|
28,95 |
|
|
|
|
|
|
|
|
|||||
МИН |
|
|
12,89 |
|
11,70 |
5,85 |
|
13,27 |
|
|
|
|
|
|
|
|
|||||
СО |
|
|
7,88 |
|
4,08 |
11,40 |
|
6,04 |
|
|
|
|
|
|
|
|
|
|
|
|
|
Примечание: Cmax – максимальная концентрация в плазме крови, AUC0-t – площадь под кривой «концентрация время» в интервале времени от 0 до момента t отбора последней пробы крови, М – мужчины, Ж – женщины, Ж/M – отношение значений внутрииндивидуальной вариабельности фармакокинетического параметра у женщин к соответствующему значению у мужчин, СРЗНАЧ – среднее арифметическое значение, СРГЕОМ – среднее геометрическое значение, МАКС – максимальное значение, МИН – минимальное значение, СО – стандартное отклонение, * - значения, превышающие 30% (высокая вариабельность), ** - значения демонстрируют превышение внутрииндивидуальной вариабельности у женщин в сравнении с мужчинами.
В двух исследованиях с неполным повторным дизайном (2х2х3), в которых участвовало 38 субъектов мужского пола и 34 субъекта женского пола, были получены высокие значения внутрииндивидуальной вариабельности (см. таблицу 223).
306
Таблица 223. Коэффициенты внутрииндивидуальной вариабельности исследуемого и референтного
препаратов УДХК.
№ |
|
Исследуемый |
|
|
Референтный |
|
||
|
|
|
|
|
|
|
|
|
|
Мужчины |
Женщины |
Мужчины |
Женщины |
||||
|
|
|
|
|
|
|
|
|
|
CVintra |
CVintra Cmax, |
CVintra |
CVintra |
CVintra |
CVintra |
CVintra |
CVintra |
|
AUC0-t, % |
% |
AUC0-t, % |
Cmax, % |
AUC0-t, % |
Cmax, % |
AUC0-t, % |
Cmax, % |
14 |
24,93 |
22,89 |
19,81 |
34,40* |
24,92 |
30,35* |
13,31 |
38,22* |
|
|
|
|
|
|
|
|
|
15 |
51,73* |
38,34* |
42,69* |
33,84* |
46,17* |
43,78* |
34,90* |
30,75* |
|
|
|
|
|
|
|
|
|
Примечание: AUC0-t – площадь под кривой «концентрация время» в интервале времени от 0 до момента t отбора последней пробы крови; Cmax – максимальная концентрация в крови; CVintra – коэффициент внутрииндивидуальной вариабельности; * - значения, превышающие 30% (высокая вариабельность).
Таким образом, высокая внутрииндивидуальная вариабельность ФК УДХК хотя бы одного изучаемого ФК параметра наблюдалась и у мужчин, и у женщин в 4 из 12 исследований.
Т.е. частота встречаемости высокой вариабельности у мужчин и женщин одинаковая, в связи с чем анализ ассоциации между принадлежностью к определённому полу и выявлением высокой частоты внутрииндивидуальной вариабельности ФК параметров, не проводился.
Анализ средних значений внутрииндивидуальной вариабельности параметра Cmax 10
исследований со стандартным дизайном показал незначительно большие значения в группе женщин (20,92±11,40 и 20,76±7,88, соответственно). Значения отношений внутрииндивидуальной вариабельности между женщинами и мужчинами составило – 1,14, что также говорит о незначительно большей внутрииндивидуальной вариабельности у женщин.
Анализ сравнения внутрииндивидуальной вариабельности параметров Cmax у мужчин и женщин не выявил статистически значимых различий (t=-0,037; p=0,971).
В отношении параметра AUC0-t была обнаружена аналогичная тенденция – среднее значение в группе женщин 20,39±6,04 и 17,58±4,08 в группе мужчин. Отношение значений вариабельности между женщинами и мужчинами составило 1,24. Анализ сравнения внутрииндивидуальной вариабельности параметров AUC0-t у мужчин и женщин не выявил статистически значимых различий (t=-1,216; p=0,240). Можно судить о том, что внутрииндивидуальная вариабельность параметров ФК УДХК у женщин незначительно выше,
чем у мужчин, однако, различия статистически не значимы.
Таблица 224 демонстрирует, отношение средних T/R для мужчин и женщин в проведенных исследованиях БЭ и случаи выявленной клинически значимой разницы отношений средних T/R у мужчин и женщин. В 5 из 12 исследований выявлена клинически значимая разница отношений средних T/R у мужчин и женщин, т.е. примерно в 40% исследований. В литературе наличие взаимосвязи «пол–лекарственная форма» в исследованиях БЭ выявлялось с частотой
36% (4 из 11 исследований) [231] и 46% (12 из 26 исследований) [120]. Данная взаимосвязь свидетельствует о наличии более чем 20% различий между сравниваемыми препаратами у мужчин и женщин по параметрам Cmax и AUC0-t. Указанные различия обусловлены
307

характеристиками готовой ЛФ, такими как состав и технология производства. Анализ сравнения отношений геометрических средних T/R ФК параметров у мужчин и женщин не выявил статистически значимых различий для Сmax (t=-0,447; p=0,659) и для AUC0-t (t=-1,253; p=0,223).
Таблица 224. Клинически значимые различия отношений геометрических средних воспроизведенного и
референтного препаратов УДХК у мужчин и женщин.
|
|
М |
|
Ж |
Разница М-Ж |
|||
|
|
|
|
|
|
|
|
|
|
T/R |
|
T/R |
T/R |
|
T/R |
Cmax |
AUC0-t |
|
Cmax |
|
AUC0-t |
Cmax |
|
AUC0-t |
|
|
1 |
1,03 |
|
0,99 |
0,92 |
|
1,01 |
0,11 |
-0,02 |
|
|
|
|
|
|
|
|
|
4 |
1,03 |
|
1,08 |
0,96 |
|
1,05 |
0,07 |
0,03 |
|
|
|
|
|
|
|
|
|
6 |
1,10 |
|
0,72 |
0,96 |
|
1,04 |
0,14 |
-0,32* |
|
|
|
|
|
|
|
|
|
7 |
1,03 |
|
0,92 |
0,90 |
|
0,87 |
0,14 |
0,05 |
|
|
|
|
|
|
|
|
|
8 |
0,92 |
|
1,02 |
1,12 |
|
0,98 |
-0,21* |
0,04 |
|
|
|
|
|
|
|
|
|
9 |
0,83 |
|
0,87 |
0,85 |
|
1,06 |
-0,02 |
-0,20* |
|
|
|
|
|
|
|
|
|
10 |
1,07 |
|
0,95 |
1,03 |
|
0,90 |
0,03 |
0,04 |
|
|
|
|
|
|
|
|
|
11 |
0,91 |
|
1,06 |
0,99 |
|
0,92 |
-0,08 |
0,15 |
|
|
|
|
|
|
|
|
|
12 |
0,86 |
|
0,85 |
1,01 |
|
1,05 |
-0,15 |
-0,20* |
|
|
|
|
|
|
|
|
|
13 |
0,86 |
|
1,09 |
1,07 |
|
1,09 |
-0,20* |
-0,01 |
|
|
|
|
|
|
|
|
|
14 |
0,88 |
|
0,94 |
0,87 |
|
0,92 |
0,01 |
0,02 |
|
|
|
|
|
|
|
|
|
15 |
0,98 |
|
0,95 |
1,01 |
|
1,14 |
-0,03 |
-0,19 |
|
|
|
|
|
|
|
|
|
Примечание: Cmax – максимальная концентрация в плазме крови, AUC0-t – площадь под кривой «концентрациявремя», М – мужчины, Ж - женщины, М-Ж разница значений T/R у мужчин и женщин, T/R – отношение средних фармакокинетических параметров исследуемого (T) и референтного препарата (R), * - значения превышающие порог ±0,2.
Таким образом, наблюдаемая частота обнаружения взаимосвязи «пол–лекарственная форма» в нашем исследовании и по данным литературы позволяет судить о целесообразности данной оценки в исследованиях БЭ воспроизведенных препаратов в целом и в частности препаратов УДХК.
Проведен анализ ФК различий путем сравнения значений Cmax и у мужчин и женщин, принимающих оба препарата (исследуемый и референтный) в 12 исследованиях УДХК,
в которых участвовали субъекты обоего пола. В 1 исследовании были выявлены статистически значимые различия у мужчин и женщин для параметров Cmax и AUC0-t (у женщин значения выше)
(см. таблицу 225). Распределение логарифмированных данных было близко к нормальному,
поэтому для сравнения использовали критерий Стьюдента.
Таблица 225. Фармакокинетические различия у мужчин и женщин из исследований УДХК.
№ |
ФК |
Пол |
N Среднее Стандартны |
Стандартна |
t- |
Степен |
р |
|
|
параметр |
|
е отклонения |
я |
средняя |
критерий |
и |
|
|
|
|
|
ошибка |
|
свободы |
(двухсторонняя |
|
|
|
|
|
|
|
|
|
) |
№ lnCmax |
мужчины |
18 |
2,8113 |
0,44339 |
0,10451 |
-2,197 |
44 |
0,033 |
|
9 |
|
|
|
|
|
|
|
|
|
женщин |
28 |
3,1053 |
0,44264 |
0,08365 |
|
|
|
||
|
|
|
|
|
|||||
|
|
ы |
|
|
|
|
|
|
|
|
LnAUC0-t |
мужчины |
18 |
4,0824 |
0,49947 |
0,11773 |
-3,040 |
44 |
0,004 |
|
|
|
|
|
|
|
|
|
|
|
|
женщин |
28 |
4,4620 |
0,34829 |
0,06582 |
|
|
|
|
|
ы |
|
|
|
|
|
|
|
|
|
|
|
|
|
308 |
|
|
|
Примечание: № - номер исследования; ФК – фармакокинетика; N – количество субъектов анализа; t-критерий – критерий Стьюдента; р – значимость; ln – логарифм; Cmax – максимальная концентрация в плазме крови AUC0-t – площадь под кривой «концентрация время» в интервале времени от 0 до момента t отбора последней пробы крови.
С помощью полученных в результате нашего анализа значений внутрииндивидуальной вариабельности и отношений геометрических средних T/R, рассчитали симуляционные 90%
доверительные интервалы для 10 исследований воспроизведённых препаратов УДХК при допущении, что количество субъектов мужского и женского пола будет приравнено к значению общей исходной выборки. Как видно из таблицы 226, в результате проведенных расчетов, в 6 из
12 исследований получены доверительные интервалы, не укладывающиеся в допустимый диапазон 80,00-125,00 %.
Таблица 226. 90 % доверительные интервалы для отношения геометрических средних исследуемого и
референтного препаратов УДХК у мужчин и женщин.
|
|
Cmax М |
AUC0-t М |
Cmax Ж |
AUC0-t Ж |
||||
|
|
|
|
|
|
|
|
|
|
|
N |
L |
U |
L |
U |
L |
U |
L |
U |
|
|
|
|
|
|
|
|
|
|
1 |
24 |
0,9601 |
1,1026 |
0,9330 |
1,0474 |
0,8384 |
1,0077 |
0,9266 |
1,1060 |
|
|
|
|
|
|
|
|
|
|
4 |
24 |
0,9296 |
1,1507 |
0,9584 |
1,2218 |
0,9355 |
0,9914 |
0,9878 |
1,1260 |
|
|
|
|
|
|
|
|
|
|
6 |
18 |
0,9341 |
1,2977* |
0,6577* |
0,7899* |
0,8695 |
1,0523 |
0,8830 |
1,2284 |
|
|
|
|
|
|
|
|
|
|
7 |
24 |
0,8836 |
1,2094 |
0,8420 |
0,9969 |
0,8238 |
0,9757 |
0,8115 |
0,9284 |
|
|
|
|
|
|
|
|
|
|
8 |
24 |
0,8430 |
0,9940 |
0,9543 |
1,0927 |
1,0184 |
1,2417 |
0,8495 |
1,1236 |
|
|
|
|
|
|
|
|
|
|
9 |
23 |
0,7760* |
0,8899 |
0,7696* |
0,9740 |
0,6946* |
1,0304 |
0,9767 |
1,1609 |
|
|
|
|
|
|
|
|
|
|
10 |
18 |
0,9903 |
1,1500 |
0,8656 |
1,0392 |
0,9863 |
1,0858 |
0,8094 |
1,0094 |
|
|
|
|
|
|
|
|
|
|
11 |
24 |
0,8475 |
0,9727 |
0,9832 |
1,1527 |
0,9111 |
1,0767 |
0,8256 |
1,0221 |
|
|
|
|
|
|
|
|
|
|
12 |
24 |
0,7335* |
1,0030 |
0,7818* |
0,9292 |
0,8877 |
1,1480 |
0,9719 |
1,1360 |
|
|
|
|
|
|
|
|
|
|
13 |
30 |
0,7857* |
0,9429 |
0,9978 |
1,1826 |
0,9039 |
1,2558* |
0,9714 |
1,2298 |
|
|
|
|
|
|
|
|
|
|
14** |
36 |
0,7798* |
1,0099 |
0,8297 |
1,0789 |
0,7550* |
1,0158 |
0,8167 |
1,0536 |
|
|
|
|
|
|
|
|
|
|
15** |
36 |
0,7928* |
1,2239 |
0,7721 |
1,1917 |
0,8256 |
1,2493 |
0,9000 |
1,4499* |
|
|
|
|
|
|
|
|
|
|
Примечание: Cmax – максимальная концентрация в плазме крови; AUC – площадь под кривой «концентрация-время»; N – количество субъектов; М – мужчины; Ж – женщины; L – нижняя граница 90% доверительного интервала; U – верхняя граница 90% доверительного интервала; * – значения, не укладывающиеся в диапазон 80,00-125,00%; ** - границы масштабированы.
У мужчин не эквивалентные результаты были получены в 6 исследованиях (50%), у
женщин в 4 исследованиях (33%). Изучение ассоциации между принадлежностью к определённому полу и выявлением неэквивалентных результатов исследований биоэквивалентности УДХК, выполнили, используя критерий χ2 с поправкой Йетса, для чего построена таблица сопряженности (см. таблицу 227). Анализ влияния фактора гендерной принадлежности на частоту результатов выявления доверительных интервалов, не укладывающихся в диапазон 80,00-125,00 %, показал отсутствие статистически значимой взаимосвязи (χ2=0,171; р=0,679).
309

Таблица 227. Ассоциация между полом субъектов и частотой выявления не биоэквивалентных
результатов.
|
Биоэквивалентные |
Не биоэквивалентные |
|
n=14 |
n=82 |
Мужской пол |
6 |
6 |
n=12 |
|
|
Женский пол |
8 |
4 |
n=12 |
|
|
Примечание: n – количество наблюдений.
Препараты УДХК могут быть отнесены к ЛП – АЭС и включены в Печень лекарственных средств аналогов эндогенных соединений (Приложение №5). Также препараты УДХК обладают высокой внутрииндивидуальной вариабельности и могут быть включены в Печень высоковариабельных лекарственных средств (Приложение №3).
При планировании и оценке результатов исследований БЭ УДХК следует руководствоваться принципами, описанными в Приложении №2.
Фолиевая кислота.
Фолиевая кислота – синтетический аналог витамина В9 для лечения заболеваний, вызванных дефицитом фолиевой кислоты. Время достижения максимальной концентрации после приема внутрь составляет 30-60 минут. Выводится в виде метаболитов, либо в неизменном виде,
вслучае если доза превышает суточную потребность74.
Врезультате анализа баз данных было выявлено 1 исследование БЭ. Исследование было выполнено с простым перекрёстным дизайном в 2 последовательностях, 2 режимах терапии, 2 периодах. В исследовании участвовали 20 взрослых здоровых добровольцев 8 мужского и 12
женского пола. Препаратом сравнения был препарат фолиевой кислоты, представленный на рынке, т.к. в России для препаратов фолиевой кислоты референтный препарат не установлен. В исследовании изучалась дозировка 1 мг. Исследуемые препараты принимались натощак. Период отмывки в исследовании составил 7 дней, длительность забора образцов крови – 24 часа (0; 0,16; 0,25; 0,32; 0,5; 0,75; 1; 2; 3; 4; 6; 9; 12; 24 ч).
Для определения концентраций фолиевой кислоты в качестве биоаналитического метода использовали высокоэффективную жидкостную хроматографию с масс-спектрометрической детекцией аналитов, НПКО был 10 нг/мл.
В результате анализа нескорректированных на эндогенный уровень значений концентраций фолиевой кислоты были рассчитаны ФК параметры Cmax, AUC0-t, tmax. В таблице
228 представлены усредненные ФК параметры, на рисунке 56 представлены усреднённые ФК профили.
74 Фолиевая кислота. Инструкция по медицинскому применению [Электронный ресурс] // Государственный реестр лекарственных средств. URL: https://grls.rosminzdrav.ru/InstrImg/0001445096/%D0%9B%D0%9F-002991[2015]_0.pdf (дата обращения: 11.05.2020).
310
