
3 курс / Фармакология / Диссертация_Ромодановский_Д_П_Разработка_требований_для_оценки_фармакокинетики
.pdf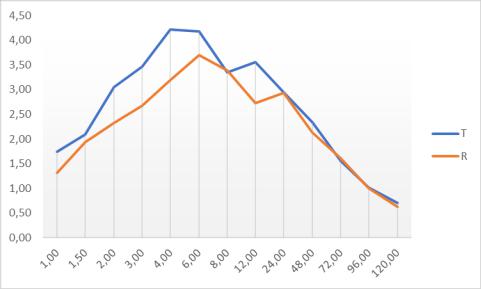
определения аналитов использовали высокоэффективную жидкостную хроматографию с ультрафиолетовой детекцией. Сведения о НПКО аналитов представлены в Приложении №1.
В результате анализа значений концентраций карбамазепина и его метаболита были рассчитаны ФК параметры Cmax, AUC0-t, tmax. В таблице 172 представлены усредненные ФК параметры. На рисунке 43 представлены графики «концентрация-время» для обоих исследований.
|
|
|
|
|
|
Таблица 172. |
||
|
Усредненные фармакокинетические параметры карбамазепина. |
|
|
|||||
№ |
Cmax T, мкг/мл |
Cmax R, мкг/мл |
AUC0-t T, мкг*ч/мл |
AUC0-t R, мкг*ч/мл |
tmax T, ч |
tmax R, ч |
||
|
(SD) |
(SD) |
(SD) |
(SD) |
(SD) |
(SD) |
||
|
|
|
карбамазепин |
|
|
|
|
|
|
|
|
|
|
|
|
||
1 |
4,51 (1,03) |
4,08 (0,62) |
239,95 (51,44) |
224,24 (62,19) |
6,00 (3,38) |
9,08 (7,13) |
||
|
|
|
|
|
|
|
|
|
2* |
2,48 (0,37) |
2,56 (0,38) |
181,53 (39,24) |
181,32 (37,32) |
31,11 |
(5,41) |
29,00 |
(5,69) |
|
|
|
|
|
|
|
|
|
|
|
|
карбамазепин-10,11-эпоксид |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
0,12 (0,02) |
0,13 (0,02) |
8,35 (2,06) |
8,57 (1,62) |
25,33 |
(15,10) |
19,67 |
(14,11) |
|
|
|
|
|
|
|
|
|
2* |
0,16 (0,03) |
0,16 (0,04) |
10,28 (2,78) |
9,72 (3,62) |
39,11 |
(8,18) |
37,78 |
(8,59) |
|
|
|
|
|
|
|
|
|
Примечание: Cmax – максимальная концентрация в крови; AUC0-t – площадь под кривой «концентрация время» в интервале времени от 0 до момента t отбора последней пробы крови; tmax – время достижения максимальной концентрации; T – исследуемый препарат; R – референтный препарат; SD – стандартное отклонение; * - пролонгированные лекарственные формы.
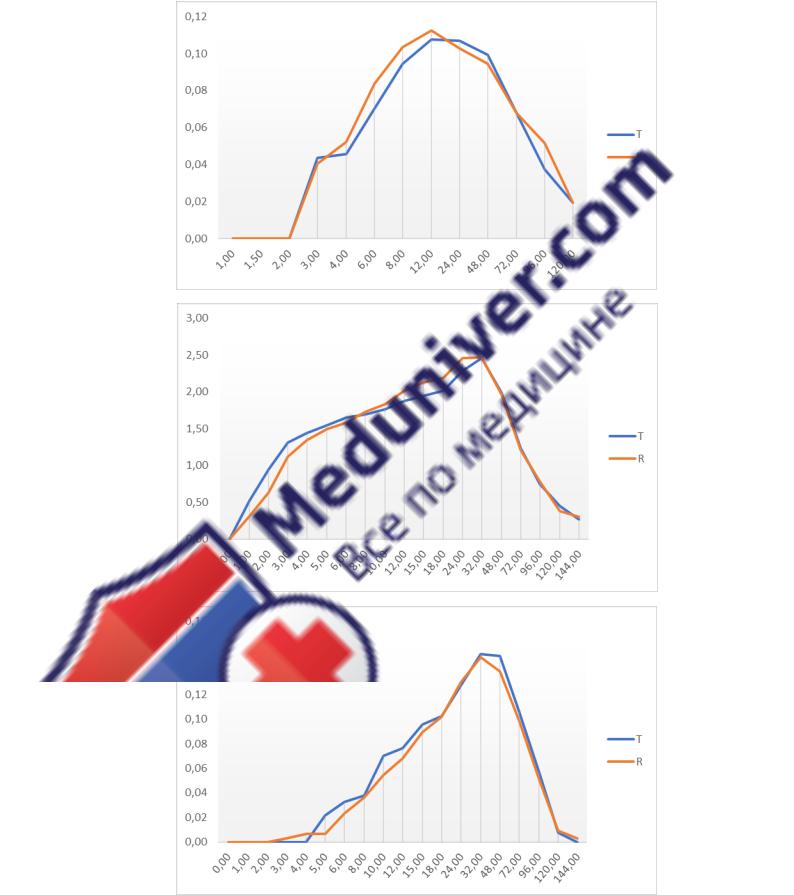
Рисунок 43.
Усредненные фармакокинетические профили карбамазепина.
1а
251
1б
2а
2б
Примечания: 1 – усредненные графики концентрация-время исследования №1: а – исходное соединение, б – метаболит; 2 – усредненные графики концентрация-время исследования №2: а – исходное соединение, б – метаболит; T – исследуемый препарат; R – референтный препарат.
252

Полученные результаты позволяют судить о том, что tmax карбамазепина находиться в районе 6-9 часов после приема ЛФ с немедленным высвобождением, 29-31 часов после приема пролонгированной ЛФ, для метаболита карбамазепина tmax был 20-25 часов и 38-40 часов,
соответственно.
Средние значения Cmax ЛФ немедленного высвобождения находились на уровне 3,5-4,5
мкг/мл для исходного соединения и 0,10-0,15 мкг для активного метаболита. Средние значения
Cmax ЛФ с пролонгированным высвобождением находились на уровне 2-3 мкг/мл для исходного соединения и 0,13-0,20 мкг/мл для активного метаболита.
Аналитическую методику определения карбамазепина следует планировать с учетом ожидаемой максимальной концентрации и имеющегося оборудования. Например, в случае ЛФ немедленного высвобождения - НПКО менее 0,175-0,225 мкг/мл для исходного соединения и менее и 0,005-0,0075 мкг/мл для метаболита. В случае пролонгированной ЛФ НПКО менее 0,1-
0,15 мкг/мл для исходного соединения и менее и 0,0065-0,01 мкг/мл для метаболита.
Период полувыведения карбамазепина составляет 36 часов, поэтому при выборе точек забора образцов крови для ФК анализа препаратов с немедленным высвобождением можно ограничиться общей длительностью 72 ч. Для ЛФ с пролонгированным высвобождением может быть рекомендована длительность отбора крови до 144 часов (6 t1/2). Более частый отбор образцов крови следует планировать в диапазоне времени достижения Сmах около 6-9 ч для препаратов немедленного высвобождения и 29-31 часов для препаратов пролонгированного высвобождения.
Период отмывки с учетом длительности периода полувыведения должен быть 9-14 дней.
Результаты анализа внутрииндивидуальной вариабельности представлены в таблице 173,
и демонстрируют, что в исследованиях БЭ карбамазепина не выявлена высокая внутрииндивидуальная вариабельность параметров ФК AUC0-t и Cmax.
Таблица 173. Коэффициенты внутрииндивидуальной вариабельности карбамазепина и метаболита.
№ |
карбамазепин |
карбамазепин-10,11-эпоксид |
|||
|
|
|
|
||
CVintra AUC0-t, % |
CVintra Cmax, % |
CVintra AUC0-t, % |
CVintra Cmax, % |
||
|
|||||
|
|
|
|
|
|
1 |
16,88 |
10,67 |
27,02 |
26,79 |
|
|
|
|
|
|
|
2 |
7,49 |
6,61 |
12,48 |
5,52 |
|
|
|
|
|
|
|
Примечание: AUC0-t – площадь под кривой «концентрация время» в интервале времени от 0 до момента t отбора последней пробы крови; Cmax – максимальная концентрация в крови; CVintra – коэффициент внутрииндивидуальной вариабельности.
Результаты проведенного анализа подтверждают ранее опубликованные данные о коэффициентах внутрииндивидуальной вариабельности карбамазепина (без данных по метаболиту) [367]. Согласно публикации в 10 исследованиях биоэквивалентности карбамазепина по параметру Cmax в 6 исследованиях вариабельность не превышала значение 10 % и в 4 – 20%. В
отношении параметра AUC0-t в 1 исследовании была показана высокая вариабельность (более
30%), в 5 – вариабельность не превышала 20% и в 4 – 10%.
253

Таким образом, можно судить, что препараты карбамазепина не обладают высокой вариабельностью. При расчете размера выборки можно ориентироваться на значение CVintra – 1720%, т.к. в проанализированных исследованиях максимальная вариабельность карбамазепина была 17%, а по данным литературы, в большинстве исследований она не превышала 20%.
Препараты карбамазепина относятся к препаратам с УТД, т.к. терапевтическое окно между эффективными концентрациями карбамазепина и концентрациями, связанными с развитием СНЯ узкое; неоптимальные дозы или концентрации препарата могут привести к недостаточной эффективности или к тяжелым НР48,49. Согласно инструкции референтного препарата карбамазепин подлежит терапевтическому мониторингу на основе анализа концентраций действующего вещества. Карбамазепин не обладает высокой внутрииндивидуальной вариабельностью, вместе с тем наблюдаются существенные межиндивидуальные различия равновесной концентрации в терапевтическом диапазоне доз.
Стоит отметить, что результаты 2 проанализированных исследований демонстрируют БЭ препаратов в традиционных границах признания БЭ 80,00-125,00%. При использовании подхода с сужением границ БЭ до 90,00-111,11% препараты не биоэквивалентны в исследовании №1 и для карбамазепина и для метаболита. В исследовании №2 препараты не биоэквивалентны по активному метаболиту. Однако сужение границ БЭ требует увеличения размера выборки, поэтому если в рассмотренные исследования было бы включено больше участников, то скорее всего, БЭ была бы подтверждена, т.к. значения точечной оценкой (отношения геометрических средних исследуемого и референтного препараторов) были в пределах 90,00-111,11%, а внутрииндивидуальная вариабельность ФК параметров не превышала 30%.
В исследованиях №1 и №2 участвовали только субъекты мужского пола, поэтому анализ влияния фактора принадлежности к определенному полу на ФК препаратов карбамазепина не проводился.
Препараты карбамазепина могут быть включены в Перечень лекарственных средств с узким терапевтическим диапазоном (см. Приложение №4). При планировании и оценке результатов исследований БЭ карбамазепина следует руководствоваться принципами, описанными в Приложении №2.
Левотироксин.
Левотироксин – является синтетическим левовращающим изомером тироксина, по своему
48Product-Specific Draft Guidance on Carbamazepine. [Электронный ресурс] // United States Food and Drug Administration. URL: https://www.accessdata.fda.gov/drugsatfda_docs/psg/Carbamazepine_oral%20tablet_016608_RV09-
15.pdf (дата обращения: 11.05.2020).
49Product-Specific Draft Guidance on Carbamazepine Extended-release tablets. [Электронный ресурс] // United States Food and Drug Administration. URL: https://www.accessdata.fda.gov/drugsatfda_docs/psg/Carbamazepine_ER%20tab_020234_RV03-15.pdf (дата обращения: 11.05.2020).
254

действию идентичному тироксину, синтезируемому щитовидной железой (т.е. лекарственное средство аналог эндогенного соединения). Максимальная концентрация в крови достигается через 5-6 часов. Период полувыведения 6-7 дней50.
В результате анализа базы данных ФГБУ «НЦЭСМП» о результатах клинических исследований препаратов левотироксина было отобрано 2 исследования БЭ.
Оценка 2-х исследований БЭ левотироксина показала, что в рассмотренных исследованиях был выбран стандартный простой перекрёстный дизайн. Препаратом сравнения в 1 исследований был препарат Эутирокс® - признанный референтным препаратом, согласно данным Государственного реестра лекарственных средств. Во 2 исследовании в качестве препарат сравнения был использован не референтный препарат. В 1 исследовании сравнивались ЛФ с немедленным высвобождением в дозировках 100 мкг, во 2 – ЛФ с пролонгированным высвобождением в дозировке 300 мкг. Данные о периоде отмывки, длительность отбора, количестве временных точек отбора и количестве субъектов, включённых в статистический анализ, представлены в Приложении №1. В обоих исследованиях в крови определяли – свободные Т4 (левотироксин) и метаболит - Т3 (трийодтиронин). Сведения о биоаналитическом методе определения аналитов и НПКО аналитов представлены в Приложении №1.
В результате анализа значений концентраций Т3 и Т4 левотироксина были рассчитаны ФК параметры Cmax, AUC0-t, tmax. В таблице 174 представлены усредненные ФК параметры. На рисунке 44 представлены графики концентрация-время для исследования №1. В обоих исследованиях не учитывался эндогенный уровень Т3 и Т4. Однако известно, что в организме человека имеются эндогенные уровни как левотироксина, так и его метаболитов51 [133].
Таблица 174.
Усредненные фармакокинетические параметры левотироксина.
№ |
Cmax T, |
Cmax R, |
AUC0-t T, |
AUC0-t R, |
tmax T, ч |
tmax R, ч |
|
(SD) |
(SD) |
(SD) |
(SD) |
(SD) |
(SD) |
|
|
|
Т3 |
|
|
|
|
|
|
|
|
|
|
1 |
8,39 (2,45) нг/мл |
8,43 (2,31) нг/мл |
89,92 (40,19) |
87,97 (40,00) |
3,67 |
3,71 |
|
|
|
ч*нг/мл |
ч*нг/мл |
(3,05) |
(3,00) |
2 |
2,24 (0,60) нмоль/л |
2,47 (0,68) нмоль/л |
69,89 (17,75) |
78,11 (19,31) |
2,42 |
2,28 |
|
|
|
нмоль/л |
нмоль/л |
(1,18) |
(0,89) |
|
|
|
Т4 |
|
|
|
|
|
|
|
|
|
|
1 |
10,08 (2,25) нг/мл |
10,33 (2,38) нг/мл |
626,14 (243,10) |
620,54 (211,40) |
3,75 |
4,42 |
|
|
|
ч*нг/мл |
ч*нг/мл |
(2,15) |
(2,95) |
2 |
146,41 (33,54) |
153,41 (32,36) |
НД |
4938,34 (742,60) |
2,31 |
2,06 |
|
нмоль/л |
нмоль/л |
|
нмоль/л |
(0,84) |
(0,76) |
50Эутирокс®. Инструкция по медицинском применению [Электронный ресурс] // Государственный реестр лекарственных средств. URL: https://grls.rosminzdrav.ru/InstrImg/0000009746/%D0%9F_N015039_01[2017]_0.pdf (дата обращения: 11.05.2020).
51Product-Specific Draft Guidance on Levothyroxine Sodium. [Электронный ресурс] // United States Food and Drug Administration. URL: https://www.accessdata.fda.gov/drugsatfda_docs/psg/Levothyroxine%20sodium_draft_Oral%20tab_RLD%20021116%20 %20%20%20%20%20%20%20%20%20%20%20%20%20021210%20%20%20%20%20%20%20%20%20%20%20%20 %20%20021301%20%20%20%20%20%20%20%20%20%20%20%20%20%20021342%20%20%20%20%20%20%20%2 0%20%20%20%20%20%20021402_RC12-14.pdf (дата обращения: 11.05.2020).
255
Примечание: Cmax – максимальная концентрация в крови; AUC0-t – площадь под кривой «концентрация время» в интервале времени от 0 до момента t отбора последней пробы крови; tmax – время достижения максимальной концентрации; T3 – трийодтиронин; T4 – левотироксин; T – исследуемый препарат; R – референтный препарат; SD – стандартное отклонение.
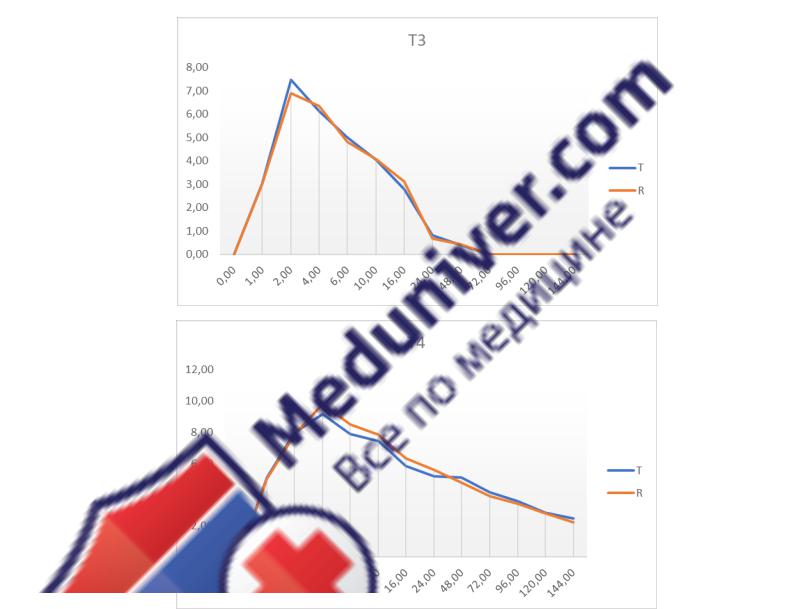
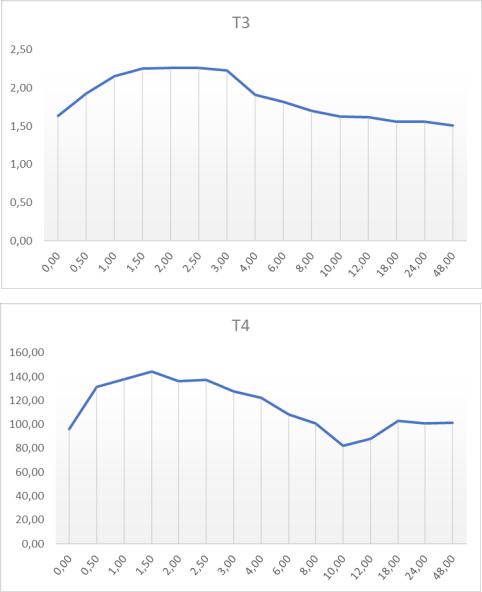
Рисунок 44.
Усредненные фармакокинетические профили левотироксина.
1а
1б
256
2а
2б
Примечания: 1а – усредненные графики концентрация-время (нг/мл-ч) исследования №1 для Т3, 1б – усредненные графики концентрация-время (нг/мл-ч) исследования №1 для Т4; 2а усредненные графики концентрация-время (нмоль/л-ч) исследования №1 для Т3; 2б - усредненные графики концентрация-время (нмоль/л-ч) исследования №1 для Т4; T – исследуемый препарат; R – референтный препарат. Результаты исследования №2 были не полными, т.к. в архиве частично отсутствовали страницы отчета с данными концентраций Т3 и Т4 для исследуемого препарата.
Полученные результаты позволяют судить о том, что tmax для T3 находиться в районе 2-4
часов, для T4 - в районе 2-6 часов после приема, средние значения Cmax T3 находились на уровне
6-8 нг/мл, для Т4 – 8-10 нг/мл.
Аналитическую методику определения T3 и T4 следует планировать с учетом ожидаемой максимальной концентрации и имеющегося оборудования, например, НПКО менее 0,3-0,4 нг/ мл для определения Т3 и менее 0,4-0,5 нг/мл для Т4.
Период полувыведения тироксина составляет 6-7 дней [89, 102, 133, 137, 138, 155, 218, 287, 409], поэтому при выборе точек забора образцов крови для ФК анализа можно ограничиться общей длительностью 48-72 ч, т.к. ЛФ левотироксина - с немедленным высвобождением. Более
257

частый отбор образцов крови следует планировать в диапазоне времени достижения Сmах T3 и Т4 около 2-6 часов. Период отмывки с учетом длительности периода полувыведения должен быть около 35 дней.
Результаты анализа внутрииндивидуальной вариабельности представлены в таблице 175,
и демонстрируют, что в исследовании №1 выявлена высокая внутрииндивидуальная вариабельность параметров ФК AUC0-t и Cmax, для Т3 и AUC0-t для Т4. В исследовании №2 вариабельность обоих ФК параметров была умеренной.
Таблица 175. Коэффициенты внутрииндивидуальной вариабельности Т3 и Т4.
№ |
Т3 |
|
Т4 |
|
||
|
|
|
|
|
|
|
CVintra AUC0-t, % |
|
CVintra Cmax, % |
CVintra AUC0-t, % |
|
CVintra Cmax, % |
|
|
|
|
||||
|
|
|
|
|
|
|
1 |
41,19 |
|
35,94 |
36,86 |
|
23,67 |
|
|
|
|
|
|
|
2 |
17,47 |
|
16,95 |
НД |
|
13,85 |
|
|
|
|
|
|
|
Примечание: AUC0-t – площадь под кривой «концентрация время» в интервале времени от 0 до момента t отбора последней пробы крови; Cmax – максимальная концентрация в крови; CVintra – коэффициент внутрииндивидуальной вариабельности; T3 – трийодтиронин; T4 – левотироксин; НД – нет данных, т.к. в архиве отсутствовали страницы отчета с данными концентраций Т4 для исследуемого препарата.
Результаты проведенного анализа противоречивы и неоднозначны. Ранее опубликованные данные о коэффициентах внутрииндивидуальной вариабельности левотироксина не демонстрировали высокую вариабельность [155]. Согласно публикации по параметру Cmax вариабельность была на уровне 7%, по параметру AUC0-t – 4,5%. Согласно данным
FDA препараты левотироксина также не обладают высокой вариабельностью51. Таким образом, можно судить, что препараты левотироксина не обладают высокой вариабельностью. Результаты, полученные в исследовании №1, скорее являются исключением и, по всей видимости, обусловлены внешними по отношению к действующему веществу причинами,
например, такими как состав или технология производства воспроизведенного препарата. При расчете размера выборки в исследования БЭ препаратов левотироксина можно рекомендовать ориентироваться на CVintra 10-20% (например, 17% как в исследовании №2).
Препараты левотироксина относятся к препаратам с УТД, т.к. терапевтическое окно между эффективными концентрациями левотироксина и концентрациями, связанными с развитием СНЯ узкое; неоптимальные дозы препарата могут привести к недостаточной эффективности, поэтому требуется индивидуальная титрация дозы с учетом терапевтического лекарственного мониторинга на основе анализа концентраций.
Стоит отметить, что результаты 2 проанализированных исследований демонстрируют БЭ препаратов в традиционных границах признания БЭ 80,00-125,00%. При использовании актуального в настоящее время подхода с сужением границ БЭ до 90,00-111,11% - препараты не биоэквивалентны по результатам обоих исследований. Вместе с тем, если в рассмотренные исследования было бы включено больше участников, то, скорее всего, БЭ была бы подтверждена,
258
т.к. значения точечной оценкой (отношения геометрических средних исследуемого и референтного препараторов) были в пределах 90,00-111,11%, а внутрииндивидуальная вариабельность ФК параметров не превышала 30%. Как известно, сужение границ БЭ требует увеличения размера выборки см. таблицу 13.
В исследованиях №1 и №2 участвовало 42 субъекта, из которых 23 (55%) было мужского пола и 19 (45%) женского. Были рассчитаны коэффициенты внутрииндивидуальной вариабельности левотироксина для отдельных популяций субъектов мужского и женского пола из исследований. В исследовании №1 наблюдались высокие значения внутрииндивидуальной вариабельности для AUC0-t у мужчин и женщин (см. таблицу 176). Более высокие значения продемонстрированы в группе мужчин.
Таблица 176. Данные о внутрииндивидуальной вариабельности Т3 и Т4у мужчин и женщин.
|
М |
Ж |
|
М |
|
Ж |
Ж/М |
Ж/М |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Cmax, % |
|
AUC0-t, % |
Cmax, % |
|
AUC0-t, % |
Cmax |
AUC0-t |
|
|
|
|
|
|
|
|
|
|
|
1-Т3 |
12 |
12 |
28,16 |
|
47,75* |
32,09* |
|
33,53* |
1,14 |
0,70 |
|
|
|
|
|
|
|
|
|
|
|
1-Т4 |
12 |
12 |
26,79 |
|
43,12* |
21,70 |
|
32,51* |
0,81 |
0,75 |
|
|
|
|
|
|
|
|
|
|
|
2-Т3 |
11 |
7 |
20,83 |
|
19,49 |
9,76 |
|
15,11 |
0,47 |
0,78 |
|
|
|
|
|
|
|
|
|
|
|
2-Т4 |
11 |
7 |
20,83 |
|
НД |
6,18 |
|
НД |
0,30 |
НД |
|
|
|
|
|
|
|
|
|
|
|
Примечание: Cmax – максимальная концентрация в плазме крови; AUC0-t – площадь под кривой «концентрация время» в интервале времени от 0 до момента t отбора последней пробы крови; М – мужчины; Ж – женщины; Ж/M – отношение значений внутрииндивидуальной вариабельности фармакокинетического параметра у женщин к соответствующему значению у мужчин; T3 – трийодтиронин; T4 – левотироксин; НД – нет данных, т.к. в архиве отсутствовали страницы отчета с данными концентраций Т4 для исследуемого препарата; * - значения превышающие 30%.
В связи с недостаточным количеством данных статистический анализ влияния фактора гендерной принадлежности на высокую вариабельность параметров ФК не проводился.
Таблица 177 демонстрирует, отношение средних T/R для мужчин и женщин в проведенных исследованиях БЭ и оценку наличия клинически значимой разницы (±0,2) отношений средних T/R у мужчин и женщин. Наличие значений, превышающих границу ±0,2, косвенно говорит о наличии взаимосвязи «пол-лекарственная форма» (имеются меж-половые различия, обусловленные формой дозирования). Т.е. референтный и воспроизведённый препарат могут быть не взаимозаменяемы у субъектов разного пола. В проанализированных исследованиях БЭ левотироксина в исследовании №1 обнаружена клинически значимая разница отношений геометрических средних T/R у мужчин и женщин для обоих параметров Cmax и AUC0- t. Таким образом, можно предположить наличие различий в готовой ЛФ воспроизведенного лекарственного препарата в сравнении с референтным, которые могут вносить вклад в вариабельность ФК левотироксина у мужчин и женщин, что также подтверждается анализом коэффициента внутрииндивидуальной вариабельности, который оказался более 30% и у мужчин, и у женщин.
259

Таблица 177. Клинически значимые различия отношений геометрических средних воспроизведенного и
референтного препарата левотироксина у мужчин и женщин.
|
|
М |
|
Ж |
Разница М-Ж |
|||
|
|
|
|
|
|
|
|
|
|
T/R |
|
T/R |
T/R |
|
T/R |
Cmax |
AUC0-t |
|
Cmax |
|
AUC0-t |
Cmax |
|
AUC0-t |
|
|
1-Т3 |
0,84 |
|
0,89 |
1,19 |
|
1,17 |
-0,34* |
-0,28* |
|
|
|
|
|
|
|
|
|
1-Т4 |
0,93 |
|
0,94 |
1,03 |
|
1,05 |
-0,09 |
-0,11 |
|
|
|
|
|
|
|
|
|
2-Т3 |
0,92 |
|
0,91 |
0,88 |
|
0,86 |
0,04 |
0,05 |
|
|
|
|
|
|
|
|
|
2-Т4 |
1,02 |
|
НД |
0,85 |
|
НД |
0,17 |
НД |
|
|
|
|
|
|
|
|
|
Примечание: Cmax – максимальная концентрация в плазме крови; AUC0-t – площадь под кривой «концентрация время» в интервале времени от 0 до момента t отбора последней пробы крови; М – мужчины; Ж – женщины; М-Ж разница значений T/R у мужчин и женщин; T/R – отношение средних фармакокинетических параметров исследуемого (T) и референтного препарата (R); T3 – трийодтиронин; T4 – левотироксин; * - значения превышающие ±0,2.
Проведён анализ сравнения значений Cmax и AUC0-t левотироксина у мужчин и женщин,
принимающих оба препарата (исследуемый и референтный) в каждом из описанных выше исследований. Выявлено, что статистически значимые различия параметров Cmax и AUC
левотироксина между мужчинами и женщинами не выявлены (см. таблицу 178).
Таблица 178. Анализ фармакокинетических различий у мужчин и женщин из исследований
левотироксина.
№ |
ФК |
Пол |
N |
Средний |
Сумма |
|
U- |
|
Z |
|
р |
параметр |
ранг |
рангов |
|
критерий |
|
|
(двухсторонняя) |
||||
|
|
|
|
|
|
|
|||||
|
lnAUC0-t |
мужчины |
24 |
24,21 |
581,00 |
281,000 |
-0,144 |
0,885 |
|||
|
|
|
|
|
|
|
|
|
|
|
|
1- |
женщины |
24 |
24,79 |
595,00 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
Т3 |
lnCmax |
мужчины |
24 |
24,33 |
584,00 |
284,000 |
-0,082 |
0,934 |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
женщины |
24 |
24,67 |
592,00 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
lnAUC0-t |
мужчины |
24 |
23,54 |
565,00 |
265,500 |
-0,474 |
0,635 |
|||
|
|
|
|
|
|
|
|
|
|
|
|
1- |
женщины |
24 |
25,46 |
611,00 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
Т4 |
lnCmax |
мужчины |
24 |
23,38 |
561,00 |
261,000 |
-0,557 |
0,578 |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
женщины |
24 |
25,63 |
615,00 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
lnAUC0-t |
мужчины |
22 |
20,05 |
441,00 |
120,000 |
-1,103 |
0,270 |
|||
|
|
|
|
|
|
|
|
|
|
|
|
2- |
женщины |
14 |
16,07 |
225,00 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
Т3 |
lnCmax |
мужчины |
22 |
19,77 |
435,00 |
126,000 |
-0,909 |
0,363 |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
женщины |
14 |
16,50 |
231,00 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
2- |
lnCmax |
мужчины |
22 |
20,43 |
449,50 |
111,500 |
-1,379 |
0,168 |
|||
Т4 |
женщины |
14 |
15,46 |
216,50 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
Примечание: № - номер исследования; ФК – фармакокинетика; N – количество субъектов анализа; U-критерий – критерий Манна-Уитни; Z – стандартизованная оценка; р – значимость; ln – логарифм; Cmax – максимальная концентрация в плазме крови, AUC0-t – площадь под кривой «концентрация время» в интервале времени от 0 до момента t отбора последней пробы крови; T3 – трийодтиронин; T4 – левотироксин.
Аналогичный анализ субпопуляций исследуемого и референтного препарата также показал отсутствие статистически значимых различий у мужчин и женщин в обеих субпопуляциях для обоих ФК параметров Т3 и Т4 в исследованиях.
С помощью полученных в результате нашего анализа значений внутрииндивидуальной вариабельности и точечной оценки, рассчитали симуляционные 90% доверительные интервалы для исследований воспроизведённых препаратов левотироксина при допущении, что количество
260
