Эндометриоз. Клинические и теоретические аспекты
Таблица 8.1
БИОЛОГИЧЕСКАЯ ХАРАКТЕРИСТИКА ИММУНОГЛОБУЛИНОВ
Класс |
Число |
Молек. |
Период |
Биологическая |
|
подклассов |
масса |
полу- |
функция |
|
|
|
распада |
|
|
|
|
|
|
igG |
4 |
150000/ |
23 дня |
циркулирует |
|
|
160000 |
|
экстраваскулярно, |
|
|
|
|
взаимодействуя с |
|
|
|
|
микробами и |
|
|
|
|
токсинами |
|
|
|
|
|
igM |
2 |
900000/ |
6 дней |
выполняет |
|
|
1000000 |
|
функцию"антитела |
|
|
|
|
тревоги" |
|
|
|
|
|
igA |
2 |
170000/ |
5 дней |
участвует в |
|
|
180000 |
|
создании местного |
|
|
|
|
иммунитета |
|
|
|
|
|
igD |
0 |
180000 |
3 дня |
находится на |
|
|
|
|
поверхности |
|
|
|
|
лимфоцитов |
|
|
|
|
|
igE |
0 |
190000 |
2 дня |
ответственней за |
|
|
|
|
развитие |
|
|
|
|
аллергических |
|
|
|
|
реакций |
|
|
|
|
|
Созревание и функциональная активность лимфоидных клеток обусловлены многочисленными межклеточными сигналами, большая часть которых осуществляется с помощью гуморальных медиаторов иммунитета. К последним относятся низкомолекулярные гуморальные продукты моноцитов, макрофагов и лимфоцитов (лимфокины) с молекулярной массой 10 000 - 80 000.

А.Н. СтрижаковиА.И. Давыдов
Промоноциты, моноциты и макрофаги, обладающие активным фагоцитозом и пиноцитозом, составляют так называемую «систему мононуклеарных фагоцитов». Указанная система выполняет три основные функции:
1)функцию фагоцитоза - катаболизирует антиген, переводя его в неиммунное состояние;
2)продуцирует факторы, способствующие дальнейшей элиминации антигена;
3)выделяет главный антиген для полного его рас-
познавания и последующего уничтожения лимфоцитами.
Резидентные макрофаги, большинство из которых располагается на поверхности серозных покровов, а часть - свободно плавает в перитонеальной жидкости, составляют первую линию защиты брюшной полости. Как правило, они первыми распознают чужеродные антигены, а в дальнейшем поглощают, катаболизируют и уничтожают эти антигены. Помимо прочего, резидентные макрофаги обладают способностью связываться с чужеродными антигенами, преобразуя их для последующего этапа уничтожения: в лимфатическом узле макрофаги стимулируют пролиферацию Т-хелперов, которые, в свою очередь, обеспечивают продукцию лимфокинов, активацию Т-лимфоцитов-киллеров и В-лимфоцитов. Под влиянием лимфокинов В-лимфоциты трансформируются в плазматические клетки, способные секретировать высокоспецифические антитела, которые не только активно связываются с антигеном, но и сохраняют «информацию» о них, что позволяет инактивировать антиген при повторном вторжении.
Процесс поглощения частиц антигена мононуклеарными фагоцитами включает две фазы: первоначально рецепторы клетки (на поверхности макрофагов имеются рецепторы к иммуноглобулину и комплементу) при-

Эндометриоз. Клинические итеоретическиеаспекты
крепляются к антигену (особенно, если последний покрыт антителами и комплементом), а непосредственно захвату антигена предшествует его разрушение с помощью лизосомальных ферментов. Современные данные свидетельствуют, что перитонеальные макрофаги продуцируют некоторые факторы роста и фибронектин, которые могут участвовать в процессе регенерации ткани, но вместе с тем и стимулировать образование спаек у больных эндометриозом9. Итак, резидентные макрофаги выполняют функцию «надзора» за репаративными процессами в брюшной полости; они предохраняют организм хозяина от вторжения чужеродных клеток (в т.ч., элементов канцерогенеза), а в комплексе с активированными макрофагами - обезвреживают дегенеративные фрагменты тканей. Резидентные макрофаги распознают и уничтожают чужеродные антигены и/или преобразуют их для последующей ликвидации их лимфоцитами. Кроме этого, макрофаги синтезируют особые вещества, способные индуцировать активацию и пролиферацию лимфоцитов и, следовательно, репарацию тканей. Механизм их биологического действия включает следующие основные аспекты:
1)маскирование чужеродного антигена для уничтожения его лимфоцитами;
2)продукция интерлейкина-1 и активация лимфоцитов;
3)синтез цитокинов;
4)стимулирование выработки промоноцитов и моноцитов;
5)иммобилизация активированных макрофагов;
6)продукция комплемента и простагландинов;
7)фагоцитоз клеток-мишеней и цитотоксическая активность;
8)повреждение ткани;

____________ А.Н. Стрижаков и AM. Давыдов_____________
9) образование спаек;
10) репарация ткани (фактор стимуляции фибробласта, фибронектин, эластаза, коллагеназа).
Состояниеиммунитетаубольныхгенитальным эндометриозом
Детально вопросы иммунного статуса больных эндометриозом впервые опубликованы в серии работ Н.В. Старцевой5' (справедливо уточнить, что гипотезу об иммунном происхождении эндометриоза впервые выдви-
нули М. V. Jonesco et G. Popesco23). В исследованиях Н.В.
Старцевой, проведенных на высоком методическом уровне, достоверно установлено, что эндометриоз развивается на фоне нарушенного иммунного гомеостаза (наличие Т-клеточного иммунодефицита, угнетение функции Т-супрессоров, активизация гиперчувствительности замедленного типа, снижение активности Т-лим- фоцитов при одновременной активации В-лимфоцитар- ной системы). Во всех наблюдениях эндометриоза, независимо от фазы менструального цикла, диагностирована повышенная активность трансформации В-клеток в бласты под воздействием митогена, а степень Т-имму- нодефицита коррелировала с тяжестью и распространенностью патологического процесса. В целом, в работах Н.В. Старцевой выявлены общие признаки иммунодефицита и аутоиммунизации при эндометриозе, свидетельствующие об ослаблении иммунного контроля и, обеспечении, таким образом, условий для имплантации и развития жизнеспособных фрагментов эндометрия вне зоны их нормального расположения. В последующих научных изысканиях, проведенных в этом направлении, внимание исследователей акцентировано на уточнении механизмов нарушений иммунологического контроля,

Эндометриоз. Клинические и теоретические аспекты
связанных с мониторингом роста чужеродных тканей. В частности, в качестве предмета поиска ученых выбрано изучение активности естественных киллеров в организме больных эндометриозом.
Естественная цитотоксичность лимфоцитов обнаружена сравнительно недавно , однако важность этой реакции для поддержания физиологического гомеостаза не вызывала сомнений. Основу феномена естественного цитотоксического воздействия составляет способность лимфоцитов интактных и неиммунизированных организмов уничтожать чужеродные типы клеток при совместном культивировании без участия системы комплемента и антител . В системе иммунологического надзора естественным киллерам (клетки-эффекторы естественной токсичности) отводится место «первой линии обороны». Именно естественные киллеры непосредственно участвуют в элиминации трансформированных чужеродных антигенов34. Инициативная роль естественных киллеров в системе иммунологического надзора не исключает возможность, что дефицит активности этих клеток предопределяет некоррегируемую имплантацию и развитие жизнеспособных эндометриальных фрагментов, проникших в брюшную полость вследствие ретроградной менструации. Следует отметить, что на снижение активности Т-киллеров при эндометриозе указывают многочисленные сведения литературы, в том числе и последних лет. В соответствии с этой концепцией, предполагается, что риск развития эндо-метриоза определяется двумя основными факторами:
а) интенсивностью ретроградного менструирования, определяющего количество элементов эндометрия, проникших в брюшную полость; б) уровнем компетентности защитной системы ес тественных киллеров.

А.Н. Стрижаков иА.И.Давыдов
Согласно данной гипотезе, в норме наблюдается равновесие между количеством ретроградных эндометриальных клеток и уровнем цитотоксичности естественных киллеров, конечным итогом которого является полная элиминация фрагментов эндометрия. Сдвиг этого равновесия в одну или другую сторону (первичный дефект естественных киллеров при нормальной интенсивности ретроградного менструирования или интенсификация последнего, когда даже неизмененный уровень токсичности не способен полностью инактивировать чужеродные ткани) приводит к возникновению эндометриоза. Естественно, сочетание этих факторов также обуславливает патологическую имплантацию фрагментов эндометрия (рис. 8.1).
Вместе с тем, многие вопросы, связанные с представленным патомеханизмом развития эндометриоза остаются неуточненными: во-первых, в ряде работ не обнаружена взаимосвязь между нарушениями иммунного статуса и эндометриозом31' ; во-вторых, окончательно не изучено влияние иммунных повреждений на тяжесть клинического течения заболевания (выраженность болевого синдрома, дисменорея, диспареуния, бесплодие) и, в-третьих, достоверно не установлено - является ли эндометриоз причиной или следствием нарушений иммунного гомеостаза.
Не менее противоречивы и аспекты, касающиеся развития аутоиммунных реакций у больных эндометри-
озом. В 1980 г. J.C. Weed et P. С. Arguemburger27 обнаружи-
ли отложения комплемента в эндометриоидных гетеротопиях, постулируя опосредуемое макрофагами развитие аутоиммунного ответа. В дальнейшем наличие аутоантител к ткани эндометрия при эндометриозе установлено в исследованиях как отечественных, так и зарубежных авторов, что послужило основанием для пере-
Эндометриоз. Клинические итеоретическиеаспекты
ИНТЕНСИВНОСТЬ УРОВЕНЬ РЕТРОГРАДНОГО ЦИТОТОКСИЧНОСТИ МЕНСТРУИРОВАНИЯ
©©
равновесие отсутствие
эндометриоза
нарушение равновесия
<-►©© эндометриоз
©©нарушение^> равновесия
эндометриоз нарушение
равновесия
»«в эндометриоз
Рис. 8.1. Значение интенсивности ретроградного менструирования и уровня цитотоксичности в патогенезеэндометриоза

А.Н. Стрижаков иА.И.Давыдов
смотра позиций в отношении этиопатогенеза данного заболевания и позволило рассматривать эндометриоз в качестве аутоиммунного процесса. Однако, специфичность обнаруживаемых антител вызывает определенные сомнения; более того, остается неясным, почему развитие аутоиммунной реакции не приводит к склерозированию гетеротопий.
По-видимому, на основании только показателей иммунного статуса в периферической крови не представляется возможным полностью отразить локальные процессы, определяющие состояние гомеостаза в малом тазу. Поэтому, в настоящее время особое внимание уделяется изучению биохимического профиля перитонеальной жидкости. При этом особое внимание отводится макрофагам, которые непосредственно реагируют на присутствие чужеродных элементов. Достоверно установлено, что у больных эндометриозом наблюдается не только увеличение концентрации макрофагов в перитонеальной жидкости, но и усиление их активности, в частности, способности к фагоцитозу, хемилюминесценции и т.д. Помимо прочего, зарегистрирована четкая зависимость между тяжестью течения эндометриоза и степенью выраженности макрофагальной реакции в перитонеальной жидкости19,42, а исследования последних лет обнаружили повышение содержания макрофагов и в эндометриоиднои ткани '.
Изложенное выше убеждает, что исследование тка- нево-макрофагальной реакции при эндометриозе представляет одно из наиболее перспективных направлений в изучении патогенетических аспектов возникновения и развития данного заболевания. За последнее десятилетие расшифрованы многие механизмы участия макрофагов в развитии реактивных состояний организма. Основу цитотоксического эффекта макрофагов составляет их

Эндометриоз. Клинические и теоретические аспекты
способность генерировать ряд физиологических активных агентов, инициирующих тканевое поражение. В механизме поражающего действия этих агентов выделяют три аспекта, первый из которых обусловлен генерацией клетками свободнорадикальных продуктов кислорода (супероксиданион, радикал гидроксила, хлорамин и гипохлорная кислота синтезируются в ходе коопера-
тивного взаимодействия макрофагов и тканевых элемен-
тов)18'29'30.
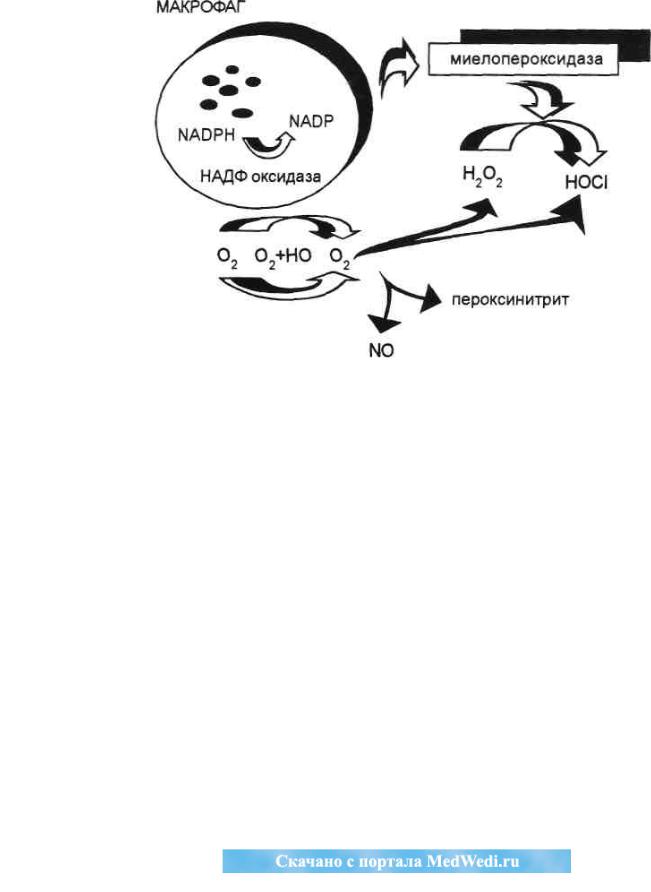
Окисление кислорода в лейкоцитах происходит с выделением достаточно токсичных продуктов - супероксиданиона и радикала гидроксила. Последние могут трансформироваться в гидроперекись водорода, которая является субстратом для не менее токсичных веществ, образующихся под влиянием высвобождающегося из макрофагов фермента миелопероксидазы - гипохлорной кислоты и хлорамина. Наконец, при взаимодействии супероксиданиона с высвобождающимся из лейкоцитов и тканей оксидом азота возможно формирование сильно токсического продукта пероксинитрита (рис. 8.2). Свободные радикалы непосредственным образом приводят к формированию периваскулярного отека в микроциркуляторном русле, способствуя тяжелым ишемическим расстройствам в тканях. После имбибиции ткани активными макрофагами свободнорадикальные продукты разрушают и клеточные структуры и волоконный каркас тканей .
Второй важный механизм поражающего действия активированных макрофагов связан с высвобождением из них нейтральных протеаз, в частности, эластазы и коллагеназы, которые содержатся в грануляционном аппарате клеток и высвобождаются при их активации. Активированные миелопероксидазои энзимы атакуют матрикс тканей, приводя к их дезорганизации16.
А.Н.СтрижаковиА.И.Давыдов
Рис. 8.2. Генерация свободнорадикальных продуктов с участием макрофагов
И, наконец, лейкоциты генерируют целый ряд физиологически активных агентов, влияющих на процессы воспаления и ишемии, а также регулирующих различные функции организма, в том числе и репродуктивную. Среди этих агентов выделяют простагландины и цитокины. Роль простагландинов в репродуктивной системы женщины нами подробно освещена в главе 5. Поэтому в данной главе изложены только концепции клинического значения цитокинов при эндометриозе.
Цитокины - соединения пептидной природы, высвобождаемые при воспалении, ишемии, иммунологических конфликтах и обладающие широким диапазоном