
МИНИСТЕРСТВО ОБЩЕГО И ПРОФЕССИОНАЛЬНОГО
ОБРАЗОВАНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
МОСКОВСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ
ДИЗАЙНА и ТЕХНОЛОГИИ
Методические указания к лабораторной работе № 84
Изучение работы полупроводниковых приборов
(диода и транзистора).
Москва - 2002
Печатается по постановлению Редакционно-издательского Совета МГУДТ.
Работа рассмотрена на заседании кафедры физики и рекомендована к печати.
Заведующий кафедрой доц. Шапкарин И.П.
Авторы: доц. Родэ С.В.
доц. Белокуров В.Н.
доц. Разинова С.М.
Методические указания к лабораторной работе №84 по разделу “Электромагнетизм”. “Изучение работы полупроводниковых приборов (диода и транзистора)”.
г. Москва
Типография МГУДТ. 2002 г.
Методические указания содержат теоретическое введение и описание практической части к лабораторной работе, связанной с изучением работы полупроводниковых приборов (диода и транзистора).
@ МГУДТ 2002
ЛАБОРАТОРНАЯ РАБОТА № 84
ИЗУЧЕНИЕ РАБОТЫ
ПОЛУПРОВОДНИКОВЫХ ПРИБОРОВ
(ДИОДА И ТРАНЗИСТОРА).
Цель работы: Ознакомление с работой полупроводникового диода и транзистора и снятие их основных характеристик.
Приборы и принадлежности: полупроводниковый диод, транзистор, измерительные приборы (вольтметры и миллиамперметры).
Теоретическое введение.
1.Строение полупроводниковых материалов, их энергетические уровни.
В зависимости от способности проводить электрический ток, твердые тела делят на проводники, полупроводники и изоляторы. Различия в проводимости между проводниками (металлами), полупроводниками и изоляторами вызваны различием в строении твердых тел и электронных оболочек атомов, из которых они состоят.
Атом любого элемента состоит из положительного заряженного ядра и движущихся вокруг ядра электронов. Заряд Z ядра определяется числом протонов. Заряд электрона по модулю равен заряду протона. Число электронов, движущихся вокруг ядра атома, равно порядковому номеру Z элемента в Периодической системе Менделеева, вследствие чего при нормальных условиях заряд атома вещества равен нулю, т.е. атом электрически нейтрален.
Электроны в атоме образуют электронные оболочки с порядковыми номерами n = 1, n = 2, n = 3, . . . . На каждой оболочке могут находиться 2 n2 электронов.
При этом каждому элементу присуще вполне определенное, характерное для него расположение электронов вокруг ядра.
Полупроводник германий Geимеет порядковый номер=32. Четыре его электронные оболочки содержат 32 электрона (рис.1). В первой ближайшей к ядру оболочке имеются два электрона, во второй - 8, в третьей - 18, в четвертой - 4. Электроны трех внутренних оболочек являются “устойчивыми” и не принимают участие в химических реакциях. Электроны, расположенные во внешней оболочке связанные с ядром атома более слабо. Их называют внешними или валентными, так как они определяют способность его атомов вступать в химическую связь с определенным числом других атомов. ВалентностьGe, имеющего во внешней оболочке четыре электрона, равна четырем.
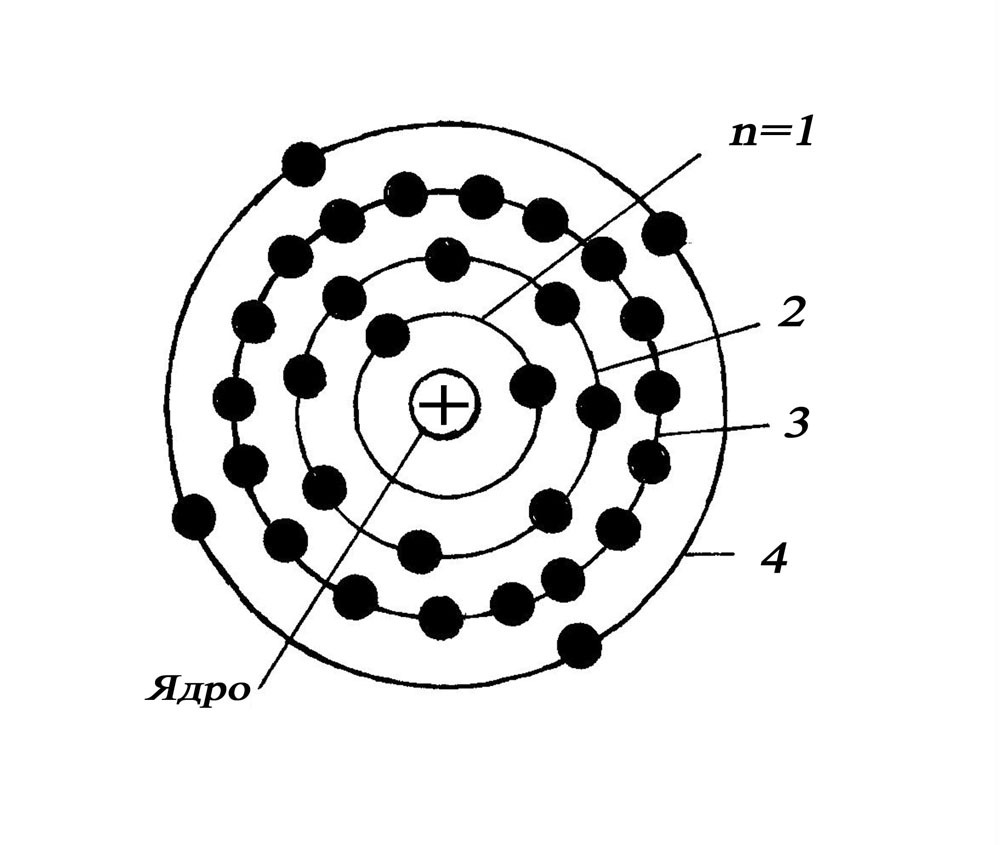
Рис.1.
Германий, кремний и другие представители полупроводников являются кристаллическими веществами: они характеризуются определенным, закономерным расположением атомов. Атомы образуют кристаллическую решетку, состоящую из отдельных элементарных ячеек.
Каждый атом германия (кремния и др.), например атом 2 на рис.2а, находится на одинаковом расстоянии от четырех соседних атомов решетки (атомов 1,3,4,5) и образует с ними ковалентные связи, известные как наиболее устойчивые. Эти четыре атома располагаются в вершинах правильного тетраэдера, в центре которого находится данный атом.
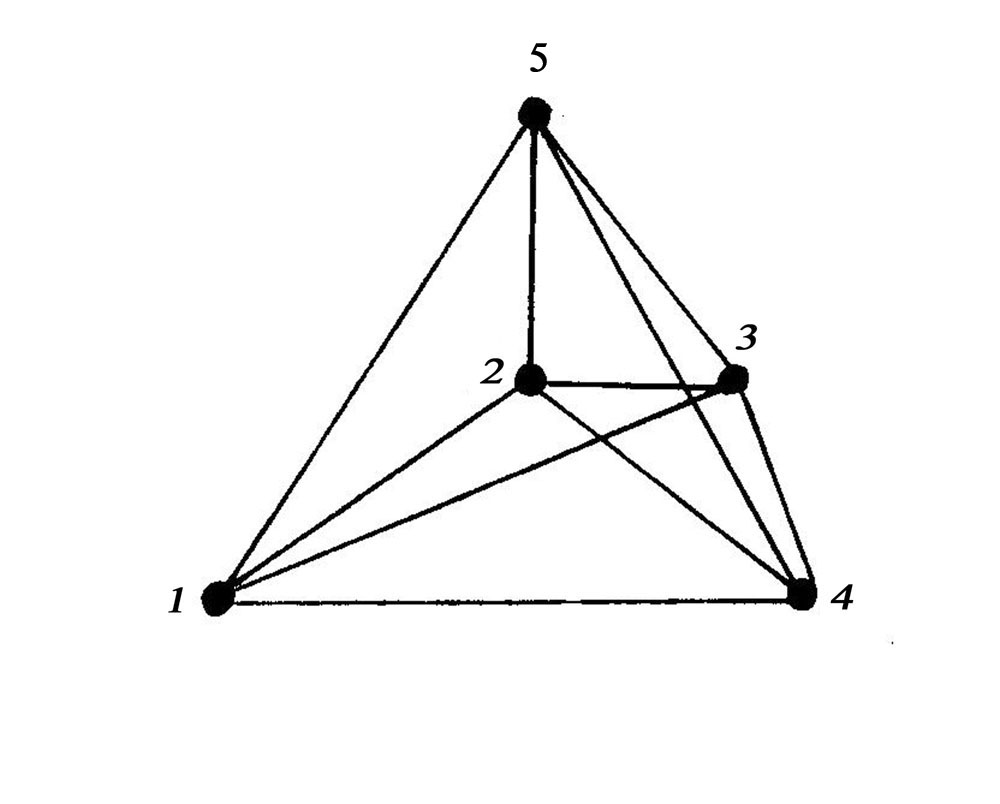
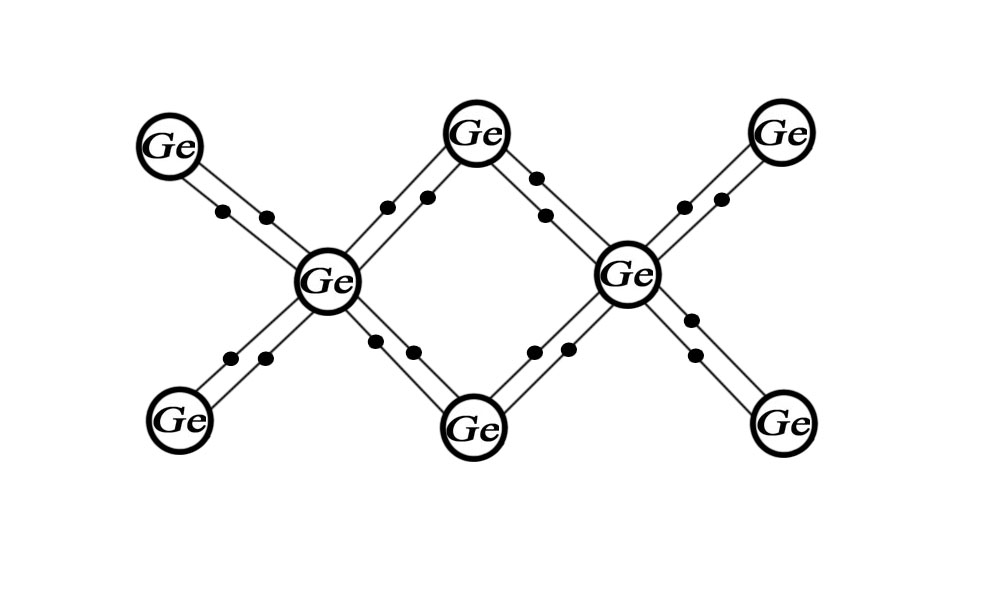
Рис.2а. Рис.2б.
На рис 2б. показана упрощенная схема связи атомов в кристаллической решетке.
Согласно законам квантовой механики, каждый электрон в атоме вещества может занимать только определенный разрешенный энергетический уровень. Все остальные энергетические уровни для данного электрона являются невозможными, как их принято называть, запрещенными.
На рис.3а графически показаны энергетические уровни электронов одного атома германия. Каждая частица, входящая в состав кристалла, взаимодействует с огромным количеством соседних частиц, причем все они находятся в непрерывном движении.
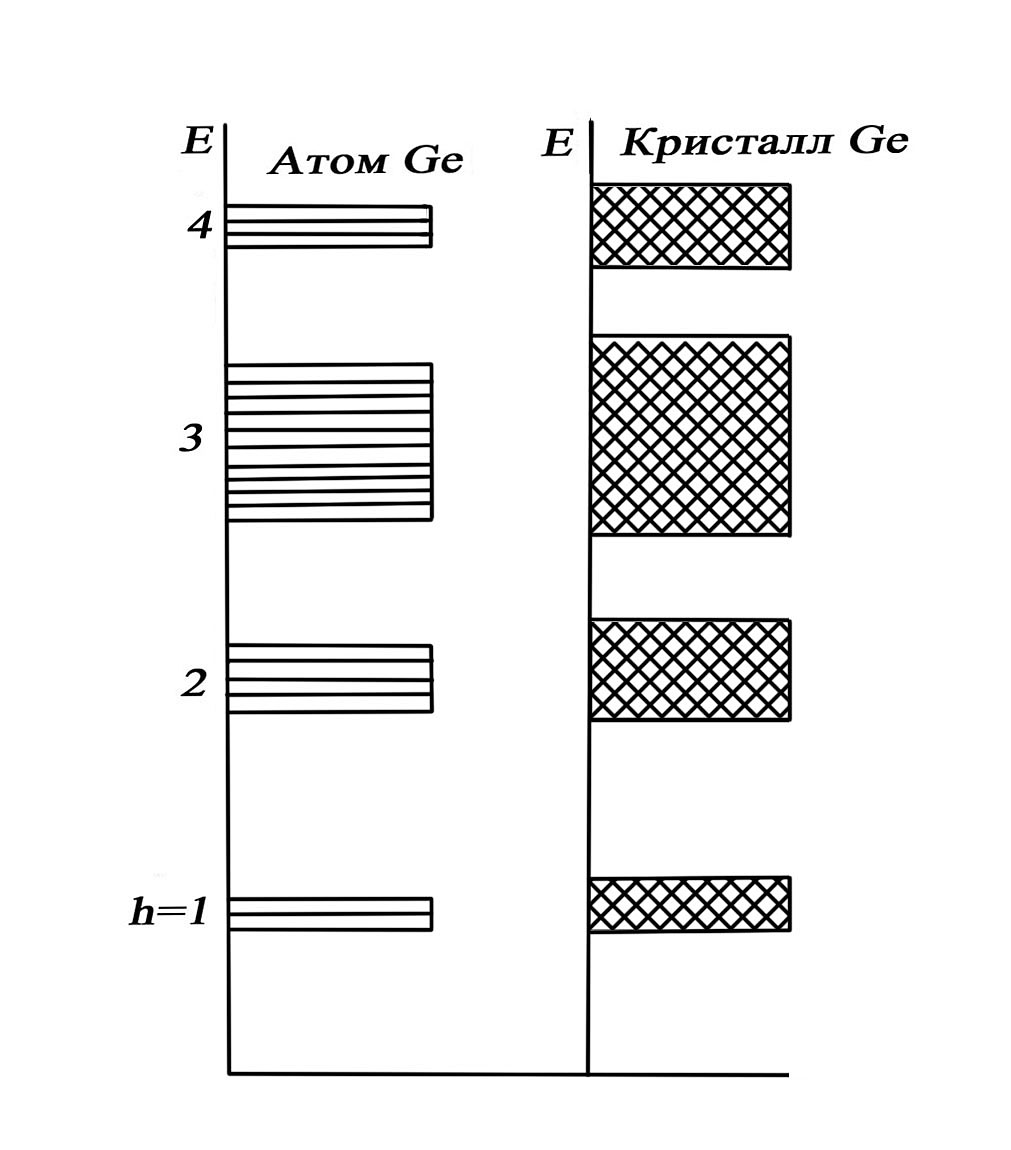
Рис.3а. Рис.3б.
Что происходит с энергетическими уровнями атомов в твердом теле?
Если сблизить два атома на расстояние меньше 1 нм, то электронные оболочки этих валентных электронов настолько перекроются, что энергетические уровни перестанут соответствовать энергетическим уровням свободного атома. При образовании кристалла происходит качественное изменение системы энергетических уровней. Если энергетические уровни электрона в изолированном атоме представляют узкие линии, то в кристалле происходит расщепление уровня. Вследствие большого числа энергетических уровней в кристалле и малого различия между ними эти уровни сливаются в непрерывные широкие разрешенные энергетические зоны, разделенные запрещенными зонами (рис.3б).
Расщепление уровней присуще всем электронам атома, для разных уровней оно различно. Структуру зон определяют расщепляющиеся уровни валентных электронов.
Наименьшей энергией ионизации обладают электроны внешней, т.е. валентной, оболочки германия, которые и определяют электропроводимость химически чистого германия. Энергетические уровни электронов образуют валентную (заполненную) зону. В этой зоне электроны находятся в устойчивом связанном состоянии. Чтобы освободить какой-либо электрон этой зоны, необходимо затратить некоторую энергию. Следовательно, электроны, находящиеся в свободном состоянии, занимают более высокие энергетические уровни. Зона более высоких энергетических уровней, расположенная выше валентной зоны и отделенная от нее запрещенной зоной, объединяет незаполненные (свободные) энергетические уровни и называется зоной проводимости.
Чтобы электрон перевести из валентной зоны в зону проводимости, необходимо сообщить ему извне энергию. Ширина запрещенной зоны, которую должен преодолеть электрон, чтобы перейти из устойчивого состояния (из заполненной зоны) в свободное состояние (в зону проводимости), является одним из главных критериев разделение твердых тел на металлы, полупроводники и изоляторы (рис. 4).
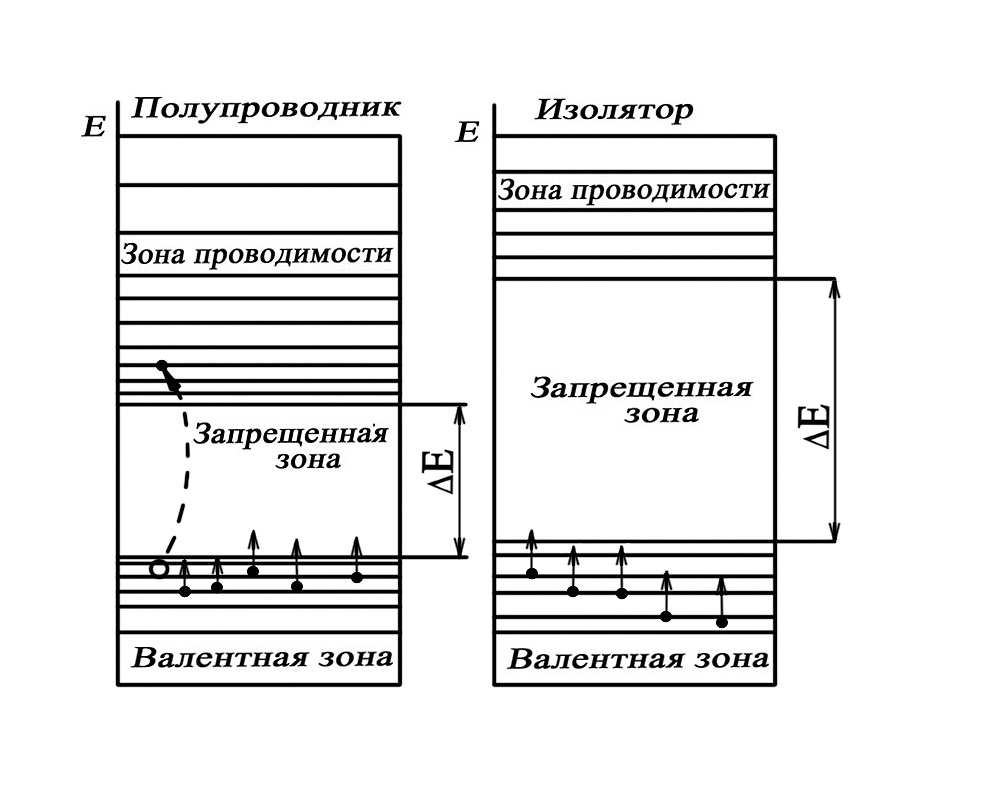
Рис.4
Высокая электропроводимость металлов объясняется отсутствием запрещенной зоны между валентной зоной и зоной проводимости и наличием при комнатной температуре достаточного количества электронов в зоне проводимости.
Чтобы вызвать электропроводимость полупроводника, т.е. перевести некоторое количество электронов из валентной зоны в зону проводимости, необходимо преодолеть запрещенную зону Е. Для этого электронам нужно сообщить энергию, не меньшую ширины запрещенной зоны. Ширина запрещенной зоны полупроводников составляет, например, 0,72 эВ для германия и 1,11 эВ для кремния. Значительная ширина запрещенной зоны изоляторов (больше 2 эВ) объясняет практическое отсутствие электропроводимости этих веществ.
