
Полезные материалы за все 6 курсов / Ответы к занятиям, экзаменам / Химия лекции
.pdf
|
|
|
|
Классификация |
|
|
|
|
|
|
|
ГЦС |
|
|
|
|
Предельные |
|
|
|
Непредельные |
||
(лактамы, ангидриды) |
|
Ароматические |
(пирролин) |
||||
|
|
|
|
|
|
||
|
Моноциклические |
|
|
Конденсированные |
|||
5-членные |
6-членные |
Бициклические |
|
Полицикли- |
|||
|
|
|
с 1-м ГА N |
N |
Трициклические |
ческие |
|
с 1-м ГА |
с 2-мя ГА |
|
|
||||
|
N |
N |
|
N |
N |
|
Резерпин, |
|
|
|
|
||||
|
|
|
|
|
H |
N |
морфин |
N |
N |
N |
N |
Пурин |
|
|
|
|
Акридин |
|
|||||
H |
H |
|
|
|
|
|
|
Пиррол ИмидаПиримиПиридин |
|
|
|
||||
|
зол |
дин |
|
|
|
|
|
Конденсированными ГЦ наз-ся соединения, молекулы которых состоят из двух и более циклов, имеющих как минимум два общих атома углерода.
Номенклатура
Сложна. Поэтому широко используются тривиальные и полутривиальные названия. Некоторые закономерности можно отметить лишь для N-содержащих ГЦ.
5-членные ГЦ с двумя гетероатомами, содержащие N, наз-ся азолами. Вид второго гетероатома обозначается приставкой. Например, ОКСА – О- оксазол, тиа – S–тиазол.
6-членные ГЦ с атомом N имеют окончание -ИН. Например, пиридИН, пиримидИН.
Производные ГЦ наз-ся и по МН, и рациональной номенклатуре. Нумерацию в кольце начинают с наиболее электроотрицательного гете-
роатома и продолжают в сторону наименьших номеров, обозначающих другой гетероатом, либо двойную связь, либо функциональную группу.
Если второй гетероатом располагается слева в кольце, то нумерацию ведут по часовой стрелке:
|
|
|
|
|
|
|
|
|
4 |
|
||
4 |
|
N 3 |
4 |
|
N 3 |
5 |
|
N 3 |
||||
5 |
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
||
2 |
5 |
2 |
6 |
2 |
||||||||
|
||||||||||||
|
N1 |
|
O 1 |
|
|
N 1 |
||||||
По рациональной номенклатуре атомы, стоящие рядом с гетероатомом,
обозначаются буквами греческого алфавита ( , , , , и т.д.) и строится |
|||||
|
|
4 |
|
|
название |
|
|
|
CH3 |
3-метилпиридин, |
|
5 |
|
|
|
||
|
|
|
3 |
-метилпиридин, |
|
|
|
|
|
||
|
|
|
|
|
|
6 |
|
N |
|
2 |
|
|
|
|
|||
|
|
1 |
|
|
|
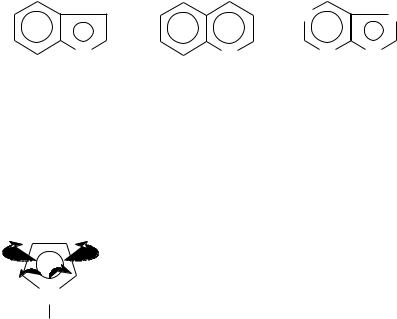
-пиколин
При нумерации конденсированных ГЦ важно определить главный цикл и атомы, участвующие в конденсации, т.к. они, как правило, не нумеруются. В конденсированных циклах с бензолом главным является ГЦ. В других конденсированных ГЦ главным является ГЦ с большим числом гетероатомов, либо больший ГЦ, если они одинаковы, то главным будет цикл, содержащий азот:
|
4 |
|
5 |
4 |
|
|
6 |
|
|
5 |
|
3 |
6 |
|
3 |
1 N |
5 |
N 7 |
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
||
6 |
|
2 |
7 |
|
2 |
|
2 |
4 |
8 |
|
|
N1 |
|
N1 |
|
|
3N |
N 9 |
|
|
7 |
8 |
|
|
|
||||
|
|
|
|
|
|
|
|
||
|
Индол |
Хинолин |
|
|
Пурин |
||||
|
|
|
Пятичленные ГЦ с одним гетероатомом |
||||||
|
|
|
|
|
|
Пиррол |
|
|
|
|
4 |
|
Ароматическое соединение. Молекула плоская, все |
||||||
5 |
|
2 |
атомы цикла находятся в sр2-гибридизации, выпол- |
||||||
|
няется правило Хюккеля. Двухэлектронная орби- |
||||||||
|
N1 |
|
|||||||
|
|
таль атома N образует шестиэлектронное облако, |
|||||||
|
|
|
|||||||
|
H |
|
поэтому |
атом |
азота |
|
не участвует в образовании |
||
связи по донорно-акцепторному механизму. Пиррол не обладает оснóвными св-вами. Он ацидофобен, т.е. способен прото-
нироваться сильными к-тами, затем полимеризуется и осмоляется.
Атом азота отдает два электрона в -электронную систему кольца, являясь ЭД заместителем I-го рода. Т.о., пиррол – электронноизбыточная система: на 5 атомов цикла приходится 6 электронов, поэтому для него наиболее характер-
ны р-ции SE, они протекают довольно легко.
Смещение электронной плотности от атома N в цикл увеличивает полярность связи N H. Пиррол – слабая к-та.
Химические св-ва
Р-ции замещения в цикле
1) Р-ции SE идут, в первую очередь, в положения 2, 5, а затем 3, 4. Это р- ции галоидирования, нитрования, сульфирования, ацилирования, алкилирования:
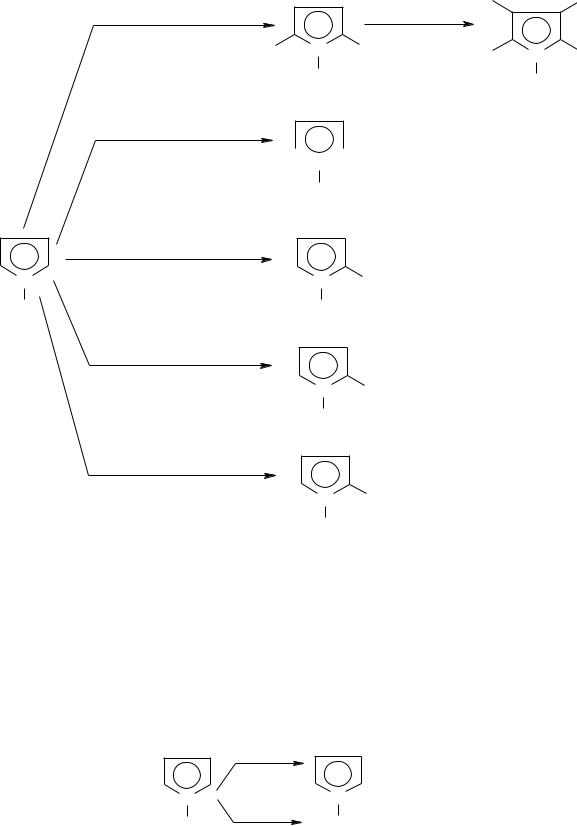
+2 Br2
-2 HBr
CH3-CO-NO2
Нитроацетат
+C5H5N.SO3, NaOH
Сульфопиридин
N
H
+CH3-CO-Cl
Ацетилхлорид
-HCl
+CH3I
-HI
|
|
|
+2 Br2 |
Br |
|
Br |
|
|
|
|
|
|
|
Br |
N |
Br |
-2 HBr |
Br |
N |
Br |
|
|
|
|
H H
2,5-Дибромпиррол 2,3,4,5-Тетрабромпиррол
+CH3COOH
 N
N 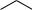 NO2 Уксусная к-та
NO2 Уксусная к-та
H
2-нитропиррол
|
+ C5H5N |
N |
SO3H |
H |
Пиридин |
|
|
2-Сульфопиррол |
|
N |
COOCH3 |
H
2-Ацетилпиррол
N CH3 H
2-Метилпиррол
2) Р-ции SN не характерны, т. к. пиррол электронноизбыточная система.
II. Кислотно-оснóвные св-ва
В связи с полярностью связи N H пиррол проявляет слабые кислотные св-ва (подобно спиртам). Он образует соли с металлическим калием и 30 % р- ром КОН.
|
2 K |
|
+ KH |
|
|
|
|
N |
KOH |
N |
+ HOH |
|
|
||
H |
|
K |
|
|
|
Пирролат калия Пирролат калия
III. Окислительно-восстановительные св-ва
Пиррол стоек к действию окислителей. При восстановлении (гидрировании) пиррола образуются продукты частичного или полного восстановления:
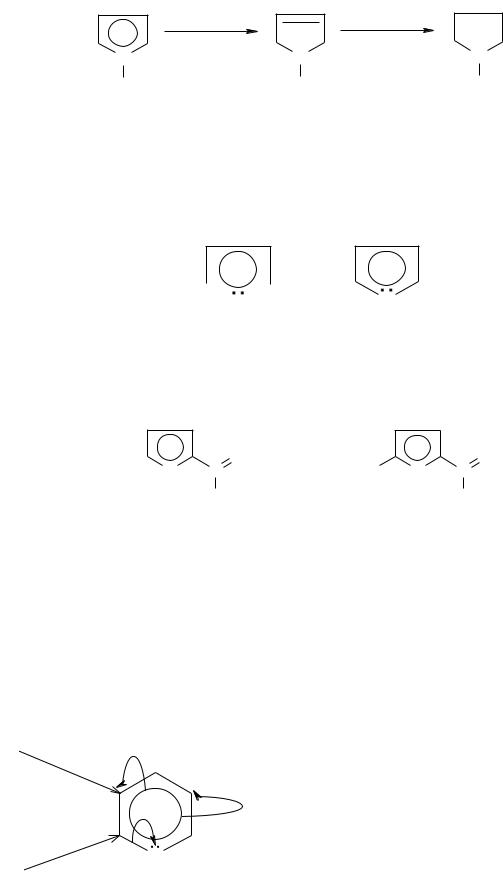
|
+H2,Cat,t,P |
+H2,Cat,t,P |
N |
N |
N |
H |
H |
H |
|
Пирролин |
Пирролидин |
Пирролидин входит в состав АК (пролин, оксипролин). Винилпирролидин полимеризуется и образует полимер перистон – заме-
нитель плазмы крови.
Фуран Тиофен
 O
O  S
S
В фуране и тиофене электронная пара атомов O и S, так же как и пиррольного атома N, включается в сопряжение с р – электронами атома углерода, образуя единую электронную систему, отвечающую правилу Хюккеля.
Наиболее важные производные фурана:
O C O |
O2N O C O |
H |
H |
Фурфурол |
5 - нитрофурфурол |
5 – нитрофурфурол является исходным вещ-вом для синтеза антибактериальных препаратов: фурацилина, фуразолидона, солафура и др.
Шестичленные ГЦ
SE |
|
|
|
|
|
|
|
|
− |
− |
|
|
|
||
|
|
|
|
SN |
+ N |
+ |
|
|
|
|
|
Пиридин
Ароматическое соединение. Молекула плоская, все атомы кольца находятся в sp2 – гибридизации, выполняется правило Хюккеля. Атом азота поставляет в -электронное облако один электрон. Т.к. атом азота более электроотрицателен, чем атом углерода, то электронная плотность кольца смещается к нему, он выполняет роль заместителя (ЭА) II-го рода. Неподеленная пара электронов гибридной р- орбитали свободна, поэтому пиридин проявляет оснóвные св-ва и не проявляет кислотные.
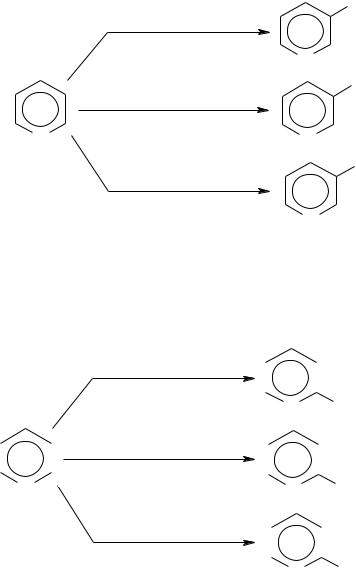
Р-ции SE протекают с трудом в - положения, р-ции SN протекают легче и преимущественно в – положения.
Химические свойства
I Р-ции замещения в цикле
1) Р-ции SЕ (нитрование, сульфирование, галоидирование)
|
|
+HO-NO2,H2SO4,t |
NO2 |
|
|
|
|
||
|
|
-H2O |
3-Нитропиридин |
|
|
|
N |
||
|
|
|
||
− |
− |
+HO-SO3H,t |
SO3H |
|
3-Сульфопиридин |
||||
|
|
-H2O |
||
|
N |
N |
||
|
|
|||
|
|
+Br2, Cat, t |
Br |
|
|
|
3-Бромпиридин |
||
|
|
|
||
|
|
-HBr |
N |
|
|
|
|
–NO2, –SO3H, –Br группы входят в 3,5 – положения, как и для бензола с ЭА заместителем.
2) Р-ции SN |
|
+ − |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+KOH кристал., t |
|
|
|
|
2-Гидроксипиридин |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-KH |
|
|
N |
|
OH |
|
|
|
|
|
|
|
|
||
|
|
|
+ |
CH3ONa, t |
|
|
|
|
2-Метоксипиридин |
|
|
|
|
|
|
|
|||
+ |
|
|
метилат натрия |
|
|
|
|
||
.. |
|
|
|
|
|
|
|||
|
N |
|
-NaH |
|
|
N |
|
OCH3 |
|
|
|
|
|
NaNH2 амид натрия, t |
|
|
|
|
2-Аминопиридин |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-NaH |
|
|
N |
|
NH2 |
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
||
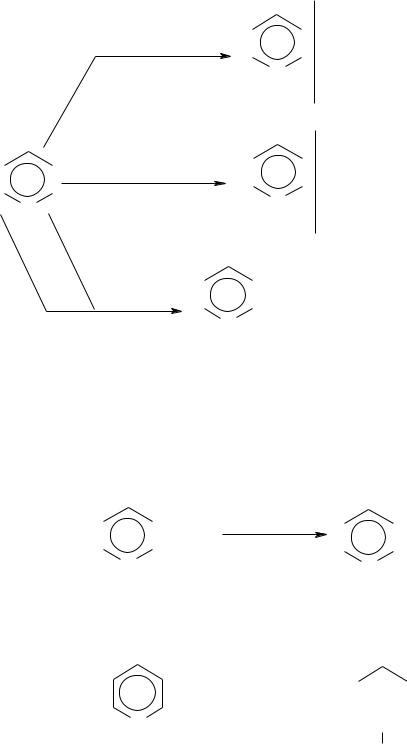
II. Кислотно-оснóвные св-ва
Атом азота имеет неподеленную электронную пару на гибридной орбитали, поэтому подобно аминам пиридин проявляет оснóвные св-ва, образуя соли с к-тами, и нуклеофильные св-ва, присоединяя другую положительную частицу:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
+ |
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
+ - |
|
|
+ - |
|
|
|
|
|
|
+ |
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
+ HCl + HCl |
|
|
|
|
Cl- |
|
|
|
|
Cl-Cl− |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
N Хлорид пи иния диния |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
H |
|
|
|
|
|
Хлорид пири- |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|
+ |
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
+ - |
+ - |
|
|
|
|
|
|
+ |
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
+ HOH+ HOH |
|
|
|
|
Br- |
|
|
|
|
Br-OH− |
||||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
N |
N |
|
|
|
|
|
N |
|
|
|
|
N |
|
|
|
|
|
|
- |
|||||||||
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H ГидроксидГидроксидпир пиридиния |
||||||||||||
|
|
+ - |
|
+ - |
|
|
|
|
|
|
|
|
+ |
|
|
|
+ |
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
CH I |
CH I |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
3 |
|
|
3 |
|
|
|
|
|
|
|
|
NI |
- |
|
|
|
|
I |
- |
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
Йодистый метилпиридиний |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Йодистый метилпиридиний |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
CH3 |
|
|
|
|
|
|
|
|
|
||||
III. |
Окислительно-восстановительные св-ва |
|||||||||||||||||||||||||||
Наличие сопряженной системы делает пиридин стойким к действию |
||||||||||||||||||||||||||||
окислителей. Однако гомологи окисляются легко, образуя к-ты: |
||||||||||||||||||||||||||||
|
|
|
|
|
|
CH |
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
COOH |
|||
|
|
|
|
|
|
|
|
|
|
|
|
K2Cr2O7, t |
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
+ 3O |
|
-H2O |
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
4-Метилпиримидин |
|
|
4-Пиридинкарбоновая к-та |
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
изоникотиновая к-та |
||||||||
Р-ция восстановления, как и бензола, протекает в жестких условиях:
Cat, t, P
+ 3H2 

 N
N  N
N 
H
Пиперидин
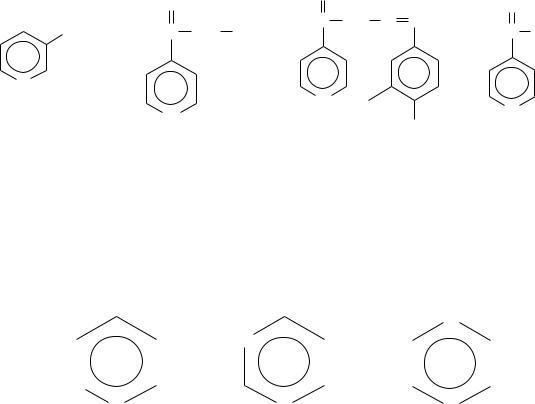
Пиперидин входит в состав анестетика промедола. Производные пиридина: алкалоиды, витамины В1, РР, ферменты, лекарственные противотуберкулезные и др. препараты:
|
O |
O |
|
|
O |
|
|
|
|
|
|
||
COOH |
C NH NH2 |
C |
NH N |
CH |
C |
N(C2H5)2 |
|
|
|
||||
N |
|
|
|
|
|
|
|
|
N |
H3CO |
|
N |
|
|
N |
|
OH |
|
||
|
|
|
|
|
|
|
Никотиновая к-та, |
|
|
|
|
|
|
Витамин РР |
Тубазид |
|
Фтавизид |
|
Кордиамин |
|
|
|
|
|
|
|
|
Шестичленные ГЦ с двумя гетероатомами
Из этой группы ГЦС наиболее важным являются ГЦ, содержащие два атома N. Они имеют общее название диазины и различаются взаимным расположением атомов N:
|
|
4 |
|
|
4 |
|
|
|
N |
|
|
|
|
|
|
|
|
4 |
|
||
|
3 |
|
|
N 3 |
|
|
|
|
|
|
|
5 |
|
5 |
|
|
3 |
5 |
|
||
|
2 |
6 |
|
2 |
6 |
|
|
2 |
6 |
|
N |
|
|
|
|
||||||
|
|
|
|
|
|
|||||
1 |
|
|
1 |
|
|
|
|
|||
|
|
|
|
|
|
|
1 |
|
||
|
|
N |
|
N |
|
|
N |
|||
Пиридазин, |
Пиримидин, |
|
Пиразин, |
|||||||
1,2- диазин |
1,3- диазин |
1,4- диазин |
||||||||
Все эти изомеры содержат сопряженную шестиэлектронную систему, ароматичны. Наличие двух атомов N в кольце еще больше, чем в пиридине, понижает электронную плотность на атомах углерода. Это приводит к снижению реакционной активности диазинов в р-циях SE и, напротив, облегчает р-ции SN по сравнению с пиридином. При этом уменьшаются и оснóвные св-ва диазинов. Они являются очень слабыми основаниями и образуют соли только с одним эквивалентом сильной к-ты, несмотря на наличие двух центров основности.
Среди производных диазинов, имеющих биологическое значение и применяемых в медицине, наиболее важными являются гидрокси- и аминопроизводные пиримидина. К ним, в первую очередь, относятся нуклеиновые основания и барбитуровая к-та.
Пиримидиновые нуклеиновые основания
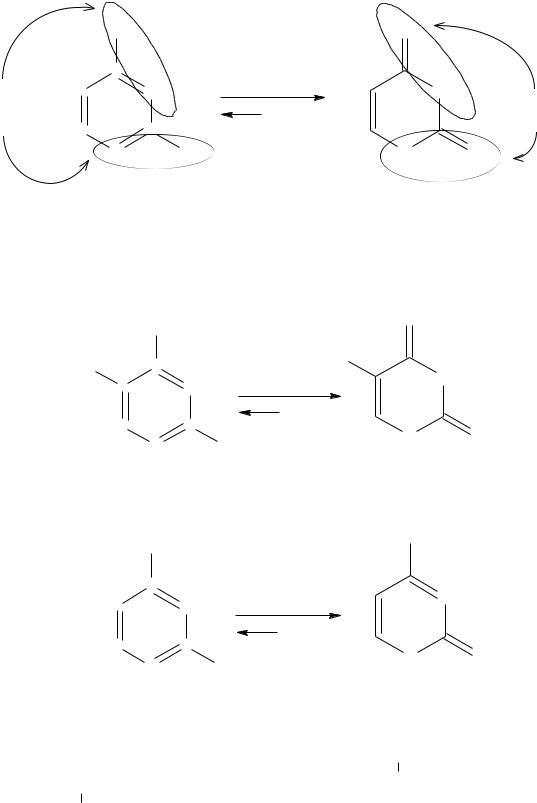
Производные пиримидина – урацил, тимин и цитозин – наз-ся нуклеиновыми основаниями, т.к. являются компонентами нуклеиновых к-т (НК). Эти производные существуют в лактимной и лактамной таутомерных формах, причем в равновесной системе преобладают лактамные формы:
|
OH |
|
O |
|
||
|
4 |
|
|
|
|
|
ЛактИМные |
5 |
N 3 |
|
NH |
ЛактАМные |
|
|
|
|
|
|||
фрагменты |
6 |
2 |
|
|
фрагменты |
|
|
|
|
|
|||
|
N |
OH |
|
N |
O |
|
|
1 |
|
|
H |
|
|
|
|
|
|
|
||
|
Урацил, |
|
2,4-Диоксипиримидин |
|||
2,4-дигидроксипиримидин |
||||||
|
|
|||||
|
|
|
|
H2O |
|
|
|
|
5 – Фторурацил – противораковое средство |
||||
|
|
OH |
|
O |
|
|
|
|
|
|
|
||
|
H3C |
4 |
|
H3C |
|
|
|
|
|
NH |
|
||
|
5 |
N 3 |
|
|
||
|
|
|
|
|||
|
6 |
2 |
|
N |
O |
|
|
|
N |
OH |
|||
|
|
H |
|
|||
|
|
1 |
|
|
||
|
|
|
|
|
||
|
|
Тимин, |
|
2,4-Диоксо-5- |
||
|
|
Тимин, |
|
2,4- |
|
|
2,4-диокси-5-метилпиримидин, |
метилпиримидин |
|||||
|
2,4-диокси-5-Метилпир |
Диоксо-5-метил |
||||
|
5-метилурацил |
|||||
|
имидин,5-метилурацил |
пиримидин |
|
|||
|
|
NH2 |
|
NH2 |
|
|
|
|
|
|
|
||
|
|
4 |
|
N |
|
|
|
5 |
N 3 |
|
|
||
|
|
|
|
|||
|
6 |
2 |
|
N |
O |
|
|
|
N |
OH |
|||
|
|
H |
|
|||
|
|
1 |
|
|
||
|
|
|
|
|
||
|
|
Цитозин, |
|
4-Амино-2-оксо- |
||
|
4-амино-2-оксипиримидин |
пиримидин |
|
|||
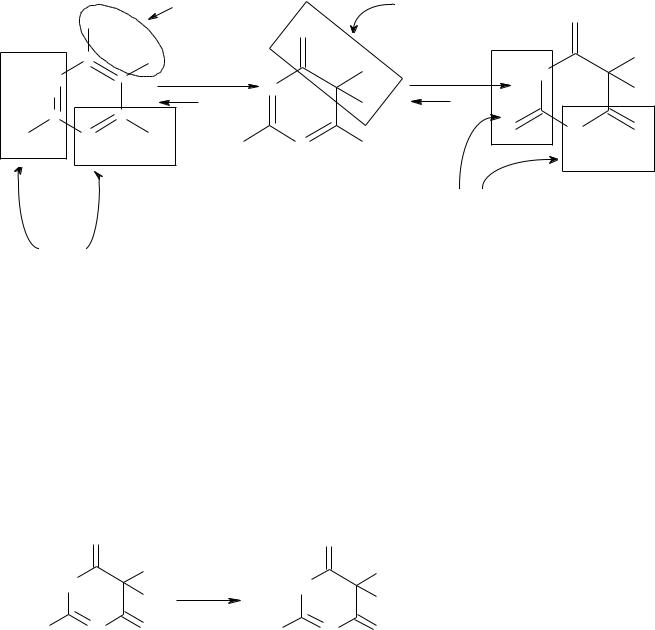
Барбитуровая к-та
Она может существовать в нескольких таутомерных формах, из которых изобразим только три:
|
|
|
Енольный фрагмент |
|
Кетонный |
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
O |
фрагмент |
O |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
4 |
|
H |
|
|
|
|
H |
|
|
|
|
H |
HN |
|
||
|
N |
5 |
|
|
|
|
||
|
|
|
|
|
|
|||
|
|
N |
|
|
|
H |
||
|
3 |
|
|
|
|
|
||
|
|
|
|
|
|
|
||
|
2 |
6 |
|
|
|
H |
|
|
|
|
|
|
|
|
|
||
HO |
N |
|
OH |
|
|
O |
N |
O |
|
HO |
N |
OH |
H |
|
|||
|
1 |
|
|
|
||||
|
|
Тригидрокси- |
|
|
|
Триоксо- |
|
|
|
|
|
форма |
|
|
Лактамные |
|
|
|
|
|
|
|
форма |
|
||
|
|
|
|
|
|
фрагменты |
|
|
|
|
|
|
|
|
|
|
|
Лактимные
фрагменты
Барбитуровая к-та проявляет сразу два вида таутомерии лактимлактамную и кето-енольную. Следовательно, структуру барбитуровой к-ты можно представить и как 2,4,6 – тригидроксипиримидин (тригидроксиформа), и как 2,4,6 – триоксопиримидин (триоксоформа).Преобладающий таутомер – триоксоформа. Подвижность атомов водорода, особенно в енольной гидроксильной группе обусловливает кислотные св-ва барбитуровой к-ты, которая является, более сильной, чем уксусная. Производные барбитуровой к-ты, содержащие заместители у атома С–5, наз-ся барбитуратами и применяются в качестве снотворных средств:
O |
|
O |
|
R |
+NaOH |
R |
|
HN |
HN |
||
R' |
-H2O |
R' |
|
HO N O |
NaO N O |
||
|
|||
Барбитураты |
|
Натриевая соль |
|
|
барбитуратов |
||
|
|
Барбитал: (веронал)
R=R =C2H5 –
Фенобарбитал:
R=C2H5 - ,
R =C6H5 - .
Для барбитуратов невозможна кето-енольная таутомерия, т.к. в молекуле отсутствуют атомы водорода при С–5. Барбитураты проявляют более слабые кислотные св-ва, чем свободная барбитуровая к-та, и со щелочами образуют водо-растворимые соли.
Конденсированные ГЦС
Важнейшая конденсированная система пурин состоит из двух сочлененных колец – имидазола и пиримидина. Пурин – ароматическое соединение: имеет плоский цикл, все атомы цикла находятся в sp2 – гибридизации, сопря-
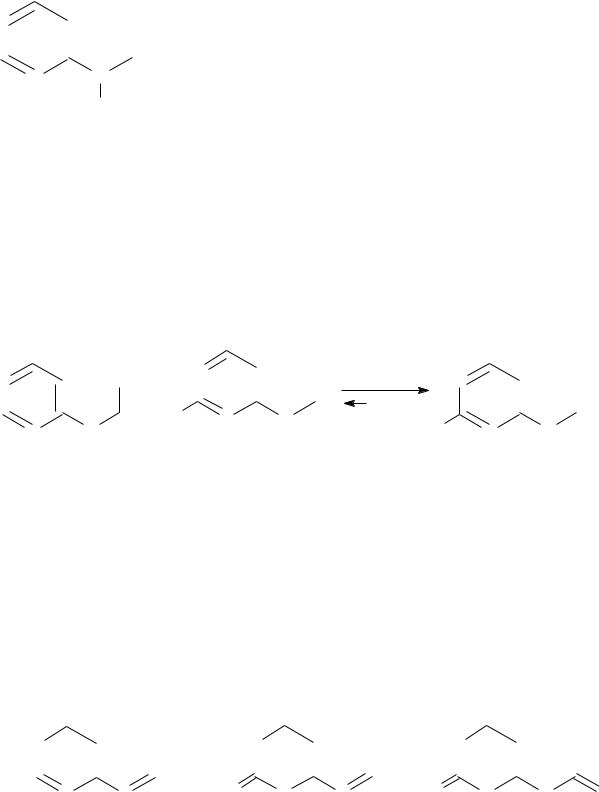
женная система, состоящая из 10 р–электронов, включая неподеленную пару электронов у атома N-9, что отвечает правилу Хюккеля (4n+2=10, n=2).
|
|
|
|
|
|
|
|
|
|
Пурин – бесцветное кристаллическое вещ-во, т. пл. 216- |
:N |
6 |
5 |
|
|
|
|
N : |
2170С, хорошо растворимо в воде, плохо – в эфире, хло- |
||
|
|
|
||||||||
|
1 |
|
|
|
7 |
|
|
|
роформе. |
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
2 |
3 |
4 |
|
9 |
8 |
|
|
|
Пурин амфотерен благодаря циклу имидазола и образует |
|
|
|
|
|
||||||
|
|
|
|
.. |
|
|
|
|
||
|
|
N |
|
|
N |
|
|
|
|
соли с сильными к-тами за счет пиридиновых атомов |
|
|
.. |
|
|
|
|
|
|
|
|
Hазота и с основаниями за счет –NH кислотного центра имидазола.
Пуриновая система входит в состав многих биологически важных соединений: HK, витаминов, алкалоидов, лекарственных средств. К наиболее значимым производным пурина относятся гидрокси- и –аминопурины.
Пуриновые нуклеиновые основания
В состав НК входят нуклеиновые основания аденин и гуанин. Из двух таутомерных форм гуанина (лактимная и лактамная) более устойчивой является
лактамная, в виде которой гуанин входит в состав НК. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
NH |
2 |
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
||||
|
|
NH |
|
|
|
|
|
|
|
|
|
OH |
Лактимная форма |
|
|
|
|
|
|
O |
|
|
|
Лактамная форма |
||||||||||||||
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
||||||||||||||||
|
|
NH6 2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
6 |
|
5 |
|
|
|
|
7 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
6 |
|
|
5 |
|
|
|
7 |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
7 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
7 |
|||||||
N |
|
|
|
5 |
|
|
N |
|
N |
|
|
N |
HN |
|
|
|
|
|
6 |
|
|
5 |
|
|
|
|
|
N |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
N |
7 |
|
|
|
|
|
|
N |
|
N |
|
|
|
N |
HN |
7 |
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
||||||||
7 |
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
7 |
|
|
|
|
|
|
|
|
|
|
|
|
N |
|||
N |
6 |
5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
6 |
|
5 |
|
|
|
|
|
|
||||||||||
2 |
1 |
|
|
|
|
|
7 |
|
|
8 |
|
|
|
|
|
|
|
|
|
|
|
2 1 |
|
|
|
|
|
|
|
|
|
|
7 |
|
|
|
||
|
3 |
|
|
4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
3 |
|
|
4 |
|
|
|
|
|
8 |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
2 |
|
3 |
|
|
|
|
|
|
8 |
H N |
|
|
|
|
|
|
|
|
H N 2 |
|
3 |
|
|
|
|
|
|
|
8 |
|||||||||
|
2 |
N |
44 |
N |
8 |
|
|
|
|
|
|
|
|
|
|
|
4 |
|
4 |
|
|
8 |
|
|
|
|||||||||||||
|
|
N3 |
|
|
99 |
|
|
|
|
H 2N |
|
|
|
|
|
|
|
|
H N |
|
|
|
3 |
|
|
|
9 |
9 |
|
|
|
|||||||
|
|
|
|
N 9 |
|
|
|
|
|
|
|
|
|
N |
2 |
|
|
|
|
|
|
|
N |
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
2 |
|
N |
|
|
|
|
|
N |
|
|
|
|
9 |
|
|
|
||||||||||||
|
|
N |
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
H2N |
|
|
|
N |
|
|
|
N |
|
|
|
|
|||||||
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
||||
|
|
|
|
|
|
HH |
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
HH |
|
|
|
|
|||||
Аденин, Аденин, 6-аминопурин 6-аминопурин
Следует отметить, чтолактимнаяв отличиеформаот самого пуриналактамнаяатом водородаформа в аде-
лактимная форма лактамная форма
нине и гуанине зафиксирован в положении 9. В такой форме эти основания связаны с остатком углевода в нуклеозидах и НК.
Гидроксипроизводные пурина
Это гипоксантин, ксантин и мочевая к-та – продукты превращения в организме НК.
|
O |
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|||
|
|
|
|
|
|
NH |
HN |
|
|
|
|
|
NH |
HN |
|
|
|
|
|
|
NH |
|
|||
HN |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
N |
O |
N |
|
N |
O |
N |
|
N |
O |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
H |
|
H |
|
|||||
|
Гипоксантин, |
|
|
Ксантин, |
|
|
Мочевая к-та, |
|
|||||||||||||||||
6-гидроксипурин |
2,6-дигидроксипурин |
2,6,8-тригидроксипурин |
|||||||||||||||||||||||
