
Полезные материалы за все 6 курсов / Ответы к занятиям, экзаменам / Химия лекции
.pdf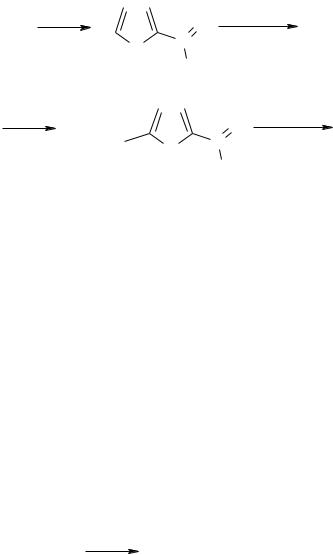
IV. Специфические р-ции
1. Действие разб. р-ров щелочей Эпимеры: глюкоза, фруктоза и манноза легко превращаются друг в друга,
образуя равновесные системы. Этот процесс наз-ся эпимеризацией.
2. Действие конц. р-ров к-т |
|
|
|
||||||||||
Конц. р-ры НС1 и Н2SО4 |
вызывают дегидратацию моносахаридов: из пен- |
||||||||||||
тоз образуется фурфурол, из фруктозы – 5-гидроксиметилфурфурол. |
|||||||||||||
C H O |
|
|
t |
|
|
|
|
|
O |
Анилин, t |
|||
|
|
|
|
|
|
|
|||||||
5 |
|
|
|
|
|
|
|
|
|
Красное окрашивание |
|||
5 |
10 |
-3H2O |
|
|
|
|
C |
|
|
|
|||
|
|
|
|
O |
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
Рибоза |
|
|
|
Фурфурол |
|
|
|
||||||
|
|
|
|
|
|
|
|
||||||
C6H12O6 |
|
t |
|
|
|
|
|
|
|
|
|
O |
Резорцин, t |
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
Красное окрашивание |
|||
|
|
|
|
|
|
|
|
|
|
|
|||
-3H2O |
HOCH2 |
|
|
|
|
C |
|
||||||
|
|
|
O |
|
(р-ция Селиванова) |
||||||||
H
Фруктоза |
5-Гидроксиметил- |
|
|
|
фурфурол |
3. Брожение Это распад моносахаридов под действием ферментов микроорганизмов,
приводящий к образованию различных продуктов. В зависимости от конечного продукта различают:
а) спиртовое брожение
фермент
C6H12O6  2C2H5OH + 2CO2
2C2H5OH + 2CO2
Этанол
б) молочнокислое
фермент
C6H12O6  2CH3-CH(OH)-COOH
2CH3-CH(OH)-COOH
Молочная к-та
в) масляное
фермент
C6H12O6 |
CH3-CH2-CH2-COOH + 2H2 + 2CO2 |
Масляная к-та
Используемая литература:
1.Биоорганическая химия: учебник / Н.А. Тюкавкина, Ю.И. Бауков, С.Э. Зурабян. – М.: ГЭОТАР-Медиа, 2010. – 416 с.;
2.Органическая химия: учеб. Пособие для вузов/ А.М. Ким. – 4-е изд., испр. И доп. – Новосибирск: Сиб. Унив. Изд-во, 2004. – 844 с.

ЛЕКЦИЯ 3
Тема: Биологически активные высокомолекулярные вещества: углеводы 2
Цель лекции: изучение строения и химических свойств ди - и полисахаридов и их роль в организме.
Содержание: Строение, изомерия, химические свойства ди- и полисахаридов. Дисахариды. Восстанавливающие и невосстанавливающие дисахариды: сахароза; мальтоза; лактоза. Строение молекулы, химические свойства. Полисахариды живых организмов. Гликоген. Крахмал. Понятие о кислых гетерополисахаридах. Биологическая роль углеводов в организме.
Олигосахариды - это углеводы, содержащие в молекуле 2-10 моносахаридных остатков. Наиболее важны дисахариды, то есть сахариды, содержащие два моносахаридных остатка. К ним относятся сахароза, мальтоза, лактоза и целлобиоза. При гидролизе их образуется два моносахарида. Сахароза – невосстанавливающий дисахарид, остальные – восстанавливающие. Все дисахариды являются гликозидами и содержат в своем составе –D–глюкозу.
Молекула сахарозы состоит из –D–глюкозы и –D–фруктозы:
6
CH2OH |
|
|
|
|
|
5 |
O |
|
|
CH2OH |
|
|
|
|
|
||
4 OH |
|
1 |
|
O |
|
|
2 |
|
|
|
|
3 |
OH |
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
-D-Глюкоза |
|
|
OH |
Гликозид - |
|
|
|
|
–H2O |
гликозидная связь |
|
|
|
|
|
||
6 |
|
|
HOH2C |
O |
|
HOH2C |
O |
OH |
|
||
|
|
|
|||
5 |
H |
2 |
|
H |
H2OH |
|
H2OH |
|
|
||
4 |
3 |
|
|
|
|
|
|
1 |
|
|
|
OH |
|
|
|
OH |
|
|
|
|
|
|
|
-D-Фруктоза -D-Глюкопиранозил-(1→2)- -D-фруктофуранозид
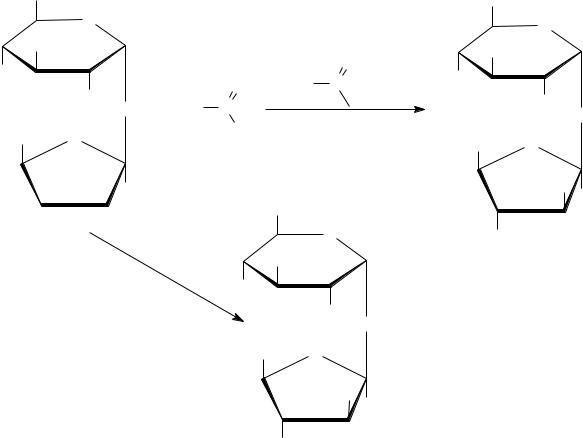
При образовании сахарозы оба моносахарида участвуют своими полуацетальными гидроксилами. Поэтому циклическая форма будет закреплена и оксоформа (открытая) не образуется. Такой сахар обладает свойствами многоатомного спирта и гликозида. Восстанавливающие свойства отсутствуют : проба Троммера и реакция Толленса отрицательны. Подобно моносахаридам сахароза вступает в р-ции с Ме (активным), образует простые и сложные эфиры, дает качественную р-цию с Сu(ОН)2 – синее окрашивание:
CH2OH
O
OH
OH |
O |
+ 8 CH3 |
|
HOH2C O
|
|
H |
|
H2OH |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
+8 CH3I |
|||
|
|
|
|||
|
|
|
–8 HI |
||
|
|
CH3 |
|
== R |
|
|
|
|
|||
|
|
|
CH2OAc |
|
|
|
|
O |
|
|
O |
|
OAc |
|
|
|
|
|
|
O |
CH3 C |
== Ac |
|
|
C |
|
|
OAc |
O |
|
– 8 HCl |
|
|
|
Cl |
|
|
|
|
|
AcOH2C |
O |
|
|
|
|
|
||
|
|
|
Ac |
H2OAc |
|
CH2OR |
|
|
|
|
|
|
|
|
|
O |
|
OAc |
|
|
OR |
Окта-О-ацетилсахароза |
||
OR
O
ROH2C O
R
H2OR
OR
Окта-О-метилсахароза
Сахароза, как гликозид, легко гидролизуется в кислой среде с образованием –D–глюкозы и –D–фруктозы. При этом происходит изменение угла вращения поляризованного света. Сахароза обладает правым вращением (+66,50), образующаяся фруктоза – левым (-920), глюкоза – правым (+52,50). Разница – -400.
Это явление называется инверсией сахара. Смесь глюкозы и фруктозы – инвертным сахаром. Природный инвертный сахар – мед.
Сладость сахарозы принята за 1, тогда фруктоза имеет сладость 1,73, глюкоза – 0,74, сорбит – 0,6, маннит – 0,4.
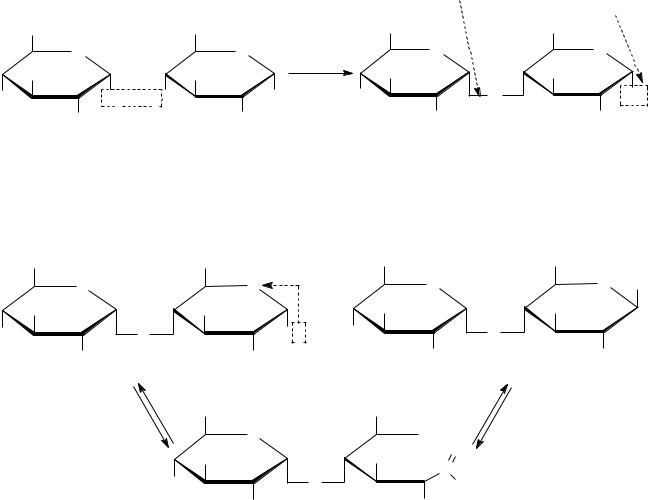
Специфические реакции
1.Сахароза после гидролиза дает положительную реакцию Селиванова, так как при гидролизе образуется фруктоза.
2.Проба Троммера и реакция Толленса отрицательны, так как в щелочной среде сахароза не гидролизуется.
Сахароза применяется в медицине для приготовления порошков, таблеток, сиропов, микстур и пр.
Важнейшими представителями восстанавливающих дисахаридов являются мальтоза, лактоза и целлобиоза.
|
|
|
|
|
|
-Гликозидная связь |
|
|
|
|
|
|
|
Полуацетальный гидроксил |
|
CH OH |
|
|
|
CH OH |
|
CH2OH |
CH2OH |
2 |
|
|
|
2 |
|
|
|
|
O |
|
|
O |
|
O |
O |
OH |
1 |
+ |
4 |
OH |
– H2O |
OH |
OH |
|
|
|
|
|
|
OH |
|
|
|
OH |
HO |
OH |
|
O |
|
|
OH |
|
|
OH |
|
OH |
OH |
|
|
|
-D-Глюкоза |
|
Мальтоза, |
|
|
|
|
|
|
|
|
-D-Глюкопиранозил-(1→4)- -D-глюкопираноза |
|
В растворе мальтоза существует в виде циклической и открытой формах (3 формы) за счет мутаротации:
CH OH |
CH OH |
CH2OH |
CH2OH |
2 |
2 |
|
|
O |
O |
O |
O OH |
OH |
OH |
OH |
OH |
O |
OH |
|
O |
OH |
OH |
OH |
OH |
-Циклическая форма |
-Циклическая форма |
||
|
CH2OH |
CH2OH |
|
|
O |
OH |
|
|
OH |
OH |
O |
|
|
||
|
|
C |
|
|
|
O |
H |
|
|
|
|
|
OH |
OH |
|
Открытая форма
Химические свойства
Мальтоза – это альдегидо-спирто-гликозид.
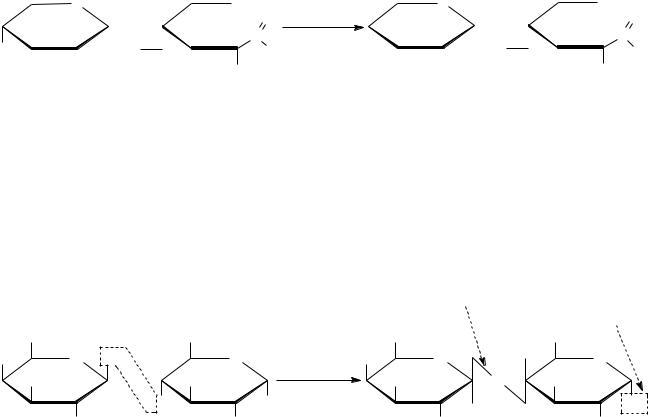
I. Реакции открытой формы по -С группе. Мальтоза дает все реакции по альде-
гидной группе с HCN, NH2OH, NH2–NH2, восстановления, окисления. Проба Троммера и реакция Толленса положительны:
CH OH |
|
|
CH OH |
|
|
CH OH |
|
|
CH2OH |
|
|||||||
|
2 |
|
|
|
|
2 |
|
Cu(OH)2, |
|
|
2 |
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
O |
|
|
|
|
OH |
|
|
O |
|
|
|
|
||||
|
|
|
|
|
OH–, t |
|
|
|
|
|
|
||||||
OH |
|
|
OH |
O |
OH |
|
|
OH |
O |
||||||||
|
|
|
|
O |
|
|
C |
– Cu2O , |
|
|
|
|
|
O |
|
|
C |
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
OH |
|||
|
|
|
|
|
|
Красный |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
OH |
|
|
|
|
OH |
–2 H2O |
|
|
OH |
|
|
|
|
OH |
||
|
|
|
|
|
|
|
|
|
|
Мальтобионовая кислота |
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||
Углеводы, дающие положительную пробу Троммера, называются восстанавливающими.
II. Реакции по – ОН гр. аналогичны реакциям для сахарозы.
III. Мальтоза гидролизуется в кислой среде с образованием 2-х молекул глюкозы.
|
|
|
|
|
|
-Гликозидная связь |
|
|
|
|
лактоза |
|
|
|
Полуацетальный гидроксил |
||
|
6 |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
CH2OH |
|
|
CH2OH |
|
CH2OH |
|
CH2OH |
OH |
5 |
O |
OH |
O |
OH |
O |
|
O |
|
|
|
|
|
|
|
|
|
4 OH |
1 |
+ |
4 OH |
–H2O |
OH |
O |
OH |
|
|
3 |
2 |
HO |
OH |
|
|
OH |
|
|
|
|
|
|||||
|
|
|
|
|
|
|||
|
|
OH |
|
OH |
|
OH |
Лактоза, |
OH |
-D-Галактоза |
|
-D-Глюкоза |
|
|
|
|||
|
-D-Галактопиранозил-(1→4)- -D-глюкопираноза |
|||||||
|
|
|
|
|
||||
Лактоза существует в растворе в виде трех форм : двух циклических и одной открытой. Лактоза восстанавливающий дисахарид и обладает всеми
свойствами, характерными для мальтозы. Лактоза содержится в женском молоке и способна подавлять рост бактерий.
Полисахариды
Это высокомолекулярные углеводы, содержащие сотни и даже тысячи моносахаридных остатков.
Из полисахаридов широко известны целлюлоза, крахмал и гликоген. Они построены из одного и того же моносахарида – D-глюкозы. Общая формула
(С6Н10О5)n.
Целлюлоза (клетчатка) – самый распространенный не только полисахарид, но и органическое вещество в природе. Древесина примерно на 50% состоит из целлюлозы, а хлопок и лен представляют практически чистую целлюлозу.
В целлюлозе остатки D–глюкопиранозы связаны между собой –(1→4) – гликозидной связью:
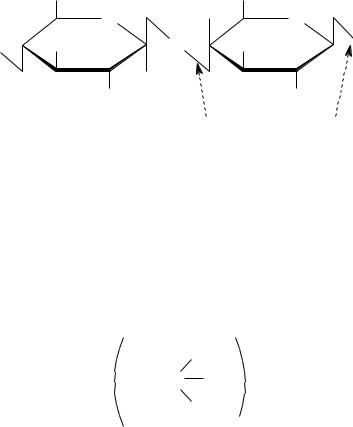
|
CH2OH |
|
CH2OH |
|
|
|
O |
O |
|
• • • O |
OH |
1 O |
4 OH |
O • • • |
|
|
OH |
OH |
|
|
|
|
Гликозидные связи |
|
Цепь, построенная из тысячи остатков D–глюкозы, имеет линейное строение. Линейные цепи закреплены Н–связями между моносахаридными звеньями внутри одной цепи. Между параллельно уложенными цепями полисахарида также возникают Н-связи, придающие жесткость всей структуре. Отсюда высо-
кая механическая прочность целлюлозы.
С химической позиции целлюлоза – многоатомный спирт, содержащий три гидроксильные группы в каждом моносахаридном звене, и способный образовывать с участием этих групп простые и сложные эфиры:
OR C6H7O2 OR
OR
 n
n
В эфирные группы могут быть превращены либо все, либо часть гидроксильных групп фрагмента полисахарида, где R–алкил или остаток органиче-
ской или неоранической кислоты (в сложных эфирах). Целлюлоза не проявляет восстанавливающих свойств.
Простые эфиры целлюлозы – метилцеллюлоза R=CH3 и натрийкарбоксиметилцеллюлоза R=СН2 СООNa – образуют вязкие водные р-ры или гели и применяются в фармации в качестве загустителей, эмульгаторов и стабилизаторов мазей и эмульсий. Карбоксиметилцеллюлоза R=СН2СООН и диэтиламиноэтилцеллюлоза (сокращенно ДЭАЭ-целлюлоза) R=СН2СН2N (C2H5)2 обладают способностью ионитов и применяются в биохимических исследованиях.
Эфир уксусной к-ты (триацетат) применяют в производстве кинопленки и электроизоляционной пленки. Из этого полиэфира вырабатывают также ацетатное волокно. Из целлюлозы получают и другие искусственные волокна : вискозное и медноаммиачное.
Широко применяются эфиры целлюлозы с азотной к-той. Тринитрат целлюлозы – взрывчатое вещество, применяется в производстве пороха. Смесь мо- но-и динитратов целлюлозы используют в производстве целлулоида, лаков, взрывчатых вещ-в.
Гидролизом целлюлозы в промышленности вырабатывают глюкозу, брожением которой получают этиловый спирт. Другие области применения целлюлозы: строительный материал, производство бумаги, картона.
Крахмал – другой распространенный растительный полисахарид, состоящий из двух фракций: амилопектина (основной компонент – 80-90%) и амило-
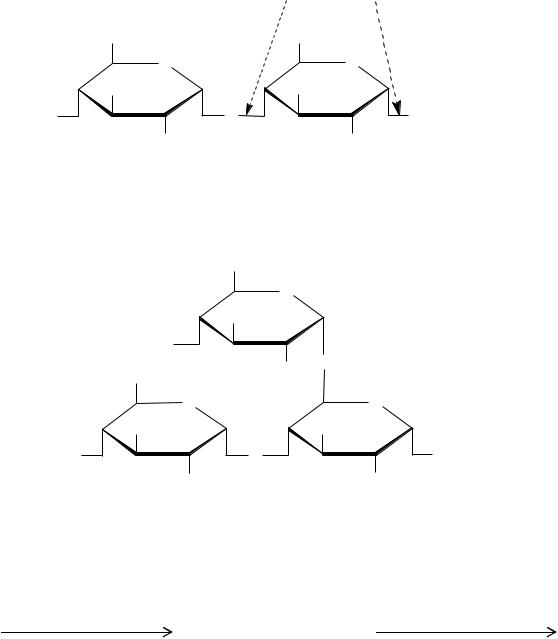
зы. Амилоза, как и целлюлоза, построена из (1→4) – связанных остатков D– глюкопиранозы.
Однако в отличие от целлюлозы, гликозидная связь в амилозе имеет-конфигурацию, в результате чего полисахаридная цепь приобретает иное пространственное строение, напоминающее спираль.
Амилоза + I2 → синее окрашивание
|
|
Гликозидные связи |
CH2OH |
|
CH2OH |
|
O |
O |
OH |
1 |
4 OH |
. . . O |
O |
O . . . |
|
OH |
OH |
Фрагмент цепи амилозы
Амилопектин имеет разветвленное строение. В основной цепи остатки D- глюкопиранозы связаны -(1→4) – гликозидной связью, а в местах ветвления –
-(1→6)-связью:
|
|
|
CH2OH |
|
|
|
|
O |
|
Боковая цепь |
|
|
OH |
1 |
|
• • • O |
|
|
6 |
|
|
|
|
|
|
CH2OH |
|
OH |
CH2 |
|
|
|
|
|
|
|
O |
|
O |
Основная цепь |
OH |
1 |
2 |
OH |
• • • O |
|
|
O |
O • • • |
|
|
OH |
|
OH |
Амилопектин +I2 → фиолетовое окрашивание
В организме крахмал подвергается гидролизу :
|
Амилаза слюны |
Желудочный сок |
Крахмал |
Декстрины крупные |
|
|
Амилаза панкреотического сока |
Мальтаза кишечни- |
ка |
|
|
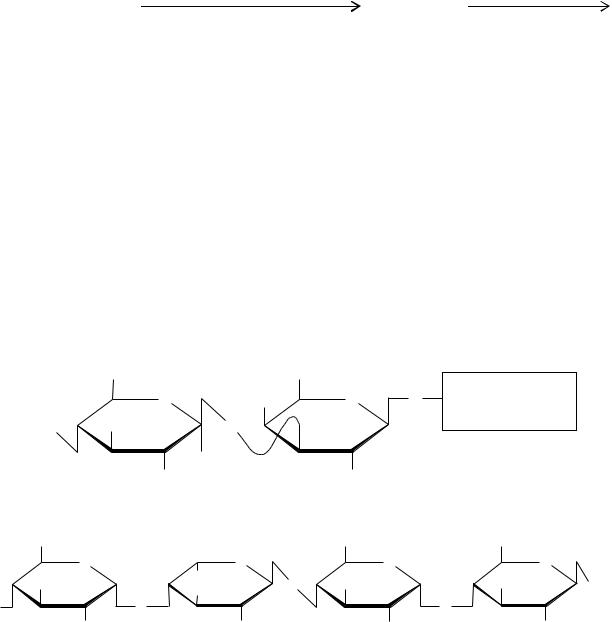
Декстрины мелкие |
Мальтоза |
–D-глюкоза.
–D-Глюкоза поглощается ворсинками кишечника, попадает в кровеносное русло и используется как источник энергии. Избыток глюкозы полимеризуется в гликоген и откладывается в печени про запас.
Проблема ожирения возникает потому, что количество гликогена в тканях ограничено. После синтеза 50-60г гликогена на 1кг ткани из глюкозы начинает вырабатываться жир.
Гликоген (животный крахмал) имеет сходное строение с амилопектином, однако разветвленность его больше, чем амилопектина.
Гетерополисахариды – это углеводы, при гидролизе которых образуются молекулы различных моносахаридов и их производных. К последним относятся гепарин, гиалуроновая к-та, хондроитинсерная к-та.
Все гетерополисахариды построены по одному принципу. Дисахаридная единица состоит из уроновой к-ты и аминосахара в сульфированной и ацилированной форме, соединенных -гликозидной связью :
|
COOH |
|
CH2OH |
|
|
|
|
|
O |
HO3SO |
|
O |
O |
Тетрасахаридный |
|
|
|
фрагмент |
|
||||
|
|
|
|
|
|
|
|
• • • O |
OH |
O |
|
|
|
|
|
|
OH |
|
|
NHCOCH3 |
|
|
|
|
|
Ходроитин -4-сульфат |
|
|
|
|
|
CH2OSO3H |
|
|
CH2OSO3H |
CH2OH |
|
||
|
O |
O |
|
|
O |
O |
|
OH |
|
COOH |
O |
OH |
|
OH |
O • • • |
|
OH |
|
|||||
• • • O |
O |
|
|
|
|
O |
|
|
NHSO3H |
OSO3H |
|
|
NHSO3H |
OH |
|
Фрагмент цепи гепарина
Соединительная ткань распределена по всему организму (кожа, хрящи, сухожилия, суставная жидкость, роговица, стенки крупных кровеносных сосудов, кости) и обусловливает прочность и упругость органов, эластичность их соединения, стойкость к проникновению инфекции. Полисахариды соединительной ткани связаны с белками.
Полисахариды соединительной ткани иногда называют кислыми мукополисахаридами, т.к. они содержат уроновые к-ты, остатки серной и уксусной к-т.
Функции углеводов: 1) энергетическая; 2) строительная; 3) наследственная; 4) защитная; 5) поддержание постоянного осмотического давления и свертываемости крови; 6) лекарственные препараты и компоненты к ним.
Энергетическая функция. Потребность человеческого организма удовлетворяется за счет углеводов. При нормальной трудовой деятельности энергети-
ческие затраты человека покрываются за счет углеводов на 55-60%, жиров на
20-25%, белков на 15-20%.
Калорийность углеводов, то есть энергия, выделяемая в процессе их диссимиляции с образованием СО2 и Н2О, составляет 16-17 кДж/г. Источником глюкозы является гликоген и крахмал, поступающий с пищей. Глюкоза – обязательный компонент крови (3,3 –3,5 ммоль/л цельной крови).
Особенно чувствительны к снабжению глюкозой нервные клетки. При недостатке глюкозы возникают судороги, потеря сознания. Постоянная концентрация глюкозы зависит от двух гормонов адреналина (гормон надпочечников), регулирующего расщепление глюкозы, и инсулина (гормон поджелудочной железы), регулирующего синтез гликогена из глюкозы..
Используемая литература:
1.Биоорганическая химия: учебник / Н.А. Тюкавкина, Ю.И. Бауков, С.Э. Зурабян. – М.: ГЭОТАР-Медиа, 2010. – 416 с.;
2.Органическая химия: учеб. Пособие для вузов/ А.М. Ким. – 4-е изд., испр. И доп. – Новосибирск: Сиб. Унив. Изд-во, 2004. – 844 с.
ЛЕКЦИЯ 4
Тема: Биологически важные гетероциклические соединения.
Цель лекции: изучение строения и химических свойств биологически важных гетероциклических соединений и их производных и их роль в организме.
Содержание: Понятие о гетероциклических соединениях (ГЦ). Классификация, номенклатура, биологическая роль. ГЦ с одним и двумя гетероатомами. Конденсированные ГЦ. Строение и химические свойства ГЦ: ароматичность; реакции SN SE; окислительно-восстановительные свойства; кислотно-основные свойства. Понятие о лактим-лактамной таутомерии. Метаболиты и лекарственные препараты содержащие гетероциклы.
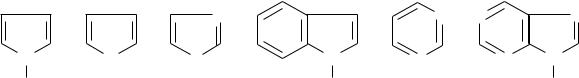
ГЦС называются молекулы, в цикл которых, кроме атомов углерода, входит один или несколько гетероатомов, чаще всего это N, О, S.
|
|
N |
|
N N |
N |
N |
O |
S |
N |
N |
N N |
H |
|
|
H |
|
H |
Пиррол |
Фуран |
Тиазол |
Индол |
Пиримидин |
Пурин |
Биологическая функция Химия ГЦС явл-ся одним из важных разделов органической химии. Мно-
гие жизненноважные сое-ния содержат гетероциклы. (ГЦ) – это ферменты (дегидрогеназа, декарбоксилаза и др.), витамины (В1, В6, В12 и др.), гормоны, алкалоиды, антибиотики (пенициллин). ГЦ входят в состав нуклеиновых к-т (НК): аденин, гуанин, тимин, цитозин, урацил – азотистые основания – материальные носители наследственности. Четыре пиррольных кольца, соединенные метиленовыми мостиками (-СН=) образуют порфириновую структуру, которая в сочетании с Fe+2 образует основу гемоглобина, с Мg+2 – хлорофилла, с Со+2 – вита-
мина В12.
ГЦ составляет основу многих химиотерапевтических препаратов: фурацилин, фурагин – содержат ядро фурана; 5-НОК, энтеросептол – ядро хинолина; антипирин, амидопирин – ядро пиразола, орат калия – ядро пиримидина; рибоксин – ядро пурина.
