
- •Микроболигия. Рейтинг №1
- •Современная классификация вирусов. Признаки, положенные в основу классификации.
- •Особенности биологии вирусов. Структура и химический состав вирусов.
- •Фазы взаимодействия вируса с клеткой. Репродукция вирусов.
- •Бактериофаги. Фазы взаимодействия фага с бактериальной клеткой. Умеренные и вирулентные фаги. Лизогения. Применение фагов в медицине и микробиологии.
- •Культивирование, индикация и идентификация вирусов.
- •Вирус краснухи. Свойства. Лабораторная диагностика. Препараты для специфической профилактики и терапии.
- •Вирус бешенства. Свойства. Механизм заражения. Патогенез заболевания. Лабораторная диагностика. Препараты для специфической профилактики.
- •Пикорнавирусы. Классификация. Вирусы полиомиелита, Коксаки, еcно. Свойства. Патогенез заболеваний. Лабораторная диагностика. Препараты для специфической профилактики и терапии.
- •Герпесвирусы. Классификация. Вирус простого герпеса 1 и 2 типа. Свойства. Патогенез заболеваний. Лабораторная диагностика.
- •Возбудитель гепатита а. Таксономия. Характеристика. Лабораторная диагностика. Специфическая профилактика.
- •Возбудитель гепатита в. Таксономия. Характеристика носительства. Лабораторная диагностика. Препараты для специфической профилактики.
Бактериофаги. Фазы взаимодействия фага с бактериальной клеткой. Умеренные и вирулентные фаги. Лизогения. Применение фагов в медицине и микробиологии.
Бактериофаги – специфические вирусы бактерий, которые вызывают их лизис или изменяют их свойства.
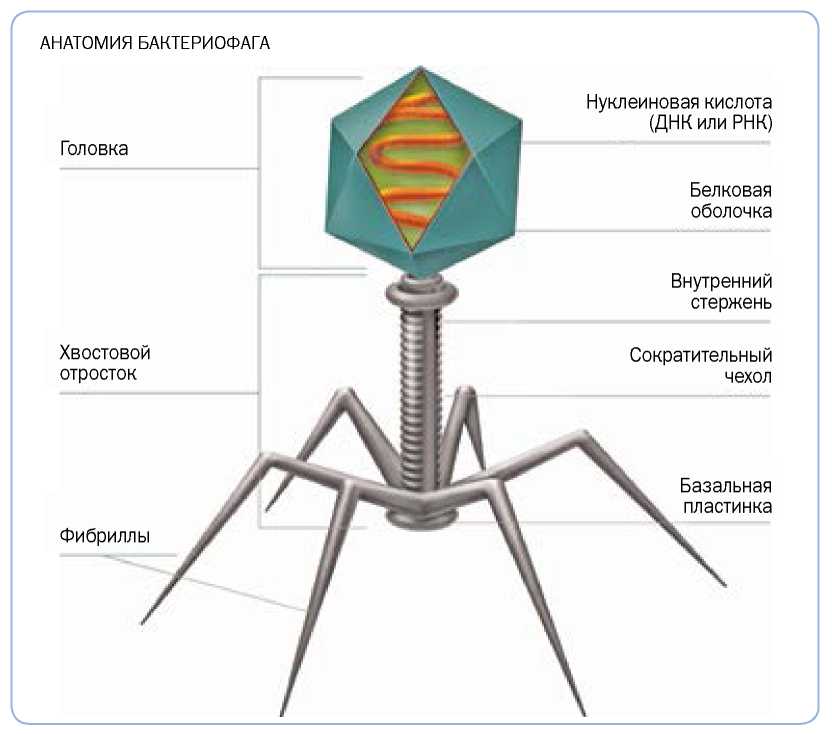
Фазы взаимодействия фага с бактерией:
Адсорбция фага на рецепторы бактерий. К ним фаг крепится фибриллами. Происходит при наличии комплементарных рецепторов в клеточной стенке бактерий.
Проникновение ДНК фага в бактерию. При этом слои клеточной стенки разрушаются под действием фагового лизоцима. После чехол отростка сокращается и внутренний стержень прокалывает оболочку клетки. ДНК проникает внутрь.
Синтез фаговой иРНК, белков капсида, которые участвуют в синтезе фаговой ДНК. Внутриклеточное развитие фага. ДНК бактериофага направляет клеточные системы на синтез компонентов, необходимых для репродукции фагов.
Морфогенез фага, т.е. пустые фаговые капсиды заполняются нуклеиновой кислотой и формируются зрелые частицы фага. Происходит созревание фага. Части фага формируются отдельно.
Выход фаговых частиц из клетки благодаря лизису бактерии фаговым лизоцимом, накапливающимся при репродукции фага. Бактериофаги выходят в окружающую среду.
Вирулентные (литические) фаги для внедрения в бактерию адсорбируются на специфических рецепторах клетки, в т.ч. на липополисахариде, липопротеине, тейхоевых кислотах, протеинах, пилях. Характерен продуктивный тип взаимодействия (приводит к лизису).
Умеренные бактериофаги взаимодействуют с бактериями по продуктивному или интегративному типу:
Продуктивный тип, как и у вирулентных фагов, заканчивается лизисом бактерии
При интегративном типе ЛНК умеренного фага встраивается в хромосому бактерии, реплицируется вместе с геномом бактерии, не вызывая лизиса. ДНК фага, встроенная в хромосому – профаг, культура бактерий – лизогенная, сам процесс – лизогения.
Бактериофаги используют для профилактики, лечения инфекций, а также диагностики (например, для фаготипирования при выявлении источника инфекции). С лечебной целью используют бактериофаги в зависимости от вида и типа возбудителя. Также фаги используют в генной инженерии как векторы, переносящие участки ДНК.
Фаготипирование – метод эпидемиологического маркирования. Используют для выявления источника инфекции. Выделение бактерий одного фаговара от разных больных говорит об общем источнике заражения.
При определении фаговара бактерий с помощью фаготипирования на чашку Петри с плотной питательной средой, засеянную чистой культурой возбудителя в виде газона, наносят капли различных диагностических типоспецифических фагов. Бактерии, чувствительные к фагу, лизируются (образуется стерильное пятно – колония фага).
Культивирование, индикация и идентификация вирусов.
Культивирование:
В организме лабораторных животных
В эмбрионах птиц (куриный эмбрион)
В культурах клеток (HeLa (бессмертные клетки человека), Vero (из эпителия почки африканской зеленой мартышки), первичные (клетки организма), Сей-Чо (яичники китайского хомячка) (полуперививаемые и перевиваемые), тканей
Индикация:
По ЦПД. Происходят морфологические изменения. Например, вирус полиомиелита вызывает мелкозернистую деструкцию клеток; аденовирусы – скопление клеток в виде виноградных гроздьев; корь – образование симпластов – многоядерных клеток.
По образованию включений – скоплений вирусов в клетках. Они имеют различную форму и размеры. Их окрашивают по Романовскому-Гимзе.
По гемадсорбции. Клетки, зараженные вирусами, могут адсорбировать эритроциты. Вирусы выходят на поверхность клеток и связывают эритроциты.
По РГА. Гемагглютинация – склеивание эритроцитов под влиянием вирусов.
По "цветной" реакции. Клетки культуры выращиваются на жидкой среде с индикатором (метиленовым красным). Индикатор меняет цвет под действием кислых продуктов метаболизма при росте нормальных клеток. Если клетки заражены вирусом, то метаболизм нарушается, кислые продукты не образуются и индикатор не меняет цвет (сохранение красного цвета).
Идентификация: с помощью иммунологических реакций (РСК, РН, РИФ, ИФА, РТГА).
Вирусы – возбудители острых респираторных заболеваний. Вирусы гриппа. Классификация. Биологические свойства. Антигенная структура вирусов гриппа и ее изменчивость. Патогенез гриппа. Иммунитет. Лабораторная диагностика. Препараты для специфической профилактики и терапии.
Грипп (Influenzavirus)– острое инфекционное вирусное заболевание, характеризующееся поражением респираторного тракта, лихорадкой, общей интоксикацией, нарушением деятельности ССС и НС.
Семейство Orthomyxoviridae Ортомиксовирусы включает 3 рода – А (человек и животные), В (человек), С.
Наибольшим антигенным разнообразием и эпидемиологической опасностью обладает вирус гриппа А.
Структура:
Геном – однонитевидная сегментированная –РНК, связанная с белками полимеразного комплекса (РВ1, РВ2, РА).
Капсид – состоит из нуклепротеина NP. Нуклеокапсид окружен матриксным белком М1 и мембранным белком М2.
Суперкапсид – состоит из HA и NA. HA и NA при репродукции встраиваются в мембрану клетки хозяина.
Тип симметрии – спиральный.
HA – липучка – связывается с рецепторами чувствительных клеток.
NA – иголка – модифицирует эти рецепторы, что способствует проникновению вириона в клетку путем эндоцитоза, попадая в нижние отделы респираторного тракта; способствует выходу вириона из клетки.
Вирусы гриппа имеют внутренние и поверхностные антигены. Внутренние типоспецифические АГ представлены нуклепротеинами (NP-белком) и М-белками. Поверхностные АГ – гемагглютинин (HA) и нейраминидаза (NA).
Структура поверхностных АГ вирусов гриппа А постоянно меняется (NA – 9 подтипов, HA – более 15), но от человека стабильно выделяют Н1, Н2, Н3 и N1, N2. Вирус гриппа В более стабилен, еще стабильнее вирус гриппа С.
Изменчивость антигенной структуры вируса гриппа А обусловлена 2 процессами:
Антигенный шифт – редкие изменения структуры HA и NA, обусловленные полной заменой гена, который контролирует HA и NA. Происходит при попадании 2 разных подтипов вируса в одну клетку. Приводит к появлению нового подтипа, что вызывает пандемии.
Антигенный дрейф – незначительные частые изменения структуры HA и NA, происходящие из-за точечных мутаций, которые приводят к появлению новых сероваров, незначительно отличающихся от предыдущих. Вызывают периодические эпидемии.
Патогенез гриппа А: вирус гриппа → попадание в эпителий верхних дыхательных путей (входные ворота) (может проникать сразу в альвеолы, вызывая острую пневмонию) → первичная репродукция в эпителии, воспаление, отек, шелушение эпителия → вирусемия, интоксикация из-за всасывания продуктов распада клеток → поражение капилляров, увеличение их проницаемости, разрушение эндотелия сосудов, нарушение гемодинамики, геморрагия в легких и миокарде → взаимодействие с ИКК (Т-, В-лф, макрофаги, ДК), развитие вторичного ИДС и аутоиммунной патологии, что располагает к присоединению вторичной инфекции.
Инкубационный период: 1-3 дня.
Иммунитет: постинфекционный иммунитет длителен и прочен, но высокоспецифичен. Гуморальный (Ig A и G против H и N), клеточный (Т-киллеры, макрофаги).
Лабораторная диагностика:
Отделяемое носоглотки, мазки-отпечатки слизистой носа для обнаружения генома.
Парные сыворотки больного для обнаружения антител
Методы:
Экспресс-диагностика. Антигены с помощью РИФ, геном с помощью ПЦР.
Вирусологический метод. Выделение вируса в курином эмбрионе, культуре клеток Vero, в лабораторных животных. Индикация по гибели, клиническим и патоморфологическим изменениям, ЦПД, образование «бляшек». Идентификация по АГ структуре (РСК, РТГА, ИФА, РБН)
Серологический метод. 4-кратное увеличение титра антител в парных сыворотках больного (РТГА, РСК, ИФА, РБН)
Препараты для экстренной профилактики: ингибиторы N, арбидол, римантадин.
Для неспецифической профилактики: препараты альфа-интерферона и оксолина.
Специфическая профилактика – вакцины (живые, инактивированные цельновирионные, химические, сплит-вакцины).
Вирусы – возбудители острых респираторных заболеваний. Свойства парамиксовирусов. Возбудители кори и паротита. Патогенез заболеваний, вызванных разными паравирусами. Лабораторная диагностика. Препараты для специфической профилактики и терапии.
Пармамиксовирусы – семейство сложных РНК-вирусов.
Механизм передачи – респираторный.
Вирион окружен суперкапсидом с гликопротеиновыми шипами (белок слияния (F), прикрепительные белки N, H, гликопротеин G). Под суперкапсидом лежит нуклеокапсид, состоящий из однонитевой –РНК, связанной с нуклеопротеином (поддерживает геномную структуру), транскриптазой и фосфопротеином. Нуклеокапсид связан с матриксным белком.
Резистентность: чувствительны к высокой температуре, дезинфектантам; устойчивы к ннизким температурам.
Корь – острое антропонозное инфекционное заболевание, характеризующееся лихорадкой, катаральным воспалением слизистых ВДП и глаз, а также пятнисто-папулезной сыпью на коже.
Эпидемический паротит – острая детская высококонтагиозная антропонозная инфекция, характеризующаяся поражением околоушных слюнных желез, реже – других органов.
Патогенез кори: слизистые оболочки ВДП и глаз (входные ворота) → репродукция в эпителии и региональных лимфатических узлах → вирусемия → поражение эндотелия капилляров, что вызывает появление сыпи → развитие отека и некрозов тканей.
Инкубационный период: 8-17 дней.
Патогенез паротита: ВДП (входные ворота) → репродукция в эпителии слизистых ВДП, околоушных слюнных железах → вирусемия → попадание в яички, поджелудочную и щитовидную железы, мозговые оболочки (орхит, панкреатит, менингит, менингоэнцефалит).
Инкубационный период: 14-21 день.
Лабораторная диагностика кори:
Обнаружение в патологическом материале (смыв носоглотки, соскобы сыпи, кровь, моча) и в зараженных культурах клеток (в них характерно наличие многоядерных клеток и антигенов) (РИФ, РТГА, РН, ПЦР).
Серологическая диагностика (РСК, РТГА, РН).
Лабораторная диагностика паротита:
Материал исследования – слюна, цереброспинальная жидкость, моча, сыворотка крови.
Культивация на культуре клеток куриного эмбриона.
Идентификация с помощью РТГА, РИФ, РН, РСК.
При серологическом методе в парных сыворотках больного с помощью ИФА, РСК, РТГА определяют IgM- и IgG-антитела.
Лечение и профилактика кори:
Лечение иммуномодуляторами и рибавирином.
Профилактика: детям до 1 года подкожно вводят живую аттенуированную вакцину Л-16 или ассоциированную вакцину КПК (корь, паротит, краснуха). В очагах ослабленным детям вводят нормальный Ig-человека, который эффективен при введении до 7 дня инкубационного периода.
Лечение и профилактика паротита:
Для лечения и поздней профилактики используют специфический Ig.
Активный иммунитет у детей старше 1 года создают живой вакциной КПК.
