
634
.pdf3.При растворении 58,3 г K2SO4 в 300 г воды температура кипения повысилась на 1,340. Определить кажущуюся степень диссоциации соли.
4.Рассчитать ионную силу, коэффициент активности
иактивность 0,1 М AlCl3.
Вариант 12
1.Найти кажущуюся степень диссоциации 1,8 М раствора бромида натрия, изотоничного с 3М-ным раствором глюкозы при 270С.
2.Вычислить температуру замерзания раствора
14,616 г хлорида натрия в 500 г воды, если при 180С Росм раствора 2,11∙106 Па. Плотность раствора 1,1 г/см3.
3.Определить температуру кипения 1н раствора серной кислоты. Степень диссоциации кислоты в растворе 91%. Плотность раствора 1,03 г/см3.
4.Рассчитать ионную силу, коэффициент активности
иактивность 0,001М Al2(SO4)3.
Вариант 13
1.Раствор 0,608 г бензойной кислоты в 25 г воды кипит при 100,1040С. Определить степень электролитической диссоциации и силу электролита.
2.Растворы хлорида кальция и фосфата натрия содержат одинаковое количество молей в 1 л воды. Какой из растворов обладает большим осмотическим давлением, если кажущиеся степени диссоциации солей равны. Дать обоснованный ответ.
3.Определить температуру замерзания водного раствора MgCl2. Концентрация раствора 0,75 масс.%, кажущаяся степень диссоциации соли 97%.
51
4.Рассчитать ионную силу, коэффициент активности
иактивность 0,01 М Na2HPO4.
Вариант 14
1.Определить осмотическое давление раствора 0,608
гбензойной кислоты в 25 г воды при 200С, если раствор кислоты кипит при 100,1040С.
2.Раствор 0,2 моль хлорида алюминия в 100 г воды замерзает при -5,490С. Определить кажущуюся степень диссоциации соли в растворе.
3.Осмотическое давление 0,025 М раствора электролита 1,36∙105 Па при 00С. Кажущаяся степень диссоциации электролита 70%. На сколько ионов диссоциирует молекула электролита?
4.Рассчитать ионную силу, коэффициент активности и активность 0,005М NaHCO3.
Вариант 15
1.При какой температуре замерзает раствор 3,35 г нитрата кальция в 50 г воды? Кажущаяся степень диссоциации соли 69,5%.
2.Осмотическое давление 8 л раствора, содержащего 2 моля К2НРО4, равно 1,12∙106 Па при 250С. Определить кажущуюся степень диссоциации соли.
3.Вычислить температуру замерзания раствора 22,232 г хлорида натрия в 1000 г воды, если при 180С осмотическое давление раствора равно 2,11∙106 Па. Плотность раствора 1,1 г/см3.
4.Рассчитать ионную силу, коэффициент активности
иактивность 0,001М Ca(OH)2.
52

Тема 5. РЕАКЦИЯ СРЕДЫ ВОДНЫХ РАСТВОРОВ. БУФЕРНЫЕ РАСТВОРЫ
Ионное произведение воды:
HOH  H+ + OH -.
H+ + OH -.
Константа диссоциации воды:
К |
[H ] [OH ] |
1,8 |
10 16. |
||
[H2O] |
|
||||
|
|
|
|||
[H O] |
1000 |
|
1000г |
55,5 моль |
. |
|
|||
|
|
|
|||||||
2 |
|
M H |
|
|
18г / моль |
|
л |
|
|
|
|
|
|
|
|
|
|||
|
|
O |
|
|
|
|
|||
|
|
2 |
|
|
|
|
|
|
|
Ионное произведение воды: |
|
|
|
|
|
||||
KW = [H+]∙[H2O] = K∙[H2O] = 1,8∙10-16∙55,5 = 10-14 |
(5.1). |
||||||||
[H+] = [OH -] = 10-7 моль/л |
|
|
нейтральная среда; |
||||||
[H+] > [OH -] > 10-7 (10-6, 10-5, … 100) моль/л |
кислотная среда; |
||||||||
[H+] < [OH -] < 10-7 (10-8, 10-9, … 10-14) моль/л |
щелочная среда. |
||||||||
Количественная |
характеристика |
кислотности |
- |
||||||
водородный показатель: |
|
|
|
|
|
|
|
||
|
|
pH = - lg [H+] |
|
|
|
(5.2) |
|||
|
или |
[H+] = 10 -pH |
|
|
(5.3). |
||||
|
|
рН+рОН = 14 |
|
|
|
(5.4) |
|||
Реакция среды водных растворов - важнейшее условие протекания всех биохимических процессов, деятельности микроорганизмов, ферментов, роста и развития растений.
53
Шкала кислотности
[H+]100 10-1 |
10-2 10-3 10-4 |
10-5 10-6 10-7 10-8 10-9 |
10-10 10-11 10-12 10-13 10-14 |
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
pH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
|
8 |
9 |
10 |
11 |
12 |
13 |
14 |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
усиление кислотности |
нейтраль- |
|
усиление основности |
|
|
|
||||||||||||||||||||||
|
|
|
|
ная |
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Примеры расчета рН водных растворов
1. Раствор сильной кислоты:
HCl |
H+ + Cl-; |
|
Ск = 0,1 экв/л; [H+] = Cк = 0,1 = 10-1 моль/л; рН = -lg [H+] = -lg 10-1 = 1.
2. Раствор слабой кислоты:
CH COOH |
|
CH COO - + H+; |
|
3 |
|
3 |
|
К к [CH 3COO ] [H ] ; [CH 3COOH]
[H ] [CH 3COO ]; [CH 3COOH] Cк ;
|
|
|
[H ]2 |
|
[H ] |
|
|
|
|
|
|
К |
к |
|
; |
К |
к |
С |
к |
(5.5). |
|||
Cк |
|||||||||||
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
К |
к |
1,85 10 |
5 (приложение, табл. 5); С |
к |
0,1экв л ; |
||||
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
||||
[H ] 1,85 |
10 5 0,1 |
1,85 10 6 1,36 10 3 моль л ; |
|||||||
рН lg[ H ] lg1,36 10 3 |
[lg1,36 lg10 3 ] |
[0,1335 3] 2,8665. |
|
3. Раствор сильного основания: |
|
|
NaOH |
Na+ + OH -; |
|
[OH -] = C0 = 0,1 = 10-1моль/л; |
|
|
|
54 |
|

рОН = -lg [OH -] = -lg 10-1 = 1; рН = 14 – рОН = 14 – 1 = 13.
4. Раствор слабого основания:
|
|
NH OH |
|
|
|
NH + |
+ OH -. |
||
|
|
4 |
|
|
|
4 |
|
||
|
|
[NH ] [OH ] |
|
|
|
|
|||
К 0 |
4 |
|
|
|
; |
|
|
|
|
[NH |
4 OH ] |
|
|
|
|||||
|
|
|
|
|
|
||||
[NH ] [OH ], [NH |
OH ] C |
. |
|||||||
|
4 |
|
|
|
|
4 |
0 |
|
|
|
|
[OH ]2 |
|
|
|
|
|
|
|
|
|
||||
|
K0 |
|
[OH ] |
K0 C0 |
(5.6) |
||
|
C0 |
||||||
|
|
|
|
|
|
||
|
|
|
|
|
|
||
C0 0,1экв л; |
К0 1,79 (приложение, табл.5) |
||||||
[OH ] 
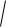 1,79 10 5 10 1
1,79 10 5 10 1 
 1,79 10 6 1,34 10 3 моль
1,79 10 6 1,34 10 3 моль л ;
л ;
рОН lg [OH ] lg1,34 10 3 |
[lg1,34 lg10 3 ] |
[0,1271 3] 2,8729; |
|
рН 14 2,8729 11,1271. |
|
5. Водные растворы солей
Реакции воды с солями называются гидролизом солей.
а) рН раствора соли, образованной слабым основанием и сильной кислотой:
NH4Cl + HOH |
|
|
|
|
NH4OH + HCl; |
|
|
|||
|
|
|
|
|
|
|||||
NH4+ + Cl - + HOH |
|
|
|
|
NH4OH + H+ + Cl -; |
|||||
|
|
|
|
|||||||
NH4+ + HOH |
|
|
|
NH4OH + H+. |
|
|
||||
|
|
|
|
|||||||
Константа равновесия: K |
[NH |
OH ] [H |
] |
|
||||||
4 |
|
|
. |
|||||||
|
|
|
|
|
||||||
|
|
|
|
|
|
[NH4 ] [H2O] |
|
|
||
55

Константа гидролиза:
|
К [H |
2O] |
[NH |
OH ] [H ] |
|
[NH |
OH ] [H ] [OH ] |
|
||
К Г |
4 |
|
|
4 |
|
|
. |
|||
[NH ] |
[NH ] [OH ] |
|||||||||
|
|
|
|
4 |
|
|
|
4 |
|
|
[H ] [OH ] K |
|
|
|
|
|
|
|
[NH |
|
] [OH |
] |
K |
|
|
|
|
||||||||||||||||||||||||||
|
|
|
, |
|
|
|
|
|
|
4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
. |
|
|
|||||||||||||||
W |
|
|
|
|
|
[NH 4OH ] |
|
|
|
|
0 |
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
К Г |
|
|
|
|
КW |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
K0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
или, учитывая, что |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
[NH |
OH ] [H ], [NH |
|
] C |
|
|
[H ]2 |
|
|
KW |
, |
|
|
|
|||||||||||||||||||||||||||||
4 |
|
c |
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Cc |
|
|
|
|
|
K0 |
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
получим: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
К |
|
|
|
[H ]2 |
|
; |
|
[H ] |
|
|
|
K |
W |
C |
c |
. |
|
(5.7) |
|
|
||||||||||||||||||||
|
|
Г |
|
Cc |
|
|
|
|
|
|
K0 |
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
Сс = 0,1 экв/л, К0 = 1,79∙10-5 (приложение, табл. 5), KW = 10-14, |
||||||||||||||||||||||||||||||||||||||||||
тогда |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
[H ] |
|
|
K |
W |
C |
c |
|
|
|
1 10 14 10 |
1 |
|
7,47 10 6 |
моль |
, |
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
K0 |
|
|
|
|
|
|
|
|
|
1,79 10 5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
л |
|
|
|||||||
рН lg[H ] lg 7,47 10 6 5,13.
б) рН раствора соли, образованной сильным основанием и слабой кислотой:
CH3COONa + HOH  CH3COOH + NaOH;
CH3COOH + NaOH;
CH3COO- + Na+ + HOH |
|
CH3COOH + Na+ + OH -; |
|
CH3COO- + HOH  CH3COOH + OH -.
CH3COOH + OH -.
56

|
[CH |
COOH] [OH ] |
|
|
|
|
|
|
|
|||||||||||
|
K |
|
3 |
|
|
|
|
|
|
|
|
|
; |
|
|
|
|
|
|
|
|
[CH |
|
COO ] [H |
O] |
|
|
|
|
|
|
|
|||||||||
|
|
|
3 |
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
К Г K [H 2 O] |
[CH |
|
COOH] [OH ] |
|
[CH |
COOH] [OH ] [H ] |
|
||||||||||||
|
|
|
|
3 |
|
|
|
|
3 |
|
|
. |
||||||||
|
|
|
|
[CH |
COO ] |
[CH |
COO ] [H ] |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
3 |
|
|
|
[OH ] [H ] K |
W |
; |
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
[CH |
COO ] [H ] |
К к . |
|
|
|
|
|
|
|
|||||||||||
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
[CH 3COOH] |
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
К Г |
|
КW |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Kк |
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
или, учитывая, что |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
[CH |
COOH] [H |
], [CH |
COO ] C |
|
|
[OH ]2 |
|
KW |
, |
||||||||||||||
c |
|
|
|
|
|||||||||||||||||||
3 |
|
|
|
|
3 |
|
|
|
|
|
|
|
Cc |
|
|
|
|
|
Kк |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
получим: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
[OH ]2 |
[OH ] |
|
|
K |
W |
C |
c |
|
|
|
|
|||||||
|
|
К |
|
|
|
|
; |
|
|
|
|
|
. (5.8) |
||||||||||
|
|
Г |
Cc |
|
|
|
|
K к |
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Сс = 0,1 экв/л,
Кк = 1,86∙10-5 (приложение, табл.5),
КW = 10-14,
тогда:
[OH ] |
1 10 14 10 1 |
|
7,33 10 6 |
моль л , |
|
|
1,86 10 5 |
|
|||
рОН lg [OH ] lg 7,33 10 6 |
[lg 7,33 lg10 6 ] |
||||
[0,8651 6] 5,1349, |
|
||||
pH 14 pOH 14 5,1349 8,8651.
57

в) рН раствора соли, образованной слабым основанием и слабой кислотой:
CH3COONH4 + HOH |
|
CH3COOH + NH4OH; |
|
CH3COO- + NH4+ + HOH  CH3COOH + NH4OH.
CH3COOH + NH4OH.
(1)NH4+ + HOH  NH4OH + H+
NH4OH + H+
(2)CH3COO- +HOH  CH3COOH + OH -
CH3COOH + OH -
NH4+ + CH3COO- + 2HOH  NH4OH + CH3COOH + H+ + OH -.
NH4OH + CH3COOH + H+ + OH -.
|
K |
[NH OH ] [CH COOH] [H ] [OH ] |
; |
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
4 |
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
[NH ] [CH COO ] [HOH]2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
4 |
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
KГ K0 [H2 0] |
[NH |
4 |
OH ] [CH COOH] [H ] [OH ] |
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
; |
|
|
|
|
|
||||||||||
|
|
|
[NH |
] |
[CH COO |
] [H ] |
[OH ] |
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4 |
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
[H ] [OH |
] K , |
[NH ] [OH ] |
K |
|
[CH COO ] [H |
] |
K |
|
|||||||||||||||||||||||||
|
|
|
4 |
|
|
|
|
, |
|
|
3 |
|
|
|
|
|
|
. |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
W |
|
|
[NH4OH ] |
|
|
0 |
|
|
|
[CH3COOH] |
|
|
|
к |
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
КW |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
K Г |
|
|
|
|
|
|
|
|
|
|
|
[H ] |
KW Kк |
. |
(5.9) |
|
|
|
|
|
|||||||||||||
|
K0 Kк |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
K 0 |
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
Константа гидролиза зависит от силы кислоты и |
|
||||||||||||||||||||||||||||||||
основания, образующих соль, и не зависит от концентрации |
|
|||||||||||||||||||||||||||||||||
соли. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
К0 = 1,79∙10-5, Кк = 1,86∙10-5 (приложение, табл.5), тогда: |
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
10 14 1,86 10 5 |
|
|
|
|
|
|
|
|
1,02 10 7 моль |
|
|
|
|
|
|
|||||||||||||||
|
[H ] |
|
|
1,04 10 14 |
л |
|
|
|
||||||||||||||||||||||||||
|
|
|
|
1,79 10 5 |
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
pH -[lg1,02 lg10 -7 ] [0,01 7] 6,99
Так как Кк < К0, реакция среды слабокислая.
58
Буферные растворы Буферные растворы состоят из слабой кислоты и соли
слабой кислоты и сильного основания (CH3COOH + CH3COONa) или слабого основания и соли слабого основания и сильной кислоты (NH4OH + NH4Cl).
Буферные растворы поддерживают постоянное значение рН при:
подкислении |
в определенных |
|
подщелачивании |
||
пределах . |
||
разведении |
||
|
Механизм буферного действия
СH3COOH |
|
CH3COO- + H+; |
|
||
CH COONa |
|
CH COO- + Na. |
3 |
3 |
|
|
|
|
[H ] [CH |
COO ] |
|
[H ] K |
|
|
[CH |
COOH] |
|
|||||||
К |
|
|
|
3 |
|
|
|
|
; |
|
3 |
|
|
|
; |
|||
к |
|
[CH |
COOH] |
|
|
к |
[CH |
|
COO ] |
|||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
3 |
|
|
|
|
|
|
|
|
|
3 |
|
|
|
||
[CH |
COOH] C |
; |
[CH |
COO ] C |
, |
|
|
|
|
|
||||||||
|
|
3 |
|
|
|
к |
|
|
|
3 |
|
c |
|
|
|
|
|
|
где Ск - концентрация кислоты; Сс - концентрация соли. Тогда получим:
[H ] K |
|
|
Ск |
. (5.10) |
|
к |
Сс |
||||
|
|
|
|||
|
|
|
|
Подкисление:
CH3COONa + HCl → CH3COOH + NaCl
CH3COO- + Na+ + H+ + Cl- → CH3COOH + Na+ + Cl- CH3COO- + H+ → CH3COOH.
Ионы Н+ связываются солью в слабую кислоту. Концентрация ионов Н+ и рН в буферном растворе остается постоянной.
59
Подщелачивание:
CH3COOH + NaOH → CH3COONa + H2O CH3COOH + Na+ + OH- → CH3COO- + Na+ + H2O CH3COOH + OH- → CH3COO- + H2O.
Ионы ОН- связываются кислотой в слабый электролит - воду.
Концентрация ионов H |
|
|
KW |
|
и рН остается |
|
[OH ] |
||||
постоянной. |
|
|
|
|
|
Разведение: При разведении сохраняется постоянным отношение Ск/Сс, в уравнении (5.5), поэтому [H+] не меняется.
Буферная емкость - интервал рН, в котором проявляется буферное свойство. Определяется количеством сильной кислоты или основания, которое необходимо добавить к 1 л раствора, чтобы изменить его рН на единицу:
Б |
|
|
С V |
|
|
, |
(5.11) |
|
|
|
|
|
|||
( pH |
2 |
pH |
1 |
) V |
|||
|
|
|
буф |
|
|
где С - концентрация сильного основания или кислоты,
моль/л;
V - объем добавленной кислоты или основания, мл; Vбуф - объем буферного раствора, мл;
рН1 и рН2 - водородные показатели до и после добавления сильной кислоты или основания.
Б рК K 1, |
(5.12) |
где рКА = - lg КK.
Для ацетатного буфера КК = 1,8∙10-5 (приложение, табл. 6),
рКК = - lg 1,8∙10-5 = 4,74, тогда Б 4,74 1.
60
