
POLIMERIZATsIYa
.pdf
А.А.СОБАНОВ, Л.М. БУРНАЕВА
ПОЛИМЕРИЗАЦИЯ
МЕТОДИЧЕСКИЕ УКАЗАНИЯ К ЛАБОРАТОРНЫМ РАБОТАМ
ПО КУРСУ
ВЫСОКОМОЛЕКУЛЯРНЫЕ СОЕДИНЕНИЯ
К А З А Н С К И Й Ф Е Д Е Р А Л Ь Н Ы Й У Н И В Е Р С И Т Е Т
Химический институт им. А.М. Бутлерова
2013
Печатается по решению методической комиссии Химического института им. А.М. Бутлерова
Кафедры высокомолекулярных и элементоорганических соединений
Авторы-составители:
канд. хим. наук, доцент А.А.Собанов;
канд. хим.наук, доцент Бурнаева Л.М.,
Полимеризация / Сост. А.А. Собанов, Л.М. Бурнаева – Казань: Издательство Казанского федерального университета,
2013. - с.
Пособие предназначено для студентов IV курса Химического института им. А.М. Бутлерова.
Казанский федеральный университет, 2013

ПОЛИМЕРИЗАЦИЯ
Воснове методов синтеза высокомолекулярных соединений лежат две группы процессов – полимеризация и поликонденсация.
К реакциям полимеризации относят процессы, в которых из низкомолекулярных веществ (мономеров) образуются высокомолекулярные соединения, причём состав повторяющейся структурной единицы соответствует составу мономера.
Вэтом случае повторяющуюся структурную единицу называют моно-
мерным звеном или составным звеном.
К реакциям поликонденсации относят процессы, в которых образование высокомолекулярных соединений сопровождается выделением низкомолекулярных продуктов. Поскольку в этом случае состав повторяющейся структурной единицы не одинаков с составом мономера, её принято называть составным звеном (но не мономерным).
Реакции полимеризации в свою очередь подразделяют на цепные и сту-
пенчатые.
Для цепной полимеризации присущи признаки, характерные для цепных процессов: в частности – возникновение активных частиц, каждая из которых вызывает цепь последовательных реакций.
Ступенчатая полимеризация внешне напоминает поликонденсацию (по структуре полимера и некоторым закономерностям), но протекает без выделения побочного продукта. Обычно реакция связана с присоединением функциональной группы одного мономера к функциональной группе другого, сопряжённое с миграцией атома водорода, отсюда другое название реакции –
полиприсоединение или миграционная полимеризация.
O |
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
OH |
|
|
|||||
nCH |
|
CH |
|
1 |
|
|
|
+ nH N |
2 |
|
( |
|
2 |
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
R |
|
CH |
|
CH |
|
R |
|
NH |
NH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
) |
|
||||
|
|
|
|
|
R NH CH |
|
CH R CH CH |
||||||||||||||||||||||||
2 |
|
|
|
|
|
|
|
2 |
2 |
2 |
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
2 n |
|||||
По количеству участвующих в полимеризации мономеров, реакции подразделяют на гомополимеризацию (полимеризация одного мономера) и сополимеризацию (совместная полимеризация двух и более сомономеров).
n CH2 CH |
( CH2 |
|
CH ) n |
гомополимеризация |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C6H5 |
|
|
|
C6H5 |
|
||||
сополимеризация
n CH |
|
CH + m CH |
|
CH |
|
CH |
|
CH |
( |
CH |
|
CH |
)( |
CH |
|
CH |
|
CH |
|
CH |
) |
|||
|
|
|
|
|
|
|
|
|||||||||||||||||
2 |
|
2 |
2 |
2 |
|
|
n |
2 |
|
|
|
|
2 m |
|||||||||||
|
|
C6H5 |
|
|
|
|
|
|
|
|
C6H5 |
|
|
|
|
|
|
|
|
|||||

Полимеризация – сложный многоуровневый процесс. Формально его можно разделить на три стадии:
инициирование - образование активного центра, которое происходит в результате химического, физического или механического воздействия на мономер
M + A  B*
B*
рост цепи - последовательное, многократное присоединение молекулы мономера к активному центру
B* + M |
|
BM* |
BM* + M |
|
BMM* |
................................. |
||
BM M* + |
M |
BM M* |
n |
|
n +1 |
обрыв цепи - исчезновение активного центра на конце растущей цепи*
BM n +1M*  BMn+2
BMn+2
По характеру активного центра реакции полимеризации подразделяют на радикальную, катионную, анионную, анионно-координационную (протекающую без полного разделения зарядов в молекуле).
Возможность протекания реакции полимеризации оценивается термодинамическими и кинетическими факторами. Однако они невзаимосвязаны и характер оценки может не совпадать.
РАДИКАЛЬНАЯ ПОЛИМЕРИЗАЦИЯ Радикальная полимеризация – это цепная реакция соединения мономер-
ных молекул, осуществляемая при участии активных частиц с неспаренным электроном – свободных радикалов, образующихся при гомолитическом разрыве химических связей. По радикальному механизму полимеризуются соединения с углерод-углеродными кратными связями. Соединения с другими кратными связями по радикальному механизму не полимеризуются.
Возможность мономеров полимеризоваться по радикальному механизму определяется их строением и условием проведения процесса. Поскольку каждый элементарный акт реакции представляет собой атаку неспаренным электроном π-связи мономера, то последняя должна быть определённым образом поляризована. Из классических представлений атаке будет подвергаться атом углерода, несущий частичный положительный заряд. Рассмотрим два вариан-
* - приведённая здесь последняя схема носит формальный характер, не отражает механизма процесса, а служит отображением сути – исчезновение активного центра

та поляризации молекулы монозамещённого винильного мономера с электроноакцепторным и электронодоннорным заместителями (Y).
R. + |
δ+ |
|
|
δ- |
|
|
|
|
|
|
|
. |
(1) |
||
CH2 |
|
|
CH |
R |
|
|
CH2 |
|
|
CH |
|||||
|
|
|
|
|
|
||||||||||
|
|
||||||||||||||
|
|
|
|
|
Y |
|
|
|
|
|
|
|
Y |
|
|
. |
δ+ |
|
δ- |
|
|
|
|
|
|
|
. |
|
|||
R + |
CH |
|
|
CH |
R |
|
CH |
|
CH |
(2) |
|||||
|
|
|
|
||||||||||||
|
|
||||||||||||||
|
|
|
2 |
|
|
|
|
|
|
|
2 |
||||
|
Y |
|
|
|
|
|
|
|
Y |
|
|
|
|||
Атаке будет способствовать наличие частичного положительного заряда на β-углеродном атоме, который контролируется электроноакцепторным характером заместителя Y (как по индукционному, так и по мезомерному механизму). Возникающий в результате реакции (1) радикал будет энергетически более выгоден вследствие стабилизации его заместителем, чем в случае электронодонорного заместителя (2). Поэтому для второго варианта полимеризация не характерна и в лучшем случае возможно образование низкомолекулярных смолообразных продуктов.
Так как возможность перекрывания орбиталей атакующего радикала и электронов π-связи весьма чувствительна к стерической загруженности атакуемого атома углерода мономера, то первый вариант и в этом случае предпочтительнее. Наличие одного даже очень объёмного заместителя не лишает мономера к способности к полимеризации по радикальному механизму, а уменьшает лишь скорость реакции. Введение второго заместителя затрудняет реакцию (с учётом и электронного фактора), при увеличении его размера (радиус более 2.1 Å) процесс становится невозможным. К этому же приводит наличие двух заместителей у соседних атомов углерода, не вызывающих поляризации молекулы мономера.
Например, легко полимеризуются хлорэтилен (винилхлорид – СН2=СНCl) и 1,1-дихлорэтилен (винилиденхлорид – СН2=ССl2), 1,2- дихлорэтилен (СНCl=СНCl) теряет способность к полимеризации. Легко полимеризуется стирол (СН2=СНС6Н5), хуже - -метилстирол (СН2=С(СН3)С6Н5), лишены способности к полимеризации 1,1-дифенилэтилен (СН2=С(С2Н5)2 и 1,2-дифенилэтилен С6Н5СН=СНС6Н5.
Рассмотрим отдельные стадии радикальной полимеризации.
I. Иницирование. На этой стадии генерируемый каким-либо образом активный радикал атакует молекулу мономера
R + M
+ M  RM
RM
В зависимости от метода получения свободных радикалов различают:

а) термическую полимеризацию, когда свободные радикалы образуются путём раскрытия двойной связи под воздействием тепла. Механизм термического инициирования изучен недостаточно. Одной из причин является то, что инициирование может осуществляться термическим распадом случайных примесей (в том числе и следов кислорода, избавиться от присутствия которого в мономере достаточно сложно). Тем не менее, для стирола и метилметакрилата доказана возможность термического инициирования. Большинством авторов установлена бимолекулярность реакции и, что возникающие первоначально бирадикалы трансформируются в моно радикалы, и рост цепи осуществляется с их участием.
Предполагаемая схема термической полимеризации стирола выглядит следующим образом: при нагревании, с увеличением энергии теплового движения, столкновение молекул мономера приводит к образованию бирадикалов
CH2 CHPh + CH2 CHPh |
t |
[PhCH CH |
+ CH |
CHPh] |
|
||||
|
|
2 |
2 |
|
PhCH CH2 CH2 CHPh
Далее возможна реакция передачи цепи на мономер, результатом которой является образование двух монорадикалов, начинающих рост цепей полимера
PhCH CH2 |
CH |
|
CHPh |
+ CH |
CHPh |
|
2 |
|
2 |
||
PhCH |
CH2 CH |
CHPh |
+ CH3 CHPh |
||
Термическая полимеризация протекает крайне медленно, скорость её зависит от температуры. Однако увеличение скорости за счёт повышения температуры приводит к нежелательным последствиям: уменьшается молекулярная масса, увеличивается вероятность деструктивных процессов, возрастает нерегулярность строения молекул, а из-за возрастания доли реакций передачи цепи на полимер увеличивается степень разветвлённости молекул. Тем не менее, термическую полимеризацию используют для получения стирола, отверждения лаковых покрытий и ряде производств.
б) фото полимеризацию, протекающую при облучении мономера светом обычно в интервале длин волн 250 – 360 нм. Возможно использование лазерного излучения и в определённых условиях диапазона видимого света. Предполагается, что молекула мономера, поглотив квант света, переходит в возбуждённое состояние и может претерпевать гомолитический разрыв с образованием радикалов, например:

|
h |
|
C6H5 + |
CH |
CH2 |
CH2 CHPh |
CH2 |
CHPh* |
|
|
|
|
|
|
|||
|
|
|
C6H5CH |
CH |
+ H |
Однако не всё электромагнитное излучение, поглощенное мономером и вызвавшее возбуждение его молекул, приводит к образованию соответствующего количества радикалов. Это является следствием того, что возбуждение снимается за счёт концентрационной (столкновение возбуждённой и невозбуждённой молекулы, сопровождающейся передачей части энергии последней) и спонтанной (выброс кванта поглощённого электромагнитного излучения) дезактивации. Эффективность фото инициирования оценивают квантовым выходом ( ), величина которого характерна для каждого мономера и характеризует его способность к фото полимеризации.
С целью повышения эффективности инициирования и увеличения скоро-
сти реакции применяют фотоинициаторы и фотосенсибилизаторы.
Фотоинициаторы – вещества, поглощающие свет и распадающиеся на свободные радикалы легче, чем молекулы мономера. В качестве них используют дикарбонильные соединения (циацетил, дибензоил), перекиси.
O |
O |
|
O |
|
O * |
O |
|||||||||||
|
|
|
|
|
|
|
hν |
|
|
|
|
|
|
|
|
|
|
RC |
|
CR |
RC |
|
CR |
2 RC |
|||||||||||
|
|
|
|||||||||||||||
Фотосенсибилизаторы (Ф)– вещества, молекулы которых поглощают свет в области спектра, в которой молекулы мономера не возбуждаются (например, видимая область), и передают им свою энергию возбуждения.
Ф + hν |
Ф* +M Ф + M* |
В качестве таковых используются вещества с развитой системой сопряжения – красители (эозин, флуоресцеин), бензофенон, дикарбонильные соединения и др. В процессе инициирования могут участвовать и растворители, например, четырёххлористый углерод. Увеличение эффективности инициирования и существенное возрастание скорости полимеризации связано с взаимодействием возбуждённой молекулы мономера с CCl4 и образованием активных свободных радикалов.
C6H5CH |
|
CH2* + CCl |
C H CH |
|
CH Cl |
+ CCl |
|
|
|||||||
|
|
||||||
4 |
6 |
5 |
2 |
3 |
|||
В отсутствие CCl4 с большей вероятностью происходит спонтанная или концентрационная дезактивация возбуждённых молекул мономера.
Невысокая энергия активации стадии инициирования позволяет вести фотополимеризацию при температурах, при которых полимеризация, инициируемая другими методами, не протекает.

в) радиационную полимеризацию, когда образование свободных радикалов происходит при облучении мономеров , , -излучением, быстрыми электронами и другими частицами высокой энергии.
Квант ионизирующего излучение по принципу Гейзенберга вызывает возбуждение целой области в веществе, при этом атомы, составляющие молекулу мономера, теряют электрон, который способен произвести многочисленные вторичные акты ионизации.
M |
излучение |
M+ |
_ |
+ e |
|||
|
|
|
Расходуя свою энергию на образование ионов и так называемых “быстрых” электронов (электронов с высокой энергией), этот электрон превращается в “тепловой” электрон (е–). Последний захватывается ионами, которые превращаются в возбуждённые молекулы
M+ + e-  M*
M*
Возбуждённая молекула может претерпевать распад с образованием активных радикалов
M*  R1 + R2
R1 + R2
Взависимости от строения мономера и конкретных условий механизм реакции может меняться от радикального до ионного.
Недостатком данного вида полимеризации является то, что при облучении происходит частичная деструкция полимерных цепей, которая при малых дозах облучения заключается в отщеплении подвижных атомов, что приводит
кобразованию разветвленных и сетчатых структур. Правда, в определённых случаях, это является положительным моментом и используется при отверждении лаковых покрытий и композитов. Используется радиационная полимеризация и для получения ряда полимеров – полиэтилена, полистирола поливинилхлорида и др.
г) инициированную полимеризацию, являющуюся наиболее распространённым методом синтеза высокомолекулярных соединений, при котором повышение скорости реакции достигается созданием в системе свободных радикалов без участия молекул мономера. Радикалы генерируются за счёт введения специальных добавок – инициаторов.
Вкачестве инициаторов возможно использование свободных радикалов. Источником свободных радикалов может служить, например, динитрилтетрафенилянтарной кислоты, который представляет собой равновесную смесь динитрила и дифенилцианметила.
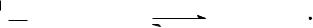
|
|
C6H5 |
C H |
|
|
|
|
C6H5 |
||||||
|
|
|
|
|
|
6 |
|
5 |
|
|
|
|
|
|
NC |
|
C |
|
C |
|
CN |
|
2 NC |
|
C |
||||
|
|
|
|
|||||||||||
|
|
|
||||||||||||
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C6H5 |
C H |
5 |
|
|
|
C6H5 |
||||||
|
|
|
|
|
6 |
|
|
|
|
|
|
|||
Введение свободных радикалов практикуется редко. Обычно в реакционную смесь добавляют соединения, легко распадающиеся в условиях реакции на радикалы. Так как энергия активации гомолитического распада инициаторов меньше (для перекисей 120-155 кДж/моль), чем энергия образования свободных радикалов из мономера, то введение инициатора позволяет понизить температуру реакции, повысить скорость первой стадии полимеризации – инициирование и, соответственно суммарную скорость реакции.
В качестве инициаторов используют различного рода перекиси - органические (бензоила, третбутила, гидроперикись изопропилбензола и др.), неорганические (персульфаты калия, натрия, аммония, перекись водорода), азо- и диазосоединения (динитрил азобисизомасляной кислоты, диазоаминобензол, метилфенилтриазин). Количество используемого инициатора колеблется в пределах 0,1 – 1% от массы мономера.
При нагревании перекисей происходит гомолитический разрыв О-О связей или элиминирование азота в случае диазосоединений с образованием свободных радикалов. Скорость инициирования мало зависит от природы мономера, и выбор инициатора определяется температурой, при которой достигается необходимая скорость образования свободных радикалов. Рабочие области некоторых наиболее употребляемых инициаторов приведены в табл. 1.
Таблица 1. Температуры распада инициаторов радикальной полимеризации.
|
Иницитор |
Рабочая область |
|
|
|
|
температур, С |
Название |
|
Формула |
|
|
|
||
|
|
|
|
Перекись бензоила |
|
С6Н5-СО-О-О-СО-С6Н5 |
80-95 |
|
|
|
|
Перекись трет-бутила |
|
(СН3)3С-О-О-С(СН3)3 |
120-140 |
|
|
|
|
Гидроперикись изопро- |
|
С6Н5С(СН3)2-О-О-Н |
130-140 |
пилбензола |
|
|
|
|
|
|
|
Динитрил азобисизомас- |
|
(CN)(CH3)2C-N=N-C(CH3)2(CN) |
40-70 |
ляной кислоты |
|
|
|
|
|
|
|
Метилфенилтриазин |
|
CH3-N=N-NH-C6H5 |
100-110 |
|
|
|
|
Диазоаминобензол |
|
C6H5-N=N-NH-C6H5 |
120-130 |
|
|
|
|
Одной из характеристик инициатора является эффективность инициирования (f), представляющая собой отношение числа радикалов, вызвавших полимеризацию, к общему числу радикалов, образовавшихся в результате распада инициатора. Появление этой характеристики связано с так называемым клеточным эффектом и побочными превращениями первичных радикалов.
Клеточный эффект заключается в том, что образующиеся в первый момент после распада инициатора радикалы окружены молекулами мономера и растворителя (как в “клетке”). Пока они не успели разойтись, кроме атаки молекулы мономера, возможна их первичная рекомбинация.
R O O R |
R O + O R |
Внешне это выглядит как равновесие между инициатором и продуктами его распада. Данное обстоятельство сохраняет инициатор на всё время проведения реакции полимеризации. В то же время некоторые радикалы способны к дальнейшим превращениям, а их продукты к рекомбинации между собой или с первичными радикалами. Например, при распаде перекиси бензоила образуются первоначально бензоатные радикалы, а затем – фенильные.
O
C6H5OC O C6H5C O 
|
|
O |
O |
||||||
|
|
|
|
|
|
|
|
|
|
O |
|
CC6H5 |
2C6H5C |
|
O |
||||
|
|
||||||||
|
|
|
|
C6H5 + |
CO |
||||
|
|
|
|
|
2 |
|
|
|
|
Кроме присоединения к молекулам мономера (инициирование) они могут взаимодействовать друг с другом, понижая эффективность инициирования.
O |
|
|
|
|
|
O |
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C6H5C |
|
O |
+ C H |
|
C H C |
|
O |
|
C H |
||||||||
|
|
||||||||||||||||
|
|
|
|
||||||||||||||
|
|
|
|
|
6 |
5 |
|
6 |
5 |
|
|
|
6 |
5 |
|||
C6H5 + |
C6H5 |
|
C H |
|
C H |
|
|||||||||||
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
6 |
5 |
|
6 |
|
5 |
|
|
|
||
В зависимости от способности первичных радикалов к побочным превращениям эффективность инициирования для различных инициаторов колеблется в довольно широких пределах. Для перекиси бензоила f составляет пооряка 0.8, для динитрила азобисизомасляной кислоты в пределах 0.5 – 0.7, а перекиси трет-бутила – 1.
При проведении полимеризации под действием перекисей часто используют окислительно-восстановительное инициирование. В этом случае в систему вводят восстановитель – промотор. Особенностью окислительновосстановительного инициирования является снижение энергии активации расщепления перекисей (40-55 кДж/моль), что позволяет проводить процесс полимеризации при более низких температурах, снижая тем самым возможность протекания побочных процессов. Например, полимеризация метилме-
