
- •Раздел I. Особенности термодинамики, как науки.
- •I.1. Основные определения термодинамики.
- •Пример 3. Химические реакции и фазовые превращения:
- •Правило знаков для потенциалов:
- •I.2. Теплота, работа, внутренняя энергия.
- •I.3. Равновесные и неравновесные взаимодействия. Статические и нестатические процессы.
- •I.4. Состояния системы. Уравнения состояния системы.
- •I.5. Реальные свойства газа. Уравнение состояния реального газа.
- •I.6. Работа и теплота. Свойства работы и теплоты.
- •I.7. Характеристические функции.
- •Мнемонический приём для термодеформационной системы:
- •I.8. Дифференциальные соотношения термодинамики.
- •Раздел II. Теория теплоёмкостей однородных систем.
- •II.1. Классификация теплоемкостей по единицам количества вещества и видам процессов.
- •II.2. Общая формула теплоёмкостей однородных систем.
- •II.3. Внутренняя энергия и теплоёмкость идеального газа.
- •II.4. Зависимость теплоёмкостей от давления, объёма и температуры.
- •II.5. Зависимость теплоёмкостей от температуры. Истинная и средняя теплоёмкости.
- •Раздел III. Вычисление энтропии.
- •III.1. Три группы формул для вычисления энтропии.
- •III.2. Уравнение адиабаты реального газа в общем виде.
- •Раздел IV. Политропный (политропический) процесс.
- •IV.1. Уравнение политропы. Определение показателя политропы.
- •IV.2. Работа, теплота и внутренняя энергия в политропном процессе.
- •IV.3. Изменение энтропии в политропном процессе.
- •Раздел V. Исследование изопроцессов. Работа, теплота, внутренняя энергия в изопроцессах.
- •Раздел VI. Второй закон термодинамики.
- •V рис. 18. Произвольный прямой обратимый цикл.
II.3. Внутренняя энергия и теплоёмкость идеального газа.
Используем
уравнение состояния идеального газа
pv
= RT
для нахождения частных производных
![]() ,
,![]() входящих в уравнения (74) и (75):
входящих в уравнения (74) и (75):
Для этого продифференцируем уравнение Менделеева-Клайперона pv=RT:
p dv + v dp = R dT, откуда имеем
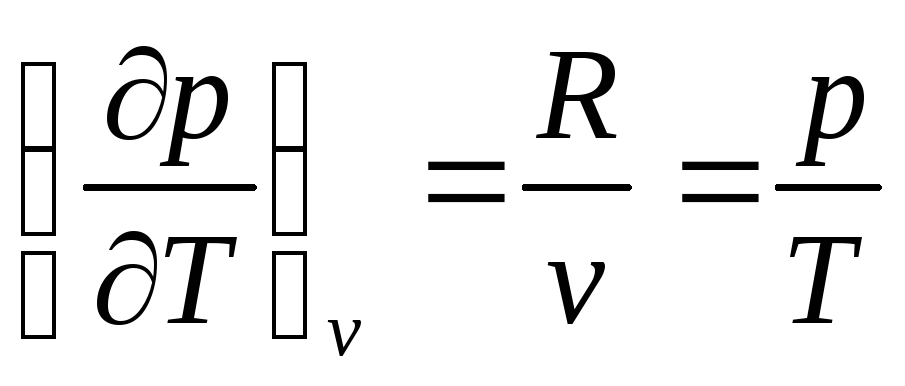 (77)
(77)
 (78)
(78)
Подставим
в (73*) значение
![]() из
уравнения (77) для идеального газа:
из
уравнения (77) для идеального газа:
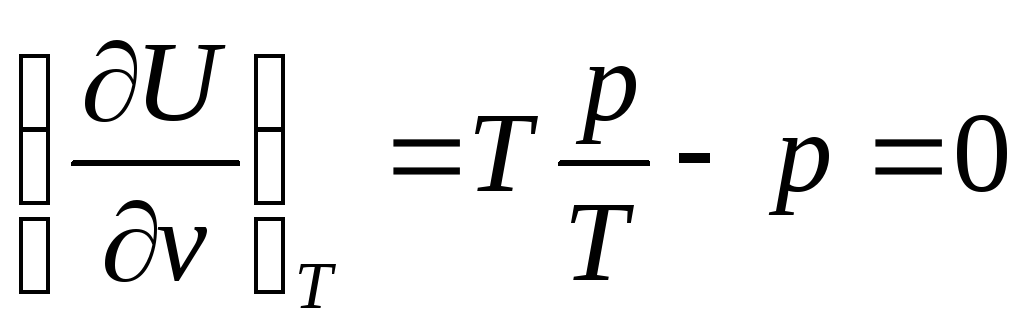




Окончательно
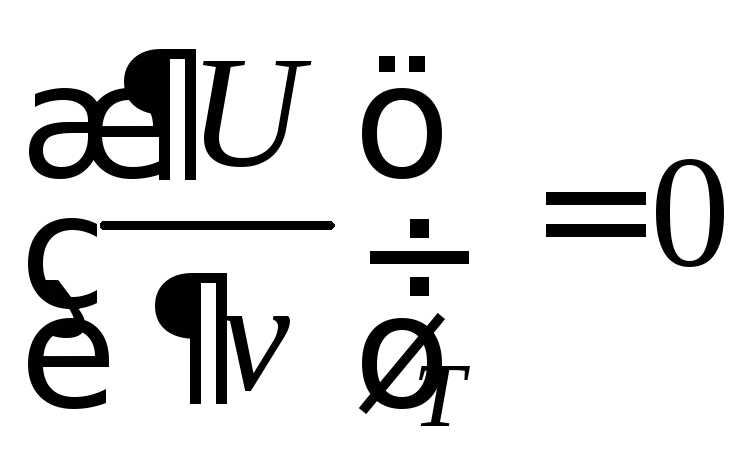 (79)
(79)
Таким образом, внутренняя энергия идеального газа от величины объёма не зависит. Математически этот факт записывается как
UU(v) (79*)
Исследуем
вопрос о зависимости внутренней энергии
идеального газа от величины давления.
Найдем частную производную 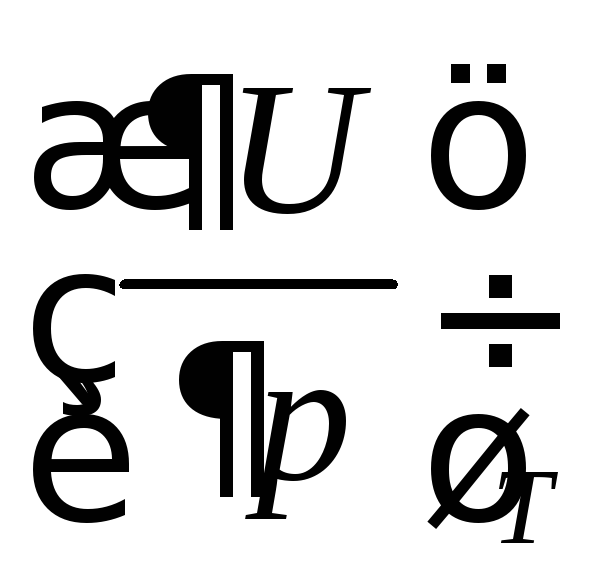 , для чего запишем ее в виде произведения
двух частных производных:
, для чего запишем ее в виде произведения
двух частных производных:
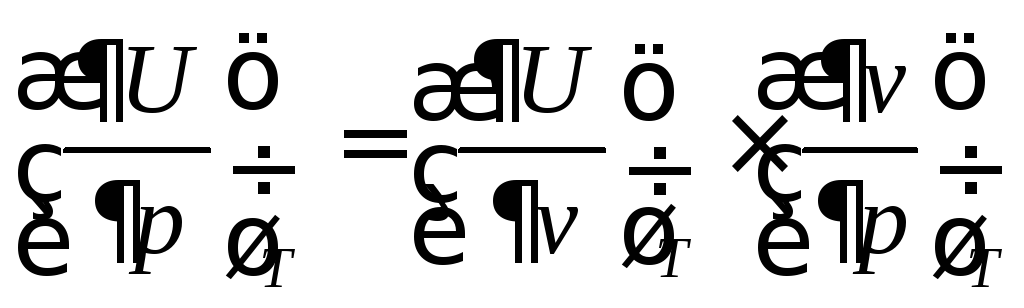
Из
(79) 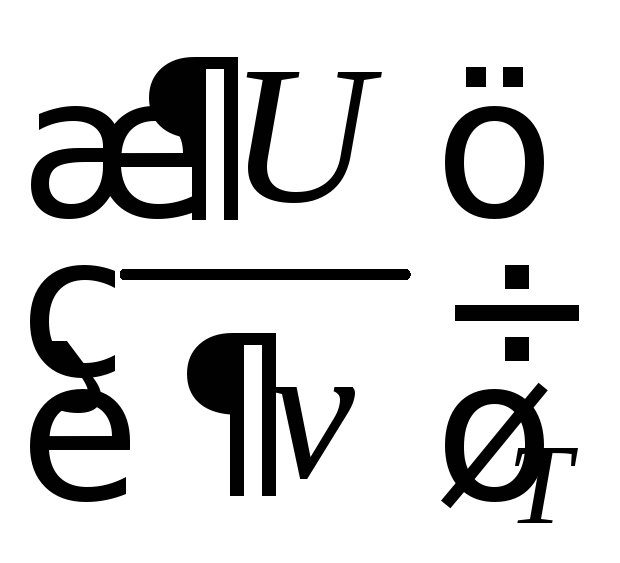 =0.
Изотермическая сжимаемость по своей
физической сути величина конечная, т.е.
=0.
Изотермическая сжимаемость по своей
физической сути величина конечная, т.е.
 .
.
Тогда окончательно
 =0
(80)
=0
(80)
Из формулы (80) следует, что внутренняя энергия идеального газа не зависит от величины давления, то есть UU(р)
Следовательно, внутренняя энергия идеального газа зависит только от температуры.
Ранее было получено
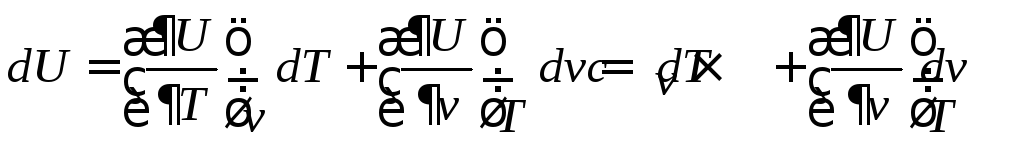
Так
как из (79)
![]() ,
то
,
то
dU = cv dT (81)
Интегрируя (81) получим:
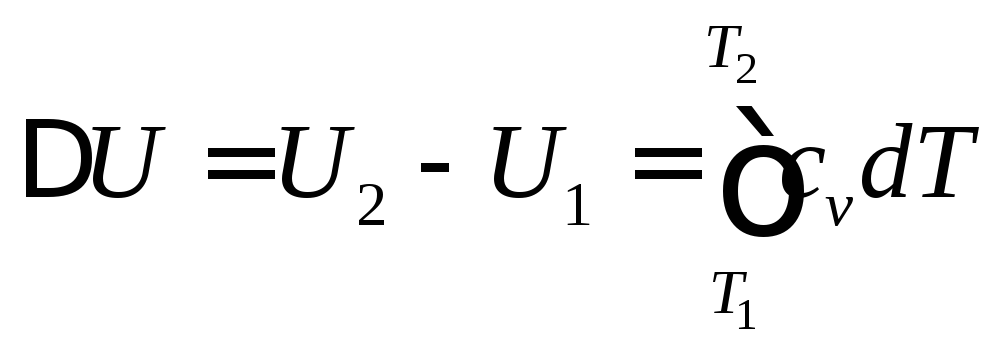 (82)
(82)
Общая формула (82) – используется для расчета изменения внутренней энергии во всех процессах идеального газа. Для вычисления по этой формуле нужно знать зависимость Сv от Т.
Е сли
в диапазоне температур отT1
до T2,
cv
взять средним значением (сv),
то, после интегрирования (82) получим
сли
в диапазоне температур отT1
до T2,
cv
взять средним значением (сv),
то, после интегрирования (82) получим
 U
= cv(T2-T1)
(83)
U
= cv(T2-T1)
(83)
Формула (83) в дальнейшем будет использоваться в инженерных расчетах для определения изменения внутренней энергии идеального газа в любом процессе.
Значение
внутренней энергии из (81) после
интегрирования запишется как
![]() ,
гдеU0
– постоянная интегрирования, определяемая
особым образом.
,
гдеU0
– постоянная интегрирования, определяемая
особым образом.
Получим формулу для массовой изобарной теплоёмкости идеального газа. Подставим в формулу (75)
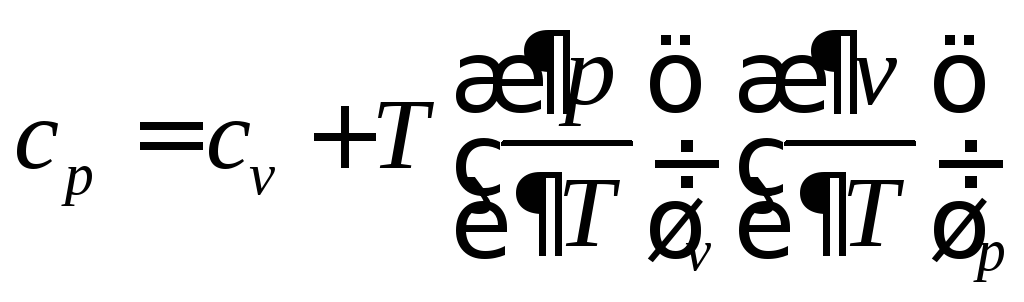 ,
значения частных производных из (77) и
(78):
,
значения частных производных из (77) и
(78):
![]()
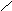
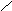
Окончательно
![]() (85)
(85)
Формула (85) называется уравнением Майера. Из этой формулы следует, что массовая изобарная теплоёмкость больше массовой изохорной теплоёмкости идеального газа на величину удельной газовой постоянной R.
Для мольных теплоёмкостей уравнение Майера запишется в виде:
![]() =
8314
=
8314![]() (86)
(86)
Таким образом молярная изобарная теплоемкость больше молярной изохорной на величину универсальной газовой постоянной.
Отношение изобарной теплоемкости к изохорной называется показателем адиабаты
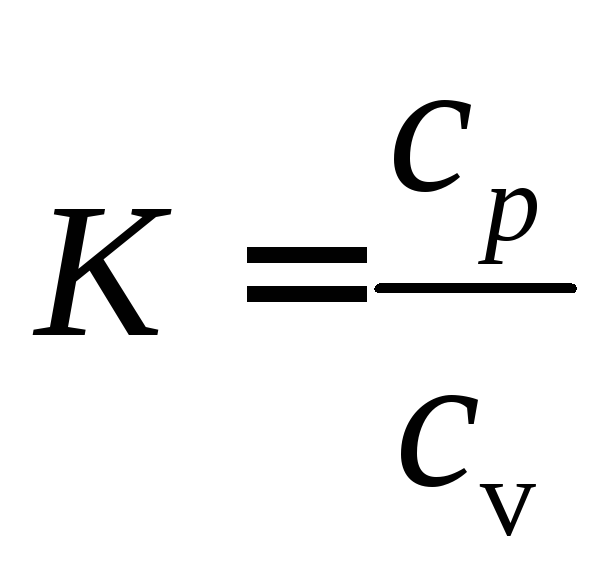 (87)
(87)
Иногда показатель адиабаты называют коэффициентом Пуассона. В соответствие с уравнением Майера К > 1.
В инженерных расчетах для всех двухатомных газов, включая воздух, полагают K1,4.
В действительности, с ростом температуры показатель адиабаты слабо убывает.
