
ответы теплотехника
.pdf
Билет №1
1вопрос: Основные термодинамические параметры состояния газа.
Давление
Р– мера силы, которая действует на единицу поверхности:
Р= lim ∆Fn / ∆S = dFn/ dS,
где DS → 0; ∆Fn – сила, направленная перпендикулярно участку поверхности.
Удельный объем
V – величина, обратная плотности rвещества: v = 1 / r= dV/ dm,
где dV– бесконечно малый элемент объема; dm– масса вещества.
Моль Количество вещества, которое содержит число молекул, равное числу атомов, содержащихся в 12
г изотопа углерода 12С, называется молем.
Число Авогадро
NA= 6,02 ч 1023 моль-1. Величина, необходимая при расчетах. Показывает, сколько молекул содержится в одном моле любого вещества.
Молярная масса
М– масса одного моля:
М= NAm × 1 а. е. м,
где NA– число Авогадро; m– молекулярная масса.
Молярная масса [M] = кг/моль и молярный объем [VM] = м3/моль.
Объем одного моля – молярный объем: VM = M / r
где M– молярная масса; r– плотность вещества.
Формулы для определения числа молей вещества и числа молекул вещества имеют следующий вид:
u= m /M= V/ VM,
N = uNA= (m / M)NA = (V/ VM)NA.
Температура За меру температуры принято брать среднюю кинетическую энергию поступательного движения
молекул. Если два тела при соприкосновении не обмениваются энергией путем теплообмена, можно говорить, что эти тела имеют одинаковую температуру и в системе существует тепловое равновесие.
2вопрос: Материальный баланс процесса горения: Для расчета процессов горения
твердого и жидкого топлива составляют материальный баланс процесса горения.
Материальный баланс процесса горения выражает количественные соотношения между исходными веществами (топливо, воздух) и конечными продуктами (дымовые газы, зола, шлак) При сжигании твердого и жидкого топлива горючие вещества могут окисляться с образованием оксидов различной степени окисления. Стехиометрические уравнения реакций горения углерода, водорода и серы можно записать так:
а) С+О2=СО2;
б) С+(1/2)·О2=СО; в) S+О2=SО2;
г) H2+(1/2)·О2=H2О;

При расчете объемов воздуха и продуктов сгорания условно принимают, что все горючие вещества окисляются полностью с образованием только оксидов с наивысшей степенью окисления (реакции а, в, г).
Из уравнения (а) следует, что для полного окисления 1 кмоль углерода (12 кг) расходуется 1 кмоль, т. е. 22,4 м3, кислорода и образуется 1 кмоль (22,4 м3) оксида углерода. Соответственно для 1 кг углерода потребуется 22,4/12 = 1,866 м3 кислорода и образуется 1,866 м3 СО2. В 1 кг топлива содержится Сp/100 кг углерода. Для его горения необходимо 1,866·Сp/100 м3 кислорода и при сгорании образуется 1,866 Сp/100 м3 CO2.
Аналогично из уравнений (в) и (г) на окисление горючей серы (µs = 32), содержащейся в 1 кг топлива, потребуется (22,4/32) Spл/100 м3 кислорода и образуется такой же объем SO2. А на
окисление водорода ( 









 ), содержащегося в 1 кг топлива, потребуется 0,5·(22,4/2,02) Нp/100 м3 кислорода и образуется (22,4/2,02) Нp/100 м3 водяного пара.
), содержащегося в 1 кг топлива, потребуется 0,5·(22,4/2,02) Нp/100 м3 кислорода и образуется (22,4/2,02) Нp/100 м3 водяного пара.
Суммируя полученные выражения и учитывая кислород, находящийся в топливе( 










 ),после несложных преобразований получим формулу для определения количества кислорода, теоретически необходимого для полного сжигания 1 кг твердого или жидкого топлива, м3/кг:
),после несложных преобразований получим формулу для определения количества кислорода, теоретически необходимого для полного сжигания 1 кг твердого или жидкого топлива, м3/кг:
Ввоздухе содержится кислорода примерно 21 % по объему, поэтому количество воздуха, теоретически необходимое для полного сжигания 1 кг топлива V0, м3/кг, составляет:
Впроцессе полного горения с теоретически необходимым количеством воздуха образуются газообразные продукты, которые состоят из CO2, SO2, N2 и H2O - оксиды углерода и серы являются сухими трехатомными газами. Их принято объединять и обозначать через RO2 = CO2 + SO2.
Вопрос3 Теплопроводность. Уравнение Фурье и его анализ.
Теплопроводность — это перенос тепловой энергии структурными частицами вещества (молекулами, атомами, ионами) в процессе их теплового движения. Такой теплообмен может происходить в любых телах с неоднородным распределением температур, но механизм переноса теплоты будет зависеть от агрегатного состояния вещества Закон ФУРЬЕ
Q = -λ grad tFτ [Дж]
Количество теплоты, проходящее через изотермическую поверхность площадью F за время τ , пропорционально температурному градиенту.
λДж ® 0 < λ < 400 - коэффициент теплопроводности.м× К
Знак минус в формуле показывает, что теплота и градиент направлены в разные стороны.
λ- физическая характеристика материала (зависит от температуры, определяется экспериментально, величина табличная).
λ- количество теплоты, проходящее между двумя изотермическими поверхностями площадью 1м3 за 1с при единичном температурном градиенте.
Анализ уравнения устанавливает количественную связь между тепловым потоком и разностью температур в двух точках тела: количество переданной теплоты пропорционально градиенту температуры, времени и площади сечения F, перпендикулярного к направлению распространения теплоты.
БИЛЕТ №2
1 вопрос Термодинамическая система и окружающая среда.

Термодинамической системой называется совокупность тел поведение которых изучается термодинамическими методами. Все остальные тела, не входящие в состав термодинамической системы, объединяются в понятии окружающая среда.
Поведение окружающей среды и изменения, происходящие в ней, при термодинамическом анализе не рассматриваются. Для термодинамического исследования системы безразлично, из чего состоит окружающая среда и что в ней происходит. Если методами термодинамики исследуются поведение и свойства какого-нибудь вещей Можно рассматривать как одно тело так и его части. например газ в цилиндре двигателя, тут
термодинамической системой является газ, а окружающей средой — стенки цилиндра и поршень.
Вещество, которое совершает работу в той или иной машине, обычно называют рабочим телом. Часто при рассмотрении тех или иных вопросов окружающую среду представляют в виде одного или нескольких тел с определенными свойствами.
Система, которая лишена возможности обмениваться энергией с окружающей средой, называется изолированной. Такая изолированная термодинамическая система находится в определенном состоянии, которое не может измениться само собой, без воздействия на систему окружающей среды, если же система не изолирована и обменивается энергией с окружающей средой, то ее состояние изменяется. Изменение состояния термодинамической системы в результате обмена энергией с окружающей средой называется термодинамическим процессом.
2 вопрос Скорость химических реакций окисления горения топлив. Влияние температуры, давления и концентрации на скорость горения.
3 вопрос Коэффициент теплопроводности, его физический смысл, факторы, влияющие на его значение.
Коэффициент теплопроводности (Вт/(м*К)) - численная характеристика теплопроводности материала, равная количеству теплоты, проходящей через материал толщиной 1 м и площадью 1 кв.м за час при разности температур на двух противоположных поверхностях в 1 град.C. Коэффициент теплопроводности газов определяется формулой
Где: i — сумма поступательных и вращательных степеней свободы молекул (для двухатомного газа i=5, для одноатомного i=3), k — постоянная Больцмана, M — молярная масса, T — абсолютная температура, d — эффективный диаметр молекул, R — универсальная газовая постоянная. Из формулы видно, что наименьшей теплопроводностью обладают тяжелые одноатомные (инертные) газы, наибольшей — легкие многоатомные (что подтверждается практикой, максимальная теплопроводность из всех газов — у водорода, минимальная — урадона, из не радиоактивных газов - у ксенона).
Теплопроводность зависит от многих показателей. В их число следует включить плотность, влажность, температуру, структуру, текстуру и минеральный состав вещества.
БИЛЕТ N 3
1 вопрос Равновесное и неравновесное состояние термодинамической системы
Термодинамическая система может находиться в различных соотношениях со средой. Неравновесное состояние, это при котором в системе происходит или может в любой момент начаться одностороннее направленное изменение её параметров может вследствие несоответствия их с параметрами состояния среды.
Своеобразной разновидностью неравновесного является стандартное (установившиеся) состояние. В нем система находится как бы в покое, без видимого изменения её параметров благодаря воздействию внешних по отношению к данной системе процессов. Равновесным является такое состояние системы, при котором действие процессов внутри
системы приводит к её выходу из равновесия, полностью компенсируется противодействием процессов, идущих во внешней среде.
Необходимым условием равновесия является равенство соответствующих интенсивных параметров и химических потенциалов компонентов во всех частях системы. Существуют различные виды равновесных состояний:

-стабильная, при которой система устойчива как к бесконечно малым, так и к конечным изменениям параметров её состояния, т.е. для вывода системы из равновесия необходимо затратить работу
-устойчивое
-подвижное (мобильное)
-неустойчивое (лабильное)
Таким образом, если хотя бы один из параметров состояния изменяется, то изменяется и состояние системы, т.е. происходит термодинамический процесс, который представляет совокупность изменяющихся состояний.
2 вопрос Методы расчетов и определения температуры горения
3 вопрос Свободная и вынужденная конвекция жидкости. Основной закон конвективного теплообмена.
Различают свободную и вынужденную конвекцию. В случае свободной конвекции движение в рассматриваемом объеме жидкости возникает за счет неоднородности в нем массовых сил. Например, если жидкость с неоднородным распределением температуры, и, как следствие, с неоднородным распределением плотности находится в поле земного тяготения, то в ней возникает свободное гравитационное движение.
Вынужденное движение рассматриваемого объема жидкости происходит под действием внешних поверхностных сил, приложенных на его границах, за счет предварительно сообщенной кинетической энергии (например, за счет работы насоса, вентилятора, ветра).
Вынужденное движение может сопровождаться свободным. Чем больше разница температур отдельных частиц среды и чем меньше скорость вынужденного движения тем больше влияние Относительного движения. Но при больших скоростях вынужденного движения - влияние свободной конвекции становится пренебрежимо мало.
Понятие конвективного теплообмена охватывает процесс теплообмена при движении жидкости или газа. При этом перенос теплоты осуществляется одновременно конвекцией и теплопроводностью. Под конвекцией теплоты понимают перенос теплоты при перемещении макрочастиц жидкости или газа в пространстве из области с одной температурой в
область с другой температурой. Конвекция возможна только в подвижной среде, здесь перенос теплоты неразрывно связан с переносом самой среды.
Если в единицу времени через единицу поверхности нормально к ней проходит масса
|
|
|
|
жидкости |
, где - скорость жидкости, а - ее плотность, то вместе с ней переносится |
||
энтальпия i: |
|
|
|
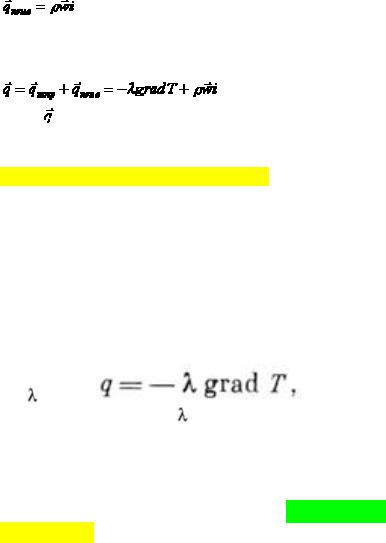
. |
(1) |
Конвекция теплоты всегда сопровождается теплопроводностью, т.к. при движении жидкости или газа неизбежно происходит соприкосновение отдельных частиц среды, имеющих различные температуры. В результате конвективный теплообмен описывается уравнением
. |
(2) |
Здесь 
 является локальным (местным) значением плотности теплового потока за счет конвективного теплообмена. Первое слагаемое в правой части уравнения (2) описывает перенос теплоты теплопроводностью, второе – конвекцией.
является локальным (местным) значением плотности теплового потока за счет конвективного теплообмена. Первое слагаемое в правой части уравнения (2) описывает перенос теплоты теплопроводностью, второе – конвекцией.
КОНВЕКТИВНЫЙ ТЕПЛООБМЕН - необратимый процесс переноса теплоты в движущихся средах с неоднородным полем темп-ры, обусловленный совместным действием конвекции и молекулярного движения.
Наиб. важный для практики случай - К. т. между движущейся средой и поверхностью её раздела с др. средой (твёрдым телом, жидкостью или газом) - наз. конвективной теплоотдачей. Вследствие вязкости движущейся среды она "прилипает" к поверхности раздела, в результате местная скорость среды относительно этой поверхности равна нулю. Поэтому плотность конвективного теплового потока, подходящего к поверхности раздела (или отходящего от неё), может быть описана с помощью закона теплопроводности (закона Фурье):
где - |
коэф. молекулярной теплопроводности, Т - |
температура среды. Если |
характеризует физ. свойства среды, то градиент температуры |
формируется под действием конвективного движения среды. Чем интенсивнее конвекция, тем больше градиент температуры.
БИЛЕТ N4
Вопрос №1 Понятие о термодинамическом процессе.
Термодинамической системой будем называть совокупность материальных тел, взаимодействующих как между собой, так и с окружающей средой; все другие материальные тела, находящиеся за пределами границ рассматриваемой системы, принято называть окружающей, или внешней средой.Если хотя бы один из параметров состояния меняется, то изменяется состояние системы, т. е. происходит термодинамический процесс, представляющий собой совокупность изменяющихся состояний рассматриваемой системы.
Все процессы, происходящие в термодинамической системе, можно разделить на равновесные и неравновесные. Равновесными называют процессы, представляющие собой непрерывную последовательность равновесных состояний системы (равновесное состояние системы подробно рассматривается в гл. 5; оно характеризуется, в частности, тем, что все части системы имеют одинаковую температуру и одинаковое давление). Неравновесным называют процесс, при протекании которого система не находится в состоянии равновесия (т. е. при протекании процесса различные части системы имеют различные значения температуры, давления, плотности, концентрации и т. д.).
Процесс, протекающий в системе, будет тем ближе к равновесному, чем меньше время выравнивания возмущений равновесного состояния системы, связанных с протеканием этого процесса, по сравнению с характерным временем процесса.
чем выше скорость протекания процесса, тем, как правило, большая неравномерность имеет место в системе при осуществлении этого процесса. В частности, в рассмотренном процессе сжатия газа в цилиндре различия в давлении газа в разных точках объема цилиндра и соответственно разность давлений по обе стороны поршня будут тем больше, чем выше скорость движения поршня. Если скорость перемещения поршия весьма мала, то и давления газа в различных точках объема цилиндра будут различаться весьма мало; при этом необходимое избыточное давление с внешней стороны поршия также будет весьма мало. Иными словами, чем

меньше скорость осуществления процесса, тем ближе этот процесс к равновесному.
Любой реальный процесс является в большей или меньшей степени неравновесным. Однако в принципе эта неравновесность может быть сделана сколь угодно малой в результате уменьшения скорости осуществления процесса. Таким образом, равновесный процесс является предельным случаем неравновесного процесса при стремлении скорости этого процесса к нулю; поэтому равновесные процессы иногда называют квазистатическими.
Вопрос №2 Температуры горения топлива.Тепло, выделяющееся при сгорании
топлива, воспринимается продуктами сгорания, которые нагреваются до определенной температуры, называемой температурой горения. Различают калориметрическую, теоретическую и действительную температуры сгорания топлива.
Вуравнение теплового баланса реального горения входят составляющие, величина которых зависит не только от теплофизических свойств топлива, но и от условий, при которых протекает горение. Например, от степени подогрева топлива и воздуха, потерь теплоты при горении, тепловосприятия в топке, коэффициента избытка воздуха.
Чтобы выявить потенциальные возможности топлива, вводят понятие горения без подогрева топлива и воздуха при идеальном адиабатическом процессе, т. е. горения с теоретическим количеством воздуха, без потерь теплоты и без теплообмена в топочной камере и с окружающей средой. Полученная в этих условиях температура продуктов сгорания называется теоретической. Калориметрическая температура отражает влияние подогрева топлива и воздуха и коэффициента избытка расхода воздуха α на температуру адиабатического горения. Повышение температуры подогрева топлива и воздуха увеличивает приход теплоты в зону горения и повышает температуру горения, а увеличение коэффициента избытка воздуха a вызывает увеличение объема продуктов сгорания Vг, что понижает температуру горения. Поэтому в зависимости от влияния этих факторов калориметрическая температура может быть выше или ниже теоретической.
Вреальных условиях не все тепло, выделяющееся при горении, идет на нагрев продуктов реакции, так как часть тепла передается экранной системе топочной камеры и некоторое количество тепла теряется в окружающую среду; кроме того, при высоких температурах происходит диссоциация части продуктов сгорания (СО2 и Н2О), сопровождающаяся поглощением тепла.
Для каждого типа топки, вида и способа сжигания топлива разработана специальная методика расчета теплообмена в топке и определения действительной температуры газов на выходе из топки.
Отношение действительной температуры горения топлива к теоретической
называется пирометрическим коэффициентом.
Вопрос №3 Физический смысл коэффициента теплоотдачи,факторы, влияющие на его значение.
Коэффициент теплоотдачи α характеризует процесс передачи тепла от некоторого теплоносителя (жидкость или газ) к твердой стенке. Определяется параметрами данного теплоносителя (режим течения, скорость, теплофизические характеристики типа плотности, вязкости и теплопроводности), а также характеристиками той части стенки, которая омывается данным теплоносителем (характерный размер, наличие оребрения и.д.).
Коэффициент теплопередачи k характеризует процесс передачи тепла между двумя теплоносителями через разделяющую их твердую стенку. Определяется коэффициентами теплоотдачи обоих теплоносителей и параметрами теплопередающей стенки (ее толщина и теплопроводность).
Разница между теплоотдачей α и теплопередачей k состоит в следующем. Суммарный перенос тепла складывается из нескольких стадий: стадия теплопереноса в первой среде, стадия теплопереноса от первой среды к стенке, стадия теплопереноса в самой стенке, стадия теплопереноса от стенки ко второй среде, стадия теплопереноса во второй среде. Коэффициенты теплоотдачи описывают отдельные стадии этого суммарного теплопереноса на стадии средастенка. А коэффициент теплопередачи описывает суммарный теплоперенос в целом со всеми его
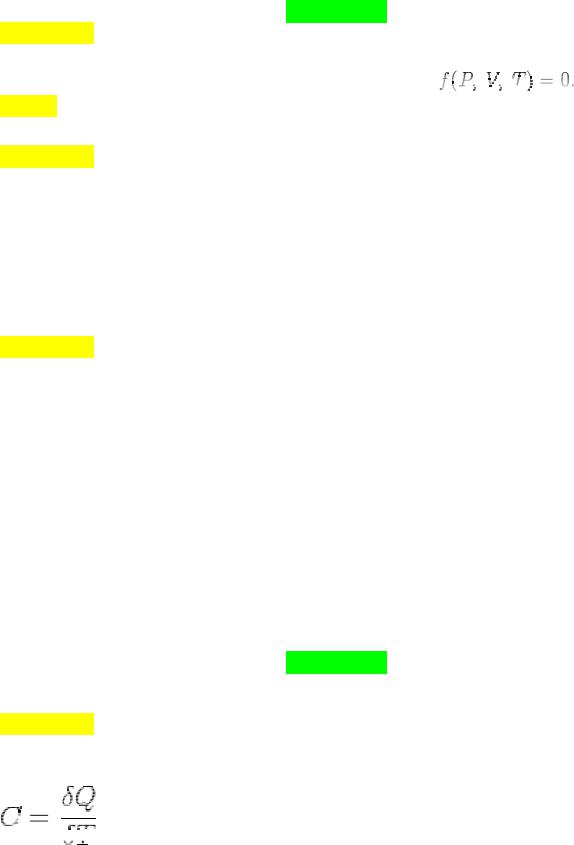
стадиями. По этой причине вначале всегда рассчитываются коэффициенты теплоотдачи α, а затем через них рассчитывается коэффициент теплопередачи k.
БИЛЕТ N5
Вопрос №1 Термодинамическое уравнение состояния
Термическое уравнение состояния связывает макроскопические параметры системы. Для системы с
постоянным числом частиц его общий вид можно записать так: |
|
|
или другими |
|
словами выражает связь между давлением Р температурой Т и удельным объемом V
(или плотностью) гомогенного вещества в состоянии равновесия
Вопрос №2 Коэффициент избытка воздуха при сжигании топлив, его определение.
Коэффициент избытка воздуха -это отношение действительно израсходованного при горении количества воздуха к теоретически необходимому.
Отношение действительного расхода воздуха Vд, подаваемого на сжигание топлива, к его теоретическому значению Vт называют коэффициентом избытка воздуха:
α = Vд / Vт
Коэффициент избытка воздуха в общем случае зависит от вида сжигаемого топлива, его состава, типа горелок, способа подачи воздуха, конструкции топочного устройства и т.д. Для сжигания природного газа обычно принимают α = 1,05... 1,15.
Вопрос №3 Критерии теплового подобия и их физический смысл
При анализе и решении сложных тепловых явлений и процессов, а также обработке и обобщении данных экспериментальных исследований в теории теплопередачи применяют безразмерные теплофизические комплексы, называемые критериями теплового подобия. Эти же критерии распространяются и на процессы сушки для изучения миграции влаги в материале, ее испарения и т. д., и тогда их называют гигрометрическими или влагообменными критериями подобия . Применительно к нагреванию и сушке древесины используют безразмерные критерии теплового, гигрометрического и гидродинамического подобия
основные критерии подобия,изпользуемые при тепловых расчетах
1.Рейнольдс Re (определяет режим течения жидкости - ламинарный или турбулентный)
2.Прандтль Pr (отношение кинематической вязкости к коэффициенту температуропроводности)
3.Грасгоф Gr (естественная конвекция)
4.Нуссельта Nu (вынужденная конвекция)
5.Био Bi (критерий термической массивности тела, определяется как отношение сопротивления передачи тепла теплопроводностью к сопротивлению передачи тепла конвекцией)
6.Фурье Fo (безразмерное время)
БИЛЕТ N6
Вопрос №1 Теплоемкость идеальных газов. Уравнение Майера.
Теплоемкость идеального газа — это отношение количества теплоты, сообщенного газу, к изменению температуры δТ, которое при этом произошло.
Согласно 1 началу термодинамики существует 2 способа изменить внутреннюю энергию тела (в нашем случае идеального газа): передать ему тепло или
совершить над ним работу. Вывод формулы для теплоемкости в идеальном




 процессе
процессе
dU=δQ+δA, где δA — работа окр. среды над газом. δAокр.среды=-δAгаза
δQ=dU+δAгаза
В расчете на 1 моль:
С=δQ/∆T=(∆U+p∆V)/∆T ∆U=CV*∆T C=CV+(p∆V/∆T)

Уравнение Майера Cp = Cv + R
Оно показывает, что расширение моля идеального газа при постоянном давлении и изменении его температуры на 1 Кельвин требует дополнительного, по сравнению с изобарическим расширением, количества теплоты, необходимого для совершения работы. Это значение равно универсальной газовой постоянной
Вопрос №2 Теоретический и действительный расход воздуха при горении топлива.
Теоретический расчет воздуха для горения По соотношению объемной доли кислорода в объеме воздуха можно получить следующее равенство:
Lмин. = |
100% |
• O 2, мин. = 4,762 • O 2, мин., |
21% |
то есть для получения 1 м3 кислорода необходимо 4,762 м3 воздуха.
Теоретический расход воздуха Lмин. определяется на основании долей отдельных газов в горючей смеси:
Lмин. = ∑ri • Li мин
Действительный расход воздуха для горения. Действительный расход воздуха определяется по формуле:
L = λ • Lмин.,
где λ — коэффициент избытка воздуха.
Значение коэффициента избытка воздуха варьируется в пределах 1,1 — 1,4. Более высокий коэффициент приводит к избыточному горению и увеличивает потери кислорода вместе с отходящим газом. Значение коэффициента избытка определяется по формуле:
λ= CO2, макс.
CO2, изм
Вопрос №3. Основное уравнение конвективного теплообмена в критериальной
форме
Используя теорию подобия из системы дифференциальных уравнений можно получить уравнение теплоотдачи для конвективного теплообмена в случае отсутствия внутренних источников тепла в следующем критериальной форме:Nu = f2(Х; Ф; X0; Y0; Z0; Re; Gr; Pr) где:X0;Y0;Z0 – безразмерныекоординаты;Nu = α ·l0/λ - критерий Нуссельта (безразмерный коэффициент теплоотдачи), характеризует теплообмен между поверхностью стенки и жидкостью (газом);
Re = w·l0/ν - критерий Рейнольдса, характеризует соотношение сил инерции и вязкости, и определяет характер течения жидкости (газа);
Gr = (β·g·l03·∆t)/ν2 - критерий Грасгофа, характеризует подьемную силу, возникающую в жидкости (газе) вследствие разности плотностей;
Pr = ν/а = (µ·cp)/λ - критерий Прандтля, характеризует физические свойства жидкости (газа); l0 – определяющий размер (длина, высота, диаметр).
