
Фармакология
.pdfГлава 5
СРЕДСТВА, РЕГУЛИРУЮЩИЕ ФУНКЦИИ ИСПОЛНИТЕЛЬНЫХ ОРГАНОВ И СИСТЕМ
Средства, регулирующие функции исполнительных органов, могут прямо воздействовать на клетки этих органов (тканей), либо оказывать косвенное влияние, опосредованное гуморальными факторами и нервной системой. Регуляция функций исполнительных органов посредством ЛВ, действующих первично на ЦНС или эфферентную иннервацию, изложена ранее.
1. СРЕДСТВА, ОКАЗЫВАЮЩИЕ ПРЯМОЕ ВЛИЯНИЕ НА ГЛАДКИЕ МЫШЦЫ
Морфологические и функционально-биохимические основы действия
Мышечный слой всех полых внутренних органов образован гладкомышеч- ными клетками (ГМК). В стенке артериол и венул их длина не превышает 20 мкм, но мышечные волокна беременной матки человека достигают 500 мкм. Диаметр ГМК составляет от 1,5-2 мкм (артериолы) до 15-20 мкм (матка). Поверхностная (плазматическая) мембрана ГМК включает структурные, ферментные, транспортные и рецепторные белки. Последние обеспечивают чувствительность ГМК к медиаторам пара- и/или симпатических нервов, а также к многочисленным гуморальным факторам: гормонам, простаноидам, кининам, гистамину, ангиотензинуII и др. Набор мембранных рецепторов и их плотность (кол-во на единицу поверхности) в ГМК разных органов генетически предопределен. Например, ГМК матки имеют рецепторы окситоцина, отсутствующие в ГМК большинства других органов. ГМК сосудов имеют, напротив, рецепторы, активируемые вазопрессином, ангиотензином, но не окситоцином. Н1- гистаминовые рецепторы имеются в ГМК бронхов, кишечника, матки, сосудов, а их плотность особенно высока в ГМК бронхов и посткапиллярных (капиллярно-венозных) сфинктеров.
Сократительный механизм ГМК представлен миофибриллами, состоящими из миофиламентов, построенных из актина и миозина. В отличие от поперечно исчерченных мышц гладкие мышцы не содержат тропонина. В ГМК сеть гладкого эндоплазматического ретикулума (ЭПР) развита слабо, занимая 2-7 % от объема клетки (в миокардиоцитах - до 20 % объема). Однако, ЭПР ГМК способен аккумулировать ионы Ca, а следовательно, регулировать их внутриклеточную концентрацию, от которой зависит базальный (миогенный) тонус гладкой мышцы. Эндогенные вещества и их имитаторы, способные повышать тонус и вызывать сокращение ГМК, повышают внутриклеточную концентрацию ионов Ca с 0,1 до 1 мкмоль/л. Возрастание внутриклеточной концентрации ионов Ca осуществляется при деполяризации ГМК и открытии п/з Ca-каналов (“медленных”), но чаще всего достигается в результате активации мембранных рецепторов, сопряженных с фосфолипазой С (см. рис. 3). В результате усиления образования инозитолтрифосфата (IP3) высвобождаются ионы Са из эндоплазматической сети ГМК (рис. 12). Высвободившиеся ионы Са активируют кальмодулин, а Са/кальмодулин способен активировать киназу легких цепей миозина. Эта киназа фосфорилирует легкие цепи
120
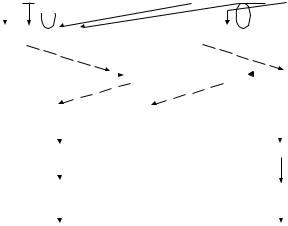
миозина, что делает возможным взаимодействие миозина с актином и укорочение (сокращение) мышечного волокна.
СОСУДЫ |
|
|
МАТКА |
|
||||||||||||||||
|
AT |
|
|
V1 |
|
|
|
|
OT |
|
|
ÏÃF β 2 |
||||||||
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
Gq |
|
|
|
|
|
Gs |
|
|
|
|
|
|||
фосфолипаза С |
|
Аденилат-циклаза |
||||||||||||||||||
фосфоинозитиды |
|
IP3 |
öÀÌÔ |
|
|
|
|
ÀÒÔ |
||||||||||||
|
|
|
|
|||||||||||||||||
Äåïî Ñà2+ в эндоплазматическом ретикулюме (ЭПР) |
||||||||||||||||||||
Высвобождение |
|
|
Ñà2+ èç ÝÏÐ |
|
|
|
|
|
|
|
||||||||||
|
|
Поглощение Са2+ ÝÏÐ |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Повышение Са2+ в цитозоле |
Понижение Са2+ в цитозоле |
|||||||||||||||||||
Сокращение |
|
|
|
|
|
Расслабление |
|
ìûøö |
||||||||||||
ìûøö |
|
|
||||||||||||||||||
|
|
|
||||||||||||||||||
Ðèñ.12. Важнейшие пути регуляции внутриклеточной концентрации ионов Са в гладкомышечных клетках под влиянием эндогенных регуляторов. АТ, V1, ÎÒ, ÏÃF, β2 - мембранные рецепторы в гладкомышечных клетках (сосудов и матки), активируемые соответственно ангиотензином-11, вазопрессином, окситоцином, простагландином F2a и адреналином; IP3 - инозитол-1,4,5-трифосфат, G - ГТФ-зависимые белки. Сплошные стрелки - процесс, пунктирные - влияние.
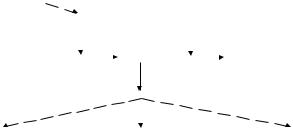
Расслабление гладких мышц происходит в результате снижения внутриклеточной концентрации ионов Са, которое может осуществляться путем уменьшения вхождения Са2+ через п/з Са-каналы, путем усиленного выведения Са2+ из ГМК посредством Са/Na-обменника и Са-АТФазы сарколеммы либо за счет усиленного поглощения Са эндоплазматическим ретикулумом (при активации Са-АТФазы ЭПР). На эти процессы существенно влияют некоторые вторичные посредники. Повышение вн/клеточной концентрации цАМФ уменьшает время открытого состояния п/з Са-каналов и усиливает поглощение ионов Са элементами ЭПР. Особенно важна роль активации гуанилатциклазы и повышения концентрации цГМФ, который является главным внутриклеточным посредником в релаксации ГМК. Релаксирующее действие цГМФ осуществляется посредством фосфорилирования специфи- ческой G-киназы. Эта киназа ингибирует фосфолипазу С, повышает активность Са-АТФазы ЭПР и фосфатазы легких цепей миозина. Дефосфорилирование последних фосфатазой сопровождается дезагрегацией актомиозина (рис. 13).
121
NO |
|
|
|
|
|
|
|
|
|
ÃÖ |
ÔÄÝ |
|
|
||||||
ÃÒÔ |
|
|
|
öÃÌÔ |
|
|
|
5’-ÃÌÔ |
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
||||
Понижение активности |
|
|
G- |
киназа |
|
Повышение активности |
|||
|
|
|
|
|
|
|
|||
|
Дефосфорилирование |
|
|||||||
ФЛС, вн/кл. концентра- |
|
цепей миозина и |
|
Ñà2+ - АТФазы ЭПР и |
|||||
öèè IP è Ñà2+ |
дезагрегация актомиозина |
усиленное поглощение |
|||||||
3 |
|
|
|
|
|
|
|
|
им ионов Са |
|
|
|
|
|
|
|
|
|
|
Ðèñ.13. Схема синтеза и метаболизма циклического гуанозинмонофосфата (цГМФ), поясняющая его роль в механизмах релаксации гладкомышечных клеток (сосудов)
ГТФ - гуанозинтрифосфат, ГЦ - гуанилатциклаза, ФДЭ - фосфодиэстераза, NO - оксид азота, ФЛС - фосфолипаза С, ЭПР - эндоплазмати- ческий ретикулюм. Сплошные стрелки - процесс, пунктирные - влияние.
1.1.МАТОЧНЫЕ СРЕДСТВА
Êматочным относятся средства, непосредственно действующие на миометрий. Они могут увеличивать частоту и амплитуду ритмических сокращений матки (родоускоряющие), вызывать тоническое (спастическое) ее сокращение (кровоостанавливающие) или понижать сократительную активность (токолитики). Ритмические сокращения матки усиливаются прозерином (см.), но его эффект обусловлен влиянием на иннервацию матки. Пря-
мое влияние на ГМК матки оказывают окситоцин, простагландины, алка-
лоиды спорыньи, β2-адреномиметики. В зависимости от характера влияния на миометрий их относят к родоускоряющим, кровоостанавливающим
средствам или токолитикам.
Фармакология родоускоряющих средств
Мощным стимулятором ритмической активности миометрия является гормон окситоцин. Этот октапептид синтезируется в нейронах паравентрикулярного и супраоптического ядер гипоталамуса и накапливается в задней доле гипофиза, откуда поступает в систему кровообращения, регулируя тонус и сократительную активность матки, секрецию молока (посредством высвобождения лактогенного гормона) и его отделение (в связи с возбуждением миоэпителиальных клеток молочной железы).
Содержащие естественный или синтетический окситоцин препараты, а также питуитрин (свободная от примесей вытяжка из задней доли гипофиза убойного скота, содержащая помимо окситоцина также вазопрессин), используются как родоускоряющие средства. Окситоцин активирует специфические мембранные рецепторы в ГМК матки, увеличивая в них внутриклеточную концентрацию Са2+ (см. рис. 12). При этом частота и амплитуда сокращений беременной матки увеличива-
122
ется, вялые схватки становятся более сильными, что обеспечивает продвижение плода по родовым путям. Тонус матки лишь несколько повышается. Окситоцин вводят внутримышечно (0,5-2 ЕД) или капельно внутривенно при слабости родовой деятельности для ее усиления. Он может быть использован также при гипотонических послеродовых маточных кровотечениях, хотя в последнем случае алкалоиды спорыньи более эффективны. Питуитрин применяют по тем же показаниям, но в отличие от окситоцина он повышает САД за счет содержащегося в нем вазопрессина.
В последние годы в качестве средств родоускорения и для искусственного прерывания беременности широкое применение получили простагландины. Они образуются во многих тканях путем циклооксигеназного превращения арахидоновой кислоты (см. рис. 20) и обладают широким спектром биологического действия. Из большого числа этих эндогенных регуляторов только PGE2 è PGF2 стимулируют миометрий. PGF2 (коммерческое название динопрост ,энзапрост F)) усиливает ритми- ческие сокращения как беременной так и небеременной матки, повышает тонус миометрия, но одновременно расслабляет шейку матки. Аналогично действует PGE2 (динопростон, энзапростон Е). Эти свойства позволяют применять динопрост и динопростон для ускорения родов и производства абортов по медицинским показаниям. Различия в действии этих веществ касаются их побочных эффектов: динопрост вызывает спазм бронхов и может повышать ОПС, тогда как PGЕ2 понижает тонус бронхов, ОПС и системное артериальное давление. Это позволяет использовать динопростон у беременных с явлениями нефропатии и повышенным САД.
Как средства родоускорения ПГЕ2 è ÏÃF2 имеют перед окситоцином то преимущество, что вызываемое ими усиление сокращения матки сопровождается расширением шейки матки. При использовании для ускорения родов окситоцина с целью расширения шейки матки часто необходимо применять препараты группы атропина.
Фармакология маточных кровоостанавливающих средств
К этой группе относятся некоторые алкалоиды спорыньи (“маточных рожков”, Secale cornutum), а именно эргометрин и эрготамин. Алкалоиды группы эрготоксина (эргокристин, эргокорнин, эргокриптин) обладают преимущественно α- адреноблокирующим и прямым сосудосуживающим действием, оказывая на матку лишь слабое влияние. В медицинской практике обычно используют эрготал (смесь фосфатов алкалоидов спорыньи) и эргометрина малеат.
Эргометрин хорошо всасывается в ЖКТ, действует быстрее других алкалоидов. При внутреннем и парентеральном введении он вызывает длительное (несколько часов) тоническое сокращение миометрия. При этом сосуды , идущие между мышечных волокон матки, пережимаются, что способствует образованию в них тромбов и ведет к остановке маточного кровотечения. В качестве родоускоряющих средств алкалоиды спорыньи не должны назначаться, поскольку передавливание межмышечных плацентарных сосудов приведет к внутриутробной асфиксии плода. Эргометрина малеат и эрготал используют в акушерской практике при кровотечениях после ручного отделения последа, при ранних послеродовых атони- ческих кровотечениях, кровянистых отделениях после аборта, а также в отдаленном послеродовом периоде для ускорения инволюции (обратного развития) матки.
123
Токолитические средства
Токолитики (от tokos - роды) - ЛВ, уменьшающие сократительную активность миометрия и используемые для профилактики преждевременных родов. Преждевременные роды (до 37 недель) составляют менее 7 % всех родоразрешений, но являются причиной почти 70 % случаев перинатальной смертности. Основным свойством токолитиков является способность угнетать сокращения гладких мышц матки. Таким действием обладают блокаторы “медленных” Са-каналов, например верапамил. Однако их токолитический эффект выражен слабо, поскольку повышение внутриклеточной концентрации Са2+ в ГМК матки достигается не столько путем поступления их извне, сколько посредством высвобождения из внутриклеточ- ных депо (рис. 12). Снижение сократительной активности миометрия вызывает индометацин и другие ингибиторы циклооксигеназы, нарушающие синтез PGE2 è PGF2, которые являются важнейшими эндогенными стимуляторами сокращений матки (рис. 12). Выраженным токолитическим действием обладают β-адреноми- метики. Предпочтение отдается фенотеролу (Partusisten), избирательно активирующему β2-адренорецепторы миометрия и обладающему наиболее продолжительным действием (см. гл. 3, раздел 2.1). Для профилактики преждевременных родов партусистен назначают в таблетках по 5 мг каждые 2-3 часа, но не более 30-40 мг/ сутки. Применение столь высоких доз нередко вызывает тахикардию, мышечную слабость, снижение САД. Тиреотоксикоз, сердечные аритмии и глаукома являются противопоказанием к его назначению.
Применение β2-адреномиметиков не всегда обеспечивает необходимую степень токолитического эффекта. Это обусловлено особенностями нервно-гумораль- ной регуляции сократительной функции миометрия. Девственная матка человека более чувствительна к факторам, сокращающим матку, чем расслабляющим. С 16ой недели беременности в результате усиления под влиянием прогестерона синтеза GS белка (см. рис. 12) чувствительность к расслабляющим матку факторам повышается. Максимальное содержание GS белка достигается к 30-32-ой неделе беременности, а к 40-ой неделе постепенно уменьшается и инозитолтрифосфатный путь сопряжения, зависимый от содержания Gq белка, вновь становится преобладающим. Преждевременные роды возникают, когда соотношение Gq/GS досрочно сдвигается в сторону Gq белка. Однако в таких условиях относительного дефицита GS белка в мышечных клетках миометрия чувствительность последних к β-адре- номиметикам оказывается сниженной.
Средства и препараты.
Oxytocin в амп. по 1 мл, содержащих 5 ЕД.
*Pituitrinum pro injectionibus в амп. по 1 мл, содержащих 5 ЕД. Dinoprostum в амп., содержащих 1 и 5 мг порошка, который растворяется
перед употреблением в 100 или 500 мл изотонического раствора глюкозы и вводится в/в капельно.
*Ergometrini maleas в табл. по 0,0002 (0,2 мг) и в амп по 1 мл 0,02 % раствора (0,2 мг).
Ergotalum в табл. по 0,001 (1 мг) и амп. по 1 мл 0,05 % раствора (0,5 мг). *Fenoterolum (Partusisten) см. гл. 3, разд. 2.1.
124
1.2. МИОТРОПНЫЕ ВАЗОКОНСТРИКТОРЫ (ВАЗОПРЕССОРЫ)
Сосудосуживающим действием обладают аналептики (см.), повышающие САД в результате возбуждающего влияния на сосудодвигательный центр. Общее периферическое сопротивление (ОПС) и САД повышают α-адреномиметики (мезатон, норадреналин), имитирующие влияние симпатических нервов, или эфедрин (см.), усиливающий их сосудосуживающее влияние. Все эти средства - нейротропные вазопрессоры.
Прямым вазоконстрикторным действием обладают вазопрессин и ангиотен- зин-II. Последний образуется из ангиотензиногена (белка плазмы крови) под влиянием ренина, выделяемого юкстагломерулярными клетками почек. Выделение ренина усиливается при повышении функции симпато-адреналовой системы и при гипоксии почек. Ренин осуществляет превращение ангиотензиногена (полипептид) в ангиотензин-I (декапептид), который под влиянием ангиотензин-конвертазы (ди- пептидил-пептидазы плазмы) превращается в ангиотензин-II (октапептид, АТ-II). Активируя ангиотензиновые рецепторы в ГМК артериол и увеличивая в них внутриклеточную концентрацию Са2+ (см. рис. 12), АТ-II вызывает их сокращение, сужение артериол, повышение ОПС и САД. Несколько повышается также тонус вен. В связи с повышением САД возникает рефлекторная брадикардия. Одновременно АТ-II усиливает функцию альдостерон-продуцирующих клеток коры надпочечников. Высвобождаемый в кровоток альдостерон усиливает реабсорбцию ионов Na+ эпителием почечных канальцев, что сопровождается задержкой Na+ в организме, гиперосмией крови и вторичной задержкой воды. Таким образом, гипертензивное действие АТ-II обусловлено не только его вазоконстрикторным влиянием, но и увеличением объема циркулирующей плазмы (ОЦП).
Практическое применение находит не сам АТ-II, а его амид - Angiotensinamidum. Хотя он расщепляется эндопептидазами тканей медленнее, чем АТ-II, его вводят внутривенно капельно, подбирая скорость введения достаточную для поддержания САД на необходимом уровне. Вазопрессин применяют в виде содержащего его препарата Pituitrinum pro injectionibus. В качестве вазопрессора он используется редко. Однако помимо вазоконстрикторной вазопрессин обладает также антидиуретической активностью. Воздействуя на V2 рецепторы (см. рис. 3) и увеличивая проницаемость дистальных канальцев почек и собирательных трубочек, вазопрессин усиливает реабсорбцию воды и уменьшает диурез. Это свойство антидиуретического гормона используется при лечении несахарного мо- чеизнурения.
Основное применение миотропные вазоконстрикторы находят при лечении острой сосудистой недостаточности (коллапса). Коллапс обусловлен расширением артериол и сопровождается внезапным падением ОПС и САД ниже 70 мм. рт. ст.. При этом нарушается кровоснабжение почек, сердца, жизненно важных центров мозга, что непосредственно угрожает жизни. При коллапсе центрального происхождения, напр., обусловленном угнетением сосудодвигательного центра при наркозе фторотаном, эфиром, тиопенталом-натрия или наблюдаемом при некоторых инфекционных заболеваниях (крупозная пневмония), повышение САД и нормализация кровоснабжения жизненно важных центров и органов может достигаться применением аналептиков (см.). Последние, однако, неэффективны при коллапсах
125
периферического происхождения, которые имеют место, напр., при передозировке ганглиоблокаторов, симпатолитиков и веществ с α-адреноблокирующей активностью (празозин, аминазин, дроперидол и др.) или при некоторых инфекциях (брюшной, сыпной тифы и др.). При этой форме коллапса необходимо использовать α-адреномиметики или ангиотензинамид. Последний наиболее активен при коллапсе, обусловленном передозировкой альфа-адреноблокаторов.
Снижение САД при шоке не является показанием для применения вазопрессоров. Напротив, они противопоказаны при геморрагическом, травматическом и ожоговом шоках, поскольку снижение САД при этой патологии не является результатом расширения сосудов и снижения ОПС, а возникает вследствие гиповолемии (уменьшение объема циркулирующей плазмы, ОЦП) и снижения сердечного выброса. При этом компенсаторно развивается спазм артериол (особенно кишечника), ведущий к нарушению микроциркуляции и избыточному высвобождению эндогенных веществ (гистамин, кинины, простагландины E и F и др.), усиливающих проницаемость капиллярной стенки и усугубляющих гиповолемию. Для устранения гиповолемии используются плазмозаменители (см.), а в качестве повышающего САД средства при кардиогенном шоке допустимо применение дофамина (см.), увеличивающего сердечный выброс.
1.3. МИОТРОПНЫЕ СПАЗМОЛИТИКИ
Спазмолитики - это ЛВ, расслабляющие гладкую мускулатуру внутренних органов, устраняющие ее спастическое сокращение. Многие вещества устраняют спазм гладких мышц, препятствуя спазмирующему влиянию на ГМК парасимпатических и симпатических нервов. Так действуют М-холиноблокаторы при кишеч- ной или печеночной колике, ганглиоблокаторы или α-адреноблокаторы при гипертоническом кризе. О таких ЛВ говорят как о нейротропных спазмолитиках.
Миотропными спазмолитиками являются ЛВ, расслабляющие гладкие мышцы в результате прямого влияния на ГМК органов. Миотропный спазмолитический эффект таких веществ является следствием снижения внутриклеточной концентрации Са2+ в ГМК. Это достигается разными путями и поэтому миотропные спазмолитики по механизму действия можно подразделить на несколько групп: антагонисты Са2+, ингибиторы фосфодиэстеразы (ФДЭ), активаторы К+-каналов и ЛВ, действующие подобно эндотелиальному релаксирующему фактору (ERF). К антагонистам кальция относятся магния сульфат, верапамил (изоптин) и нифедипин (коринфар). Два последних выделяют в группу блокаторов Са-каналов, поскольку эти вещества способны блокировать потенциалозависимые Са-каналы и препятствовать вхождению ионов Са внутрь ГМК. Антагонизм ионов магния и кальция, описанный еще Рингером, основан на том, что оба эти иона могут проникать внутрь ГМК через открытые п/з Са-каналы, но скорость продвижения Mg2+ по ним в 10 раз ниже скорости продвижения ионов Са. Активаторы К-каналов, к которым принадлежит Minoxydil, усиливают выход К+ из ГМК вследствие чего развивается гиперполяризация и снижается чувствительность этих клеток к гуморальным и нервным факторам, вызывающим возбуждение и сокращение гладких мышц. К ингибиторам ФДЭ-I относят производные изохинолина (изохинолиновый алкалоид опия папаверин и синтетическое вещество “ношпа”) и производные
126
ксантина (теобромин, теофиллин и водорастворимый препарат последнего эуфиллин). Ингибируя ФДЭ-I, которая метаболизирует цАМФ до 5'-АМФ, эти ЛВ увели- чивают внутриклеточную концентрацию цАМФ, что усиливает поглощение ионов Са из цитозоля элементами ЭПР гладкомышечных клеток, а также уменьшает время открытого состояния п/з Са-каналов.
Ингибиция ФДЭ-I изохинолиновыми и ксантиновыми спазмолитиками сопровождается также повышением внутриклеточной концентрации цГМФ. Этот механизм играет исключительную роль в механизме спазмолитического действия нитритов и нитратов (натрия нитропруссид, нитроглицерин, нитросорбид и др.), действующих подобно ERF. Эндотелиальный релаксирующий фактор идентифицирован в настоящее время с оксидом азота (NO). Эндотелиальные клетки синтезируют NO из аргинина при участии синтетазы оксида азота. Активность этого фермента может возрастать при фосфорилировании его протеинкиназой C и Са/ кальмодулин-зависимой киназой, т.е. теми киназами, активность которых высока при высоком содержании внутриклеточного Са. Таким образом, по мере возрастания внутриклеточной концентрации Са2+ и сокращения ГМК, концентрация NO в клетке тоже возрастает. Вместе с тем NO является мощным активатором гуанилатциклазы, превращающей ГТФ в цГМФ, а последний, активируя G-киназу, запускает все механизмы, ведущие к расслаблению гладкой мышцы (рис. 13). Следовательно, NO является эндогенным ауторегулятором тонуса, по крайней мере, гладких мышц сосудов. В процессе метаболизма нитратов и нитритов в организме образуется оксид азота, который выше описанным способом расслабляет ГМК (сосудов).
Разнообразие механизмов действия спазмолитиков и неодинаковое значение механизмов релаксации в гладких мышцах разных органов лежат в основе того, что определенный спазмолитик эффективнее расслабляет гладкие мышцы одного, чем другого органа. С учетом этого и сопутствующих эффектов, а также опыта клинического применения, осуществляется выбор миотропных спазмолитиков при спазмах гладких мышц разных органов (табл. 15). Выбор спазмолитика во многом определяется также особенностями фармакокинетики. При в/в введении магнезии сульфата или дибазола быстрое выделение ионов Mg почками и высокая скорость элиминации дибазола обусловливают кратковременность (1,5-3 часа) их действия. Поэтому их используют для купирования гипертонических кризов. Действие апрессина (гидролазин), напротив, развивается медленно (через 3-4 часа ввиду адсорбции белками плазмы 80 % вещества). У большинства людей он медленно элиминирует и еще определяется в моче через 24 часа после орального введения. Поэтому апрессин применяется для систематического лечения гипертонической болезни. Кратковременно действует (30-40 мин.) также нитроглицерин. Продолжительность действия большинства других миотропных спазмолитиков - 4-6 часов.
Средства и препараты.
*Magnesii sulfas выпускается в амп. по 5, 10 и 20 мл 20 % и 25 %-го растворов, которые вводятся внутривенно или внутримышечно.
Dibazolum (Bendazolum) в табл. по 0,02 и в амп. по 2 и 5 мл 0,5 % или 1 % раствора. Для купирования гипертонического криза вводят в/в 6-8мл 0,5 % раствора. Вместе с папаверина гидрохлоридом выпускается в табл. “Paрazolum”.
Nospanum (Drotaverinum) â òàáë. ïî 0,04 è â àìï. ïî 2 ìë 2 % ð-ðà.
127
Таблица 15 Миотропные спазмолитики, используемые при спазмах гладких мышц
разной локализации
|
ВАЗОД И Л Я Т А Т О РЫ |
|
|
|
|
||
Артерио- |
Артериове- |
|
|
Бронхо- |
Спазмо- |
|
|
лярные |
нозные |
Веноди- |
Корона- |
дилата- |
литики |
|
|
(снижающие |
(улучш. |
латато- |
родила- |
òîðû |
ÆÊÒ |
|
|
ÎÏÑ) |
микроцир- |
ðû |
таторы |
|
|
|
|
|
куляцию) |
|
|
|
|
|
|
Магния |
Натрия |
Нитро- |
Дипири- |
Теофиллин |
Папаверина |
|
|
сульфат |
нитро- |
глицерин |
дамол |
Эуфиллин |
гидрохлорид |
|
|
Верапамил |
пруссид |
Молси- |
Карбо- |
Верапамил |
Ношпа |
|
|
Нифедипин |
|
домин |
кромен |
|
|
|
|
Миноксидил |
|
|
|
|
|
|
|
Апрессин |
|
|
|
|
|
|
|
Дибазол |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
*Euphyllinum (Aminophyllinum)- смесь теофиллина с 1,2-этилендиамином, придающим растворимость теофиллину. Выпускается в табл. по 0,15 и в амп., содержащих 1 мл 24 % раствора или 10 мл 2,4 % раствора.
2. АНТИАНГИНАЛЬНЫЕ СРЕДСТВА
Средства, применяемые для устранения (купирования) или профилактики гипоксии (ишемии) миокарда и обусловленных ею приступов стенокардии (грудной жабы, Angina pectoris), называются антиангинальными. В основе коронарной недостаточности, признаком которой является стенокардия, лежит несоответствие между потребностью сердца в кислороде и реальной его доставкой к миокарду, т.е. объемной скоростью коронарного кровотока (ОСКК). Причиной такого несоответствия может быть спазм коронарных артерий, либо невозможность компенсаторного усиления ОСКК при усиленной деятельности сердца. В физиологических условиях при усилении физической или психической деятельности человека усиливается также работа сердца (МОК) за счет увеличения силы и (или) частоты сердечных сокращений. Посредством рефлекторных механизмов и гуморальных факторов усиление деятельности сердца сопровождается увеличением ОСКК и доставки кислорода за счет расширения коронарных сосудов. Недостаточность этих рефлекторных и гуморальных механизмов, имеющая место при ишемической болезни сердца (ИБС), приводит к тому, что усиление деятельности сердца и возросшие его потребности в кислороде, не сопровождаются компенсаторным усилением ОСКК. Имея ввиду эти причины возникновения ишемии миокарда и стенокардии, фармакотерапию коронарной недостаточности можно осуществлять либо путем расширения коронарных артерий, либо снижая выполняемую сердцем работу, а следовательно, уменьшая потребность сердца в кислороде.
128
Из числа применяемых в настоящее время антиангинальных средств можно выделить группу веществ, антиангинальный эффект которых обусловлен почти исключительно их коронарорасширяющим действием (валидол, дипиридамол, карбокромен), и β-адреноблокаторы, антиангинальный эффект которых обусловлен уменьшением работы сердца и потребности его в кислороде. Однако большинство антиангинальных средств (нитриты, нитраты, блокаторы Са-каналов) способны как уменьшать потребность сердца в кислороде, так и увеличивать его доставку. Те антиангинальные средства, действие которых развивается быстро, используются при острой коронарной недостаточности (для купирования приступов стенокардии). Те средства, действие которых развивается не обязательно быстро, но продолжается несколько часов, используются для лечения хронической коронарной недостаточности, т. е. для профилактики стенокардии и инфаркта миокарда.
2.1. ФАРМАКОЛОГИЯ КОРОНАРОРАСШИРЯЮЩИХ СРЕДСТВ
Способностью расширять коронарные артерии и устранять коронароспазм обладает валидол (см. гл. 2). Он расширяет спазмированные сосуды сердца рефлекторно, раздражая окончания чувствительных нервов в слизистой оболочке полости рта. Его слабый и кратковременный эффект (15-20 мин.) позволяет использовать этот препарат лишь в начальном периоде ИБС для купирования приступа стенокардии.
Из числа резорбтивно действующих веществ в качестве коронародилататоров изредка используют дипиридамол (курантил), уменьшающий тонус мышц коронарных артерий и артериол, увеличивающий ОСКК. Действие его развивается медленно (2-3 день), но продолжительно. Влияние дипиридамола на ГМК коронарных артерий обусловлено подавлением тканевого захвата аденозина, являющегося эндогенным коронарорасширяющим фактором, интенсивно образующимся при гипоксии миокарда. Применение дипиридамола для профилактики стенокардии или инфаркта миокарда целесообразно и потому, что он тормозит агрегацию тромбоцитов и тромбообразование -процесс усугубляющий течение инфаркта. Применяемый для тех же целей карбокромен (интенкордин) вызывает стойкое расширение коронарных сосудов и, как полагают, способствует развитию и функционированию коллатералей. В связи с относительно низкой эффективностью карбокромен назначают при начальных стадиях ИБС со стенокардией напряжения. Ни дипиридамол, ни карбокромен существенно не влияют на общую гемодинамику, уровень САД и деятельность сердца.
2.2. БЕТА-АДРЕНОБЛОКАТОРЫ КАК АНТИАНГИНАЛЬНЫЕ СРЕДСТВА
Неселективные (анаприлин) и кардиоселективные (небиволол, атенолол, метопролол) бета-адреноблокаторы устраняют адренергические влияния на сердце. В связи с этим уменьшается частота и сила сердечных сокращений и выполняемая сердцем работа (МОК), что сопровождается существенным снижением потребности миокарда в кислороде. Этому способствует снижение САД и уменьшение постнагрузки на сердце, которые имеют место при длительном назначении β-адре- ноблокаторов. Несмотря на то, что блокада β2-адренорецепторов ГМК сопровождается некоторым сужением коронарных сосудов, доставка кислорода к миокарду,
129
