
- •ФГБОУ ВО РостГМУ Минздрава России ВОЕННЫЙ УЧЕБНЫЙ ЦЕНТР
- •УЧЕБНО-ВОСПИТАТЕЛЬНЫЕ ЦЕЛИ.
- •УЧЕБНЫЕ ВОПРОСЫ
- •Введение
- •УЧЕБНЫЙ ВОПРОС №1.
- •КЛАССИФИКАЦИЯ
- •УЧЕБНЫЙ ВОПРОС №2.
- •Историческая справка
- •Историческая справка
- •Историческая справка
- •Для справки:
- •Для справки:
- •МОЛЕКУЛЯРНАЯ МОДЕЛЬ
- •Физико-химические свойства синильной кислоты
- •Токсикологическая характеристика синильной кислоты
- •Механизм токсического действия и патогенез интоксикации.
- •Митохондриальная дыхательная цепь в норме
- •Митохондриальная дыхательная цепь (схема пассажа электронов)
- •Механизм токсического действия и патогенез интоксикации.
- •Механизм токсического действия и патогенез интоксикации.
- •Механизм токсического действия и патогенез интоксикации.
- •Клиника поражения.
- •Клиника поражения.
- •Клиника поражения.
- •Клиника поражения.
- •Клиника поражения.
- •Клиника поражения.
- •Особенности поражения галоидными производными синильной кислоты.
- •Антидотная терапия.
- •Антидотная терапия.
- •Антидотная терапия.
- •АМИЛНИТРИТ
- •Антидотная терапия.
- •Антидотная терапия.
- •Антидотная терапия.
- •Антидотная терапия.
- •Антидотная терапия.
- •Антидотная терапия.
- •Антидотная терапия.
- •Антидотная терапия.
- •Антидотная терапия.
- •УЧЕБНЫЙ ВОПРОС №3.
- •Токсикология оксида углерода.
- •Механизм действия и патогенез
- •Механизм действия и патогенез
- •Механизм действия и патогенез
- •Механизм действия и патогенез
- •Клиника поражения СО
- •Клиника поражения СО
- •Антидотная терапия.
- •Антидотная терапия.
- •Антидотная терапия.
- •Взрывные и пороховые газы.
- •УЧЕБНЫЙ ВОПРОС №4.
- •МОЛЕКУЛЯРНАЯ МОДЕЛЬ
- •Токсикологическая характеристика
- •Токсикологическая характеристика
- •Патогенез интоксикации
- •Клиника поражения
- •Антидотная терапия
- •Антидотная терапия
- •Антидотная терапия
- •ЗАКЛЮЧЕНИЕ
- •Благодарю за внимание!

Для справки:
В мирное время синильная кислота и ее соли (цианиды) находят довольно широкое применение в промышленности (для извлечения из руд серебра и золота, для золочения и серебрения предметов, для крашения и протравливания тканей и т.д.), в сельском хозяйстве (средство в борьбе с вредителями плодовых деревьев), транспорте (для дезинсекции и дератизации) и т.д. Производятся они в большом количестве, что и делает возможными случаи интоксикации при производстве, транспортировке и использовании синильной кислоты и ее солей. Особенно опасны случаи аварий на предприятиях химической промышленности, производящих или использующих синильную кислоту, а также их разрушения в результате применения ядерного оружия или других средств вооруженной борьбы в военное время. С каждым годом растет производство пластических материалов. Сгорание таких материалов сопровождается выделением синильной кислоты и уже известны факты поражения синильной кислотой в очагах пожаров.

Для справки:
Отравления синильной кислотой возможны и в случае употребления растительных продуктов, содержащих гетерогликозиды. Таких растений известной более 2000.
Отдельные случаи отравления цианидами встречаются и в медицинской практике в случае использования для лечения препаратов, содержащих циан-группу (например, нитропруссид натрия).
Таким образом, диагностика и лечение поражений синильной кислотой и цианидами являются актуальными не только в военное, но и в мирное время.
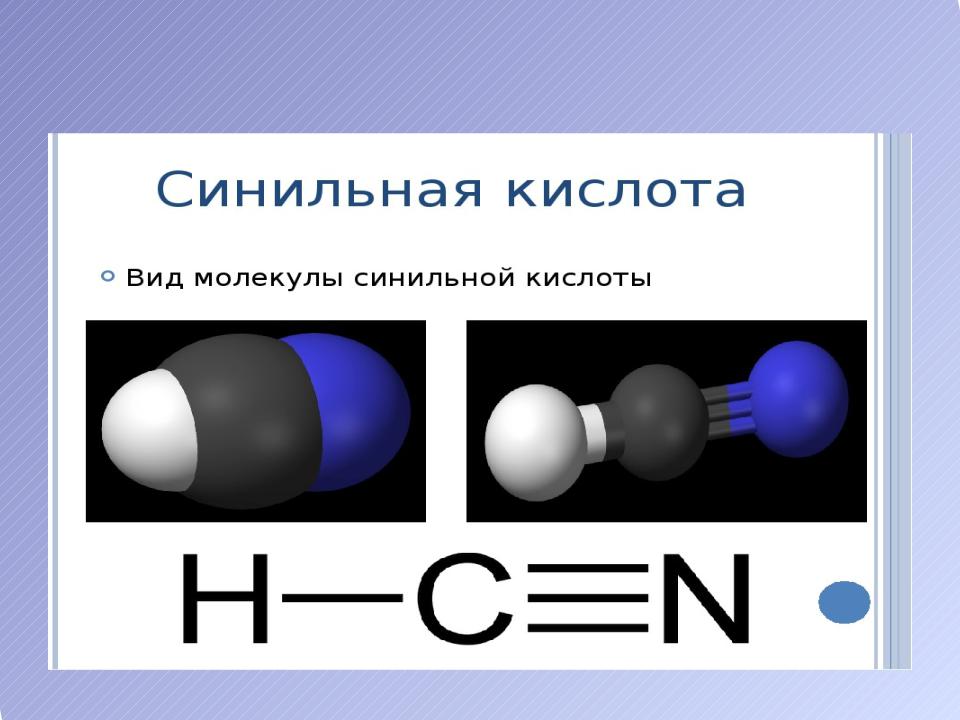
МОЛЕКУЛЯРНАЯ МОДЕЛЬ

Физико-химические свойства синильной кислоты
Синильная кислота - бесцветная жидкость с запахом горького миндаля (при малых концентрациях).
Довольно низкая температура кипения (+26° С), высокая летучесть (900 мг/л при 20° С) и низкая плотность паров (0,93) определяют ее незначительную стойкость на местности: летом на открытой местности - 20-30 мин, зимой - до 60 мин, однако, при отсутствии ветра, особенно ночью, в воронках, лощинах, окопах "места застоя" пары могут задерживаться до 3-4 часов. Температура замерзания - -14° С, очень хорошо растворяется в воде и органических растворителях.

Токсикологическая характеристика синильной кислоты
Очаг - нестойкий, быстродействующий. Зараженное облако быстро поднимается вверх и смещается по ветру.
Токсичность синильной кислоты очень высока (средне- смертельная доза -1,5 мг/л*мин), но все же меньше, чем нервно-паралитических отравляющих веществ. Основным путем проникновения паров синильной кислоты в организм является ингаляционный. Однако, при создании очень высоких концентраций паров в атмосфере не исключено проникновение и через кожные покровы. Возможно пероральное поражение - с зараженной водой или продуктами питания (особенно солями синильной кислоты).

Механизм токсического действия и патогенез интоксикации.
Синильная кислота и цианиды относятся к типичным ферментным ядам с высокоизбирательным механизмом действия.
Точкой приложения их действия являются окисленные формы железа Fе3+ и меди Сu2+ цитохромоксидазы (цитохрома А3) -
конечного фермента цепи тканевого дыхания. Хотя окисленная форма железа в процессе передачи электронов возникает в атомах железа других ферментов цитохромной системы (цитохромы В,
С1 , С, А 1) CN-ион с ними не взаимодействует. Это объясняется тем,
что все координационные связи железа в этих цитохромах заняты R-группами аминокислотных остатков белка, в то время как в молекуле цитохромоксидазы VI координационная связь окисленного железа остается свободной, и именно по этой связи происходит связывание CN-ионов.
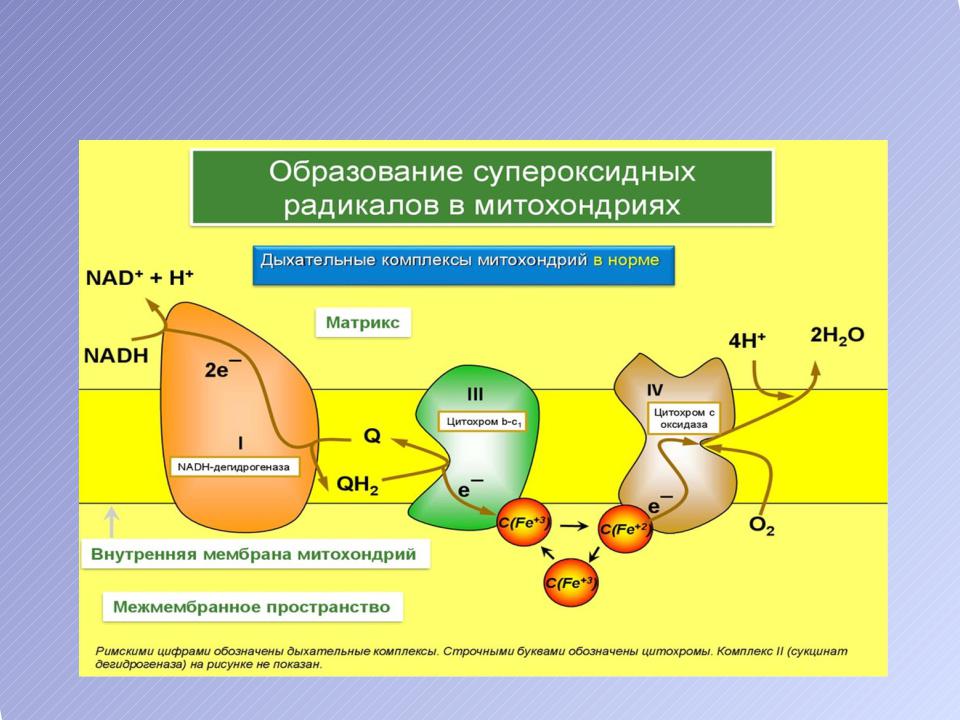
Митохондриальная дыхательная цепь в норме
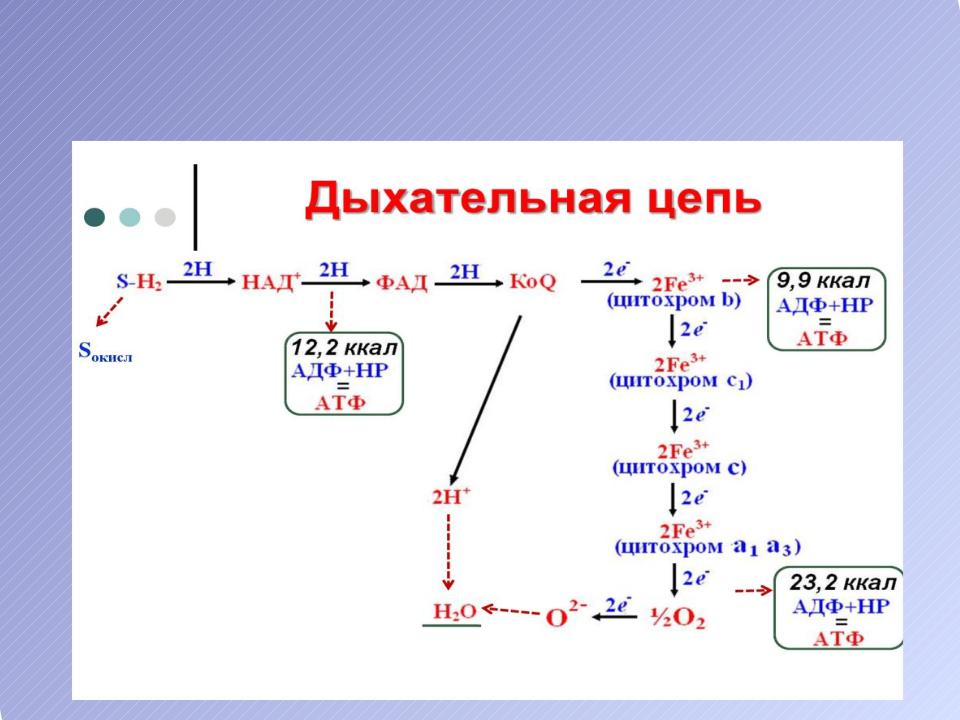
Митохондриальная дыхательная цепь (схема пассажа электронов)

Механизм токсического действия и патогенез интоксикации.
Таким образом, в результате взаимодействия циан-иона с окисленными формами железа и меди цитохромоксидазы, последние теряют способность переходить в восстановленную форму.
В результате блокируется процесс передачи электронов на кислород и соответственно соединение кислорода с ионами водорода (Н+). Это приводит к тому, что все ферменты
дыхательной цепи переходят в окисленное состояние и теряют способность к передаче электронов и, естественно, протонов. В результате тормозится вся система биологического окисления во всех органах и тканях. Следствием этого является прекращение
образования макроэргических фосфорных соединений (АТФ) в
цепи биологического окисления, что сопровождается быстрым
истощением энергетических ресурсов.

Механизм токсического действия и патогенез интоксикации.
NB! Закономерность: если в плазме крови концентрация циан-иона большая, то степень угнетения цитохромоксидазы выражена, но если в плазме крови концентрация синильной кислоты будет снижаться, то и все большее количество яда будет выходить из связанного состояния с цитохромоксидазой и переходить в плазму крови, - взята на вооружение при разработке антидотной
терапии.
