
Organicheskaia_khimiia
.pdfткани (3), в колбу (4) наливают растворитель, предназначенный для проведения экстракции.
Растворитель кипит, его пары по трубке (2) достигают обратного холодильника (1), в котором конденсируются, и жидкость стекает в экстрактор. При этом из вещества извлекается нужный компонент.
Важной деталью экстрактора является изогнутая сифонная трубка (5) небольшого диаметра, один из концов которой сообщается с патроном экстрактора, а второй выходит в кол-
растворителем. буÏолесÃÓКогда уровень раствора вещества в экстракторе достигает уровня изгиба трубки, последняя срабатывает как сифон - и практически весь раствор переливается в нижнюю колбу. Таким образом, из нерастворимой ткани (3) вымывается все растворимое вещество, которое и концентрируется в колбе
(4).
Экстрактор Сокслета ве ьма удобен при работе с объектами природного происхожд ния, и его и пользование часто является первой стади й работы по выделению из них органических соединений.
4. Перегонка
Перегонкой называют процесс, в ходе которого вещество нагревают до температуры кипения, образовавшийся пар отводят и к нденсируют. Перегонка применима, если вещество устойчиво при температуре кипения.
Существует три способа перегонки жидкости: а) при нормальном давлении (простая и фракционная перегонка); б) при пониженном давлении (перегонка в вакууме); в) с водяным паром.
Перегонка при нормальном давлении (простая пере-
гонка). Этот способ применяют, если разница в температурах кипения веществ, входящих в состав разделяемой смеси, не менее 80-100°С или если основное вещество необходимо отделить от нелетучих примесей.
Установка (рис. 8) для перегонки этим способом обязательно должна иметь сообщение с атмосферой. Перегонку
51

нельзя проводить досуха, в колбе всегда должно оставаться немного жидкости. Колбу (1) подберите такого размера, чтобы перегоняемая жидкость заполняла ее не более чем на 2/3 объема. При соединении колбы с холодильником (4) через соединительную трубку (2) необходимо, чтобы ее конец выступал в холодильник не менее чем на 2-3 см. Очищенное вещество через аллонж (5) собирается в колбе-приёмнике (6). Ртутный шарик термометра (3) должен находиться на 0,5 см ниже отверстия отводной трубки.
кипения – непроточную воду (т. е. воду, которая осталась в холодильнике после прекращения ее подачи) или воздушный холодильник.
Если температура кипения перегоняемой жидкости не выше 120ÏолесÃÓ-130°С, то применяют проточное водяное охлаждение. При перегонке жидкости с более высокой температурой
Рисунок 8 – Установка для простой перегонки
Если перегоняемая смесь (7) состоит из компонентов, температуры кипения которых близки, и которые не образуют азеотропных сме ей, применяют дробную или фракционную перегонку (рис. 9).
Для этого обычно используют дефлегматоры (2) и ректификационные колонки с термометром (1). Сущность действия дефлегматора состоит в том, что при прохождении по нему
52

паров происходит их охлаждение и частичная конденсация, в первую очередь, высококипящего компонента. Конденсиру- ю щиеся пары в виде жидкости (флегмы) стекают в перегонную колбу (6). Это обеспечивает высокую эффективность разделения смеси. Если температура кипения перегоняемых жидкостей не выше 80°С (спирт, ацетон, эфир, бензол, и др.), то нагревание следует проводить только на водяной бане (8). Очищенная жидкость, проходя через холодильник (3) конденсируется и направляется аллонжем (4) в стакан-приёмник
( 5).
ÏолесÃÓРисун к 9 – Прибор для фракционной перегонки Перег нка при пониженном давлении (перегонка в
вакууме). Применяют в том случае, если перегоняемые вещества полностью или частично разлагаются при температуре кипения (при атмосферном давлении). Если перегонку проводить при пониженном давлении, то температура кипения веществ понижа тся, а значит, уменьшается возможность их разложения. В связи с изменением температуры кипения всегда нужно фиксировать величину атмосферного давления, при котором производят перегонку. Установка (рис.10) предназначенная для перегонки при пониженном давлении состо-
53
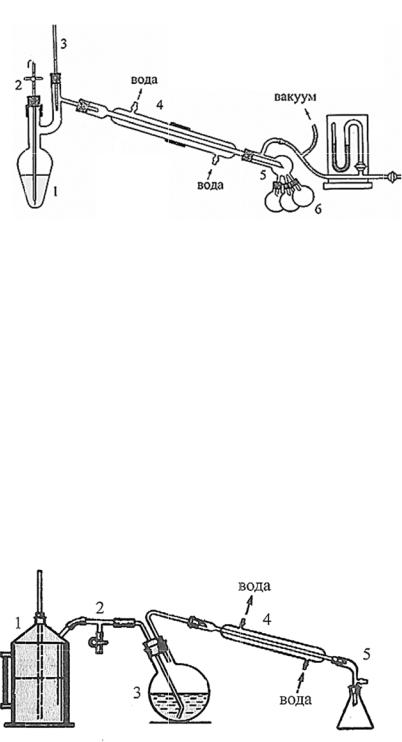
ит из перегонной колбы (1), капилляра (2), термометра (3), прямого холодильника (4), алонжа-паука (5), колбыприе мника (6).
ПерегонкаÏолесÃÓс водяным паром. Этим пособом пользуются для выделения из смес й вещ тв, которые кипят при
Рисунок 10 – Прибор для перегонки под уменьш енным давлением
довольно высокой темп ратуре, а поэтому не исключена возможность их разложения. П р гонять с водяным паром можно только органические в щ ства, которые нерастворимы или труднорастворимы в воде, а также не взаимодейству ю- щие с ней. Кр ме тог , эт т метод применяется для разделения таких смесей веществ, из которых только одно улетучивается паром.
Рисунок 11 – Установка для перегонки с водяным паром
54
Прибор, который применяется при перегонке с водяным паром (рис. 11), включает в себя парообразователь (1), стеклянную трубку (2), круглодонную колбу (3), прямой холодильник (4), алонж (5).
Опыт 4. Проведение перегонки
Небольшое количество спирта (около 30 см3), загрязненного любой растворимой примесью (водой, ацетоном, пиридином и др.), очистите методом простой перегонки (рис.8).
Исходя из количества взятого и очищенного спирта, рас-
ноÏолесÃÓразделить, испо ьзуя п р гонку в вакууме и с водяным паром.
считайте массовую долю спирта в первоначальной смеси.
Следует обратить внимание на показание термометра в процессе перегонки. Сохраняется ли оно все время постоян-
ным?
По итогам работы сделайте вывод о правильности выбо-
ра растворителя, выходе и тепени чи тоты вещества.
Вопросы и задания
1. |
В чём отличия про той перегонки от фракцион- |
ной? |
|
2. |
Приведите прим ры см й веществ которые мож- |
К нтр ьные в просы
1. Какие физические методы идентификации веществ используют в лаб рат рии органической химии?
2. При какой температуре используют водяной обратный холодильник?
3. Какой способ нагревания применяется при кипячении легковоспламеняющихся жидкостей?
4. Приведите порядок проведения перекристаллизации. На чем основан принцип кристаллизации веществ?
5. Как при кристаллизации получить наиболее крупные кристаллы?
6. Расскажите о порядке и мерах безопасности при фильтровании при помощи воронки Бюхнера и колбы Бунзена.
55
7. Перечислите условия подбора растворителя при кристаллизации.
Лабораторная работа № 3
Алканы. Алкены. Алкины
Цель: познакомиться с лабораторными способами получения некоторых представителей гомологических рядов предельныхÏолесÃÓ, этиленовых и ацетиленовых углеводородов и изучить их свойства. Сравнить реакционную способность алканов, алкенов и алкинов.
Реактивы и материалы: обезвоженный ацетат натрия; натронная известь (смесь порошков оксида кальция с гидроксидом натрия, 3:1), насыщенный ра твор бромной воды, 1 % раствор перманганата калия, 5 % ра твор брома в четыреххлористом углероде, конц нтрированные ки лоты: соляная, серная, азотная, конц нтрированный ра твор аммиака, 1 н раствор карбоната натрия, 0,2 н раствор нитрата серебра, аммиачный раствор х орида м ди (I) (1г СuCl2 на 2 мл NН3 и 10 мл воды), 1% спиртовой раствор фенолфталеина, лакмусовая бумага синяя, пентан (гексан, гептан), жидкий непредельный углеводор д, кер син, жидкий ацетиленовый углеводород (фенилацетилен), пес к.
Оборуд вание: ступка, пестик, газоотводная трубка с пробкой, стеклянная лопатка, набор пробирок в штативе, спиртовка.
Опыт 1. Получение и изучение свойств метана
В ступке тщательно растирают обезвоженный ацетат натрия натронной известью (весовое соотношение 1:2). Смесь помещают в пробирку (высота слоя 6-8 мм), закрывают пробкой с газоотводной трубкой и закрепляют в лапке штатива.
56
В одну пробирку наливают 2 мл раствора перманганата калия и подкисляют 1-2 каплями концентрированной серной кислоты, в другую пробирку наливают 2 мл бромной воды.
Подготовленную смесь нагревают в пламени спиртовки и конец газоотводной трубки поочередно вносят в растворы перманганата калия и бромной воды. Пропускание газа проводят в течение 20-30 с. После этого газоотводную трубку переворачивают вверх и поджигают газ у конца газоотводной трубки. Какой цвет пламени?
После охлаждения пробирки к содержимому добавляют несколькоÏолесÃÓкапель концентрированной соляной кислоты.
Вопросы и задания
1. Почему используется безводный ацетат натрия? Зачем необходима натронная известь? Составьте схему реакции получения метана.
2. Как изменяется окра ка ра творами перманганата калия и бромной водой при пропу кании через них метана? К какому гомологическому ряду отно ит я метан?
3. Каков цвет плам ни при горении метана? Почему? Напишите схему р акции гор ния.
4. Для чего прод ывают посл дний опыт с концентрированной со яной кис отой? Опишите наблюдаемые явления и составьте схему реакции.
5. Сделайте выв д по учении метана в лаборатории и о его св йствах.
Опыт 2. Получение и изучение свойств этилена
В сухую пробирку помещают две стеклянные лопатки сухого песка, наливают 1 мл этанола и осторожно 3 мл концентрированной серной кислоты, закрывают пробкой с газоотводной трубкой. Смесь осторожно нагревают, не допуская сильных толчков реакционной смеси.
Так же, как в опыте 1, изучают взаимодействие газа с раствором перманганата калия и бромной водой, горение этилена на воздухе.
Вопросы и задания
57
1. В качестве чего при получении этилена используется песок?
2. Какова роль концентрированной серной кислоты в реакции получения этилена? Ответ подтвердите схемами реакций.
3. Как изменяется окраска растворов перманганата калия и бромной водой при пропускании через них этилена? Почему? К какому гомологическому ряду относится этилен? Напишите схемы проведенных реакций.
5. Сделайте вывод о получении этилена в лаборатории и о его свойствах.
4. Каков цвет пламени при горении этилена? Почему? НапишитеÏолесÃÓсхему реакции горения.
Опыт 3. Получение и изучение свойств ацетилена
В сухую пробирку с газоотводной трубкой помещают кусочек карбида кальция и приливают к нему 3-5 мл воды. Наблюдают выделение газа.
Полученный ацетил н пропу кают через заранее приготовленные растворы: раствор п рманганата калия (2 мл), подкисленного концентрированной с рной кислотой (2-3 капли),2 мл бромной воды,2 мл аммиачного раствора хлорида меди (I) и раств ра гидр ксида диамминсеребра (I) .
Для приг т в ения п еднего в пробирку вносят 2 капли раствора нитрата серебра и несколько капель концентрированного раств ра аммиака (до исчезновения вначале образующегося осадка оксида серебра (I)).
Так же, как и в предыдущих опытах, изучают горение ацетилена на воздухе.
После проведения опыта в пробирку, в которой получали ацетилен, добавляют каплю фенолфталеина. Какой цвет раствора?
Вопросы и задания
1. Составьте схему реакции получения ацетилена с использованием структурных формул.
58
2. Объясните обесцвечивание раствора перманганата калия при пропускании ацетилена. Составьте и уравняйте методом электронного баланса (или методом полуреакций) уравнение окислительно-восстановительной реакции, принимая, что конечными продуктами являются оксид углерода (IV), сульфат марганца (II), сульфат калия и вода.
3. Объясните, почему происходит обесцвечивание бромной воды при пропускании ацетилена. Напишите схему реакции.
4. Отметьте изменения, происходящие при взаимодействииÏолесÃÓацетилена с аммиачными растворами хлорида меди (I) и гидроксидом диамминсеребра (I). Напишите схемы реакций. Какие алкины не могут вступать в реакции с данными реагентами? Как еще называют раствор гидроксида диамминсеребра (I)?
5. Что вы наблюдаете при горении ацетилена? Напишите уравнение реакции горения ацетилена на воздухе.
6. Какие наблюд ния вы отм тили после добавления в пробирку для получ ния ац тил на индикатора? Почему?
7. Сделайте вывод получ нии ацетилена в лаборатории и о его свойствах.
Опыт 4. Изучение действия концентрированных серной и аз тн й кис т на предельные и этиленовые углеводороды
В дну пр бирку наливают 1 мл алкана, в другую 1 мл алкена. Параллельно проводят опыты сравнения: добавляют по 4 капли концентрированной кислоты (серной или азотной) в каждую пробирку. Смеси встряхивают в течение 1-2 мин.
О протекании реакции судят по следующим признакам: разогревание смеси, исчезновение слоя углеводорода, изменение окраски.
Вопросы и задания
1. Напишите схемы реакций. Отметьте скорость протекания реакции алкена с концентрированной серной кислотой.
59
2. Сделайте выводы об отношении углеводородов ( алканов и алкенов) к концентрированным кислотам.
Опыт 5. Изучение действия брома на жидкие алканы
и алкены
В сухую пробирку наливают 1 мл алкана и добавляют 1-2 капли раствора брома в четыреххлористом углероде. Содержимое пробирки встряхивают в течение 1 мин. Если изменений не происходит, осторожно нагревают пробирку до исчезновения окраски (опыт проводят в вытяжном шкафу!). После этого кÏолесÃÓотверстию пробирки подносят стеклянную палочку, смоченную концентрированным раствором аммиака, или влажную синюю лакмусовую бумажку.
Аналогично проводят опыт с жидким алкеном.
Вопросы и задания
1. Отметьте происходящие изменения, напишите схемы реакций.
2. Для чего используют конц нтрированный раствор аммиака (или индикатор)? Напишите х му реакции.
3. Сделайте вывод по данному опыту.
Опыт 6. Отношение жидких алканов и алкенов к перманганату калия
К 1 мл жидк го а кана добавляют 0,5 мл раствора перманганата калия. С держимое пробирки встряхивают в течение минуты. То же пр делывают жидким алкеном.
Вопросы и задания
1. Отметьте наблюдаемые изменения. Напишите схемы реакций.
2. Охарактеризуйте отношение алканов и алкенов к брому и окислителям.
Контрольные вопросы
1.Как изменяется агрегатное состояние алканов, алкенов
иалкинов в гомологических рядах?
60
