
- •2. Базові знання, вміння, навички, необхідні для вивчення теми
- •3. Перелік основних термінів, параметрів, характеристик, які повинен засвоїти
- •4. Теоретичні питання до заняття
- •5. Практичні завдання, які виконуються на занятті.
- •2. Базові знання, вміння, навички, необхідні для вивчення теми
- •3. Організація змісту навчального матеріалу.
- •5.1. Підготовчий етап- 35 хв.
- •5.2. Основний етап -35 хв.
- •5.3.Заключний етап – 15 хв.
Ас. Крикус О.Ю.
МІНІСТЕРСТВО ОХОРОНИ ЗДОРОВ’Я УКРАЇНИ
ВІННИЦЬКИЙ НАЦІОНАЛЬНИЙ МЕДИЧНИЙ УНІВЕРСИТЕТ
ім. М. І. ПИРОГОВА
«Затверджено»
на методичній нараді
кафедри клінічної фармації
і клінічної фармакології
Завідувач кафедри
______ проф. Яковлева О. О.
«_______»________20_____р.
МЕТОДИЧНІ РЕКОМЕНДАЦІЇ
для самостійної роботи студентів при підготовці
до практичного (семінарського) заняття
|
Навчальна дисципліна |
Побічна дія ліків |
|
Змістовний модуль |
Клінічна фармакологія ліків, що впливають на нервову систему |
|
Тема заняття №5 |
Нейротоксичність ліків |
|
Курс |
5 |
|
Факультет |
Медичний |
Вінниця – 2011
1. Актуальність теми:
Нейротоксичність властива більшості відомих речовин. Практично будь-яка гостра інтоксикація в тій чи іншій мірі супроводжується порушеннями функцій нервової системи.
Речовини для яких поріг чутливості нервової системи (окремих її гістологічних і анатомічних утворень) значно нижчий ніж інших органів і систем, і в основі інтоксикації якими лежать порушення моторних, сенсорних функцій нервової системи, пам’яті, мислення, емоцій, поведінки, умовно відносять до нейротоксикантів, навіть якщо не відомі механізми їх токсичного впливу. Вивчення особливостей дії окремих нейротоксикантів дозволяє зрозуміти механізми феномену нейротоксичності в цілому.
Нервова система- це складна система, яка забезпечує міжклітинну взаємодію і контролює більшість функцій організму. Рух, мислення, зір, слух, діяльність серця, дихання та інші фізіологічні процеси контролюються високоорганізованою системою нервових клітин, нервових волокон, рецепторів, синаптичних контактів, нейрогормонів, нейромедіаторів.
Будь-який негативний вплив на одну із ланок цієї високоорганізованої системи може мати негативні наслідки як для нервової системи, так і для організму людини в цілому.
Конкретні цілі:
1. Аналізувати причини виникнення токсичного впливу ліків на нервову систему.
2. Аналізувати роль і функції основних нейромедіаторів.
3. Знати групи найбільш нейротоксичних лікарських засобів.
4. Назвати основні порушення зі сторони нервової системи, що проявляються при
інтоксикаціях ( центральні нейротоксичні ефекти: гострі і хронічні;
периферичні нейротоксичні ефекти: гострі і хронічні).
5. Діагностична стратегія в нейротоксикології.
Теоретичний матеріал
2. Базові знання, вміння, навички, необхідні для вивчення теми
( міждисциплінарна інтеграція).
|
Назва попередніх дисциплін |
Отримані навички |
|
1. Латинська мова |
Розділ «Фармакологічна термінологія та медицина». Володіти вмінням вірного написання назви препаратів латинською мовою, згідно граматики. Володіти знаннями про закінчення в родовому відмінку іменників та прикметників різних відмін при виписуванні препаратів у рецептах. |
|
2. Нормальна фізіологія |
Розділ «Фізіологія нервової системи»- застосувати знання цього розділу. |
|
3. Біологічна хімія |
Визначити роль ацетилхоліну, норадреналіну, дофаміну, гістаміну, серотоніну, ГАМК для організму людини. Застосувати знання цього розділу при розгляді механізмів дії окремих препаратів. |
|
4. Фармакологія |
Пункт « Побічна дія ліків»(зокрема нейротоксичність) |
3. Перелік основних термінів, параметрів, характеристик, які повинен засвоїти
студент при підготовці до заняття
|
Термін |
Визначення |
|
Нейротоксичність |
Властивість хімічних речовин, впливаючи на організм немеханічним шляхом, викликати порушення структури і/чи функцій нервової системи. |
|
Нейротоксиканти |
Речовини, для яких поріг чутливості нервової системи (окремих її гістологічних і анатомічних структур) значно нижчий ніж для інших органів і систем, і в основі інтоксикації якими лежать порушення моторних, сенсорних функцій нервової системи, пам»яті, мислення, емоцій, поведінки. |
4. Теоретичні питання до заняття
1.Визначення нейротоксичності.
2.Поняття нейротоксичних речовин.
3.Структурно-функціональна організація нервової системи (НС).
4.Причини чутливості нервової системи до пошкоджуючої дії нейротоксикантів.
5.Елементи захисту нервової системи від дії нейротоксикантів.
6.Класифікація нейротоксикатів.
7.Вибірковість дії нейротоксикантів на структурні елементи НС.
8.Механіз передачі нервового імпульсу.
9.Основні нейромедіатори НС та їх функції.
10.Ознаки центральних і периферичних (гострих і хронічних) нейротоксичних ефектів.
11.Токсичний вплив етанолу, отрути змій, ботулотоксину та ін..
12.Діагностика нейротоксичного впливу лікарських препаратів.
5. Практичні завдання, які виконуються на занятті.
Цей етап передбачає виконання кожним студентом самостійно практичних робіт.
Виписати рецепти на такі препарати:
Аміназин
Дроперідол
Галоперідол
Буспірон
Діазепам
Гідазепам
Фенобарбітал
Нітразепам
Амітриптилін
Флуоксетин
Тестові завдання:
1 ВАРІАНТ
1. Гематоенцефалічний бар’єр формують:
А) астроцити, олігодендроцити, клітини мікроглії;
Б) нейрони, клітини мікроглії;
В) олігодендроцити, нейрони;
Г) астроцити, олігодендроцити.
2. Нейротоксичні гази:
А) оксид вуглецю;
Б) сірководень;
В) метилхлорид;
Г) кисень.
3. Тормозні нейромедіатори:
А) ацетилхолін;
Б) ГАМК;
В) глютамінова кислота;
Г) норадреналін.
4. Нейротоксичні ефекти можуть бути:
А) гострими, хронічними;
Б) центральними, периферичними;
В) гострими;
Г) центральними.
5. Виберіть речовини, які відносять до ейфоріогенів:
А) тетрагідроканнабінол, морфін, кокаїн, етанол;
Б) іАПФ, бета-адреноблокатори, антагоністи Са;
В) тетрагідроканнабінол, морфін, діуретини;
Г) кокаїн, морфін, статини.
2 ВАРІАНТ
Назвіть центральні нейротоксичні ефекти, які мають хронічний перебіг:
А) зміна настрою, депресія, дратівливість;
Б) порушення уваги, пам’яті, сну;
В) судоми, кома;
Г) галюцинації.
Найбільш вразливі для дії нейротоксикантів структурні елементи нервової системи:
А) нейрони, дендрити, аксони;
Б) синапси, мієлінова оболонка;
В) нейрони, гематоенцефалічний бар’єр;
Г) гематоенцефалічний бар’єр.
Шляхи проникнення нейротоксикантів в організм:
А) інгаляційно;
Б) через рот;
В) через шкіру;
Г) через одяг.
Назвіть порушення когнітивних функцій при нейротоксичній дії ксенобіотиків:
А) порушення сну, депресія, галюцинації;
Б) порушення пам’яті, мови, навчання;
В) порушення зору, слуху;
Г) порушення мови, зору, сну.
5. Найбільш нейротоксичні групи препаратів:
А) нейролептики, антидепресанти, психостимулятори, транквілізатори, ноотропні
препарати;
Б) нейролептики, антидепресанти, бета-адреноблокатори, антагоністи Са;
В) препарати калію, препарати літію, діуретики;
Г) транквілізатори, психостимулятори, антидіарейні.
ВАРІАНТ
Основні клітини нервової системи:
А) нейрони;
Б) дендрити;
В) аксон;
Г) гліальні клітини ( астроцити, олігодендроцити, мікроглія).
2. Збуджуючі нейромедіатори:
А) ацетилхолін;
Б) глутамінова кислота;
В) аспартат;
Г) ГАМК.
3. Причини чутливості нервової системи до токсикантів:
А) проникнення через гематоенцефалічний бар’єр;
Б) вплив на аксони і дендрити;
В) порушення електрохімічного балансу в елементах нервової системи;
Г) все перераховане.
4. Нейротоксичні ефекти можуть бути:
А) гострими, хронічними;
Б) центральними;
В) центральними, периферичними;
Г) гострими.
До ейфоріогенів відносяться:
А) тетрагідроканнабінол, морфін, кокаїн, етанол;
Б) іАПФ, бета-адреноблокатори, антагоністи Са;
В) тетрагідроканнабінол, морфін;
Г) кокаїн, етанол.
ВАРІАНТ
1. Назвіть центральні нейротоксичні ефекти, які перебігають хронічно:
А) порушення настрою, депресія, дратівливість;
Б) порушення уваги, пам»яті, сну;
В) судоми, кома;
Г) галюцинації.
2. Гематоенцефалічний бар’єр формують:
А) астроцити, олігодендоцити, клітини мікроглії;
Б) нейрони, клітини мікроглії;
В) олігодендроцити, нейрони;
Г) клітини мікроглії.
3. Збуджуючі нейромедіатори:
А) ацетилхолін;
Б) глютамінова кислота;
В) ГАМК;
Г) аспартат.
4. Нейротоксичні гази:
А) оксид вуглецю;
Б) сірководень;
В) метилхлорид;
Г) все перераховане.
5. Назвіть порушення когнітивних функцій при нейротоксичному впливі ксенобіотиків
А) порушення пам’яті, мови, навчання;
Б) порушення сну, депресія, галюцинації;
В) порушення зору, слуху, пам’яті;
Г) порушення мови, зору, сну.
Заключний етап
Здійснюється кінцевий тестовий контроль.
Завдання згідно бази Крок-2 (10) центру тестування МОЗ України.
К Р О К
1. Хворий 40 років пред’являє скарги на сильний головний біль.Анамнез: порізав руку при розтині вбитої лисиці. Температура тіла-39,5 С, тремтіння кінцівок. Настрій пригнічений. Просить не вмикати світло, не відчиняти двері. На стук реагує різким руховим збудженням.
Яка тактика лікаря швидкої допомоги?
А. Залишити вдома з подальшою консультацією психіатра.
В. Госпіталізувати в реанімаційне відділення.
С. Госпіталізувати в неврологічне відділення.
Д. Госпіталізувати в психіатричний стаціонар.
Е. Госпіталізувати в інфекційне відділення.
2. Хворий 45 років на фоні високого артеріального тиску після емоційного перенапруження несподівано втратив свідомість, з’явилась блювота. Об’єктивно: хворий в коматозному стані, обличчя червоного кольору, АТ- 200/100 мм.рт.ст., температура тіла-39 С. Лівобічна центральна геміплегія. Про яке захворювання слід думати?
А. Менінгоенцефаліт.
В. Епілептичний напад.
С. Ішемічний інсульт.
Д. Геморагічний інсульт.
Е. Емболія судин мозку.
3. У психічному статусі хворого 32 років стійке патологічне зниження настрою. Контактний, коротко, але по суті відповідає на питання. Мова вкрай лаконічна, в уповільненому темпі. Рухи скуті і загальмовані. Висловлює ідеї самозвинувачення і само приниження. Препарати якої групи в першу чергу показані хворому?
А. Нейролептики.
В. Антидепресанти.
С. Гіпнотики.
Д. Транквілізатори.
Е. Нормотиміки.
4. Жінка 25 років хворіє на параноідальну шизофренію 3 роки. В період загострення захворювання напружена, чує «голоси», які наказують вбити себе. Який препарат доцільно призначити в даному випадку?
А. Галоперідол.
В. Амітриптилін.
С. Аміназин.
Д. Седуксен.
Е. Сонапакс.
5. Хворому з посттравматичним гострим болем після введення морфіну стало значно легше.
Який з перерахованих механізмів дії забезпечує протишоковий ефект морфіну у цього хворого?
А. Підсилення ГАМК-ергічних реакцій.
В. Блокада центральних холінорецепторів.
С. Збудження бензодіазепінових рецепторів.
Д. Пригнічення дофамінової медіації.
Е. Стимуляція оплатних рецепторів.
6. Хворий П., 40 років стоїть на обліку у психіатра 10 років. У клінічній картині поряд з тугою, утрудненням асоціативного процесу, мовно-руховою загальмованістю, ідеями самозвинувачення і самоприниження періодично спостерігається тривожне збудження. Які препарати призначити?
А. Антидепресанти стимулюючої дії.
В. Нейролептики седативної дії.
С. Психостимулятори.
Д. Антидепресанти седативної дії.
Е. Ноотропи.
7. У М., 30 років після важкої автодорожньої черепно-мозкової травми протягом 5 років 1-2 рази в рік виникали генералізовані епілептичні напади. В останній рік напади почастішали до 1-2 разів на місяць. Що необхідно рекомендувати пацієнту для їх профілактики?
А. Ноотропні препарати.
В. Антиагреганти.
С. Антиоксиданти.
Д. Блокатори кальцієвих каналів.
Е. Антиконвульсанти.
8. Службовець багато років зловживає спиртними напоями, переніс важкий алкогольний делірій, після якого з’явились порушення пам’яті. Не запам’ятовує поточних подій. Настрій нестабільний, швидко астенізує під час бесіди. Соматично ослаблений, АТ- 160/95, тони серця ослаблені, печінка дещо збільшена, чутлива при пальпації. Яка група психотропних препаратів найбільш доцільна?
А. Психостимулятори.
В. Ноотропи.
С. Нейролептики.
Д. Транквілізатори.
Е. Препарати літію.
9. Хворий В., 45років. Даний стан розвинувся до вечора дугого дня після запою. Соматично:
Тахікардія, АТ- 160/90 мм.рт.ст.; печінка +2 см нижче краю реберної дуги. Неврологічно- розсіяна неврологічна мікросимптоматика. У психстатусі: алопсихічне дезорієнтування. Відчуває істинні зорові галюцинації. Просить захистити від чортів і павуків, яких «бачить» навколо себе. Відчуває страх. Рухливо збуджений. Критики до свого стану не має. Попередній діагноз?
А. Деліріозний стан.
В. Онейроідний синдром.
С. Аментивний синдром.
Д. Галюциноз.
Е. Параноідальний синдром.
10. Хворий 39 років має стійке зниження настрою. Контактний, але фрази дуже короткі, у сповільненому темпі.Висловлює ідеї самоприниження і самозвинувачення. Рухи скуті,
обмежені, загальмовані.Препарати якої групи Ви порекомендуєте даному пацієнту?
А. Транквілізатори.
В. Гіпнотики.
С. Нейролептики.
Д. Нормотиміки.
Е. Антидепресанти.
В кінці заняття проводиться перевірка та аналіз результатів роботи з виставленням відповідних балів і оцінки.
Алгоритм оцінювання знань студентів
1. Вихідний рівень знань 5 тестів;
2. Кінцевий рівень знань:
- тести до Крок-2 № 10;
- фармакотерапевтичні задачі;
3. Ситуаційна задача;
4. Усна відповідь.
Розподіл балів, присвоюваних студентам при засвоєнні теми «Нейротоксичність ліків»
змістовного модуля № 1 за навчальну діяльність студента виставляються оцінки за 4-ри
бальною шкалою, які потім конвертуються у бали таким чином:
|
Оцінка |
Бали |
|
«5»- відмінно |
13 балів |
|
«4»- добре |
11 балів |
|
«3»- задовільно |
9 балів |
|
«2»- незадовільно |
0 балів |
Рекомендована література:
С.А.Куценко «Основи токсикології» Санкт-Петербург, 2002р.
В.Г.Кукес «Клінічна фармакологія» Москва, 2008р.
С.М.Дроговоз «Побічна дія ліків» Харків, 2010р.
В.М.Кузнєцов, В.М.Чернявський «Психіатрія» Киів, 1993р.
А.П.Ромоданов «Атлас топічної діагностики захворювань нервової системи» Київ 1987р
Д.А.Харкевич «Фармакологія» Москва, 1999р.
А.А.Ярош «Нервові хвороби» Київ, 1985р.
МІНІСТЕРСТВО ОХОРОНИ ЗДОРОВ’Я УКРАЇНИ
ВІННИЦЬКИЙ НАЦІОНАЛЬНИЙ МЕДИЧНИЙ УНІВЕРСИТЕТ
ім. М. І. ПИРОГОВА
«Затверджено»
на методичній нараді
кафедри клінічної фармації
і клінічної фармакології
Завідувач кафедри
______ проф. Яковлева О. О.
«_______»________20_____р.
МЕТОДИЧНІ РЕКОМЕНДАЦІЇ
ДЛЯ ВИКЛАДАЧІВ
|
Навчальна дисципліна |
Побічна дія ліків |
|
Змістовний модуль |
Клінічна фармакологія ліків, що впливають на нервову систему |
|
Тема заняття № 5 |
Нейротоксичність ліків |
|
Курс |
5 |
|
Факультет |
Медичний |
Вінниця – 2011
Актуальність теми:
Нейротоксичність- це властивість хімічних речовин, діючи на організм немеханічним шляхом, викликати порушення структури та / або функцій нервової системи. В основі розвитку токсичного процесу може лежати пошкодження будь-якого структурного елементу нервової системи шляхом модифікації пластичного, енергетичного обмінів, порушення генерації, проведення нервового імпульсу по збудливим мембранам, передачі сигналу в синапсах. Нейротоксичність може бути проявом прямого і опосередкованого пошкодження інших органів і систем, дії токсикантів на нервову систему. Нейротоксичність властива більшості відомих речовин. Тому практично будь-яка гостра інтоксикація в тій чи іншій мірі супроводжується порушеннями функцій нервової системи. Речовини, для яких поріг чутливості власне нервової системи (окремих її гістологічних і анатомічних утворень) істотно нижче, ніж інших органів і систем, і в основі інтоксикації якими лежать порушення моторних, сенсорних функцій нервової системи, пам'яті, мислення, емоцій,поведінки, умовно відносять до нейротоксикантів, навіть якщо не відомі механізми їх токсичної дії.Наприклад, інтоксикація свинцем у дітей призводить до уповільнення розумового розвитку, погіршує здібності до навчання. Механізм цього феноменуневідомий, але прийнято вважати, що нейротоксичність - властивість свинцю. Вивчення особливостей дії окремих нейротоксикантів дозволяє зрозуміти механізми феноменунейротоксичності в цілому.
Структурно-функціональна організація нервової системи
Нервова система - це складна система, що забезпечує міжклітинну взаємодію і контролює більшість функцій організму. Рух, мислення, зір, слух, діяльність серця, дихання та інші фізіологічні процеси контролюються високоорганізованоюсистемою нервових клітин, нервових волокон, синаптичних контактів, нейрогормонів, нейромедіаторів.
Нервова система представлена двома відділами - центральним (центральна нервова система - ЦНС) і периферичним (периферична нервова система - ПНС). Анатомічні структури, що входять в ЦНС, це головний мозок, оптичні нерви, спинний мозок. ПНС представленаструктурами автономної та соматичної нервової системи (таблиця 1). Всіелементи ЦНС і ПНС становлять потенційну мішень для дії токсикантів.
Таблиця 1. Основні утворенняцентрального та периферичного відділів нервової системи.
|
Центральна нервова система:
-Головний мозок
-Спинний мозок
-Оптичні нерви (друга пара черепно-мозкових нервів)
Периферична нервова система:
соматичний відділ:
- Черепно-мозкові нерви
- Спинальні нерви
- Ганглії задніх корінців спинного мозку
- Периферичні нерви:
-Моторні нервово-м'язові синапси
-Спеціалізовані сенсорні рецептори
автономний відділ:
- Парасимпатичні краніальні і крижові нерви і ганглії
- Симпатичні ганглії і нерви
|
Клітинна будова ЦНС, її функції надзвичайно складні і різноманітні. Клітини, що складають нервову систему і визначають її функціональний стан, представлені нервовими клітинами (нейрони), гліальними клітинами, ендотеліальними клітинами судин мозку.
Нормальне функціонування нервової системи можливе тільки в умовах сталості середовища, що оточує нейрони. Основними характеристиками цього середовища є: адекватне постачання киснем, субстратами; сталість кислотно-лужної рівноваги, іонного складу; нормальнийвнутрішньочерепний тиск.
Підтримання сталості внутрішнього середовища мозку забезпечується діяльністю гліальних клітин, за допомогою цереброспінальної рідини, гематоенцефалічного бар'єру, завдяки мозковому кровотоку і зовнішнього дихання.
Нейрони
Основні функціональні елементи нервової системи - нейрони. Вони відрізняються від інших клітин наявністю відростків - дендритів і аксонів. Дендрит- це модифікована частина нейрону, призначена для сприйняття нервового сигналу і його проведення. Він являє собою багаторазово розгалуженийвідросток, який відходить від будь-якої частини нейрону, довжина якого рідко перевищує 1 мм. Нервова клітина може мати один і більше дендритів. Дендрити утворюють складну структурну мережу, що забезпечує комунікацію нервових клітин і інтеграцію нервової системи.
Аксон у нервової клітини тільки один. Це відросток, призначений для проведення нервового імпульсу від тіла нервової клітини до інших клітин. Діаметр аксонупостійний на всій його довжині, а довжина коливається від часток міліметра до метра.
Тіла, дендрити і аксони нервових клітин оточені клітинною мембраною, товщина якої становить близько 70 А. У мембрани нервових клітин вбудовані спеціально організовані білкові комплекси, що формують електро- і хемозбудливіканали,які регулюютьпроникність мембран для іонів Na +, K +, Cl-, Ca2 +.Градієнт концентрації іонів між внутрішнім і зовнішнім середовищем клітини формує потенціал спокою збудливоїмембрани, рівний приблизно 90 мв.
Поширенняпо аксону хвилідеполяризації мембрани з наступною її реполяризацієюлежить в основі проведення нервового імпульсу.
Проведення сигналу не єдина функція аксону. По ходу нервового відростка за допомогою механізмів швидкого аксонального струму (400 мм / день) і повільного струму (3 мм / день) здійснюється також транспорт білків, ензимів, попередників нейромедіаторів. Можливий також ретроградний струм від периферії аксонудо тіла нервової клітини. Швидкість ретроградного струму - близько 200 мм / день. Енергетика та механізми цього явища до кінця не вивчені. Не до кінця охарактеризовані і речовини, що транспортуються по аксону. Мабуть, вони мають трофічні функції.По механізму ретроградного струму, транссинаптичної передачів ЦНС можуть надходити деякі токсиканти (наприад, тетанотоксин).
Наявність відростків і системи внутрішньоклітинного транспорту, призначеної для переміщення поживних, фізіологічно активних і пластичних матеріалів на значні (в масштабах організму) відстані робить нейрони найбільш уразливими елементами нервової системи для дії токсикантів з різними механізмами дії.
Синапси
Міжклітинні взаємодії в нервовій системі здійснюються через синапси - простору між закінченням аксона і збудливою мембраною клітини, що інервується(нейрона, м'язевої, залозистої клітини). Сигнал в синапсі передається за допомогою спеціальної хімічної речовини, що виділяється нервовим закінченням і називаєтьсянейромедіатор (нейротрансміттер). Нейромедіатор який виділився дифундує через синаптичну щілину і зв'язується зі специфічним рецептором на постсинаптичній мембрані, змінюючи його властивості. Зміна властивостей рецептора запускає каскад процесів в клітині яка інервується , що супроводжується модифікацією її функціонального стану (активацією або пригніченням). Наприклад, в нервово-м'язевому синапсі нервове закінчення виділяє ацетилхолін, який, взаємодіючи з холінорецептором, викликає збудження міоциту і його скорочення. Добре доведена нейромедіаторна роль таких речовин, як дофамін, норадреналін, серотонін, ацетилхолін, гамма-аміномасляна кислота (ГАМК), глутамат. Величезна кількість хімічних речовин реалізують свою біологічну дію, втручаючись (активуючи або пригнічуючи) в процес проведення нервового імпульсу в синапсах. Іноді такі речовини називають синаптичними отрутами.
Гліальні клітини
Гліальні клітини представлені астроцитами, олігодендроцити, клітинами мікроглії. Астроглія тісно асоційована з нервовими клітинами і виконує роль стабілізатора середовища, що оточує нейрон. Її значення - формування гематоенцефалічного бар'єру.
Олігодендроцити в ЦНС і шваннівські клітини (леммоцити) ПНС оточують аксони нейронів і утворюють мієлін. Мієлінізуючі клітини, поряд з нейронами, надзвичайно чутливі до дії токсикантів оскільки мають цитоплазматичні відростки, в яких обмінні процеси йдуть менш інтенсивно, ніж в перикаріоні, а площа поверхні, доступна для дії токсикантів, істотно більша, ніж у клітин інших типів. У цьому зв'язку, мієлін дуже часто пошкоджується при інтоксикаціях. Пошкодженя може бути пов'язане з первинним ураженням самого мієліну (гексахлорбензол ), або ензимів, що регулюють його обмін (телур, купрізол). Деякі токсиканти викликають пошкодження мієліну, первинно руйнуючи нейрони (талій), аксони (н-гексан), кровоносні судини (свинець).
Мікроглія це фагоцитарна система ЦНС. Значення цих елементів глії для перебігу токсичного процесу не відомо.
Цереброспінальна рідина
Цереброспінальна рідина секретується хоріоідальнимсплетінням (клітини сплетіння морфологічно нагадують клітини епітелію ниркових канальців), омиває шлуночки мозку і резорбується ворсинками павутинної оболонки мозку. Швидкість секреції - 0,3 - 0,4 мл / хв. Абсорбція рідини починається при тиску рівному 68 мм водяного стовпа. Зі збільшенням тиску зростає швидкість абсорбції. Цереброспінальна рідина вільно проникає через епендиму, вистилає поверхню шлуночків і знаходиться в прямому зв'язку з екстрацелюлярноюрідиною мозку. Вона поширюється між нервовими клітинами, очищаючи міжклітинний простір. Цереброспінальну рідина називають лімфою мозку. Її склад відрізняється від складу плазми крові. У той час як цереброспінальна рідина містить трохи більше хлоридів, натрію, бікарбонату і магнію, чим плазма, в ній міститься трохи менше сечовини, глюкози, калію, кальцію і значно менше білка (15 - 30 мг/100 мл). Об’єм цереброспінальної рідини в дорослої людини становить близько 150 мл. В експерименті, шляхом введення токсикантів безпосередньо в шлуночки мозку лабораторних тварин (в цереброспінальну рідину), можна забезпечити їх дію на нейрони, минаючи гематоенцефалічний бар'єр.
Гематоенцефалічний бар'єр
ЦНС захищена від дії багатьох токсикантів гематоенцефалічним бар'єром. Аналогічний бар'єр оточує периферичний відділ нервової системи (гематоневральний бар'єр). Також як і в ЦНС тут є анатомічні структури з підвищеною проникністю бар'єру для токсикантів. До числа таких структур відносяться корінці дорзальних гангліїв спинного мозку і вегетативні (автономні) ганглії.
Енергетичний обмін
Маса мозку становить 2 - 3% від маси тіла, проте кількість крові, що протікає через мозок,становить у спокої близько 15% від загального обсягу (50 - 60 мл/хв/100 г тканини); мозок споживає близько 25% споживаної організмом глюкози і 20% кисню (3,5 мл/хв/100 г тканини). Такий інтенсивний енергетичний обмін необхідний головним чином для забезпечення іонного транспорту через клітинні мембрани з метою підтримки необхідного електрохімічного градієнту по обидві сторони збудливих мембран, а також для синтезу нейромедіаторів. Лише 10 - 20% виробленої енергії витрачається на підтримку структури мозку. Висока потреба в енергії для реалізації функцій і мінімальне енергоспоживання, необхідне для підтримки структури мозку, пояснюють, чому при тимчасовому порушенні церебрального кровотоку, як правило, розвиваються транзиторні мозкові явища.
Окислення глюкози - єдине джерело енергії в нервовій тканині. Резерви глюкози і кисню в мозку мізерно малі. Тому забезпечення ними повністю залежить від інтенсивності мозкового кровотоку. При повній аноксії "місцеві" запаси кисню становлять лише 7 - 10 мл і достатні для підтримки функцій мозку протягом 10 сек. Потім розвивається втрата свідомості. Необоротне пошкодження клітин мозку розвивається протягом 4 - 5 хв повної аноксії. Проте відновлення функцій можливо і після 8 хвилин аноксії за умови гарної гемоперфузії. Енергозабезпечення мозку страждає при різних типах гострих інтоксикацій, що супроводжуються порушенням зовнішнього дихання, мозкового кровотоку, кисневотранспортних функцій крові, тканинного дихання.
Мозковий кровообіг
Кровотік забезпечує постачання мозку киснем і субстратами, необхідними для підтримки пластичного та енергетичного обміну, а також видалення з тканини мозку діоксиду вуглецю, що утворюється в процесі дихання, та інших метаболітів.
Кровопостачання мозку - саморегулююча система. Це означає, що в інтервалі тиску церебральної гемоперфузії 6,65 - 20,0 кРа (50 - 150 мм Hg), швидкість мозкового кровотоку залишається незмінною. Нижче 50 мм Hg інтенсивність кровотоку зменшується пропорційно зниженню тиску. При цьому погіршується постачання мозку киснем і субстратами. Високий перфузійний тиск крові (більше 150 мм Hg) порушує механізм ауторегуляції, підвищується гідростатичний тиск в капілярах мозку, при цьому порушується функціональна цілісність гематоенцефалічного бар'єру. Мозковий кровотік тісно пов'язаний з інтенсивністю метаболічних процесів у ЦНС, як вважають, за допомогою механізму, регульованого концентрацією СО2 і іонів водню, що продукуються нейронами і клітинами глії. Основним фактором регуляції є іон водню, який безпосередньо впливає на тонус мозкових судин. Ацидоз сприяє розширенню судин і посиленню мозкового кровотоку; алкалоз викликає спазм судин і зменшує інтенсивність мозкового кровотоку. Таким чином, мозковий кровотік - найважливіша похідна кислотно-лужної рівноваги в мозку. Посилення нейрональной активності супроводжується підвищеним утворенням СО2 і ацидозом. Підвищення змісту Н + в міжклітинному просторі мозку викликає розширення судин, посилює мозковий кровотік, вимиваючи вуглекислий газ і відновлюючи нормальну кислотно-лужну рівновагу. Інтоксикації багатьма речовинами супроводжуються глибоким порушенням кислотно-лужної рівноваги (метанол, етиленгліколь, цианіди і т.д.), що згубно позначається на стані ЦНС отруєних. Ряд токсикантів надає нейротоксичний ефект, діючи на судинне русло мозку, порушуючи мозковий кровообіг (свинець, кадмій, вісмут, клофелін).
Внутрішньочерепний тиск
Внутрішньочерепний тиск визначається об’ємом цереброспінальної рідини, що протікає через мозок, крові і об'ємом самого мозку. У нормальних умовах збільшення одного із зазначених об’ємів компенсується зменшенням інших.
Причини уразливості нервової системи для токсикантів
Уразливість нервової системи для пошкоджуючоїдії хімічних речовин обумовленанаступними обставинами:
1. багато хімічних речовин легко проникають через гематоенцефалічний бар'єр, а також діють на нервові утворення, не захищені гематоенцефалічним бар'єром;
2.довгі нервові відростки (аксони і дендрити) значно збільшують площу контакту нейронуз навколишнім його середовищем, збільшуючи вразливість клітин для токсичного пошкодження;
3.для нормального перебігу фізіологічних процесів в ЦНС необхідна підтримка електрохімічного балансу в елементах нервової системи,що забезпечується численними механізмами, на які можуть впливати різні хімічні речовини;
4.нервові клітини, як правило, не в змозі регенерувати і тому їх загибель призводить до відносно стійкихнаслідків;
5.токсичні ушкодження, отримані в ранньому віці, можуть проявлятися і посилюватися по мірі старіння організму, так як втрата нейронів і інші зміни в нервовій системі прогресивно наростають у другій половині життя;
6.навіть незначні порушення структури і функції нервової системи можуть мати згубні наслідки для функціонування організму в цілому, проявлятися неврологічними, поведінковими розладами, зміною функцій інших органів і систем.
Характеристика нейротоксикантів і нейротоксичних процесів.
Нейротоксиканти
Нейротоксиканти, як і інші ксенобіотики,потрапляють в організм інгаляційно, через рот або шкіру, ін’єкційно. Ряд речовин можуть діяти кількома шляхами.
Найважливішою умовою прямої дії нейротоксикантуна ЦНС є його здатність проникати через гематоенцефалічний бар'єр. Речовини, які не проникають через гематоенцефалічний бар'єр, можуть викликати токсичні ефекти на периферії, головним чином в області синаптичних контактів нервових волокон з клітинами органів, які інервують, вегетативних і чутливих гангліїв.
Окремі токсичні сполуки, які не здатні долати гематоенцефалічний бар'єр, знайшли застосування в практиці медико-біологічного експерименту для вивчення властивостей центральної нервової системи. Вони проявляють властивості нейротоксикантів тільки при внутрішньоцеребральному або внутрішньошлуночковому способі введення (6-гідроксидофамін, 5,6-дигідрокситриптамін та ін.)
Таблиця 2. Деякі промислові агенти і екополютанти, що володіють нейротоксичністю
|
1. Органічні розчинники: бензол, ксилол, метанол, н-гексан, сірководень, метилетилкетон, перхлоретилен, стирол, толуол, трихлоретилен, 1,1,1-трихлоретан
|
|
2. Пестициди: фосфорорганічні сполуки, карбамати, метилртуть, метилбромід, хлорорганічні сполуки
|
|
3. Метали та їх сполуки: алюміній, сурма, миш'як, вісмут, золото, свинець, літій, марганець, ртуть, селен, талій, олово, кремній, цинк, тетраетилсвинець
|
|
4. Гази: оксид вуглецю, сірководень, синильна кислота, етиленоксид, метилхлорид
|
|
5. Інші: акриламід, фенол
|
Можлива вибірковадіятоксикантів на окремі елементи нервової системи. Так, деякі речовини пошкоджують нейрони (причому переважно аботіла нервових клітин, або аксони, або синапси), інші - гліальні елементи. Точки прикладання быльшостітоксикантів не визначені. Вибірковість токсичної дії, носить відносний характер. Зі збільшенням дози отрут все менш вибірковим стає пошкодження. Приклади речовин, що специфічно діють на окремі структурні елементи нервової системи, представлені в таблиці 3.
Таблиця 3.Приклади токсикантів, що вибірково діють на окремі структурні елементи нервової системи
|
Тіла нервових клітин і дендрити
|
сполуки ртуті, марганець, алюміній, глутамат, цианіди, талій, МФТГ *
|
|
Аксони
|
тетродотоксин, саксітоксін, вератрін, н-гексан, сірководень, колхіцин, акриламід, перітроіди, триортокрезілфосфат (ТОКФ)
|
|
Синапси
|
нікотин, фосфорорганічні сполуки, карбамати, хінуклединілбензілати, біциклофосфати, пікртоксинін, діетиламід лізергінової кислоти канабінол, фенамін, ботулотоксин, тетанотоксин
|
|
Мієлінова оболонка |
гексахлорфенол, теллур |
* - 1метил-4-феніл-1 ,2,3,6-тетрагідропіридин. Речовина, будучи домішкою "синтетичного героїну", викликає незворотні ураження мозку, які проявляються симптомами паркінсонізму.
Отримана патологія є наслідком впливу токсикантів на збудливі мембрани, механізми передачі нервового імпульсу в синапсах, пластичний і / або енергетичний (гіпоксія, ішемія) обмін в нервовій тканині.
Передача нервового імпульсу здійснюється за допомогою нейропередавачів-моноамінів, які виходять в синаптичну щілину з везикул пресинаптичного нервового закінчення. Одна частина нейротрансмітерів зв'язується з певними рецепторами постсинаптичної мембрани, інша частина руйнується моноаміноксидазою (МАО), а моноаміни, якізалишилися в синаптичнійщілині, піддаються зворотному захопленню через ферментативний насос пресинаптичної мембрани і передача нервового імпульсу припиняється. Потім все повторюється спочатку.
При деяких порушеннях кількість моноамінів у синаптичній щілини є недостатньою для передачі нормального нервового імпульсу. Крім того, кожен з моноамінів відповідає за певні функції і дефіцит нейромедіаторів сприяє розвитку певних клінічних проявів різної патології.
Основні нейромедіатори та їх функції
|
Нейромедіатор |
Роль та функції |
|
Серотонін |
Сон-неспання, мислення, настрій, пам'ять, апетит, регуляція больових імпульсів, центральна терморегуляція, агресивні і мотиваційні реакції, лібідо, сексуальна поведінка, активація скелетної мускулатури, регенерація мозку |
|
Норадреналін
|
Пильнаувага, налаштування на небезпеку, навчання, сон, пам’ять
|
|
Дофамін
|
Регуляція рухової активності, поведінкові реакції, розумові функції, емоційні реакції, регуляція центру блювоти, продукція низки гіпофізарних гормонів (пролактин, гормон росту) |
|
Гістамін
|
Контроль прокидання, пітуітриннагормональна секреція
|
|
Ацетилхолін
|
Збуджуючий медіатор, контроль психічних і моторних функцій, реакція пробудження, навчання
|
|
ГАМК
|
Гальмівний медіатор, регулятор збудження
|
|
Глутамінова кислота
|
Збуджуючий медіатор |
Дефіцит енергозабезпечення може бути наслідком первинного ураження клітин нервової системи (інтоксикація цианідами, похідними фторкарбонових кислот тощо) і дії токсикантів на гемодинаміку, кисневотранспортних функції крові, зовнішнє дихання. Найбільшою мірою порушення енергетичного обміну позначається на стані нейронів в яких високий рівень процесів споживання кисню і синтезу макроергів. В цілому клітини малого розміру з великою кількістю дендритів більш чутливі до гіпоксії (ішемії), ніж великі нейрони з довгими аксонами і малою кількістю дендритів (мотонейрони). Гліальні і ендотеліальні клітини менш чутливі до гіпоксії (ішемії) і за цим показником розподіляються наступним чином: олігодендроглія- астроцити- мікроглія- ендотелій капілярів- біла речовина мозку. Серед структур, утворених сірою речовиною, найбільш чутливими до гіпоксії є: кора головного мозку (малі гранулярні клітини - 4 шар), кора мозочка (клітини Пуркін'є), гіпокамп (клітини полів Н1 і Н2).
Прояви нейротоксичних процесів
Нейротоксичнийпроцес проявляється у формі порушень моторних, сенсорних функцій, емоційного статусу, інтегративних функцій мозку, таких як пам'ять, навчання. Часто порушується зір, слух, тактильна і больова чутливість і т.д. Сенсомоторні порушення призводять до появи м'язевої слабкості, парезів і паралічів. Пошкодження механізмів регуляції функцій життєво важливих органів і систем (дихальної, серцево-судинної) часом закінчується загибеллю отруєних. У ряді випадків основними проявами токсичного процесу можуть стати зміна поведінки потерпілих або експериментальних тварин.
Таблиця 4. Деякі прояви нейротоксичної дії ксенобіотиків
|
Загальні ефекти |
стомлення, втрата апетиту, ступор, наркоз, кома |
|
Рухові порушення
|
слабкість, тремор, посмикування окремих груп м'язів, порушення координації рухів, порушення рефлексів, паралічі, судоми
|
|
Сенсорні порушення
|
відчуття роздратування очей, слизових оболонок, шкіри; парестезії, тактильні порушення, больовий синдром, порушення зору, порушення слуху
|
|
Порушення когнітивних функцій
|
порушення пам'яті, порушення мови, порушення навчання
|
|
Порушення свідомості та емоцій |
порушення сну, дратівливість, неспокій, депресія, сплутаність свідомості, напруженість, ілюзії, галюцинації, марення
|
Залежно від умов дії, будови токсиканту, його нейротоксичногопотенціалу процеси, щорозвиваються перебігають гостро або хронічно.
Гострі нейротоксичні процеси зазвичай обумовлені порушеннями фізіологічних або біохімічних механізмів в нервовій системі і не пов'язані з дегенеративними змінами нейроцелюлярних елементів. Подібні ефекти зазвичай формуються після одноразової дії токсиканту у відносно високих дозах і носять оборотний характер. Як правило, таким чином розвивається інтоксикація речовинами, які порушують передачу нервового імпульсу в синапсах (численні синаптичні отрути), проведення збудження по збудливих мембранах (вератрин, тетродотоксин, саксітоксин, етанол, хлороформ та ін) і деякими речовинами, що порушують енергетичний обмін в мозку (синильна кислота, динітрофенол та ін).
Гострі нейротоксичні процеси в ЦНС виявляються або гіперактивацією нервових структур (збудження, судомний синдром), або їх пригніченням (загальмованість, оглушеність, втрата свідомості), або дезорганізацією вищої нервової діяльності з розвитком транзиторного психодислептичного стану (неадекватні емоції, ілюзії, галюцинації,марення і т.д.). При гострій інтоксикації будь-яким центральним нейротоксикантом, залежно від діючої дози, можна спостерігати окремі ознаки кожного із згаданих ефектів. Однак значне переважання в токсичній дії збудливого, гальмівного або психодислептичного елементів, дозволяє умовно відносити речовини, відповідно, до судомних, седативно-гіпнотичних і психодислептичних агентів.
Прояви гострої нейротоксичної дії на периферії - це, як правило, наслідок порушень проведення нервових імпульсів по рухових, вегетативних волокнах і блокада або перекручення сенсорної інформації, що надходить (оніміння кінцівок, парестезії, біль).
Хронічно перебігають нейротоксичні процеси обумовлені тривалою або, рідше, одноразовою дією токсикантів, і переважно порушують пластичний (свинець, тетраетилсвинець, триметилолово, талій, ртуть, ТОКФ тощо) або енергетичний (оксид вуглецю) обмін. Їх розвиток часто пов'язаний з альтерацією структурних елементів нервової системи: нейронів, їх дендритів і аксонів, мієліну, мієлінутворюючих клітин, ендотеліальних клітин.
Центральні хронічні нейротоксичні процеси, як правило, мало специфічні. Однак при інтоксикаціях деякими речовинами (тетраетилсвинець) періоду розвитку хронічних ефектів передує досить специфічна клініка гострого порушення функцій мозку.
Периферичні нейротоксичні ефекти виявляються стійкими нейропатіями. Внаслідок того, що репаративні можливості нервової системи відносно малі, навіть гострі інтоксикації можуть супроводжуватися розвитком млявих, довгострокових розладів. Так, отруєння деякими ФОС нерідко призводить до формування стійкої поліневропатії.
Один і той же токсикант, діючи в різних дозах, може викликати різні патологічні реакції. Так, гексан при гострій дії у високих дозах викликає стан оглушення, наркоз, кому (тобто формується гострий токсичний процес), а при тривалій експозиції у відносно малих дозах призводить до формування стійкої дистальної аксонопатії(хронічний токсичний процес).
Таблиця 5. Центральні нейротоксичні ефекти
|
Гострі ефекти |
Хронічні ефекти
|
|
- Запаморочення
- Ейфорія
- Збудження
- Галюцинації
- Маячня
- Психомоторне збудження
- Порушення ходи
- Порушення координації рухів
- Судоми
- Сопор
- Кома |
- Порушення настрою
- Депресія
- Дратівливість
- Порушення сну
- Порушення уваги
- Порушення пам'яті
- Зміна особистості
- Паркінсонізм
-Екстрапірамідні і мозжечкові знаки
|
Таблиця 6. Периферичні нейротоксичні ефекти
|
Гострі ефекти |
Хронічні ефекти
|
|
- Подразнення покривних тканин;
- Оніміння кінцівок;
- Парестезії;
- Порушення тонусу м'язів (до повного паралічу);
- Порушення тонусу гладкої мускулатури;
- Порушення функцій екзокринних залоз;
- Порушення серцевої діяльності та дихання
|
- Периферичні нейропатії, розвиваються в проксимальному напрямку;
- Нейропатії, що супроводжуються поведінковими порушеннями;
- Поліневропатія з залученням дистальних відділів нервів;
- Мультифокальні патологічні зміни;
- Периферична денервації
|
Далеко не завжди нейротоксичнудію речовин легко виявити. Судоми, галюцинації, втрата пам'яті діагностуються просто. Однак більшість проявів токсичного процесу можуть бути виявлені тільки фахівцями невропатологами або психіатрами. Такі явища, як сонливість, помірні головні болі, легкебезсоння, можуть тривалий час не пред'являтися отруєним в якості скарг.
Гострі нейротоксичні процеси
Судомний синдром. Конвульсанти
Відома величезна кількість речовин, як синтетичних, так і природного походження, здатних провокувати розвиток судомного синдрому у людини і експериментальних тварин. Багато з цих речовин не відносяться до вибірковихнейротоксикантів і викликають судоми, діючи у відносно високих дозах. Дія інших, навпаки, надзвичайно селективна і проявляється при попаданні в організм в незначних кількостях. Такі речовини називають конвульсантамі або судомними агентами. Їх вивчення представляє особливий інтерес, оскільки дозволяє розкривати механізми, що лежать в основі даної форми нейротоксичного процесу, розробляти ефективні протисудомні препарати.
Механізми, за допомогою яких токсиканти викликають судоми, можуть бути класифіковані на декілька логічних категорій, виходячи з уявлень, згідно з якими нормальний функціональний стан ЦНС є наслідком балансу між процесами збудження і гальмування нейрональних систем. Судоми виникають або в результаті гіперактивації процесів збудження, або пригнічення процесів гальмування (таблиця 7).
Таблиця 7. Можливі загальні механізми генерації судомного синдрому
|
Активація процесів збудження |
Пригнічення процесів гальмування |
|
- Пряма активація збудливих мембран нервових клітин;
- Активація постсинаптичних рецепторів збуджуючих нейромедіаторів;
- Збільшеннякількості збуджуючого нейромедіатора, що вивільняється в синаптичну щілину при проходженні нервового імпульсу;
- Пролонгація дії збуджуючого нейромедіатора внаслідокпригнічення механізмів руйнування або реаптейка;
- Підвищення чутливості постсинаптичних рецепторів до збуджуючих нейромедіаторів;
- Зниження потенціалу спокою постсинаптичних мембран клітин;
|
- Блокада постсинаптичних рецепторів гальмівних нейромедіаторів;
- Зменшення кількості гальмівного нейромедіатора, що вивільняється в синаптичну щілину при проходженні нервового імпульсу;
- Блок вивільнення гальмівного нейромедіатора;
- Зниження чутливості постсинаптичних рецепторів до гальмівного нейромедіатора;
- Скорочення тривалості дії гальмівного нейромедіатора в результаті активації механізмів руйнування і реаптейка |
Гальмівні процеси в ЦНС здійснюються за допомогою пресинаптичних і постсинаптичних механізмів. В обох механізмах беруть участь специфічні нейромедіаторні системи мозку. У спинному і довгастому мозку постсинаптичні гальмування здійснюється за участю гліцину. У вищих відділах ЦНС механізми пре- і постсинаптичного гальмування опосередковані вивільненням в синаптичну щілину гама-аміномасляної кислоти (ГАМК).
Основними збудливими нейромедіаторами мозку є ацетилхолін і збуджуючі амінокислоти (глутамат, аспартат).
Гостре порушення енергообміну в організмі (важке отруєння цианідами, сульфідами, фтороцтовою кислотою і т.д.) може супроводжуватися розвитком судом.
Для усунення судомного синдрому, викликаного токсикантами, крім етіотропних препаратів (там, де вони існують) рекомендують вводити засоби патогенетичної терапії. Серед найбільш вживаних:
1. Діазепам - 0,3 мг / кг, в / м;
2. Гексенал, тіопентал - до 20 мг / кг, в / в;
3.Оксибутират натрію - до 150 мг / кг, в / в, повільно;
4. Дифенін - 15 - 20 мг / кг, в / в;
5. Магнію сульфат - 50 мг / кг, в / в
6. Міорелаксанти, штучна вентиляція легенів.
Седативно-гіпнотичний ефект. Наркотики
Седативно-гіпнотичний ефект розвивається при дії на організм величезної клькостіхімічних речовин з різною будовою і механізмами токсичної дії. Гостре отруєння цими речовинами надзвичайно поширене явище в наш час. Умовно можна виділити дві основні групи:
1. Агоністи гальмівних нейромедіаторних систем мозку (в основному ГАМК-ергічної);
2. Речовини з неспецифічною, так званою "неелектролітною" (за визначенням М. В. Лазарева), дією на ЦНС.
До першої групи належать седативні, снодійні засоби, препарати для внутрішньовенної анестезії, які широко використовуються в клінічній практиці. Основними представниками є похідні барбітурової кислоти (фенобарбітал, пентабарбітал, секобарбітал та ін), бензодіазепіни (діазепам, нітразепам, феназепам та ін), деякі стероїдні препарати (алфаксолон) та ін. За існуючими уявленнями ці речовини вибірково взаємодіють з бензодіазепіновими, барбітуратними і стероїдними сайтами ГАМКА рецепторів ЦНС, підвищуючи їх чутливість до гальмівного нейрмедіатору. При передозуванні речовин (навмисної або випадкової) розвивається інтоксикація, в основі якої лежать добре вивчені ефекти:
- Седативний- пригнічення реакції організму на зовнішні подразники, зниження рівня рухової активності і мислення;
- Снодійний- сон при інтоксикаціях може бути надзвичайно глибоким і переростати в кому;
- Міорелаксуючий- повне розслаблення скелетної мускулатури відзначається лише при важких отруєннях;
- Пригнічення дихання та серцевої діяльності- основна причина смерті при отруєнні речовинами; розвивається в результаті пригнічення дихального та судинного центрів.
Представники другої групи "неелектролітів" - численні сполуки різної хімічної будови, але з близькими фізико-хімічними властивостями. Це неполярні, добре розчинні у ліпідах речовини, інертні в хімічному відношенні, не дисоціюють у воді з утворенням іонів (звідси і їх назва), при нормальних умовах представляють собою леткі рідини або гази. Основна властивість цих речовин -здатність викликати наркоз. Будь-який "неелектроліт" в тій чи іншій мірі володіє наркотичною активністю. Деякі представники групи широко використовуються в клінічній практиці, як загальні інгаляційні анестетики (галотан, енфлуран, метоксифлуран та ін). Переважна ж більшість "неелектролітів" застосовуються в промисловості (численні органічні розчинники і т.д.), сільському господарстві і для них наркотична активність лише один з механізмів токсичної дії при випадкових або навмисних інтоксикаціях. Один з найвідоміших неелектролітів - етиловий спирт, протягом багатьох сторіч використовується людиною з метою викликати транзиторну токсичну реакцію - сп'яніння.
Таблиця 8. Хімічна класифікація речовин, що володіють наркотичною активністю
|
1. Інертні гази:
-Ксенон, азот, криптон, аргон, неон - під підвищеним тиском
2. Неорганічні оксиди:
- Закис азоту
3. Аліфатичні вуглеводні:
- Метан, н-гексан, етилен, амілени, ацетилен, кротонілен
4. Циклічні вуглеводні:
- Циклопропан, циклобутан, бензол, ксилол
5. Ефіри:
- Діетиловий, дівініловий, етилвініловий
6. Спирти:
- Метанол, етанол, пропанол, етиленгліколь
7. Галогеновані вуглеводні:
- Чотирихлористий вуглець, дихлоретан, хлороформ, етилхлорид, галотан (CF3CHBrCl), норфлюран (CF3CH2F)
8. Галогеновані ефіри:
- Метоксіфлюран, енфлюран, флюроксен
9. Інші:
- Сірковуглець
|
Отруєння "неелектролітами" будь-якої будови супроводжується швидким розвитком практично однакових ефектів. Це стан, що нагадує сп'яніння, аналгезія, втрата свідомості, зниження сенсорних і автономних рефлексів, кома, міорелаксація, пригнічення дихання та серцевої діяльності. Якщо інтоксикація не призводить до загибелі потерпілого, практично всі ефекти зникають через нетривалий час (години) після припинення дії токсикантів (особливо це справедливо при інгаляційному впливі високо летючих речовин). Після виходу з важкого стану спостерігається амнезія.
Дуже часто в патологічний процес залучається не тільки ЦНС, але й інші органи і системи і не тільки в результаті порушення механізмів нейрорегуляціі, але і внаслідок "специфічної" дії речовин або їх метаболітів на печінку, нирки, серцевий м'яз, систему крові, легені і т . д. Тому багато "неелектроліти" в керівництві по токсикології фігурують як гепато-, нефро-, пульмонотоксиканти . Нарешті на нервову систему, крім седативно-гіпнотичної, деякі "неелектроліти" надають і іншу дію, пов'язану з порушенням пластичних і біоенергетичних процесів у нервовій тканині, що призводить до розвитку важких енцефало- та нейропатій. Ці ефекти розвиваються слідом за
періодом неелектролітноїдії і складають другу, відстрочену, часом тривалу, фазу інтоксикації.
Етиловий спирт
Етиловий спирт (етанол - СН3СН2ОН) - безбарвна прозора рідина зі специфічним запахом. Добре розчиняється у воді і органічних розчинниках. Температура кипіння +78,40. В основному використовується як сировина для виробництва лікеро-горілчаних виробів і в якості органічного розчинника. Основна причина гострих отруєнь - прийом речовини всередину з метою викликати сп'яніння. Важкість інтоксикації визначається концентрацією етилового спирту в крові отруєного.
Таблиця 9. Концентрація етанолу в крові людини і відповідні прояви інтоксикації
|
Концентрація етанолу в крові (г / л) |
Клінічні прояви
|
|
0,20 - 0,99 |
Легка зміна настрою, ейфорія, прогресуюче порушення координації рухів, розлад сенсорних функцій, порушення поведінки.
|
|
1,00 - 1,99 |
Виразні порушення розумової активності, порушення координації рухів аж до атаксії
|
|
2,00 - 2,99 |
Поглиблення атаксії, нудота, блювання, диплопія
|
|
3,00 - 3,99 |
Гіпотермія, 1 стадія наркозу, після виходу зі стану - амнезія
|
|
4,00 - 7,00 |
Кома, порушення дихання, смерть
|
Етиловий спирт повністю абсорбується з шлунково-кишкового тракту протягом 30 - 120 хвилин після прийому. Абсорбція здійснюється шляхом простої дифузії. Після розподілу речовина накопичується переважно у водній фазі організму. Одноразовий прийом 15 г етилового спирту чоловіком масою 70 кг призводить до появи в його крові етанолу в концентрації 0,3 г / л. Етиловий спирт легко долає гістогематичні бар'єри, у тому числі гематоенцефалічний та плацентарний.
Метаболізм етанолу в основному здійснюється в печінці. Під впливом алкогольдегідрогенази, альдегіддегідрогенази, каталази і цитохром-Р-450-залежних оксидаз. Речовина перетворюється спочатку в оцтовий альдегід, а потім оцтову кислоту, утилізується клітинами організму. Елімінація спирту здійснюється з постійною швидкістю 0,1 - 0,2 г / л крові на годину.
У малих дозах речовина викликає появу транзиторної токсичної реакції, відомої як стан сп'яніння. Навіть найлегші форми сп'яніння супроводжуються зниженням швидкості мислення, порушенням реакції на зовнішні подразники, швидке стомлення.
При вкрай важких формах отруєння може настати смерть від зупинки дихання та серцевої діяльності
Медичні заходи при наданні допомоги спрямовані на припинення всмоктування алкоголю із шлунково-кишкового тракту, прискорення його елімінації, нормалізацію функцій серцево-судинної і дихальної систем, корекцію метаболічних порушень. Антидотів етанолу, як і інших "неелектролітів", не існує.
Психодислептичний синдром. Психодислептики
Наукове вивчення психоактивних речовин почалося лише в другій половині ХХ століття. Проте вже зараз багато сполук широко використовуються в клінічній практиці, а деякі - випробовувалися на предмет можливості їх застосування з військовими цілями, як бойових отруйних речовин або диверсійних агентів.
Психоактивні речовини - будь-яка хімічна речовина (або суміш) природного або штучного походження, яка впливає на функціонування центральної нервової системи, призводячи до зміни психічного стану. Ці зміни можуть носити як позитивний (лікувальний) характер, так і негативний.
Психоактивні речовини, що впливають на вищі психічні функції, і часто використовуються в медицині для лікування психічних захворювань, називаються психотропними. Психоактивні речовини, що викликають звикання і заборонені законодавством, часто називаються наркотиками.
КЛАСИФІКАЦІЯ ПСИХОАКТИВНИХ РЕЧОВИН (ПАР)
За походженням психоактивні речовини та наркотики поділяються на рослинні, напівсинтетичні (синтезовані на основі рослинної сировини) і синтетичні, також ділять за способом дії на організм.Не всі психоактивні речовини є наркотиками, але всі наркотики є психоактивними речовинами. Поділ психоактивних речовин може також проводитися як за їх хімічною будовою, так і за дією, якувони справляють на поведінку людини, і якуможна суб'єктивно відчути.
Деякі ПАР рослинного походження
Дельта-9-тетрагідроканнабінол (з конопель);
ДМТ (діметилтріптамін) (з рослин Mimosa hostilis, Psychotria viridis тощо);
Каваін (з перцю п'янкого);
Кодеїн (з маку);
Кокаїн (з коки);
ЛСД (виробляється на основі грибків ріжки)
ЛСА (з насіння іпомеї, з ололіукві, малої гавайської деревоподібноїтроянди);
Мескалин (з кактусів Lophophora williamsii, Echinopsis pachanoi);
Морфін (з маку);
Псилоцибін (з грибів виду Psilocybe cubensis, Psilocybe semilanceata тощо);
Сальвінорін-А (з шавлії провісників);
Ефедрин (з хвойники); Атропін (з дурману, беладони);
Кофеїн [4] (з листя чаю, листя мате, гуарани, зерен кави, горіхів коли);
Мірістіцін (з мускатного горіха);
Муксімол і іботеновая кислота (з мухоморів);
Нікотин (в махорки, тютюн);
Теофілін (у чаї, мате, какао);
Туйон (в абсенті)
Етанол (в алкогольних напоях)
Евгенол (еугенол) - з мускатного горіха, кориці);
Летючі розчинники (Алкани та ефіри) - Бутан, Бензин), Толуол), Ефір);
За фармакологічними властивостями
Комбінована класифікація з урахуваням клінічних ефектів та хімічної будови.
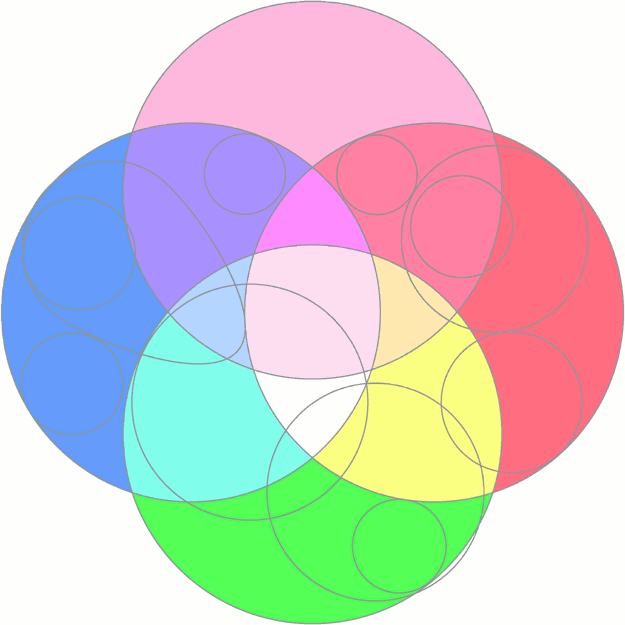
Круги ЕЙЛЕРА
НЕЙРОЛЕПТИКИ
Атипові Типові
Клозапін Галоперідол
Сульпірид Фторфеназин
Рисперідон Хлорпромазин
СТИМУЛЮЮЧІ Кветіапин Перфеназин ДЕПРЕСАНТИ
СІОЗ
Флуоксетин Седативні Снотворні
Адреноміметики Пароксетин
Сертрамін Бензодіазепіни Алкоголь
Психомоторні Холінергічні Барбітурати
ІМАО Нікотин Діазепам Хлороформ
Амфетаміни Мускарин Лоразепам Хлоралгідрат
Метилфенідат Буспірон Флунітразепам Метаквалон
Кокаін Діетилпропіон
Ефедрин Психоделіки ТЦА
Псевдоефедрин МДМА
МДЕА Маріхуана Опіати
Пурини МДА
Опіум
Кофеін Морфін
Теофілін Дисоціативи Героін
Теобромін Мескалін Метадон
LSD Закис азоту Фентаніл
Псилоцибін Кетамін
Холінолітики
Шавлія Дифенілгідрамін
Алкалоіди Атропін
мухомору Скополамін
ГАЛЮЦИНОГЕНИ
Базові групи
Синій: Стимулюючі центральну нервову систему речовини,.
Червоний: Депресанти (заспокійливі засоби).
Зелений: Галюциногени.
Рожевий: Нейролептики.
Вторинні групи
Блакитний: Перетин стимулюючих (Синій) і психоделічних галюциногенів (Зелений) - психоделіки із стимулюючим ефектом
Жовтий: Перетин депресантів (Червоний) і діссоціатівних галюциногенів (Зелений) - Діссоціотіви із заспокійливим ефектом
Світло-фіолетовий: Перетин стимулюючих (Синій) і нейролептиків (Рожевий) - Антидепресанти без седативного ефекту
Кремово-червоний: Перетин депресантів (Червоний) і нейролептиків (Рожевий) - Антидепресанти і антипсихотики з седативним ефектом.
Третинні групи
Пурпуровий: Перетин стимулюючих (Синій) і депресантів (Червоний) - Приклад: нікотин.
Білий: Перетин стимулюючих, депресантів і галюциногенів - Приклад: ТГК.
Димно-блакитний: Перетин стимулюючих, психоделічних галюциногенів і нейролептиків - Приклад: емпатогени-ентактогени.
Персиковий: Перетин депресантів,діссоціатівних галюциногенів і нейролептиків
Четвертинні групи
Світло-рожевий: Центр укладає в себе перетин всіх чотирьох секцій (стимулюючі, нейролептики, депресанти, галюциногени) - Приклад - Марихуана,містить і ТГК і каннабідіол.
Класифікація за силою впливу на психіку
Чим меншукількість речовини необхідно прийняти для того, щоб повністю відчутиїїдію, тим сильнішою, більш психоактивноювонає. Для ЛСД, наприклад, канонічна доза дорівнює 100 мікрограмів, у той час як для етанолу доза вимірюється десятками грамів. Залежно від особливостей метаболізму індивіда речовина може на нього майже не діяти або діяти набагато сильніше (гіперчутливість).Також прийнято вимірювати дозу в грамах речовини на кілограм ваги.
Розподіл по силі залежності неоднозначний. Лідерами за цим показником серед речовин вважаються героїн, кокаїн і іноді нікотин, а також алкоголь.З класів речовин виділяють опіати і стимулятори, які викликають сильну залежність, також сильну залежність можуть викликати барбітурати, хоча реакції конкретних людей на різні препарати можуть бути дуже індивідуальні.
Кава і чай, що містять пурини, надають легкий стимулюючий ефект . Під «легкими наркотиками» зазвичай мають на увазі марихуану і іноді деякі психоделіки.
Механізм дії
На ЦНС психоактивні речовини мають різноманітний вплив на різних рівняхфункціонування ЦНС: молекулярному, клітинному, системному, синаптичному.В цілому, будь-який вплив супроводжується зміною обміну речовин на тому рівні, на якому відбувається цей вплив.
Толерантність
Чим вищатолерантність до вживаної речовини, тим більші дози необхідні для отримання очікуваного ефекту.Зазвичай толерантність виробляється при прийомі речовини і з часом йде на спад. Швидко толерантність формуєтьсядокофеїну і опіатів. Чим частіше і більше речовини вживається - тим швидше зростає толерантність.
Своєрідну толерантність мають класичні психоделіки (ЛСД, псилоцибін, мескалін) - при прийомі однієї з цих речовин толерантність зростає дуже швидко, буквально через кілька годин після початку дії, але повністю спадає приблизно за тиждень.Більше того, для психоделіків характерна кростолерантність; наприклад, прийом псилоцибінуна наступний день після прийому ЛСД, залежно від індивідуальної сприйнятливості і кількості речовини, або взагалі не дасть ніякого ефекту, або ефект буде значно знижений і нетривалий.Кростолерантність психоделіків також повністю зникає приблизно за один тиждень.
Відзначають, що деякіречовини, наприклад, сальвінорин, що міститься в мексиканськійшавлії Salvia divinorum, мають зворотню толерантність; феномен того, що при тривалому вживанні для досягнення одного і того ж ефекту потрібна менша кількість речовини.
Формування залежності і синдрому відміни
Зазвичай формування залежності пов'язують із зловживанням ПАР, їхсистематичним застосуванням.Хоча дія речовин на людину дуже індивідуальна, можна сказати, що найбільш швидко з поширених речовин залежність формується при прийомі героїну і «гвинта» (кустарно виготовленого стимулятора первітину і його похідних), також можна виділити психостимулятори кокаїн та амфетамін.
Існує думка, що психологічну залежність викликають речовини, що впливаютьна обмін в організмі ендогенних нейромедіаторів (кількість яких обмежено, баланс відновлюється поступово),а фізичну - безпосередньо впливають на нервову систему (для вживання таких речовин заради задоволення характерно постійне підвищення дози).Характер впливу в обох випадках має під собою нейрохімічну основу, що задіює психіку людини.
Фізіологічна залежність формується, коли організм звикає до регулярного екзогенногопоступлення речовин, щоберуть участь у метаболізмі в результаті зменшується їх ендогенне вироблення, таким чином при припиненні надходження речовини в організм в ньому виникає обумовленафізіологічними процесами потреба в цій речовині.Це може бути пов'язано як з самою речовиною, так і з її метаболітами, наприклад героїн шляхом видалення ацетил груп метаболізується в морфін, що впливає на опіоідні рецептори. Алкоголь впливає на нервову систему, безпосередньо з'єднуючись з рецепторами ГАМК .Нікотин впливає на нікотинові холінорецептори, стимулюючи викид адреналіну.
Психологічна залежність пов'язується в основному з приємними відчуттями від речовин, що стимулюють людину до повторення досвіду їх застосування.Під дією опіатів людина може не відчувати болю і тривог, одним з варіантів дії стимуляторів є підвищення самооцінки і енергійності. Однак залежність може формуватися і при вживанні інших речовин, наприклад дісоціативів, які викликають розпад свідомості (в тріп-репорт повідомляється навіть про переживання смерті під їх дією);переживання і візуальні ефекти від психоделіків часто взагалі не можуть бути описані як приємні, проте при частому вживанні ці речовини можуть викликати розрив з реальністю. Інтоксикація каннабісом допомагає від депресії, при постійному вживанні марихуани вдходять «на задній план» ряд психосоціальних проблем.
Використовувані в якості медикаментів засобизазвичай поділяють на такі групи:
|
- Нейролептики;
- Антидепресанти;
- Психостимулятори;
- Транквілізатори;
- Ноотропні препарати.
|
У рекомендованих дозах лікарем, ці речовини пригнічують або активують, залежно від властивостей, сприйняття, емоції, пам'ять, навчання, мислення (асоціативні процеси), зберігаючи в цілому адекватне ставлення особистості до навколишньої дійсності. У великих дозах в тій чи іншій мірі ці речовини можуть провокувати порушення процесів сприйняття, емоцій, пам'яті і т.д., тобто викликати психодислептичний ефект, який характеризується неадекватною реакцією особистості на зовнішні подразники. Такою ж здатністю володіють наркотичні аналгетики, деякі засоби для наркозу, алкоголь, а серед промислових токсикантів, речовини, що мають властивості неелектролітів. Здатність викликати психодислептичний ефект у різних речовин виражена неоднаково. У деяких випадках при інтоксикаціях формуються лише мінімальні прояви, що розвиваються при дії речовин у дозах близьких до тих, що викликають пригнічення свідомості або важкі соматичні порушення. Відомі й сполуки, для яких психодислептичний ефект є основним у профілі їх токсичної активності, і розвивається при дії в дозах, які практично не викликають інших токсичних реакцій. Вивчення таких речовин має особливе значення для розуміння механізмів формування порушення психіки при гострих інтоксикаціях. Умовно їх іноді називають психодислептиками, психотоміметиками, психогеніками, психоделіками, підкреслюючи особливу здатність перекручувати функції вищої нервової діяльності.
Отже, психодислептики - це речовини, здатні в мінімальних дозах, в сотні - тисячі разів менше тих, в яких вони викликають пригнічення свідомості або соматичні розлади, перекручувати психічні процеси сприйняття, емоцій, пам'яті, навчання, мислення, робити поведінку неадекватною реальній ситуації.
Психотоксичний профіль психодислептиків неоднаковий. При отруєнні деякими з них домінує зміна емоційного статусу та деяких тонких характеристик психічної активності, інші - викликають порушення процесів сприйняття з помірним збоченням асоціативних процесів; треті - формують глибоке перекручення психічної активності, яка охоплює усі її сторони.
Це дає підставу виділити групи речовин відповідно до особливостей формованих ними токсичних процесів:
|
1. Ейфоріогени:
-Тетрагідроканнабінол, морфін, кокаїн, етанол
2.Галюциногени (ілюзіогени):
-ДЛК, псилоцин, псилоцибін, буфотенін, мескалін
3. Деліріогени:
-Атропін, скополамін, дітран, BZ, фенциклидин, фторацізин та ін
|
Ейфоріогени
Певний токсикологічний інтерес серед речовин цієї групи представляє тетрагідроканнабінол. Цю речовину виділяють з масла індійської коноплі (Cannabis indica). Висушений сік з листя рослини отримав назву гашиш. Наркомани застосовують гашиш (каннабинол) або шляхом куріння, або - через рот. Інгаляційно речовина всмоктується швидше. Через ЖКТ 95% токсиканту проникає в кров протягом 2 - 3 годин. Виведення з організму - двофазний процес: період напівелімінації в першій фазі становить 30 хвилин, у другій - 36 - 48 годин. Ефективна доза каннабінолудля людини дорівнює 0,001 - 0,01 мг / кг.
У процесі розвитку транзиторної токсичної реакції виділяють два періоди дії. У першому, короткому, спостерігається ейфорія, збудження, посилення сприйняття. У другому періоді (тривалому) розвивається сонливість, розслаблення мускулатури, сноподібнийстан, порушення відчуття часу, парестезії, порушення концентрації уваги, порушення мови, ілюзії.
Амфетаміни. Опіоіди. Вплив амфетамінів і опіоідів на нервову систему
1. Способи вживання амфетамінів. Прийом всередину і внутрішньовенне введення
2.Клінічна картина вживання амфетамінів. З боку нервової системи відзначаються порушення, що нагадують симптоми отруєння кокаїном: безсоння, тривога, генералізоване тремтіння, епілептичні напади, церебральні судинні порушення, в тому числі васкуліт, психоз (зазвичай параноідного типу).
3.Діагностика вживання амфетамінів заснована на даних анамнезу та клінічної картини, наявності супутніх системних порушень: артеріальної гіпертензії, тахікардії та інших видів аритмій. Лабораторні методи діагностики включають скринінгове дослідження на амфетаміни або їх похідні.
4.Лікування. При підозрі на передозування амфетамінів хворого необхідно терміново доставити у відділення інтенсивної терапії та призначити консультації відповідних спеціалістів.
Лікування порушень серцевого ритму, дихальної недостатності, вираженої гіпертермії і гіпертензії.
Невролог призначає корекцію нападів та інших порушень з боку нервової системи.
При вираженому психомоторному збудженні і психозі показано введення галоперидолу і бензодіазепінів.
Необхідно викликати блювоту, провести промивання шлункута призначити проносні засоби.
Для лікування наркотичної залежності необхідна консультація нарколога.
Опіоіди (наприклад, морфін, героїн)
1. Способи вживання опіоідів. Прийом всередину, вдихання при палінні або безпосередньому вдиханні порошку, внутрішньошкірні, внутрішньом'язеві або внутрішньовенні ін'єкції, через надрізи шкіри.
2.Клінічна картина при передозуванні опіоідів. З боку нервової системи відзначаються психічні порушення, гіпоксична енцефалопатія, кома, набряк головного мозку, епілептичні напади, екстрапірамідні симптоми, полінейропатія, рабдоміоліз, симптоми ураження судин головного мозку, абсцес мозку,менінгіт.
3. Діагностика заснована на даних анамнезу та клінічної картини, наявності супутніх симптомів системних порушень: пригнічення дихання, звуження зіниць (при гіпоксії зіниці можуть бути розширені), ураження серця (ендокардит).При огляді вен видно множинні сліди ін'єкцій або виявляються характерні шрами на шкірі від надрізів (округлої форми, неглибокі). Клінічними ознаками синдрому відміни є ринорея, профузне потовиділення, тремтіння, тривога, біль у животі, нудота, блювота і діарея.
4.Лікування передозування опіоідів
При підозрі на передозування опіатів хворого необхідно терміново доставити у відділення інтенсивної терапії і проконсультуватися з відповідними фахівцями.
Лікування дихальної недостатності, серцево-судинних порушень і синдрому відміни.
Необхідно почати терапію інфекційних ускладнень (ендокардиту,абсцесу) і епілептичних нападів під наглядом відповідних фахівців.
Для лікування наркотичної залежності необхідна консультація нарколога і спостереження в спеціалізованому лікувально-реабілітаційному закладі.
Повторний прийом призводить до розвитку толерантності (у тому числі до етанолу) і залежності від наркотику. Синдром відміни характеризується дратівливістю, занепокоєнням, порушенням сну, тремором, саливацією, блювотою. Хворі втрачають у вазі.
Галюциногени
Галюциногенами називають речовини, в клініці отруєння якими переважають порушення сприйняття у формі ілюзій і галюцинацій, при цьому потерпілі, як правило, не втрачають контакт з оточуючими. До числа галюциногенів відносяться деякі похідні триптаміну і фенілетиламіну, що порушують проведення нервового імпульсу в центральних серотонінергічних і катехоламінергічних синапсах. Характерною особливістю інтоксикації галлюциногенами є відсутність амнезії на пережиті події.
Більшість галюциногенів - речовини тваринного і рослинного походження, які використовувалисьлюдиною з давніх часів для самоотруєння з ритуальними цілями. Деякі токсиканти і сьогодні використовуються наркоманами. 3- 4 щоденних прийомиречовин призводить до розвитку толерантності, яка проте швидко проходить. Перехресна толерантність відзначається між мескаліном, псилоцибіном, ДЛК, деякими іншими психодислептиками. Найбільш небезпечним з галюциногенів вважається синтетична речовина - метилен диоксиамфетамін (МДА). Гострі отруєння МДА іноді закінчуються смертю.
Класичним представником групи є діетиламід лізергінової кислоти.
Діетиламід лізергінової кислоти (ДЛК)
Психодислептичні властивості ДЛК стали відомі людству 16 квітня 1943. Саме в цей день Гофман, який працював у лабораторії штолень в Базелі, випадково взяв мізерну кількість речовини всередину. В результаті розвинулася інтоксикація, що супроводжувалася порушенням психіки. З цього почалося експериментальне вивчення галюциногенів. Довгий час ДЛК розглядали, як потенційну ОР, диверсійний агент, і тому властивості його зазнали глибокого дослідження.
ДЛК - білий порошок без запаху, його сіль (тартарат) добре розчиняється у воді. При прийомі речовини всередину в дозі 0,5 мкг / кг розвиваються важкі психози. Виводить з ладу організмтоксодоза, якапри інгаляційному впливі становить 0,01 - 0,1 г хв/м3. Летальна доза для мишей - 50 мг / кг, для щурів - 15 мг / кг.
Речовина швидко всмоктується в кров. Максимальна концентрація в тканинах відзначається через 10 - 20 хвилин після прийому. У тканині мозку в цей момент міститься менше 1% від введеної кількості. Через 3 години 80% речовини визначається в стінках і вмісті кишечника, 3% - у печінці, 8% - в кістках.
У експериментальних тварин речовина порушує спонтанну поведінку і умовно-рефлекторну діяльність. Аміназин послаблює дію ДЛК, резерпін - підсилює.
Клініка отруєння ДЛК в людини складається з порушення психіки, соматичних і вегетативних порушень (таблиця 10).
Таблиця 10.Основні прояви інтоксикації ДЛК у людини (Rothlin, 1957)
|
Психічні порушення |
Порушення рухових функцій |
Вегетативні порушення
|
|
-Занепокоєння
-Емоційна нестійкість:
-Ейфорія, що змінюється депресією
-Сплутаність свідомості
-Галюцинації -Деперсоналізація
-Порушення відчуття часу |
пірамідні і екстрапірамідні знаки:
-Атаксія
-Спастичні стани
|
а) мезодіенцефальние ефекти:
-Мідріаз
-Тахікардія
-Гіперглікемія
-Пиломоторні реакції
б) бульбарні ефекти:
-Гіпотонія
-Брадикардія
-Пригнічення дихання
|
Перші ознаки отруєння з'являються через 15 - 60 хв після прийому токсиканту. Симптоми досягають максимуму через 2 - 5 годин. Загальна тривалість інтоксикації становить 12 - 24 години. Можливі спонтанні рецидиви, а також затяжні психози в результаті впливу галлюциногенуу звичайній дозі.
В основі токсичних ефектів, що розвиваються при інтоксикації ДЛК, лежить здатність блокувати центральні серотонінергічні рецептори. Однак далеко не всі серотонінолітикимають властивості психодислептиків, тому цей механізм, ймовірно не є єдиним. Особливостями дії ДЛК є:
- Здатність пригнічувати спонтанну активність серотонінергичних нейронів мозку і підвищувати рівень серотоніну в ЦНС. 10 - 20 тисяч клітин (менше 0,1% нейронів), компактно залягають в ядрах шва головного мозку, іннервують всі структури ЦНС, особливо щільно - утворення зорового аналізатора, лімбічної системи, гіпоталамуса. ДЛК не тільки блокує проведення нервових імпульсів в синапсах, утворених закінченнями аксонів цих нейронів, але і пригнічує їх активність. У результаті в нервових закінченнях накопичується нейромедіатор (в нормі вміст серотоніну в структурах мозку становить 5 - 30 нг / мг білка); -дофаміноміметичнадія.
Надання допомоги здійснюється призначенням нейролептиків (трифтазін) і седативних препаратів (бензодіазепіни). Специфічні протиотрути ДЛК відсутні.
Деліріогени
Делірій здатні викликати всі речовини, що володіють центральноюМ-холіноблокуючоюактивністю. Найбільш токсичним представником групи є речовина BZ - похідне хінуклединилбензілата, що знаходилася на постачанні армій деяких держав як ОР несмертельної дії.
До числа деліріогенів можуть бути віднесені лікарські препарати з групи нейролептиків (похідні фенотіазину) і деякі трициклічні антидепресанти (фторацизин), які у високих дозах також проявляють властивості холінолітиків. Основними симптомами інтоксикації є:
|
- Сплутаність свідомості;
- Порушення оцінки свого стану;
- Ейфорія;
- Занепокоєння;
- Порушення координації рухів;
- Галюцинації;
- Порушення контакту із зовнішнім світом;
- Гіперрефлексія;
- Гіпертермія;
- Судоми;
- Кома;
- Амнезія.
|
Отрути змій
Отрути змій, що відносяться до сімейства Elapidae (тигрова змія, тайпан, морські змії), містять нейротоксини,що вибірково діють на механізми передачі нервового імпульсу у холінергічних нервово-м'язевих синапсах.
Токсини не проникають через гематоенцефалічний бар'єр і тому їх ефект реалізується лише на периферії, головним чином у нервово-м'язевих синапсах.
Основні клінічні ознаки отруєнь, зумовлені дією нейротоксинів при укусах змій, включають: міальгію при русі, птоз, параліч язикоглоткового нерву, парез кінцівок, порушення серцевої деятеьності, гіперкаліємію, параліч дихальної мускулатури.
Блок проведення нервового імпульсу в нервово-м'язевих синапсах розвивається в три стадії. Протягом перших 5 - 10 хвилин після впливу відзначається зменшення кількості ацетилхоліну, що вивільняється при порушенні нервового волокна. У наступні 30 - 60 хвилин, при активації нейрону, реєструється підвищений викид нейромедіатора. Потім протягом 60 - 120 хвилин спостерігається поступове зниження вивільнення ацетилхоліну до повного припинення. Клінічно тривалість латентного періоду від моменту введення токсину до розвитку ефекту становить, як правило, не менше 60 хвилин. Збільшення дози речовини, що вводиться, не призводить до зменшення цього часу. У латентному періоді токсини необоротно зв'язуються з нервовими терміналами. Спроба в умовах експерименту відмити токсин від нервових закінчень біопрепарату не призводить до відновлення здатності проводити нервовий імпульс.
Ботулотоксин
Ботулотоксин - білок, що продукується мікроорганізмами Clostridium botulinum. Ці бактерії розвиваються в білковому середовищі (в анаеробних умовах) і часом є причиною масових харчових отруєнь при використанні зіпсованих консервів, копченостей, грибів і т.д. (Ботулізм). Ботулотоксин - табельна отруйна речовина армії США.
В даний час відомо більше 8 серологічних типів токсину: A, B, C, D, E, F і т.д., близьких за структурою і токсичною активностю. Ботулотоксин є протеїном з молекулярною масою 150000, складається з двох субодиниць (МВ 100000 і 50000), що не володіють протеолітичною, фосфоліпазною чи іншою ферментативною активністю. Токсини виділені в кристалічній формі. У водних розчинах частково гідролізуються, але токсичність розчину при цьому не втрачається. Речовина стійкапри кип'ятінніпротягом години.
Смертельна доза токсину для людини становить близько 5 нг / кг маси.
Речовина потрапляє в організм через шлунково-кишковий тракт із зараженою водою і їжею,а при застосуванні його у вигляді аерозолю і через органи дихання.
При дослідженні долі токсиканту в організмі встановлено, що він вибірково захоплюється нервовими терміналами холінергічних волокон; частина введеного токсину шляхом ретроградного аксонального струму транспортується в тіла нервових клітин.
Клініка ботулізму розвивається через кілька годин після дії отрути (до 36). Перші симптоми інтоксикації- це поєднання вегетативних реакцій (нудота, блювота, слинотеча) і ознак загального нездужання (головний біль, запаморочення, болі в кінцівках). Пізніше порушується функція слинних і потових залоз, акомодація органу зору, розширюються зіниці. Основним проявом інтоксикації є параліч поперечно-смугастої мускулатури, що поступово розвивається. Процес починається з очної групи м'язів. Ранньою ознакою отруєння є диплопія. Пізніше приєднується параліч м'язів глотки, стравоходу (порушення ковтання) та інших м'язових груп. Токсичний процес поступово наростає. Іноді лише на 10 добу і в пізнішістрокиможе наступити смерть від паралічу дихальної мускулатури і асфіксії. Летальність при отруєнні ботулотоксином становить від 15 до 30%, а при несвоєчасному наданні допомоги (введення антиботулінічноїсироватки, переведенняпотерпілого на штучну вентиляцію легень і т.д.) може досягати 90%.
Ботулотоксин вибірково блокує вивільнення ацетилхоліну в нервово-м'язових синапсах. У дослідах in vitro встановлено, що дія ботулотоксину призводить до пригнічення як спонтанного, так і викликаного викиду нейромедіатора. Чутливість постсинаптичного рецептора до ацетилхоліну не змінюється. Блокада передачі сигналу не супроводжується втручанням токсиканту в процеси синтезу і зберігання ацетилхоліну.
Дія речовини тривала, до декількох тижнів, і тому характер взаємодії токсину з пресинаптичними структурами-мішенями можна розглядати як необоротне. Вважають, що відновлення нормальної іннервації м'язів відбувається в результаті формування нових синаптичних контактів.
Періоду клінічних проявів передує прихований період, під час якого і відбувається зв'язування токсиканту з нервовими закінченнями. Виділяють чотири періоди дії токсину на синапс:
- Зв'язування з плазматичною мембраною холінергічних нервових закінчень;
- Інтерналізаціятоксину шляхом ендоцитозу;
- Проникнення в цитозоль синапсу за участю pH-залежної транслокази;
- Внутрішньоклітинне розщеплення токсину під впливом метал-залежних ендопротеаз з вивільненням діючої частини білкової молекули. Для деяких серотипів токсину ці молекули ідентифіковані і позначені як: SNAP-25 (серотип А), синаптобревін (серотип В), синтаксин (серотип С).
Хронічні нейротоксичні процеси. Токсичні нейропатії
Хронічні процеси, що розвиваються з боку нервової системи в результаті гострого, підгострого або хронічного впливу токсикантів можна класифікувати відповідно до ушкоджених елементів нервової системи, характером пошкодження нервових утворень і механізмів, які лежать в основі патології. Найбільш зручна морфологічна класифікація.
Таблиця 11. Характеристика хронічних нейротоксичних процесів
|
Тип |
Враженаструктура
|
Патологічна реакція |
Ознаки |
Приклади
|
|
1. |
Тіла нервових клітин |
Загибель нервових клітин (токсична нейронопатія) |
Швидкий початок, часто виключно порушення чутливості
|
Метилртуть, адріаміцин, талій, тетраетил- свинець
|
|
2. |
Мієлінова оболонка |
Сегментарна демієлінізація (токсична міелінопатія)
|
Швидкий початок, переважно моторні порушення
|
Теллур, триетил-олово, гексахлор-фенол
|
|
3. |
Аксон |
Аксональнадегенерація (Дистальна аксонопатия) |
Поступовийпочаток, моторно-сесорние порушення, симптоми "Шкарпеток і рукавичок" |
Акриламід, ароматичні вуглеводні |
Частими формами хронічного процесу є токсичні нейропатії. Проте дуже обмежена кількість речовин вибірково діє на периферичні відділи нервової системи. Більшість пошкоджує і структури ЦНС, тому токсичнунейропатіюнерідко супроводжують ознаки енцефалопатії.
В основі хронічних процесів, як правило, лежать порушення пластичного обміну в нервовій системі, що супроводжуються її структурно-морфологічними змінами. Механізми дії токсикантів, завдяки яким вони викликають порушення пластичного обміну, різноманітні і маловивчені. Різноманіття механізмів відображаєтьсяв особливостях перебігу захворювань. Так, при хронічній інтоксикації свинцем, в клініці переважають ознаки моторних порушень. Трихлоретилен викликає ураження трійчастого і лицьового нервів, яке поєднується з церебральною патологією. Хронічне отруєння миш'яком супроводжується поліневропатією з вираженим больовим синдромом. Фосфорорганічні інсектициди можуть викликати відстрочену нейропатію (прихований період: 1 - 3 тижні і більше).
Проте, не дивлячись на відмінності механізмів ураження, і цілий ряд особливостей перебігу патології, прояви токсичного процесу, як правило, близькі і більшою мірою залежать не від механізму дії токсикантів, а від анатомічного сегменту, на який вони подіяли. Дуже часто процес прогресує і після припинення дії токсиканту.
Токсичні нейропатії проявляються сегментарною демієлінізацією (токсичноюміелінопатією) і аксональноюдегенерацією (токсичнадистальнааксонопатія).
Алюміній
Алюміній надзвичайно широко розповсюджений елемент. Контакт з нимлюдини неминучий. Разом з тим випадки гострої або хронічної інтоксикації речовиною невідомі. Це пов'язано з нездатністю алюмінію проникати через бар'єри, утворені шкірою, епітелієм шлунково-кишкового тракту і легенями.
Однак в особливих умовах можлива інтоксикація алюмінієм. Так, в літературі описані випадки енцефалопатії, що супроводжувались підвищенням вмісту алюмінію в тканині головного мозку у хворих, які довго перебували на гемодіалізі.Для контролю рівня фосфатів у плазмі крові використовували алюмінійвмісну речовину.
Збільшення вмісту алюмінію в тканинімозку виявлено в осіб з хворобою Альцгеймера. Необхідні подальші спостереження та дослідження для встановлення ролі алюмінію в патології мозку.
Алюміній викликає специфічні зміни нейрофібром нейронів. Вперше ефект був встановлений при інтрацеребральному введенні кролику антигену, пов'язаного з ад'ювантом, що містить фосфат алюмінію. При ураженнях змінені нейрони виявляються практичноу всіх структурах мозку.
Талій
Основні джерела забруднення навколишнього середовища талієм - цементні заводи, теплоелектростанції (ТЕС), що працюють на вугіллі, плавильні комбінати по випуску міді, цинку, кадмію та свинцю. Вода може бути заражена талієм поблизу металоплавильнихвиробництв. В атмосфері талій може бути присутнім у формі металу, а також оксиду і сульфату. Основне виробництво, що використовує талій - випуск напівпровідників і електричних перемикальних пристроїв.
У 1920 р. у Німеччині солі талію почали застосовувати як пестициди. Діючий агент містив 2% сульфату талію. Саме в якості пестициду талій став причиною отруєння людини. У 1965 році використання талію в якості пестициду в США було заборонено, однак в інших країнах світу він продовжує використовуватися з цією метою. Талій також застосовують для виготовлення оптичних лінз, барвників, пігментів, феєрверку. Талій став найважливішою речовиною у виробництві надпровідників.
У розвинених країнах основні області споживання талію - це виробництво електроніки, фотоелектричних елементів, ламп, сцинтиляційних лічильників, напівпровідників. Речовину також використовують, як каталізатор в хімічному синтезі, у виробництві надпровідників, штучних ювелірних виробів.
Нова хвиля широкого використання талію в якості надпровідника і каталізатора, змушує уважно вивчати токсичність речовини.
Основною причиною легких отруєнь талієм є інгаляція повітря, що містить талій або споживання фруктів, оброблених цією речовиною. Оскільки метал має виражені кумулятивні властивостямі і абсорбується через шкіру (також як і ШКТ), необхідно враховувати властивості цієї речовини, як потенційного екотоксиканта.
Гострі важкі отруєння талієм, як правило, є наслідком випадкового або навмисного прийому солей металу per os. На виробництві можливі також інгаляційні впливиі діяпри попаданні на шкіру. Всмоктування речовини здійснюється швидко (протягом 1 години) і практично повністю (в дослідах на гризунах - до 100%). Сполуки талію в руках недосвідченоїі не проінструктованоїлюдини становлять велику небезпеку.
Після проникнення в кров талій поширюється по організму, проникаючи всередину клітин. Найбільша кількість металу накопичується в нирках (у медулярного шарі). Високий вміст металу визначається в серцевому м'язі, печінці та волоссі. Концентрація талію в жировій тканині і мозку низька .У крові метал рівномірно розподіляється між плазмою, лімфоцитами і еритроцитами. Талій проникає через плаценту, протее вміст його в тканинах плоду- незначний.
Основні шляхи виділення талію - через нирки та шлунково-кишкового тракт. Період напіввиведення з організму людини становить близько 30 діб.
Талій - сильний нейротоксикант. Як правило, клінічні прояви гострої інтоксикації наростають повільно протягом декількох тижнів і характеризуються розвитком гострих і підгострих ефектів.
Таблиця 12. Основні прояви інтоксикації талієм
|
1. Гострі ефекти: |
2. Підгострі ефекти:
|
|
- Нудота
- Блювота
- Болі в животі
- Тремор
- М'язова атрофія
- Паралічі
- Атаксія
- Психоз
- Судоми
- Кома
|
- Закрепи
- Шлунково-кишкові кровотечі
- Дерматит (еритема, зміна нігтів, лущення шкіри, лінії Мії)
- Парестезія
- Висхідна нейропатія
- Поліневрит
- М'язева слабкість
- Нейропатія черепно-мозкових нервів (птоз, офтальмоплегія, ретробульбарний неврит, неврит лицьового нерва)
- Атаксія
- Стомлюваність
- Емоційні порушення
- Психози
|
При пероральному отруєнні перші симптоми - нудота і блювота. Потім протягом наступних 7-14 днів розвиваються болі в животі, закрепи, відчуття важкості в шлунку, кровотеча.
Неврологічні симптоми, як правило, з'являються через тиждень і характеризуються невритами, переважно нижніх кінцівок. Через 1-3 тижні після впливу болючість по ходу нервів посилюється, розвивається атаксія, тремор. М'язеві рефлекси зберігаються зазвичай досить довго. У процес втягуються краніальні нерви.
Пошкодження блукаючого нервусупроводжується тахікардією, помірною гіпертензією, парезом кишечника. Порушення, які виявляються при електрокардіографії, нагадують стан гіпокаліємії.
Психічні розлади проявляються депресією і психозом.
При важких інтоксикаціях досить швидко розвиваються галюцинації, делірій, судоми, кома. Смерть розвивається в результаті порушень серцевої діяльності і функціїнирок.
Одужання відбувається повільно і розтягується на місяці.
При хронічному впливі, як правило, розвивається стійка нейропатія, що супроводжується слабкістю м'язів нижніх кінцівок,болючістю по ходу нервів, порушеннями інтелекту, втратою волосся. Алопеція може розвиватися через місяці після впливу талієм. Відновлення розтягується на багато місяців.
Діагностична стратегія в нейротоксикологіі
Діагностика виражених нейротоксичних ефектів не викликає ускладнень, оскільки формуються при цьому клінічні синдроми досить добре вивчені. Складним завданням є виявлення патології в осіб з мінімальною клінікою ураження, відсутністю очевидних свідчень контакту з нейротоксикантом. Проте саме такі ситуації зустрічаються найбільш часто. У цих випадках виникає питання, чи є порушення наслідком хімічних впливів або являють собою ідіопатичні захворювання нервової системи .Діагностична стратегія в подібних ситуаціях включає збір анамнезу, детальне обстеження постраждалого лікарем-фахівцем і виявлення клінічних синдромів, проведення спеціальних діагностичних тестів.
Діагностика заснована на знанні лікарем синдромів нейроінтоксикації, викликаної прийомом лікарських засобів.
Головні болі при отруєнні лікарськими препаратами
-------------------------------------------------- --------------------
Виділяють кілька патогенетичних механізмів розвитку «лікарського» головного болю:
- Якщо у хворого є схильність до головних болей або головні болі компенсовані, то прийом деяких засобів може викликати зрив компенсаторних можливостей або реалізувати наявну схильність. До таких препаратів належать оральні протизаплідні засоби, гормональні препарати, включаючи кортикостероїди, і симпатоміметики.
- Головні болі розвиваються при вазодилатації. Такий ефект викликає прийом кофеїну, ерготаміну, нітратів, ніфедипіну, гідралазину, псевдоефедрину і бронходилятаторів.
- Головні болі можуть входити в структуру синдрому відміни анальгетиків, НПЗЗ, ерготаміну, кофеїну і наркотичних препаратів.
- Деякі препарати викликають розвиток асептичного менінгіту і доброякісної внутрішньочерепної гіпертензії. До них належать, наприклад, ібупрофен, метотрексат при інтратекальному введенні, помилкове інтрадуральне введення епідуральних анестетиків.
- Деякі препарати сприяють розвитку доброякісної внутрішньочерепної гіпертензії. До них відносяться деякі антибіотики, кортикостероїди, оральні контрацептиви і анестетики.
Лікування полягає у визначенні і відміні препарату, що викликає головні болі. У деяких випадках потрібна додаткова терапія, наприклад, при розвитку асептичного менінгіту і доброякісної внутрішньочерепної гіпертензії. Якщо у лікаря є сумніви щодо діагнозу, необхідна консультація невролога. Діагностичне значення має супутня неврологічна симптоматика, відсутність позитивної динаміки після відміни препарату, який імовірно викликав головний біль.
У тих ситуаціях, коли неможливо припинити прийом ліків, що викликали головний біль, рекомендують симптоматичне лікування. Якщо препарат призначений фахівцем іншого профілю, то необхідна його консультація для вирішення питання про заміну цього препарату. У деяких випадках можна зменшити інтенсивність головного болю, змінивши режим прийому лікарського препарату.
Когнітивні порушення, поведінкові і особистісні зміни від лікарських препаратів
Ці порушення можуть бути обумовлені або прямим впливом препарату на нервову систему, або опосередкованим, наприклад, при ураженні печінки або нирок. Виразність симптомів зазвичай має дозозалежний характер.
Серед препаратів, що сприяють розвитку інтелектуальних, особистісних і поведінкових порушень, можна виділити наступні: анальгетики, бензодіазепіни, снодійні засоби і сильнодіючі антихолінергічні засоби, наприклад, антигістамінні препарати і трициклічні антидепресанти.
Рідше інтелектуальні, особистісні та поведінкові порушення спостерігаються при прийомі засобів для лікування хвороби Паркінсона (бромокриптин, препарати леводопи, амантадин), серцево-судинних захворювань, виразки шлунка та дванадцятипалої кишки (бета-блокатори, клонідин, препарати наперстянки,блокатори кальцієвих каналів), цукрового діабету (пероральні гіпоглікемічні засоби),глаукоми та інфекційних захворювань (ізоніазид і сульфаніламіди).
Деякі хіміотерапевтичні засоби (метотрексат і цитозин-арабінозид) можуть призвести до розвитку важкого токсичного ураження головного мозку - лейкоенцефалопатії.Першими ознаками цього синдрому є психічні порушення, потім прогресує пригнічення свідомості, і настає летальний результат. Одночасно з терапією вказаними засобами опромінення головного мозку або інтертекальне введення препаратів підвищують ризик розвитку цього ускладнення.
Екстрапірамідні порушення
Спектр екстрапірамідних порушень, обумовлених прийомом лікарських препаратів, великий. Тому кожного хворого з екстрапірамідними порушеннями необхідно розпитати про препарати, які він приймав.
Серед мимовільних рухів медикаментозного походження виділяють такі форми: тремор, міоклонії, дистонію, акатизію, торсійну дистонію, хорею, атетоз і паркінсонізм.
Лікарські засоби, що найчастіше викликають екстрапірамідні порушення, - це симпатоміметики, нейролептики, трициклічні антидепресанти, транквілізатори, протипаркінсонічні засоби, літій та вальпроєва кислота.
Епілептичні напади від лікарських препаратів.
Лікарські препарати можуть провокувати епілептичні припадки внаслідок різних причин:
- Зниження порогу судомної готовності у схильних осіб, наприклад, у пацієнтів з епілептичними нападами в анамнезі або обтяженим сімейним анамнезом.
- Напади можуть бути наслідком надмірно високих доз препаратів (як реакція на передозування, порушення метаболізму препарату або взаємодія декількох препаратів один з одним).
- Напад може входити в структуру синдрому відміни лікарського засобу.
- Напад може бути непрямим показником токсичного впливу на інші органи і системи або порушень обміну речовин.
Більшість епілептичних нападів, викликаних лікарськими засобами, генералізовані, хоча деякі з них починаються як фокальні, а потім переходять у вторинно генералізовані.
Серед препаратів, що сприяють розвитку нападів, можна виділити наступні: анальгетики (кокаїн і меперидин *), анестетики (лідокаїн та кетамін), антибіотики у високих дозах (пеніцилін, ампіцилін, іміпенем та цефалоспорини), протисудомні засоби (в токсичних дозах), бронходилататори,іммуносупресанти та засоби хіміотерапії (циклоспорин А, метотрексат і вінкристин), симпатоміметики (ефедрин, псевдоефедрин і фенілпропаноламін), баклофен,бензодіазепіни (клоназепам) і барбітурати.
Вегетативні порушення від лікарських препаратів.
Артеріальна гіпотензія нерідко спостерігається при прийомі антидепресантів, діуретиків, нітратів і препаратів, що мають антихолінергічні властивості.
Порушення тазових функцій (кишечника і сечового міхура) у вигляді нетримання сечі, затримки сечі, неповного випорожнення міхура і закрепів часто зустрічається при прийомі препаратів з антихолінергічними властивостями (наприклад, антигістамінні засоби та антидепресанти).Найчастіше тазові порушення спостерігаються у хворих з попереднім субклінічним дефіцитом функції цих органів, наприклад, при цукровому діабеті, розсіяному склерозі, доброякісній гіпертрофії передміхурової залози.
У деяких випадках спостерігаються порушення статевої функції.Вони обумовлені прийомом тих же препаратів, які призводять до артеріальної гіпотензіїі тазовихпорушень.
Порушення нервово-м'язевої передачі від лікарських препаратів.
Багато лікарських препаратів викликають зміни нервово-м'язевої передачі, пацієнти з вже наявним прихованим дефіцитом більш схильні до ризику розвитку ускладнень.У схильних людей антибіотики з групи аміноглікозидів, міорелаксанти і засоби, що блокують нервово-м'язеву передачу, можуть призвести до тривалих нервово-м'язевих розладів. Слід підкреслити, що ці препарати можуть викликати тимчасову слабкість і у здорових людей.Хворим міастенією і синдромом Ламберта-Ітона протипоказані засоби, що володіють потенційним впливом на нервово-м'язеву передачу. Пеніциламін може викликати порушення нервово-м'язевої передачі, що клінічно не відрізняється від міастенії.
Тим хворим, яким потрібне проведення штучної вентиляції легенів, часто вводять седативні засоби в поєднанні з препаратами, що блокують нервово-м'язеву передачу, що може призвести до тривалої її блокади.Це порушення слід запідозрити при так званій вентиляційній залежності, якщо хворий довше, ніж це вимагає його захворювання, потребує ШВЛ. Діагноз підтверджують за допомогою електроміографії (ЕМГ).Лікування полягає у скасуванні седативних засобів і препаратів, що блокують нервово-м'язеву передачу. ШВЛ продовжують до тих пір, поки не відновиться нормальна нервово-м'язева передача.
Периферичні нейропатії при отруєнні лікарськими препаратами. Отруєння наркотичними анальгетиками.
Периферичні нейропатії лікарського генезу характеризуються порушеннями чутливості по типу «рукавичок і шкарпеток», а також симетричністю пошкоджень. Вони можуть розвиватися поступово або в деяких випадках гостро.Іноді вони мають незворотний характер, але більшість повністю відновлюються після відміни препарату. Лікарські нейропатії можуть бути сенсорними або змішаними, сенсомоторними.
Серед препаратів, що сприяють розвитку периферичних нейропатій, можна виділити наступні: антимікробні засоби (наприклад, нітрофурани, деякі аміноглікозиди, ізоніазид і метронідазол), протизапальні засоби (золото і колхіцин), хіміотерапевтичні препарати (цисплатин,вінкристин і прокарбазин), піридоксин,літій і аміодарон.
Профілактика лікарської периферичної нейропатій зводиться до наступних заходів:
- Припинення прийому препаратів, що мають потенційнийтоксичнийвплив на периферичні нерви (наприклад, при появі скарг на оніміння, парестезії в кінцівках або шум у вухах).
- Систематичний контроль концентрації в плазмі препаратів, що володіютьнейротоксичним ефектом (аміноглікозиди). Слід уникати передозувань.
- Індивідуальний підбір дози препаратів хворим із захворюваннями екскреторних органів (нирок і печінки) або застосування інших препаратів, які легше метаболізуються (наприклад, не можна призначати нітрофурани пацієнтам з порушеннями функції нирок або зневодненим хворим).
Ототоксичний ефект може входити в структуру генералізованої нейропатій або спостерігатися ізольовано.Найчастіше це явище пов'язане із застосуванням аміноглікозидів (стрептоміцину, гентаміцину та тобраміцину), але може бути ускладненням лікування цисплатином, саліцилатами, хініном, фуросемідом і етакриновою кислотою.
Міопатії
Ускладненням застосування лікарських препаратів можуть бути атрофічні, запальні або некротизуючі міопатії.
Стероїдна міопатія - це найбільш частий вид лікарської міопатії. Вона характеризується слабкістю проксимальної мускулатури без болю.Діагностика цього виду міопатії може бути дуже складна у хворих, які приймають кортикостероїди для лікування поліміозиту: може знадобитися ретельне клінічне спостереження за станом пацієнта на тлі зниження дози кортикостероїдів, їх скасування або заміни на альтернативні імуносупресанти.При ізольованій стероїдній міопатії дані ЕМГ не виявляють відхилень від норми. Біопсія м'язів виявляє атрофію м'язевих волокон типу II В. III.
1. Збір анамнестичних даних
Ключем до виявлення нейротоксичних ефектів є правильний збір анамнезу. Це пов'язано з тим, що симптоматика при токсичних нейропатіях, як правило, мало чим відрізняється від ідіопатичних захворювань нервової системи. Збір анамнезу повинен бути спрямований на встановлення можливих контактів потерпілого з небезпечними речовинами у побуті та на виробництві. Опитування немаєбути надто детальним. Слід зупинятися на найбільш інформативних моментах.
Таблиця 13.Перелік питань, що розглядаються при зборі даних професійного анамнезу
|
1. Де працює пацієнт і як давно?
2. Який вид продукції випускається?
3. Який характер діяльності пацієнта на виробництві?
4. З якими токсикантами безпосередньо контактує пацієнт?
5.Який агрегатний стан цих токсикантів?
6. Чи були випадки впливу високих доз токсикантів?
7. Чи використовуються на робочому місці індивідуальні засоби захисту; які?
8.Чи є на робочому місці спеціальні пристрої кондиціонування середовища (витяжні шафи, вентиляція, дренажні пристрої)?
9. Відзначається чи є зв'язок між погіршенням самопочуття і роботою?
10. Чи були симптоми патології до вступу на роботу?
11.Чи з'являються ознаки захворювання в процесі роботи, після роботи, у вихідні дні?
12. Чи спостерігаються аналогічні порушення здоров'я у колег?
|
У тих випадках, коли збір анамнезу не дозволяє прийти до певного висновку, виправдано відвідування лікарем робочого місця пацієнта.
Якщо не вдається виявити діючий агент на виробництві, необхідно ознайомитися з побутовими умовами, звичками, хобі пацієнта, так як і тут може бути виявлений потенційний нейротоксикант. У навколишньому середовищі можна знайти найрізноманітніші хімічні сполуки, проте, їх концентрація, як правило, абсолютно недостатня для ініціації патологічних процесів. Іноді реєструються випадки масового захворювання людей в регіонах, де мали місце техногенні аварії на промислових об'єктах з викидом у навколишнє середовище великих кількостей високотоксичних речовин. Ідентифікація таких випадків не представляє великих труднощів для експертів.
2.Дослідження фахівцями
Симптоми інтоксикації, по суті, ідентичні проявам ідіопатичних форм патології нервової системи. Обмінні, інфекційні та інші фактори, викликають патологічні стани, в основі яких, також як при дії хімічних речовин, лежить загибель нейронів або їх дисфункція, аксональна дегенерація, дифузна демієлінізація і т.д.
Більше того, один і той же токсикант, як зазначалося, може викликати різні форми ураження нервової системи, і разом з тим різні токсиканти можуть провокувати близьку симптоматику. Дослідження фахівця, в зв'язку з цим, має бути максимально ретельним та направлено на виявлення всіх характерних рис перебігу конкретного захворювання. Деякі симптомокомплекси патогномонічні для токсичних уражень.Так, дистальна аксонопатія, що поєднується з гастроентеритом і випадінням волосся - ознака отруєння миш'яком і талієм.
3. Функціональні дослідження
Вивчення нервової провідності і електроміографічні дослідження хоча і не є специфічними для виявлення токсичних нейропатій, проте дають важливу кількісну характеристику патологічного процесу, що дозволяє контролювати його динаміку, а також диференціювати аксональну дегенерацію від сегментарної демієлінізації. Оскільки при аксональной дегенерації гине лише частина нервових волокон, що утворюють нерв і при цьому проведення імпульсу по ураженоу нерву повністю не переривається, не дивлячись на виразні клінічні ознаки патології, швидкість проведення збудження не змінюється,але при цьому зменшується амплітуда реєстрованого сигналу. При сегментарній демієлінізації на початкових етапах провідність по уражених волокнах не переривається, але істотно знижується швидкість розповсюдження сигналу.
Електороміографічні дослідження дозволяють оцінити вираженість денервації м'язевих волокон, що розвивається внаслідок загибелі нервових волокон, що іннервують м'яз.
Методами оцінки ступеню важкості токсичних енцефалопатій є електроенцефалографія (ЕЕГ) і психофізіологічні дослідження. При дослідженні нейропсихологічного статусу зазвичай оцінюють рівень інтелекту, мовні здібності, увагу, пам'ять, координованість рухів і т.д. Описано синдром хронічної інтоксикації органічними розчинниками. Він включає: головні болі, часту зміну настрою, сплутаність свідомості, підвищену стомлюваність, погіршення пам'яті, депресивний стан, парестезії по ходу периферичних нервів. Проте в цілому, і ці види дослідження не є специфічними в діагностиці нейротоксичних ефектів.
Конкретні цілі:
1. Аналізувати причини виникнення токсичного впливу ліків на нервову систему.
2. Аналізувати роль і функції основних нейромедіаторів.
3. Знати групи найбільш нейротоксичних лікарських засобів.
4. Назвати основні порушення зі сторони нервової системи, що проявляються при
інтоксикаціях ( центральні нейротоксичні ефекти: гострі і хронічні;
периферичні нейротоксичні ефекти: гострі і хронічні).
5. Діагностична стратегія в нейротоксикології.
