
shpory_k_ekzu_po_BKh2
.pdf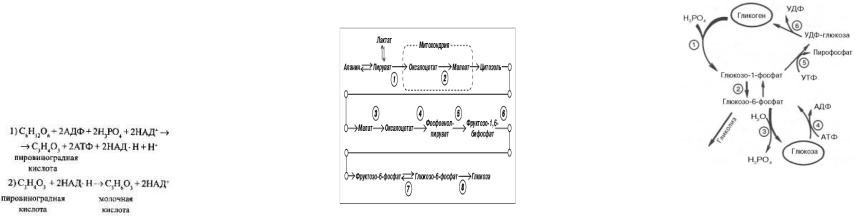
63. при молочнокислом брожении пировиноградная кислота не декарбоксилируется, а, как и при гликолизе в животных тканях, восстанавливается при участии ЛДГ за счет водорода НАДН.
Известны 2 группы молочно-кислых бактерий. Бактерии одной группы в процессе брожения углеводов образуют только молочную кислоту, а бактерии другой из каждой молекулы глюкозы «производят» по одной молекуле молочной кислоты, этанола и СО2.
Биологич. Значение: микроорг. расщепляя ферментами углевод получают АТФ и используютя ее для своей жизнедеятельности.
64.Гликолиз- распад глюкозы дихотомическим путем до пиру-вата. Биолог.роль: интенсивно работающие мышцы в условиях недостаточного обеспечения их кислородом получают за счет анаэробного процесса досьтаточное количество энергии.
КПД гликолиза составляет 50% т.к. 2моль АТФ могут аккумулировать 100кДж, а общее высвобождение э.=200кДж/моль глюкозы.
65.Химизм распада глюкозы в аэробных условиях.
Энергетический выход=1900кДж/ моль глюкозы аккумулируется в молекулах и м.б. использовано работающими механизмами клетки.
66. Глюконеогенез – синтез глюкозы из неуглеводных предшественников: основныепируват и лактат, промежуточные – глюкогенные аминокислоты и глицерин. Цикл Кори Начинается с образования лактата в мышцах в результате анаэробного гликолиза.
.Лактат переносится кровью в печень, где в процессе глюконеогенеза превращается в глюкозу, которая затем с током крови может возвращаться в работающую мышцу. Итак печень снабжает мышцу глюкозой и, следовательно, энергией для сокращений. В печени часть лактата может окисляться до СО2 и Н2О,
превращаясь в пируват и далее в общих путях катаболизма.
67-68. Пентозофосфатный путь превращения глюкозы. Представлен двумя последовате-льными ветвями: окислительной и неокислительной.
Окислительная ветвь:
1) глюкозо-6-Ф + НАДФ -> 6фос-фоглюконолактон + НАДФ*Н (фермент-дегидрогеназа) 2)6фосфоглюконолактон + Н2О -> 6фосфоглюконат + Н (фермент – лактоназа)
3)6-фосфоглюконат + НАДФ -> рибозо-5-фосфат + СО2 + НАДФ*Н (фермент – фосфоглюконатдегидрогеназа) Неокислительная ветвь: 1)рибозо-5-фосфат->рибозо-5-фо-сфат (пентозофосфатизомераза)
2)рибозо-5-фосфат -> ксилулозо-5-фосфат (пентозофосфатэпимераза)
3)ксилулозо-5-фосфат + рибозо-5-фосфат -> седогептулозо-7-фосфат + глицеральдегид-3-фосфат (транскетолаза)
4)седогептулозо-7-фосфат + глицеральдегид-3-фосфат - > фруктозо-6-фосфат + эритрозо-4-фосфат (транскетолаза)
5)ксилулозо-5-фосфат + эритрозо-4-фосфат -> фруктозо-6-фосфат + глицеральдегид-3- фосфат(транскетолаза)
Биологич.роль: образование НАДФ*Н2, синтез рибозо- 5-фосфата, который используется в реакциях синтеза РНК, ДНК, АТФ, НАД, ФАД, КоА.
69. Гликоген – депонированная форма глюкозы
Жирными стрелками указан путь распада, тонкими - путь синтеза. Цифрами обозначены ферменты: 1 - фосфорилаза; 2 - фос-фоглюкомутаза; 3 - глюкозо-6- фосфатаза; 4 - гексокиназа (глюкокиназа); 5 - глюко-зо- 1-фосфат-уридилтрансфераза; 6 - глико-генсинтаза. Можно считать, что сохранение постоянства концентрации глюкозы в крови является результатом одновременного протекания двух процессов: поступления глюкозы в кровь из печени и потребления ее из крови тканями, где она используется в первую очередь как энергетический материал.
70.Гликогенозы - Ряд наследственных болезней связан с нарушением обмена гликогена. Эти болезни получили название гликогенозов. Они возникают в связи с дефицитом или полным отсутствием ферментов, катализирующих процессы распада или синтеза гликогена, и характеризуются избыточным его накоплением в различных органах и тканях. Гликогеноз I типа (болезнь Гирке) встречается наиболее часто, обусловлен наследственным дефектом синтеза фермента глюкозо-6-фосфатазы в печени и почках.
71.Взаимопревращение углево-дов.
Неиспользованные углеводы, их фосфорилированные формы, получающиеся в результате превращения в пентозном цикле Iстадии, могут взаимодействовать между собой с образованием, как новых продуктов, ичпользующихся в различных синтетических процессах, так и неиспользованные пентозы которые могут вновь превращаться в гексозы => в конце в глюкозо-6-фосфат.
72.Глюконеогенез – синтез глюкозы из неуглеводных предшественников: основныепируват и лактат, промежуточные – глюкогенные аминокислоты и

глицерин. Цикл Кори Начинается с образования лактата в мышцах в результате анаэробного гликолиза.
.Лактат переносится кровью в печень, где в процессе глюконеогенеза превращается в глюкозу, которая затем с током крови может возвращаться в работающую мышцу. Итак печень снабжает мышцу глюкозой и, следовательно, энергией для сокращений. В печени часть лактата может окисляться до СО2 и Н2О, превращаясь в пируват и далее в общих путях катаболизма.
73.переваривание жиров. У взрослых неэмульгированные триглицериды, составляющие основную массу пищевого жира, проходят через желудок без особых изменений. После того как химус попадает в двенадцатиперстную кишку Одновременно начинается эмульгирование жира. Наиболее мощное эмульгирующее действие на жиры оказывают соли желчных кислот, попадающие в двенадцатиперстную кишку с желчью в виде натриевых солей. Большая часть желчных кислот конъюгирована с глицином или таурином. По химической природе желчные кислоты являются производными холановой кислоты. Желчные кислоты способствуют эмульгированию пищевых жиров, участвуют наряду с колипазой в активации панкреатической липазы (сдвигая ее рН в кислую сторону) обеспечивают переваривание продуктов переваривания липидов.
74. Ресинтез триацилглице-ринов в стенке кишечника. Процесс синтеза жира в энтероцитах из компонентов мицелл называется ресинтезом жира. В процессе ресинтеза происходит образование жиров, близких по составу к жирам организма. При помощи
хиломикронов осуществляется доставка пищевого (экзогенного) жира из кишечника в другие ткани (главным образом в жировую ткань. В жировой ткани из продуктов гидролиза триацилглицеринов снова происходит ресинтез жира (второй), и он депонируется там, пока не будет востребован.
Аполипопротеиныэто апобелки входящие в состав хиломикронов Апобелки выполняют не только структурную функцию,
но и обеспечивают активное участие комплексов ЛП в транспорте липидов в токе крови от мест их синтеза к клеткам периферических тканей, а также обратный транспорт холестерина в печень для дальнейших метаболических превращений. Апобелки выполняют функцию лигандов во взаимодействии ЛП со специфическими рецепторами на клеточных мембранах, регулируя тем самым гомеостаз холестерина в клетках и в организме в целом.
75.Липиды – вещества, нерастворимые в воде, но растворяющиеся в органических растворителях, содержащие в своих молекулах высшие углеводородные радикалы.
Классификация: -простые (жиры, воска)
-сложн (фосфо- и гликолипиды) -изопреноиды (стероиды, каротиноиди)
Л.участвуют в построении биологических мембран, являются важнейшим источником энеогии (триацилглицерины), обеспечивают организм витF, холестерин явл предшественником желчных кислот, стероидных гормонов, витД3, Л.выполняют защитную функц.
76.Классификация фосфоли-пидов:
глицерофосфолипиды (в роли спирта выступает глицерол), и сфинголипиды (в роли спирта – сфингозин) Биосинтез фосфолипидов триглицериды и фосфатидные синтезируются на основе глицерофосфата. Эти соединения образуются из глицерина в результате переаминирования с АТФ (катализатор- глицеро-киназа) или диоксиацетонфосфата (образуется в ходе гликолиза) в результате восстановления за счет НАДФ*Н2, катализируемого глицерофосфат дегидрогеназой. Глицерофосфат реагирует с двумя молекулами ацилКоА, образуя фосфатидные кислоты. Фосфатидная кислота под действием фосфатазы теряет остаток
фосфата. Высвободившийся диглицерид реагирует с третьей молекулой ацил-КоА, образуя триглицерид. Фосфолипиды играют важную роль в структуре и функции клеточных мембран, активации мембранных и лизосомальных ферментов, в проведении нервных импульсов, свертывании крови, иммунологических реакциях, процессах клеточной пролиферации и регенерации тканей, в переносе электронов в цепи «дыхательных» ферментов. Особая роль фосфолипидам отводится в формировании липо-протеидных комплексов.
77. |
Классификация |
сфинголи-пидов: |
|
фосфосфинголилиды |
и |
гликосфинголипиды. |
|
Сфинголипиды уч-ют в передаче клеточных сигналов (нервная ткань)
СН3-(СН2)12-СН=СН-СН-СН-NН-С-R ОН СН2
О
О Р О
О-СН2-СН2 N(СН3)3
Холин 78. Ганглиозиды — представи-тели наиболее сложно
построенных гликолипидов. Они представляют большое семейство мембранных липидов, выполняющих, повидимому, рецепторные функции. Характерной особенностью ганглиозидов является наличие остатков N-ацетилнейраминовой кислоты
Г. широко распространены в тканях мозга
79. Биосинтез кефалина. Первоначально этаноламин при участии соответствующей киназы фосфорилируется с образованием фосфо-этаноламина:
Затем фосфоэтаноламин взаимодействует с ЦТФ, в результате чего образуются цитидиндифосфатэтаноламин (ЦДФ-этаноламин) и пирофос-фат (PPi):

В следующей реакции ЦДФ-этаноламин, взаимодействуя с 1,2-дигли-церидом, образующим-ся при дефосфорилировании фосфатидной кислоты, превраща-ется в фосфатидилэтаноламин. Реакция катализируется фермен-том этаноламинфосфотрансфер-
азой: ЦДФ-этаноламин + 1,2-диглицерид –>
Фосфати-дилэтаноламин + ЦМФ Синтез лецитина:
80. Биосинтез церамида:
Интермедиатом в биосинтезе сфингомиелина является церамид (N-ацилсфингозин), который образуется при взаимодействии сфингозина с ацил-КоА. Сфингомиелин синтезируется в результате взаимодействия (реакции) церамида с ЦДФ-холином:
81. Химическое строение холестерина.
Биологическое значение:
Является важнейшим компонентом биологических мембран, из него в организме возникают кортикостероиды, половые гормоны, желчные кислоты, витД3
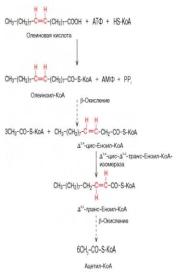
82.Бета-окисление жирных кислот. Установлено, что жирные кислоты с нечетным числом углеродных атомов окисляются таким же образом, как и жирные кислоты с четным числом углеродных атомов, с той лишь разницей, что на последнем этапе расщепления (β- окисления) образуется одна молекула пропионил-КоА и одна молекула ацетил-КоА, а не 2 молекулы ацетилКоА.
Энергетический выход:
Один цикл окисления жирной кислоты обеспечивает синтез 5молекул АТФ+12молек АТФ возникает при распаде, отщепляющегося ацетил-КоА в цикле трикарбоновых кислот. Общее кол-во молек АТФ можно рассчитать по формуле n/2*17-6 n-число углер атомов.
83.биосинтез жирных кислот:
протекает в цитоплазме клетки. В митохондриях в основном происходит удлинение существующих цепей жирных кислот. Установлено, что в цитоплазме печеночных клеток синтезируется пальмитиновая кислота (16 углеродных атомов), а в митохондриях этих клеток из уже синтезированной в цитоплазме клетки пальмитиновой кислоты или из жирных кислот экзогенного происхождения, т.е. поступающих из кишечника, образуются жирные кислоты, содержащие 18, 20 и 22 углеродных атома.
84. Образование кетоновых тел: |
|
|
||
Кетоновые |
тела |
(ацетоуксусная |
и |
бета- |
гидроксимасляная кислоты)возникают постоянно в здоровом организме и из печени поступают в кровь, откуда поглощаются периферическими тканями (особенно интенсивно используются скелетными и серд мышцами).
85. Окисление ненасыщенных ж/кислот в принципе происходит так же, как и окисление насыщенных жирных кислот, но с некоторыми особенностями. Двойные связи природных ненасыщенных жирных кислот (олеиновой, линолевой и т.д.) имеют цисконфигурацию, а в КоА-эфирах ненасыщенных кислот, являющихся промежуточными продуктами при β- окислении насыщенных жирных кислот, двойные связи имеют трансконфигурацию. Кроме того, последовательное удаление двууглеродных фрагментов при окислении ненасыщенных жирных кислот до первой двойной связи дает 3,4-ацил-КоА, а не 2,3-ацил-
КоА, который является промежуточным продуктом при |
Первичные желчные кислоты возникают в гепатоцитах |
||||||||
β-окислении ненасыщенных жирных кислот: |
|
из холестерина. При образовании холиевой кислоты |
|||||||
|
|
|
|
происходит восстановление двойной связи, окисление |
|||||
|
|
|
|
атомов 7 и 12 концевой метильной группы боковой цепи |
|||||
|
|
|
|
холестерина с последующим отщеплением пропионовой |
|||||
|
|
|
|
кислоты. Вторичные жел/кислоты образуютсяв |
|||||
|
|
|
|
кишечнике |
из |
первичных |
путемчастичного |
||
|
|
|
|
восстановления |
последних |
под |
влиянием |
||
|
|
|
|
микроорганизмов. |
|
|
|
|
|
|
|
|
|
Желчные |
кислоты |
способствуют |
эмульгированию |
||
|
|
|
|
пищевых жиров, участвуют наряду с колипазой в |
|||||
|
|
|
|
активировании пенкреатической липазы(сдвигая ее рН в |
|||||
|
|
|
|
кислую сторону), обеспечивают всасывание продуктов |
|||||
|
|
|
|
переваривания липидов. |
|
|
|
||
|
|
|
|
88-89. Биосинтез триглицеридов и фосфолшипидов |
|||||
|
|
|
|
триглицериды и фосфатидные синтезируются на основе |
|||||
|
|
|
|
глицерофосфата. Эти соединения образуются из |
|||||
|
|
|
|
глицерина |
в результате переаминирования |
с |
АТФ |
||
|
|
|
|
(катализатор- |
глицеро-киназа) |
|
или |
||
|
|
|
|
диоксиацетонфосфата (образуется в ходе гликолиза) в |
|||||
|
|
|
|
результате восстановления за счет НАДФ*Н2, |
|||||
|
|
|
|
катализируемого |
глицерофосфат |
дегидрогеназой. |
|||
86.Ненасыщенные |
ж/кислоты. |
их |
значение: |
Глицерофосфат реагирует с двумя молекулами ацил- |
|||||
Примерно 3/4 всех жирных кислот являются |
КоА, образуя фосфатидные кислоты. Фосфатидная |
||||||||
непредельными (ненасыщенными), т.е. содержат |
кислота под действием фосфатазы теряет остаток |
||||||||
двойные связи. Ненасыщенные жирные кислоты |
фосфата. Высвободившийся диглицерид реагирует с |
||||||||
человека и животных, участвующие в построении |
третьей молекулой ацил-КоА, образуя триглицерид |
||||||||
липидов, обычно содержат двойную связь между (9-м и |
Биоинтез ж/к-т протекает в цитозоле. |
|
|
|
|||||
10-м атомами углеводородов); дополнительные двойные |
Ресинтезированные в клетках кишечной стенки |
||||||||
связи чаще бывают на участке между 11-м атомом |
триглицериды, а также поступивший в эти клетки из |
||||||||
углерода и метильным концом цепи. Своеобразие |
кишечника холестерин соединяются внутри цистерн |
||||||||
двойных связей природных ненасыщенных жирных |
гладкого эндоплазматического ретикулума с небольшим |
||||||||
кислот заключается в том, что они всегда отделены |
количеством белка и образуют хиломикроны. |
|
|
||||||
двумя простыми связями, т.е. между ними всегда |
90. Липопротеиды: в сыворотке крови различают 4 |
||||||||
имеется хотя бы одна метиленовая группа (—СН=СН— |
вида липопротеидов |
|
|
|
|
||||
СН2—СН=СН—). при наличии двойной связи в |
-хиломикроны (содержат 80-90% триглицеринов, около |
||||||||
жирнокислотной цепи вращение углеродных атомов |
2% белка, образуются в эпителии кишеч-ника, являются |
||||||||
относительно друг друга ограничено. Это обеспечивает |
транспортной фо-рмой липидов (главным образом к |
||||||||
существование ненасыщенных жирных кислот в виде |
жировой ткани и печени) Клетки жировой ткани, и |
||||||||
геометрических изомеров причем природные ненасы- |
печени содержат фермент липопротеин-липазу, которая |
||||||||
щенные жирные кислоты имеют цис-конфигурацию. |
гидролизует входящие в состав хиломикрона жиры. |
||||||||
Цис-конфи-гурация делает ненасыщенную кислоту |
Жирные кислоты поглощаются и используются в |
||||||||
менее стабильной и более подверженной катабо-лизму. |
дальнейшем клетками тканей., а остатки хиломикронов |
||||||||
87.Биосинтез желчных кислот. |
|
|
в дальнейшем поглощаются печенью, |
а |
также |
||||
используются для образования липопротеинов низкой плотности.
-липопротеины очень низкой плотности ( ЛПОНП пре- бета-липопротеины) содержат свыше 50% жиров, и до 10% белков. Возникают в печени, обеспечивают транспорт триацилглицеринов из печени в жировую ткань.Подвергаются воздействию липопротеинлипазы.
-липопротеиды низк.плотности (ЛНП, беталипопротеиды). Содержат до 45% холестерина, до 25% белков.Образуются в крови из остатков хиломикронов и ЛОНП. Являются транспортной формой холестерина.ЛНП связываются с мембранными рецепторами клеток и поглощаются путем эндоцитоза -липопротеиды высокой плотности (ЛВП альфалипопротиды)содержат до 50% белков и фосфолипидов, значительное количество холестерина. ЛВП возникают в печени и посткпают в кровь где достраиваются поглощая компоненты ЛОНП и хиломикронов. ЛВП поглощают избыточный холестерин из плазматических мембран и транспортируют его вновь в печень, где он расходуется на образование желчных кислот и частично выделяется с желчью в кишечник.
91.хиломикроны синтезируютсяв клетках слизистой кишечника из продуктов переваривания пищевых липидов. Содержат до 80-90% жиров, а также фосфолипиды, эфиры холестерина, жирорастворимые витамины, представляют собой транспортную форму липидов, поступают из клеток слизистой кишечника в лимфу, а затем и в кровь.
92.Основная часть липидов (до 90 %) в мембранах представлена фосфолипидами, гликолипидами и холестери-ном. Специальные функции в мембранах выполняет фосфа-тидилинозитол, в состав кото-рого входит шестиатомный циклический спирт инозитол. Этот фосфолипид участвует в одном из механизмов пере-дачи внешних регуляторных сигналов через клеточную мембрану в клетку.
Вследствие амфифильности эти липиды в водной среде образуют многомолекулярные структуры с упорядоченным расположением молекул: гидрофобные части вытесняются из водной среды и взаи-модействуют друг с другом (как бы растворяются друг в друге), а гидрофильные части контактируют с водой и гидратируются (как бы раство-ряются в воде). Именно эта особенность строения и физии-ко-химических свойств
определяет роль фосфолипи-дов и гликолипидов в построении биологических мембран: основу мембран составляет бимолекулярный липидный слой.
93.Желчными являются кислоты холевая и хенодезоксихолевая (в гепатоцитах), дезоксихолевая и литохолевая (под влиянием микрофлоры), в малых количествах уроде-зоксихолевая., и аллохолевая.
Первичные желчные кислоты возникают в гепатоцитах из холестерина.
Первичные желчные кислоты возникают в гепатоцитах из холестерина. При образовании холиевой кислоты происходит восстановление двойной связи, окисление атомов 7 и 12 концевой метильной группы боковой цепи холестерина с последующим отщеплением пропионовой кислоты. Вторичные жел/кислоты образуютсяв кишечнике из первичных путемчастичного восстановления последних под влиянием микроорганизмов.
Желчные кислоты способствуют эмульгированию пищевых жиров, участвуют наряду с колипазой в активировании пенкреатической липазы(сдвигая ее рН в кислую сторону), обеспечивают всасывание продуктов переваривания липидов.
94.Мембраны — наиболее распространенные клеточные органеллы. Основными мембранными структурами клетки являются плазматическая мембрана, отделяющая клетку от соседних клеток или межклеточного вещества, эн-доплазматический ретикулум, пластинчатый комплекс, ми-тохондриальная и ядерная мембраны. Каждая мембрана имеет внутреннюю и внешнюю поверхности.
Поверхности одной и той же мембраны различаются по составу липидов, белков и углеводов (поперечная асимметрия). Например, в плаз-матической мембране эритро-цитов в наружном монослое двойного липидного слоя пре-обладают фосфатидилхолины, а во внутреннем
— фосфа-тидилэтаноламины и фосфа-тидил-серины. Углеводные части гликолипидов и глико-протеинов выходят на наруж-ную поверхность, иногда образуя сплошное покрытие клетки, так называемый гликокаликс; на внутренней поверхности углеводы отсутствуют. Белки, являющиеся рецепторами гормонов и других внешних сигнальных молекул, располагаются на наружной поверхности плаз-матической мембраны, а
внутрь клетки сигнал передается при участии белков внутренней поверхности мембраны.
Жидкостность мембран Двойной липидный слой имеет жидкокристаллическую
структуру: положение моле-кул липидов упорядочено, однако они сохраняют способность к диффузии в пределах слоя параллельно поверхности мембраны (латеральная диффузия).
95. Липидный состав мембран:
Вмембранах имеются фосфо-липиды двух типов — глице-рофосфолипиды и сфинго-фосфолипиды. Глицерофосфолипиды. Эти липиды являются производными фосфатидной кислоты (диацилглицеринфосфата). Сфингофосфолипиды (сфин-гомиелины). В эту групппу входят липиды, содержащие аминоспирт сфингозин. Сфингофосфолипиды являя-ются производными церами-дов (N-ацилсфингозинов); в остальном построены сходно с глицерофосфолипидами. Гликолипиды представляют собой углеводсодержащие соединения, в которых углеводная часть ковалентно связана с липидной.
Вмембранах содержатся главным образом углеводные производные церамида (N-ацилсфингозина). Общее название таких гликолипидов — гликозилцерамиды, глико-сфинголипиды (их называют также цереброзидами).
Холестерин — это предста-витель группы липидов, называемых стероидами.
Вследствие амфифильности липиды в водной среде образуют многомолекулярные структуры с упорядоченным расположением молекул: гидрофобные части вытесняются из водной среды и взаимодействуют друг с другом (как бы растворяются друг в друге), а гидрофильные части контактируют с водой и гидратируются (как бы растворяются в воде). Именно эта особенность строения и физико-химических свойств определяет роль фосфолипидов и глико-липидов в построении биоло-гических мембран: основу мембран составляет бимолекулярный липидный слой.
96. Механизмы переноса веществ через мембрану:
Простая диффузия
Небольшие нейтральные молекулы типа Н20, С02, 02, NH3 (но не NH4+), мочевина, этанол, а также гидрофобные низкомолекулярные органические вещества могут диффундировать через мембрану без
участия каких-либо специальных механизмов. Если существует трансмембранный градиент концентраций вещества, то скорость диффузии в сторону меньшей концентрации будет больше, чем в обратном направлении, и перенос веществ будет происходить, пока сохраняется градиент концентрации.
Активный транспорт перенос вещества совершается против градиента
концентра-ции. Таким способом проис-ходит перенос многих мине-ральных ионов из межкле-точной жидкости в клетку или в обратном направлении, перенос аминокислот из про-света кишечника в клетки Ки-шечника, перенос глюкозы из первичной мочи через клетки канальцев почки в кровь. Транспорт против градиента концентрации — несамопро-извольный процесс: он связан с расходованием энергии. Источником энергии может быть или гидролиз АТФ (первично-активный транспорт), или одновремен-ный перенос другого вещества, которое движется по градиенту своей концентра-ции (вторично-активный транспорт).
Ионные насосы — это белковые устройства, способ-ные избирательно присое-динять переносимый ион и гидролизовать АТФNa,K-АТФаза и Кальциевый насос (Са-АТФаза)
97.Биологическое окисле-ние определяется как савокуп-ность реакций окисления субстратов в живых клетках, основная функция которых – энергетическое обеспечение метаболизма. В организме протекает при относительно низкой температуре в присут-ствии воды, и его сворость регулируется обменом вещ-в.
98.Эндергонические и экзергонические р-и в жи-вой клетке:
Человек получает энергию за счет разложения органических веществ пищи. Самопроиз-вольные процессы — это экзергонические процессы, т. е. они сопровождаются умень-шением свободной энергии (- дельтаG), и поэтому могут служить источниками энергии для функционирования живой клетки. В результате самопроизвольного образуют-ся термодинамически стабиль-ные продукты: диоксид углерода и вода (мочевина служит для выведения избытка азота). Термо-динамически нестабильные вещества – глюкоза. В углеводах, жирах и белках (аминокислотах) содержание кислорода меньше, чем в
конечных продуктах их распада. Иначе говоря, катаболизм этих веществ связан с потреблением кислорода и реакциями окисления.
Энергия, освобождающаяся при реакциях гидролиза разных веществ, обычно невелика. Если она превышает 30 кДж/моль, то гидролизуемую связь называют высокоэнергетической (макроэргической).
99. |
Окислительное |
декарбо-ксилирование |
||
пировиног-радной |
|
кислотыВ |
результате |
|
окислительного |
декарбоксилирования |
пирува-та |
||
образуются ацетил-КоА, восстановленный НАД и диоксид углерода. процесс, катализируется сложной ферментной системой — пируватдегидрогеназным комплексом. Комплекс содержит три фермента: пируватдекарбоксила-зу, ацетилтрансферазу и дегидрогеназу дигидролипоевой кислоты. Кроме того, в реакциях участвуют пять коферментов: НАД, ФАД, тиаминдифосфат, липоевая кислота и кофермент А (КоА).На I стадии этого процесса пируват (рис. 10.8) теряет свою карбоксильную группу в результате взаимодействия с тиаминпирофосфатом (ТПФ) в составе активного центра фермента пируватдегидрогеназы (E1). На II стадии оксиэтильная группа комплекса E1–ТПФ–СНОН–СН3 окисляется с образованием ацетильной группы, которая одновременно переносится на амид липоевой кислоты (кофермент), связанной с ферментом дигидролипоилацетилтрансферазой (Е2). Этот фермент катализирует III стадию – перенос ацетильной группы на коэнзим КоА (HS-KoA) с образованием конечного продукта ацетил-КоА, который является высокоэнергетическим (макроэргическим) соединением. На IV стадии регенерируется окисленная форма липоамида из восстановленного комплекса дигидролипоамид–Е2. При участии фермента дигидролипоилдегидрогеназы (Е3) осуществляется перенос атомов водорода от восстановленных сульфгидрильных групп дигидролипоамида на ФАД, который выполняет роль простетической группы данного фермента и прочно с ним связан. На V стадии восстановленный ФАДН2 дигидролипоилдегидрогеназы передает водород на кофермент НАД с образованием НАДН + Н+. Суммарную реакцию, катализируемую пируватдегидрогеназным комплексом,
можно представить следующим образом: Пируват + НАД+ + HS-KoA –> Ацетил-КоА + НАДН + Н+ + СO2. Образовавшийся в процессе окислительного декарбоксилирования аце-тил-КоА подвергается дальнейшему окислению с образованием СО2 и Н2О. Полное окисление ацетил-КоА происходит в цикле трикарбоновых кислот (цикл Кребса).
100.Цикл Кребса:
101.Строение митохондрий: Митохондрии обычно имеют форму цилиндра с закруглен-ными концами, длиной 1-4 мкм и поперечником 0,3-0,7 мкм. Однако в разных клетках размеры и форма митох различны. Количество митох в разных клетках также различно; гепатоцит содержит около 2000 митох.
Митохи имеют внешнюю (свободно проницаема для молекул с молекулярной масс-сой примерно до 5000) и внутреннюю(образует складки — кристы,, проницаемость ограничена и избирательна ) мембраны. Содержимое пространства, ограничиваемо-го внутренней мембраной, называют матриксом.
Согласно хемиосмотической концепции, движение электро-нов по дыхательной цепи является источником энергии для транслокации протонов через митохондриальную мем-брану. Возникающая при этом разность электрохимических потенциалов (дельта мю H ) приводит в действие АТФ-синтазу, катализирующую ре-акцию АДФ + Р = АТФ. (3)
В дыхательной цепи есть только 3 участка, где перенос электронов сопряжен с нако-плением энергии, достаточным для образования АТФ, на других этапах возникающая разность потенциалов для этого процесса недостаточна. Максимальная величина коэф-фициента фосфорилирования, таким образом, составляет 3, если реакция окисления идет с участием НАД, и 2, если окисление субстрата протекает через флавиновые дегидрогеназы. Теоретически еще одну молекулу АТФ можно получить в трансгидрогеназ-ной реакции (если процесс начинается с восстановлен-ного НАДФ):
НАДФН + НАД = НАДФ + НАДН + 30 кДж/моль. (4) Функция дыхательной цепи – утилизация восстановленных дыхательных переносчиков, образующихся в реакциях ме-таболического окисления субстратов. Каждая окисли-тельная реакция в соответствии с величиной высвобож-даемой энергии «обслуживается» соответствующим дыхательным переносчиком:
НАДФ, НАД или ФАД. Соответственно своим окис- лительно-восстановительным потенциалам эти соединения в восстановленной форме под-ключаются к дыхательной цепи. В дыхательной цепи происходит дискриминация протонов и электронов: в то время как протоны перено-сятся через мембрану,создавая дельта рН. электроны дви-жутся по цепи переносчиков от убихинола к цитохро-моксидазе, генерируя разность электрических потенциалов, необходимую для образования АТФ протонной АТФ-син-тазой. Таким образом, ткане-вое дыхание «заряжает» митохондриальную мембрану, а окислительное фосфорилиро-вание «разряжает» ее.
Эффективность окислитель-ного фосфорилирования в ми-тохондриях определяется как отношение величины образо-вавшегося АТФ к поглощен-ному кислороду: АТФ/О или Р/О (коэффициент фосфо-рилирования).
102.Трансмембранный электро-химический потенциал:
Ферменты цепи переноса электронов фиксированы в митохондриальной мембране их действие векторно, т. е. характеризуется не только ве-личиной скорости реакции, но и пространственной направ-ленностью, подобно действию транспортных АТФаз. Основ-ным проявлением векторности в дыхательной цепи является перенос ионов водорода со стороны матрикса в межмем-бранное простраство .В дыха-тельной цепи есть три пункта, связанные с перекачкой про-тонов: ком-
плексы I, III и IV.
Кофермент Q при участии НАДН-дегидрогеназы (комплекс I) присоединяет элек-троны от компонентов дыхательной цепи с матриксной стороны мембраны, а освобождаются электроны и про-тоны на противоположной стороне мембраны, причем электроны акцептируются очередным компонентом дыхательной цепи, а протоны уходят в межмембранное пространство. Такой механизм называют Q-циклом. Сходным образом действует и цито-хром-с-редуктаза (комплекс III). В области цитохром-оксидазы (комплекс IV) в перекачке протонов, воз-можно, участвуют ионы Сu2.
Перенос двух электронов че-рез каждый комплекс обеспе-чивает перекачку четырех протонов.,т.о. цепь переноса электронов работает как протонный насос, перекачивая ионы водорода из матрикса на наружную сторону мембраны.
В результате по сторонам мембраны возникает разность концентраций протонов и одновременно разность электрических потенциалов со знаком «плюс» на наружной поверхности. Иначе говоря, энергия разности окисли- тельно-восстановительных по-тенциалов веществ трансфор-мируется в энергию протон-ного электрохимического по-тенциала дельта мю Н+.
Электрохимический потенци-ал понуждает протоны дви-гаться с наружной поверхно-сти внутрь, но мембрана не-проницаема для них, за иск-лючением участков, с фермен-том Н+АТФ-синтетаза, катализирующим такую реакцию:
АДФ + Н3Р04 -> АТФ + Н20 АТФ-синтетаза —крупный олигомерный белок, в кото-
ром выделяют три части: выступающую в матрикс митохи (F1), построенную из трех пар димеров альфа бета; трансмембранную (F0), обра-зующую гидрофильный канал, и промежуточную область FA. F1 содержит активные цен-тры, синтезирующие АТФ. Протоны движутся через кА-нал АТФ-синтазы, и энергия этого движения используется для образования АТФ. Меха-низмы трансформации электрохимического потенциала в энергию макроэргической свя-зи АТФ, все еще не вполне ясны.Образующаяся АТФ при участии АДФ-АТФ-трансло-казы транспортируется из матрикса на наружную сторону мембр и попадает в цитозоль. Одновременно та же транслоказа переносит АДФ в обратном направлении, из цитозоля в матрикс митохи.
103. Дыхательная цепь митох. Согласно хемиосмотической концепции, движение электро-нов по дыхательной цепи является источником энергии для транслокации протонов через митохондриальную мембрану. Возникающая при этом разность электрохимических потенциалов (дельта мю H ) приводит в действие АТФ-синтазу, катализирующую ре-акцию АДФ + Р = АТФ. (3)
В дыхательной цепи есть только 3 участка, где перенос электронов сопряжен с нако-плением энергии, достаточным для образования АТФ, на других этапах возникающая разность потенциалов для этого процесса недостаточна. Максимальная величина коэф-фициента фосфорилирования, таким образом, составляет 3, если реакция окисления идет с участием НАД, и 2, если окисление субстрата протекает через флавиновые дегидроге-
назы. Теоретически еще одну молекулу АТФ можно получить в трансгидрогеназ-ной реакции (если процесс начинается с восстановлен-ного НАДФ):
НАДФН + НАД = НАДФ + НАДН + 30 кДж/моль. (4) Функция дыхательной цепи – утилизация восстановленных дыхательных переносчиков, образующихся в реакциях ме-таболического окисления субстратов. Каждая окисли-тельная реакция в соответствии с величиной высвобож-даемой энергии «обслуживается» соответствующим дыхательным переносчиком: НАДФ, НАД или ФАД. Соответственно своим окис- лительно-восстановительным потенциалам эти соединения в восстановленной форме под-ключаются к дыхательной цепи. В дыхательной цепи происходит дискриминация протонов и электронов: в то время как протоны перено-сятся через мембрану,создавая дельта рН. электроны дви-жутся по цепи переносчиков от убихинола к цитохро-моксидазе, генерируя разность электрических потенциалов, необходимую для образования АТФ протонной АТФ-син-тазой. Таким образом, ткане-вое дыхание «заряжает» митохондриальную мембрану, а окислительное фосфорилиро-вание «разряжает» ее.
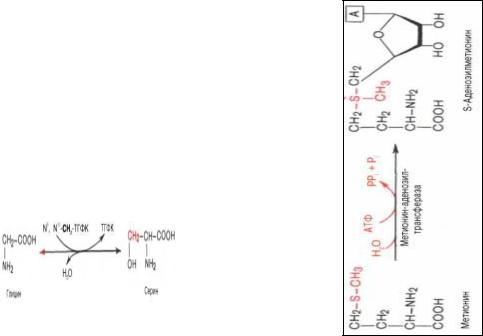
104. Глицин является единственной из всех входящих
всостав белков аминок-т, в молекуле которой нет ассиметричного атома углерода. Г.незаменим в синтезе
вборазовании белков,париновых нуклеотидов, гемма гемоглобина, парных желчных кислот, креатина, глутатиона.
Серин легко превращается в пируват под действием сериндегидратазы. В связи с этим в тканях имеются условия для превращения глицина (через серин) в пируват. Этим путем осуществляется участие глицина в обмене углеводов.
Роль тирозина в метаболизме чел. И жив.:
Молек тирозина уч-ют в биосинтезе гормонов щит.железы, также является предшественником меланинов, в биологическом процессе обеспечивающем пигментацию кожи, глаз, волос.
105.Аргинин и его роль в обмене в-в участвует в орнитиновом цикле синтеза мочевины, он является донором амидиновой группы в процессе синтеза креатина (уч-ют также глицин и метионин), А. служит источником для образования пролина(через орнитин и глутаминовую кислоту)
106. S-аденозилметионин,
Фактическим донором метильных групп в реакциях трансметилирования является не свободный метионин, а так называемый активный метионин – S- аденозилметионин, который образуется в процессе АТФ-зависимой реакции, катализируемой метионинаденозилтрансферазой.
.
Своеобразие данной реакции заключается в том, что СН3-группа ме-тионина активируется под действием положительного заряда соседнего атома серы. S- аденозилметионин участвует во всех реакциях, где метильная группа используется в биосинтетических реакциях: например, в синтезе адреналина, креатинина, тимина, фосфатидилхолина, бетаина и др.
107. Распад пуриновых оснований
Конечные продукты: мочевая кислота, СО2, Н2О,фосфаты, аммиак.
108. Распад пиримидин. Осн.:
Продукты распада:аммиак, СО2, Н2О,фосфаты
109.Обезвреживание аммиака.
Основная масса аммиака обезвреживается в печени с образованием мочвины и в почках с образованием аммонийных солей. Мочевина и соли аммония это конечные продукты азотистого обмена, они выводятся почками.
Способы :
_основной реакцией выведения аммиака является синтез глутамина под действием глутаминсинтетазы. Глутамат+NН3+АТФ->Глутамин +АДФ+Pi . Глутаминсинтетаза обладает высоким сродством к аммиаку и благодаря этой реакции в крови и в тканях поддерживается низкая концентрация NН3. Глутамин явл транспортной формой аммиака т.к. представляет собой нейтральную амино к-ту, способную протекать через клеточные мембраны путем облегченной диффузии.Образовавшийся в тканях глутамин транспортируется в почки и кишечник. В клетках киш от глутамина отщепляется амидная группа в виде NН3, образовавшийся глутамат трансаминируется с образованием аммиака: Глутамин+Н2О глутамат+
NН3
Глутамат +пируват альфа-кетоглутамат=аланин. Первая р-я катализируется глутаминазой, вторая - АЛТ -н.сист: аммиак выводится при помощи восстановительного аминирования, альфа-кетоглутарата под действием глутаматдегидрогеназы, Глутамат в дальн-м может превращаться в глутамин.
NН3
Альфа-кетоглутара глутамат
NН3 |
ГД |
глутамин |
|
Глутаминсинтетаза |
|
-из мышц избыток азота выводится в виде аланина. Аланин получается из ПВК трансаминированием. Источником ПВК в м-цах является глю и также распадающиеся аминокислоты. Аланин из мышц поступает в печень, где из него непрямым дезаминированием получается амиак и ПВК. Аммиак
обезвреживается, а ПВК включается в глюконеогенез, образовавшаяся в результате глюконеогенеза глю из печени поступает в ткани, а там окисляется до пирувата.
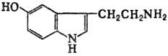
110.Синтез |
серотонина |
В организме человека и животных С. синтезируется во мн. тканях из триптофана путем его гидроксилирования (фермент триптофангидрок-силаза) с образованием 5- гид-рокси-триптофана, кот. затем под действием декарбокси-лазы ароматич. L-аминокислот превращается в С. Играет важную роль в деятельности центр. и периферич. нервной системы в качестве медиатора (передатчика) нервных импульсов.
111. гормоны задней доли гипофиза:
Вазопрессин(В) и окситоцин(О) синтезируются в рибосомах. В гипоталамусе синтезируются белки нейрофизин I, II и III способные связывать В иО и транспортировать их в нейросекреторные гранулы гипоталамуса, из ядер гипоталамуса мигрируют вдоль аксона и достигают задней доли гипофиза – резерв гормонов Химич.строние:О:
S----------------------------S
Н-Цис-Тир-Иле-Глн-Асн-Цис-Про-Лей-Гли-СО-NН2
S---------------------------S
Н-Цис-Тир-Иле-Глн-Асн-Цис-Про-Арг-Гли-СО-NН2 Физиолог.значение:
О: сокращение гладких мышц матки и циркулярных параальвеолярных мыш волокон мол.желез.
В: стимуляция сокращения гл.мышечн.волокон сосудов, регуляция водного обмена.
112. Гормоны передней доли гипофиза:
Гормон роста(СТГ), кортикотро-пин, тиротропин, пролактин, фолликулостимулирующий, лютеинизирующий СТГ под его действием усиливается синтез белка, ДНК,
РНК и гликогена, мобилизация жиров из депо и распад высших жирных кислот и глюкозы в тканях. + обладает лактогенной активностью.
Кортикотропин:: стимуляция синтеза и секреции гомонов коры надпочечников.
Пролактин: стимуляция развития мол.желез и лактации
Тиротропин: контролирование развития и функции щит.жел, регуляция и синтез в кровь тиреоидных гормонов..
113.Гормоны мозгового в-ва надпочечников:катехоламины-
Дофамин (Д), норадреналин (Н), адреналин(Адр) Биосинтез: непоср предшественник катехоламиновтирозин. Превращение тирозина в адреналин происходит в 4 этапа. Адреналин – главный продукт хромаффинных клеток мозг.слоя надпочечников. Вне мозг.в-ва Адр не образуется.
Биомед.значение:
-мозг- усил.кровотока, повыш обмена глюкозы; -ССС- увелич, частоты и силы СС, сужение периферических сосудов;
-легочн.сист- повышен.снабжения кислор., расширен. Бронхов, увеличен.вентиляции; -мышцы- повышение гликогенолиза и сократимости
-печень-повышен продукции глю, , сниж синтеза гликогена -жир.ткань-повышение липолиза, увелич уровня жирн кислот и глицерола -кожа- сниж кровотока
-скелетн м-цы-сниж поглащения и утилизации глю -ЖКТ и мочеполов систсниж синтеза белка -лимфоидная тканьповыш протеолиза.
114.Горм корк в-ва надпоч.
гормоны коркового вещества надпочечников условно делят на глюкокортикоиды (корти-костероиды, оказывающие влияние на обмен углеводов, белков, жиров и нуклеиновых кислот) и минералокортикоиды (кортикостероиды, оказывающие преимущественное влияние на обмен солей и воды) . К первым относятся кортикостерон, кортизон, гидрокортизон (кортизол), 11дезоксикортизол и 11-дегидрокортикостерон, ко вторым
– дезоксикортико-стерон и альдостерон. Установлено, что предшественником кортикостероидов является холес-терин(ол) и процесс стероидогенеза, как и нормальное гистологическое строение и масса надпочечников, регулируется АКТГ гипофиза. В свою очередь синтез АКТГ в гипофизе, а значит, и кортикостероидов в корковом веществе надпочечников регулируется гипоталамусом, который в ответ на стрессовые ситуации секретирует кортиколиберин. Глюкокортикоиды оказывают разностороннее влияние

на обмен веществ в разных тканях. В мышечной, лимфатической, соединительной и жировой тканях глюкокортикоиды, проявляя катаболическое действие, вызывают снижение проницаемости клеточных мембран и соответственно торможение поглощения глюкозы и аминокислот; в то же время в печени они оказывают противоположное действие. Конечным итогом воздействия глюкокорти-коидов является развитие гипергликемии, обусловленной главным образом глюконеогенезом. Минералокортикоиды
(дезоксикортикостерон и альдостерон) регулируют главным образом обмен натрия, калия, хлора и воды; они способствуют удержанию ионов натрия и хлора в организме и выведению с мочой ионов калия. Повидимому, происходит обратное всасывание ионов натрия и хлора в канальцах почек в обмен на выведение других продуктов обмена, в частности мочевины.
115.Гормоны пептидной природы:
Пептидные и белковые гормоны включают от 3 до 250 и более аминокислотных остатков. Это гормоны гипоталамуса и гипофиза (тироли-берин, соматолиберин, соматостатин, гормон роста, кортикотропин, тире-отропин и др. – см. далее), а также гормоны поджелудочной железы (инсулин, глюкагон).
Могут вызвать быструю ответную реакцию орг. Путемувеличения активности уже сущ-х в тканях ферментов.
116. Релизинг-факторы:
Под влияниемразличных раздражителей возникают импульсы в специализированных рецепторах, и направл в ЦНС. В гипоталамусе в ответ синтезируются биол.активн.гормональные в-ва-релизинг-факторы. Которые через портальную систему сосудов достигают гормонсинтезирующих клетокгипофиза, изменяя их активность стимулируя или тормозя.
117.гормоны ит.железы:
Тироксин, трийодтирамин и кальцитонин.
Биосинтез тироксина происходит в фолликулах щитовидной железы путем конденсации двух остатков молекул дииодтирози-на, входящих в состав тиреоглобулина - гликопротеина, содержащего ок. 5 тыс. аминокислотных остатков (из них 120-остатки
тирозина). Иодирование остатков тирозина осуществляется иодом, к-рый образуется путем ферментативного окисления иодидов, поступающих в щитовидную железу вместе с кровью. Механизм биосинтеза Т., по-видимому, включает окисление остатка дииодтирозина в тирео-глобулине до своб. радикала. Образующиеся в результате синтеза Т. остатки пировиноградной к-ты или серина остаются в составе молекулы тиреоглобулина.
У человека и высших животных он усиливает энергетич. обмен ( в т.ч. поглощение О2 тканями, увеличение теплопродукции), влияет на рост и дифференцировку тканей, стимулирует сердечную деятельность, повышает возбудимость нервной системы. У земноводных и нек-рых костистых рыб стимулирует метаморфоз. В основе механизма физиол. действия Т. лежит его взаимод. со специфич. рецепторами клеточных ядер и регулирующее влияние на процессы синтеза РНК и белка.
118.Ингсулин
человека состоит из двух пептидных цепей (А и В), соединенных двумя ди-сульфидными мостиками; третий дисульфидный мостик находится в цепи А биосинтез инсулина осуществляется в β-клетках панкреатических островков из своего предшественника проинсулина В физиологической регуляции синтеза инсулина
доминирующую роль играет концентрация глюкозы в крови. Так, повышение содержания глюкозы в крови вызывает увеличение секреции инсулина в панкреатических островках, а снижение ее содержания, наоборот,– замедление секреции инсулина. Этот феномен контроля по типу обратной связи рассматривается как один из важнейших механизмов регуляции содержания глюкозы в крови. На секрецию инсулина оказывают влияние, кроме того, электролиты (особенно ионы кальция), аминокислоты, глюкагон и секретин. Приводятся доказательства роли циклазной системы в секреции инсулина. Предполагают, что глюкоза действует в качестве сигнала для активирования аденилат-циклазы, а образовавшийся в этой системе цАМФ – в качестве сигнала для секреции инсулина.
119. роль циклических нуклеотидов в регуляции метаболизма
120. эстрогены
Основным местом синтеза женских половых гормонов – эстрогенов (от греч. oistros – страстное влечение) – являются яичники и желтое тело; доказано также образование этих гормонов в надпочечниках, семенниках и плаценте.
Основная биологическая роль эстрогенов и прогестерона, синтез которых начинается после наступления половой зрелости, заключается в обеспечении репродуктивной функции организма женщины. В этот период они вызывают развитие вторичных половых признаков и создают оптимальные условия, обеспечивающие возможность оплодотворения яйцеклетки после овуляции. Прогестерон выполняет в организме ряд специфических функций: подготавливает слизистую оболочку матки к успешной имплантации яйцеклетки в случае ее оплодотворения, а при наступлении беременности основная роль – сохранение беременности; оказывает тормозящее влияние на овуляцию и стимулирует развитие ткани молочной железы. Эстрогены оказывают анаболическое действие на организм, стимулируя синтез белка.
121.Андрогены
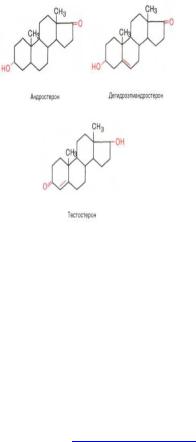
(прогестины, гормоны желтого тела), гормоны регулирующие беременность у плацентарных животных.
124. Гормоны оказывают действие на специализированные органы и ткани (органымишени) Вызывая ответные реакции на действие раздражителей.
Биологическая роль андрогенов в мужском организме в основном связана с дифференцировкой и функционированием репродуктивной системы, причем в отличие от эстрогенов андрогенные гормоны уже в эмбриональном периоде оказывают существенное влияние на дифференцировку мужских половых желез, а также других тканей, определяя характер секреции гонадотропных гормонов у взрослых. Во взрослом организме андрогены регулируют развитие мужских вторичных половых признаков, сперматогенез в семенниках и т.д. Следует отметить, что андрогены оказывают значительное анаболическое действие, выражающееся в стимуляции синтеза белка во всех тканях , но в большей степени в мышцах.
122. Пргестерон
Женский стероидный гормон позвоночных, вырабатываемый желтым телом яичника, плацентой (в меньших количествах – семенниками и корой надпочечников)
Прогестерон выполняет в организме ряд специфических функций: подготавливает слизистую оболочку матки к успешной имплантации яйцеклетки в случае ее оплодотворения, а при наступлении беременности основная роль – сохранение беременности; оказывает тормозящее влияние на овуляцию и стимулирует развитие ткани молочной железы. Эстрогены оказывают анаболическое действие на организм, стимулируя синтез белка.
123.Гестагены:
