
- •Российский национальный исследовательский медицинский университет имени н.И. Пирогова
- •Содержание
- •Строение атома
- •Заряд атома нейтральный!
- •Заполнение орбиталей
- •Виды атомных орбиталей
- •Главные характеристики атома
- •Периодический закон и периодическая система химических элементов д.И. Менделеева
- •Физический смысл Периодического закона (на примере )
- •Закономерности изменения свойств элементов
- •Семейства химических элементов
- •Характер оксидов и гидроксидов I-VII групп
- •Химическая связь
- •Механизмы образования ковалентной связи
- •Способы перекрывания электронных облаков
- •Свойства ковалентной связи
- •Типы гибридизации
- •Кристаллические решетки
- •Сравнительная характеристика кристаллических решеток
- •Валентность и степень окисления
- •Правила определения степени окисления элемента в соединении
- •Химические реакции и закономерности их протекания Классификация химических реакций
- •Методы расстановки коэффициентов в уравнениях овр
- •Обратимые химические реакции. Химическое равновесие
- •Растворы. Электролитическая диссоциация
- •Способы выражения состава раствора
- •Теория электролитической диссоциации (1887 г., Сванте Аррениус)
- •Реакции ионного обмена
- •Гидролиз
- •Случаи гидролиза солей
- •Важнейшие классы неорганических соединений
- •Металлы
Обратимые химические реакции. Химическое равновесие
Реакции, которые одновременно протекают в прямом и обратном направлениях, называют обратимыми.
Состояние химического обратимого процесса, при котором скорость прямой реакции равна скорости обратной реакции, называется химическим равновесием.
Смещение химического равновесия осуществляется по принципу Ле-Шателье: если на систему, находящуюся в состоянии химического равновесия, оказать внешнее воздействие (изменить концентрацию, температуру, давление), то равновесие смещается в сторону той реакции, которая ослабляет это воздействие.
Пример: 2SO2 + O2 ⇌ 2SO3 + Q
2V 1V 2V
|
Увеличение концентрации исходных веществ |
Равновесие смещается в сторону образования продукта реакции SO3 |
|
Уменьшение концентрации продуктов реакции | |
|
Уменьшение температуры смеси | |
|
Увеличение давления |
|
Равновесие смещается в сторону образования исходных веществ SO2 и O2 |
Увеличение концентрации продуктов реакции |
|
Уменьшение концентрации исходных веществ | |
|
Увеличение температуры смеси | |
|
Уменьшение давления |
Катализаторы и ингибиторы не оказывают влияния на смещение химического равновесия.
Растворы. Электролитическая диссоциация
Растворы – это однородные (гомогенные) системы, состоящие из двух или более компонентов и продуктов их взаимодействия.
Пример: раствор H2SO4 состоит из:
растворителя – H2O
растворенного вещества – H2SO4
гидратированных ионов, находящихся в растворе
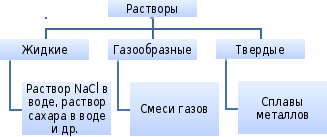
Как правило, смеси твердых веществ являются гетерогенными системами.
Растворимость – это свойство вещества растворяться в воде или в другом растворителе.
Коэффициент растворимости показывает максимальную массу вещества, которую можно растворить в 100 г растворителя при данной температуре.

Способы выражения состава раствора
Массовая доля растворенного вещества в растворе (w):
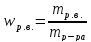
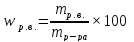
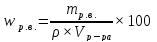
где
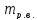 – масса растворенного вещества;
– масса растворенного вещества;
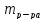 – масса раствора;
– масса раствора;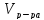 – общий объем раствора;
– общий объем раствора;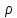 – плотность раствора.
– плотность раствора.
Молярная концентрация раствора:
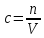
где с – молярная концентрация; n – количество растворенного вещества; V – объем раствора.
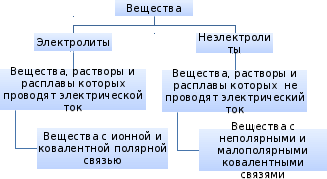
Теория электролитической диссоциации (1887 г., Сванте Аррениус)
Электролиты при растворении в воде распадаются (диссоциируют) на «+» и «-» ионы – процесс электролитической диссоциации.
Под действием электрического тока ионы приобретают направленное движение: катионы движутся к катоду, анионы к аноду.
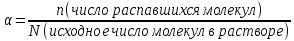
Степень
диссоциации (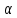 )зависит
от природы электролита и растворителя,
температуры, концентрации раствора.
)зависит
от природы электролита и растворителя,
температуры, концентрации раствора.

Реакции ионного обмена
Все реакции в водных растворах электролитов являются реакциями между ионами – ионными реакциями, уравнение этой реакции – ионными уравнениями.
Условия протекания реакций ионного обмена до конца:
Образование осадка
Образования газа
Образование малодиссоциирующего вещества
Алгоритм составления ионных уравнений:
Написать уравнение реакции в молекулярной форме.
Определить причину, за счет которой реакция обмена идет до конца и отметить это в уравнении реакции соответствующим образом (↑ или ↓).
Запишите ионы диссоциирующих веществ, указав их число и заряды.
Отметьте одинаковые ионы (они не принимают участие в реакции) в левой и правой частях уравнения реакции.
Запишите строкой ниже оставшиеся ионы и вещества (сокращенное ионное уравнение).
Сформулируйте вывод на основе сокращенного ионного уравнения.
Пример: FeCl3 + 3NaOH → Fe(OH)3↓ + 3NaCl
Fe3+ + 3Cl- + 3Na+ +3OH- → Fe(OH)3↓ + 3Na+ + 3Cl-
Fe3+ + 3OH- → Fe(OH)3↓
Вывод: реакция ионного обмена идет до конца, так как образуется осадок.
