
диссертации / 51
.pdf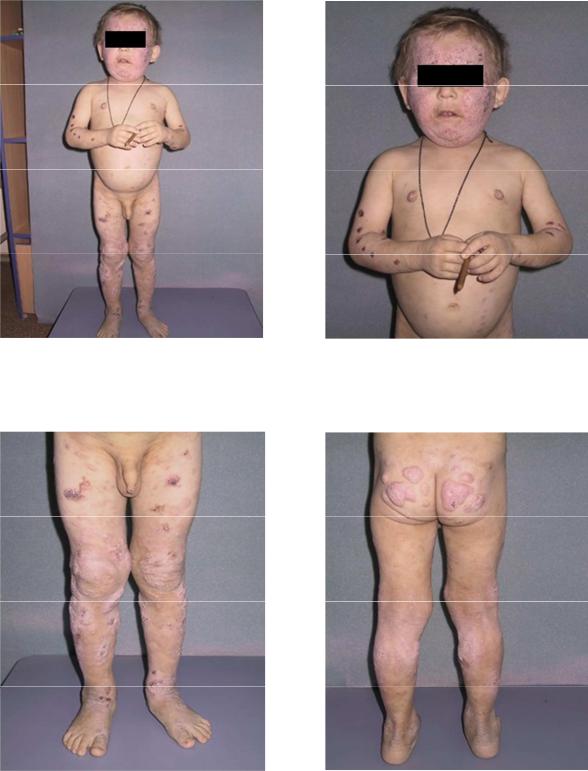
151
А. |
Б. |
В. |
Г. |
Рисунок 20 (А-Г). Тяжелый атопический дерматит. Пруригенозная форма заболевания

152
А. |
Б. |
В. |
Г. |
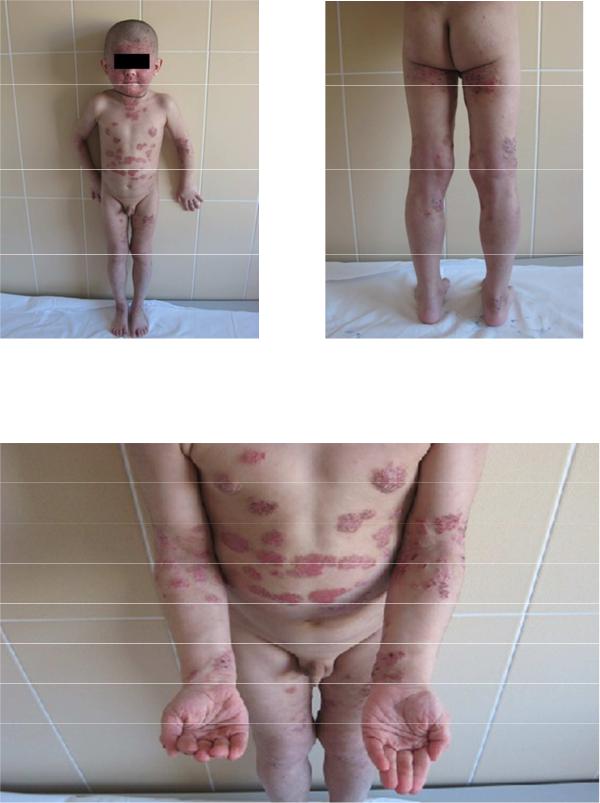
Рисунок 21 (А-Г). Тяжелый атопический дерматит. Пруригенозная форма заболевания
153
А. |
Б. |
В.

154
Г.
Д. Е.
Рисунок 22 (А-Е). Тяжелый атопический дерматит. Экссудативная форма заболевания

155
А. |
Б. |
В. |
Г. |
Рисунок 23 (А-Г). Тяжелый атопический дерматит. Экссудативная форма заболевания
156
Таким образом, проведенные нами клинические исследования, включающие сбор семейного и аллергологического анамнеза, изучение сроков
ипричин появления первых симптомов болезни, основных факторов, влияющих на обострение и дальнейшее течение заболевания, а также детальное изучение особенностей течения АД (связь с сезонностью, частота и длительность периодов обострения и ремиссии, частота различных осложнений
иклинико-морфологических форм), спектра сопутствующей патологии и осложнений выявили явную неоднородность полученных результатов.
По представленным данным литературы, а также по результатам наших собственных многолетних наблюдений, такая неоднородность может быть обусловлена различной степенью преобладания в развитии и последующем течении тяжелых форм АД у детей иммунных (главным образом IgEопосредованных) и неспецифических механизмов, характеризующихся нарушениями процессов естественной резистентности, подробное изучение которых отражено в следующих главах данной работы.
157
ГЛАВА 4. РОЛЬ ИММУННЫХ МЕХАНИЗМОВ В ФОРМИРОВАНИИ И РАЗВИТИИ ТЯЖЕЛЫХ ФОРМ АТОПИЧЕСКОГО ДЕРМАТИТА У ДЕТЕЙ 4.1. Характер изменений, интенсивность и типы продукции общего и
специфических IgE. Количество эозинофилов в кровяном русле у детей с тяжелыми формами атопического дерматита. Обоснование выделения различных патогенетических вариантов заболевания
Зарубежные ученые выделяют два клинико-патогенетических варианта АД, обозначаемые как extrinsic- и intrinsic-формы [449]. Что касается патогенеза этих форм, то Werfel T. et al. [267] свели развитие extrinsic-формы к закономерностям развития IgE-опосредованных реакций, а intrinsic-форма, с их точки зрения, является пока «черным ящиком».
В настоящей работе мы использовали в качестве основы для выделения патогенетических вариантов АД не столько величины общего IgE (у большинства больных он был повышен и превышал верхнюю границу референтных значений в 3-175 раз), сколько степень сенсибилизации организма и другие иммунные (специфические) параметры.
Степень сенсибилизации оценивали по уровню специфического IgE в сыворотке крови к наиболее распространенным видам аллергенов из разных групп. С этой целью у всех 318 детей определяли уровень специфического IgE к 27-33 аллергенам.
Анализ полученных результатов показал большой разброс индивидуальных значений, поэтому для выделения типов сенсибилизации мы сравнивали величины IgE-антител у каждого ребенка к аллергенам в пределах каждого их класса (пыльцевые, бытовые, пищевые, эпидермальные и грибковые), а также между классами. На этой основе определяли сходные типы образования IgE-антител и объединяли их в отдельные группы. Так, было выделено 5 типов образования IgE-антител, которые легли в основу выделения 5-ти типов сенсибилизации и образования 5-ти групп больных.
158
Вкаждой группе был рассчитан средний уровень специфического IgE в МЕ/мл для каждого класса аллергенов. При этом было обнаружено, что часть больных по-разному реагируют на аллергены растительного и животного происхождения, в связи с чем было проведено дополнительное сравнение этих результатов. У ряда больных мы определяли IgE-антитела и к грибковым аллергенам. Однако в связи с малочисленностью таких определений эти результаты в дальнейшие расчеты не включались. Они имели только диагностическое значение.
Витоге все результаты были суммированы (табл. 10). Они включают среднюю величину общего IgE в каждой группе, а также средние величины специфического IgE в расчете на один аллерген в МЕ/мл для:
1.аллергенов, объединяющих все 5 классов аллергенов (пыльцевые, пищевые, бытовые, эпидермальные, грибковые);
2.пыльцевых аллергенов;
3.пыльцевых и пищевых растительных аллергенов;
4.бытовых, эпидермальных и пищевых аллергенов животного происхождения.
Как видно из таблицы 10, выделенные группы действительно различаются между собой как по характеру сенсибилизации, так и по степени ее выраженности.
I группа включает больных без признаков сенсибилизации. Общий IgE в пределах нормы или ее верхней половины. Специфический IgE в большинстве случаев соответствовал нулевому или 0/I классам. В зарубежной литературе эта группа обозначается как «intrinsic»;
II группа объединяет больных, находящихся в стадии тотальной общей стимуляции образования специфических IgE ко всем исследованным
аллергенам. Средний уровень IgE-антител составляет 8,2±0,36 МЕ/мл в расчете на один аллерген для всех 5 классов аллергенов. Эта расчетная величина специфического IgE практически полностью совпадает с аналогичными величинами для пыльцевых аллергенов (7,77±0,32 МЕ/мл), а также для
159
пыльцевых и растительных пищевых аллергенов (7,12±0,47 МЕ/мл) и бытовых,
эпидермальных и пищевых аллергенов животного происхождения (8,33±0,55
МЕ/мл). Общий IgE достоверно самый высокий – 983,5 ±9,7 МЕ/мл, по сравнению с другими группами.
|
|
|
|
|
|
|
|
|
|
Таблица 10 |
|
|
|
Распределение пациентов с АД на группы в зависимости |
|
||||||||
от среднего уровня содержания в сыворотке крови специфического IgE |
|||||||||||
|
|
|
в расчете на 1 аллерген в МЕ/мл (М±m) |
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
№ |
Кол- |
Общ. |
|
|
|
|
Группы аллергенов |
|
|
||
гр. |
во |
IgE |
Все 5 групп |
|
деревья, травы |
пыльцевые, |
бытов., эпидер., |
||||
|
боль- |
(МЕ/мл) |
|
(пыльцевые) |
пищев. растит. |
пищев. животные |
|||||
|
|
|
|
||||||||
|
ных |
|
Кол-во |
Спец. |
Кол-во |
Спец. |
Кол-во |
Спец. |
Колво |
Спец. |
|
|
|
|
аллер- |
IgE |
|
аллер- |
IgE |
аллер- |
IgE |
аллер- |
IgE |
|
|
|
генов |
(МЕ/мл) |
генов |
(МЕ/мл) |
генов |
(МЕ/мл) |
генов |
(МЕ/мл) |
|
I |
83 |
36,2 |
2241 |
0,34 |
|
498 |
0,42 |
1134 |
0,28 |
1107 |
0,38 |
±4,8 |
±0,03 |
|
±0,05 |
±0,03 |
±0,05 |
||||||
|
|
|
|
|
|
|
|||||
II |
145 |
983,5 |
4785 |
8,2 |
|
966 |
7,77 |
2398 |
7,12 |
2387 |
8,33 |
±9,7 |
±0,36 |
|
±0,32 |
±0,47 |
±0,55 |
||||||
|
|
|
|
|
|
|
|||||
III |
32 |
320,1 |
1024 |
2,96 |
|
267 |
5,4±0,5 |
577 |
4,5±0,4 |
447 |
2,05±0,5 |
±5,8 |
±0,37 |
|
|||||||||
|
|
|
|
|
|
|
|
|
|
||
IV |
35 |
619,4 |
1015 |
4,45 |
|
105 |
0,03 |
525 |
2,6±0,6 |
490 |
8,2±0,6 |
|
±9,3 |
±0,3 |
|
±0,03 |
|||||||
|
|
|
|
|
|
|
|
|
|||
V |
23 |
54,8 |
621 |
1,5±0,4 |
|
121 |
2,9±0,3 |
315 |
2,1±0,5 |
306 |
1,06 |
±8,2 |
|
±0,35 |
|||||||||
|
|
|
|
|
|
|
|
|
|
||
Нормальные значения общего IgE – от 0 до 50,0 МЕ/мл; |
|
|
|
||||||||
Нормальные значения содержания специфических IgE – |
< 0,3 МЕ/мл. |
|
|||||||||
|
III |
и IV группы |
больных |
интересны тем, что |
в них |
выявляется не |
|||||
тотальная, а парциальная стимуляция образования специфических IgE. Так, в III группе значительно преобладает стимуляция образования IgE-антител к растительным аллергенам (пыльцевые и пищевые растительные). Здесь средний уровень IgE-антител составляет 4,5±0,4 МЕ/мл против 2,05±0,5 МЕ/мл для бытовых, эпидермальных и пищевых аллергенов животного происхождения.
Общий IgE высокий – 320,1 ±5,8 МЕ/мл, но достоверно ниже по сравнению с II группой больных.
160
У больных IV группы отмечается противоположная картина. Здесь значительно преобладает средний уровень IgE-антител (8,2±0,6 МЕ/мл) к аллергенам животного происхождения (эпидермальным, бытовым, пищевым животным) по сравнению с таковыми (2,6±0,6 МЕ/мл) для растительных аллергенов. Уровень общего IgE достоверно выше такового в III группе больных – 619,4 ±9,3 МЕ/мл, но достоверно ниже, чем у больных II группы.
V группа больных характеризуется избирательной сенсибилизацией к ограниченному количеству аллергенов (в большинстве случаев от 1 до 3), среди которых основными являются береза и домашняя пыль. Общий IgE на верхней границе нормы – 54,8 ±8,2 МЕ/мл или повышен незначительно.
Среди пяти выделенных групп общие черты характера сенсибилизации определяются у больных II, III, IV и V групп. Все эти группы объединяет общая расторможенность продукции специфического IgE по отношению ко всем исследованным группам аллергенам. Различаются они только по степени этой расторможенности. II группа объединяет больных с тотальной выраженной гиперпродукцией общего и специфического IgE. III и IV группы характеризуются парциальным типом гиперпродукции специфического IgE, хотя остается пока невыясненным, почему в одном случае идет гиперпродукция IgE к растительным аллергенам, а в другом – к животным аллергенам. V группа больных характеризуется сенсибилизацией к ограниченному числу аллергенов. У больных I группы признаков сенсибилизации не отмечается.
Таким образом, полученные нами результаты позволяют сделать вывод, что у больных с тяжелыми формами атопического дерматита выявляется 2 основных типа продукции общего и специфических IgE и соответствующие им 2 основных патогенетических варианта заболевания – нормоергический (83 ребенка I группы – 26,1%) и гиперергический (235 детей II, III, IV и V групп – 73,9%), что в целом совпадает с имеющимися литературными данными и нашими многолетними наблюдениями.
Нормоергический патогенентический вариант АД характеризуется нормальным уровнем общего IgE и отсутствуем сенсибилизации к различным
