
- •Синтез высокомолекулярных соединений
- •Задачи синтеза полимеров
- •Классификация процессов синтеза полимеров
- •Полимеризационно-деполимеризационное равновесие
- •Термодинамика полимеризации
- •Энтальпия полимеризации H
- •Связь температуры с равновесной концентрацией мономера
- •Фотохимическое инициирование
- •Ингибиторы радикальной полимеризации
- •Ингибиторы радикальной полимеризации
Синтез высокомолекулярных соединений
Полимеризация – химический процесс получения высокомолекулярных соединений (полимеров) из определенных низкомолекулярных веществ (мономеров).
1
Задачи синтеза полимеров
Получение макромолекул заданного химического состава и структуры;
Регулирование скорости химической реакции;
Регулирование средней молекулярной массы и характера ММР;
Получение макромолекул заданной конфигурации.
2
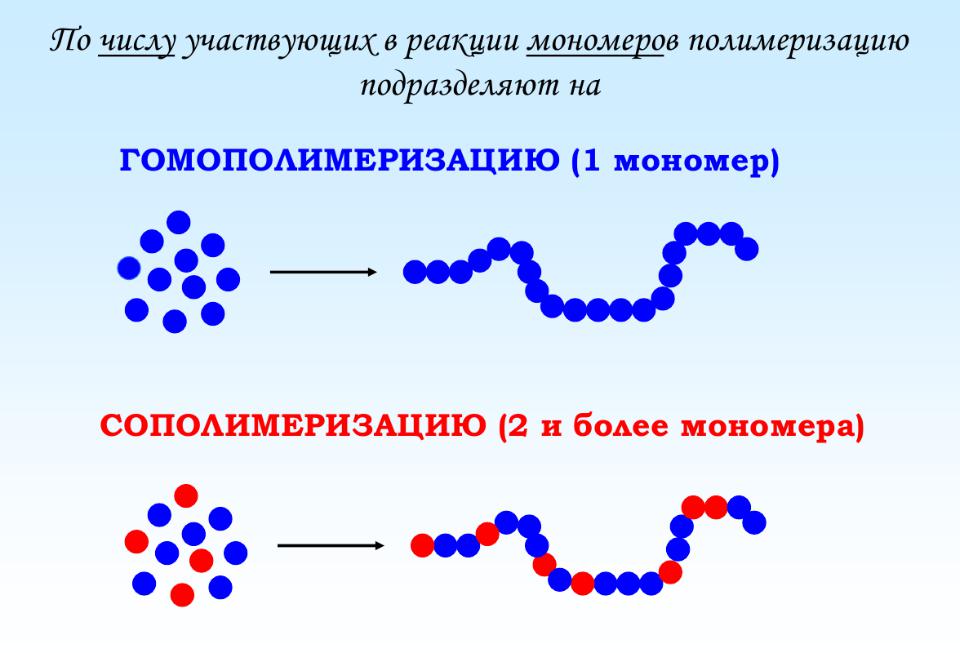
Классификация процессов синтеза полимеров
Цепная полимеризация – это процесс получения высокомолекулярных соединений, при котором рост молекулярной цепи происходит в результате последовательного присоединения молекул мономера к активному центру, локализованному на ее конце
Поликонденсация (ступенчатый синтез) Процесс, при котором рост цепи происходит в результате химического взаимодействия функциональных групп как мономеров, так и промежуточных продуктов реакции. При этом наряду с образованием макромолекул может выделяться низкомолекулярный продукт
3
4


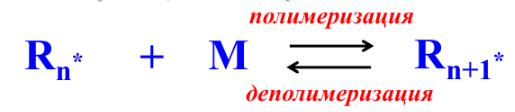
Полимеризационно-деполимеризационное равновесие
Основной стадией, определяющей длину полимерной цепи в ПОЛИМЕРИЗАЦИИ, является реакция роста
цепи. I-(M)n-M* + M → I-(M)n+1-M*
Эта реакция обратима.
Если равновесие установилось, то его называют полимеризационно-
деполимеризационным равновесием
7
Термодинамика полимеризации
G = H –T S
Процесс протекает самопроизвольно при условии G <0
Процесс невозможен при условии G > 0
Система находится в равновесии при условииG =0
8

Энтальпия полимеризации H
Полимеризация по кратным связям
Происходит разрыв 1 двойной связи и образование 1 одинарной связи (в пересчёте на мономерное звено).
Внутренняя энергия двойной связи ( - связь) выше, чем одинарной ( -связь).
Так как при полимеризации энергия системы понижается, избыточная энергия выделяется в виде теплоты, поэтому энтальпия процесса полимеризации отрицательна.
H определяется природой заместителей при кратной связи
Полимеризация с раскрытием цикла
Изменение энтальпии определяется ТОЛЬКО напряженностью цикла: разностью энергий цикла и линейной структуры и мало зависит от природы заместителей в цикле


11

