
7 семестр / Ферменты-2
.pdf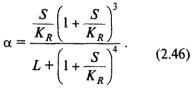
182
существовании конформеров фермента, обладающих разными свойствами в зависимости от наличия или отсутствия молекулы субстрата на связывающем центре. Важно подчеркнуть, что сигмоидальность появляется, если в системе имеется несколько центров связывания, приводящих к образованию комплексов E(S) .
Аллостерические эффекты имеют большое регуляторное значение [Ньюсхолм, Старт, 1977]*. Наличие сигмоидальной зависимости делает систему существенно более чувствительной к изменению концентрации субстрата. Проиллюстрируем это вслед за Ньюсхолмом и Стартом численным расчетом. Если предположить, что субстрат связывается лишь с формой Е, т. е. значения КT очень велики и в сумме членами S/KT можно пренебречь по сравнению с единицей, уравнение (2.43) редуцируется в форму
В этих условиях изменение концентрации субстрата, необходимое для увеличения степени насыщения, зависит от величины аллостерической константы. В табл. 2.4 приведены расчетные данные по изменению концентрации субстрата, обеспечивающей степень насыщения 0,1 и 0,9 и относительные изменения концентраций, необходимые для увеличения степени насыщения от 0,1 до 0,9. Видно, что для простой гиперболической зависимости, полученной из уравнения Михаэлиса (L = 0), для изменения степени насыщения от 0,1 до 0,9 необходимо в 80 раз изменить концентрацию субстрата. С другой стороны, в случае аллостерического механизма с аллостерической константой 104 это изменение достигается увеличением концентрации в 4 раза.
Таким образом, регуляторное значение сигмоидальности заключается в повышении чувствительности системы к концентрации субстрата и сведении к минимуму изменений концентраций, необходимых для существенного повышения или понижения активности фермента.
Кинетическая теория аллостерических взаимодействий получила большое развитие благодаря работам Б. И. Курганова. Помимо эффектов взаимодействия центров на одной молекуле белка сигмоидальная кинетика может наблюдаться и для диссоциирующих ферментных систем (Курганов Б.И. Аллостерические ферменты. Μ., 1978).
Зависимость скорости ферментативной реакции от температуры
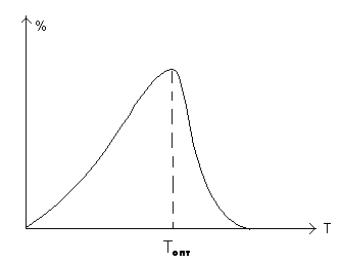
В пределах физиологических условий зависимость скорости реакции от температуры подчиняется законам химической кинетики, т.е. описывается уравнением Аррениуса. Так при увеличении температуры тела с 360С до 390С скорость биохимических процессов в организме увеличивается в 1,2 – 1,4 раза.
183
Выше определенной температуры начинается тепловая денатурация белковых молекул, в том числе и ферментов, которые при этом теряют свою биологическую активность.
Зависимость скорости ферментативной реакции от рН
Большинство ферментов характерным образом изменяют свою активность в зависимости от рН. Оптимальной активности соответствует определенная область рН, причем уменьшение и увеличение рН приводит к снижению активности. Для различных реакций значения оптимума рН колеблются в широких пределах от сильно кислой среды (например, для пепсина) до сильно щелочной (например, для щелочной фосфотазы). Поэтому для работы с ферментами необходимо поддерживать рН с помощью соответствующего буфера.
Зависимость ферментативной активности от рН определяется значением рК ионогенных групп белковой молекулы, особенно тех, которые находятся в активном центре молекулы или вблизи него (и, возможно, играют роль в связывании кофермента), а также групп, ответственных за изменение состояния активного центра путем конформационных изменений белковой молекулы. Кроме того, рН может влиять на степень ионизации или пространственную организацию субстрата.
Влияние активаторов и ингибиторов на активность ферментов
Активаторы - это молекулы или ионы, которые увеличивают
активность ферментов. Часто в качестве активаторов выступают ионы металлов (Mn2+, Mg2+, Zn2+, Co2+, K+) и хлорид-ион (Cl-). Механизм
активации ферментов под действием этих ионов может быть разным: ионы являются коферментами и входят в состав активного центра; облегчают образование ES;
облегчают присоединение кофермента к апоферменту;
184
обеспечивают образование устойчивой четвертичной структуры белков.
Ингибиторы - это молекулы или ионы, снижающие активность ферментов.
Различают два больших класса ингибиторов ферментативной активности - на основании того, ослабляется (конкурентное ингибирование) или не ослабляется (неконкурентное ингибирование) их ингибирующее действие при повышении концентрации субстрата.
Другой способ классификации ингибиторов основывается на характере места их связывания с ферментом в том же месте, что и субстрат (в активном центре), а другие - на значительном расстоянии от активного центра.
Обратимое конкурентное ингибирование аналогами субстрата
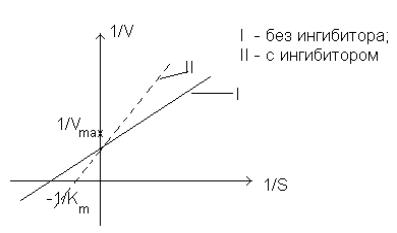
Химическая структура ингибитора (I) сходна со структурой субстрата, поэтому связывание ингибитора с ферментом происходит в активном центре фермента с образованием комплекса E-I. Этот комплекс может диссоциировать. Когда в реакционной смеси одновременно присутствуют и субстрат, и ингибитор, то они конкурируют за один и тот
же связывающий центр. При увеличении концентрации субстрата происходит вытеснение ингибитора из активного центра фермента. Таким образом, максимальная скорость ферментативной реакции в этом случае не меняется, а константа Михаэлиса (Км) уменьшается.
Примером такого ингибирования может быть ингибирование сукцинатдегидрогеназы малонатом.
|
|
|
185 |
|
|
COOH |
|
COOH |
|
|
|
|
|
|
CH2 |
-2H |
CH |
||
|
|
|
|
|
|
CH2 |
|
|
|
|
сукцинатдегидрогеназа |
HC |
||
COOH |
|
|
||
|
|
|
||
|
COOH |
|||
сукцинат |
|
фумарат |
||
Малонат (HOOC-(CH2)2-COOH) способен связываться с дегидрогеназой, образуя комплекс E-I, но отщепление атомов водорода от малоната не происходит.
Многие лекарственные препараты, широко применяемые в клинике, действуют как конкурентные ингибиторы очень важных ферментов.
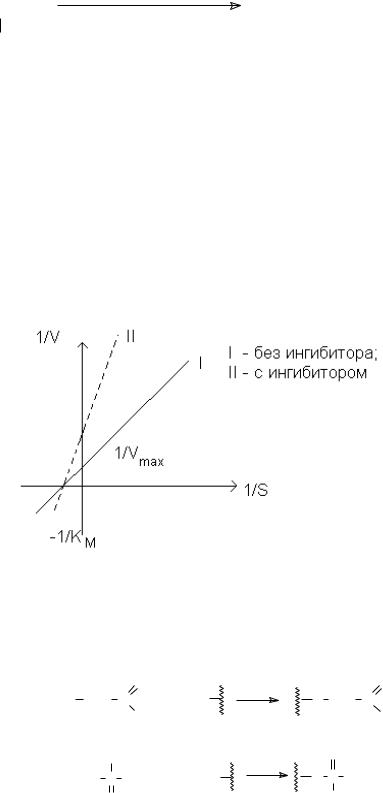
Обратимое неконкурентное ингибирование
В этом случае конкуренция между субстратом и ингибитором отсутствует. При этом ингибитор ничем не напоминает субстрат и связывается не с активным центром фермента. Обратимые неконкурентные ингибиторы понижают максимальную скорость, но не влияют на KM.
Необратимое ингибирование
Ферментативная активность может уменьшаться в присутствии многих "ядов", таких как иодацетамид, диизопропилфторфосфат (нервнопаралитический яд), ионы тяжелых металлов (Ag+, Hg2+), окисляющие
O |
|
I CH2 C |
+ HS |
NH2 |
|
иодацетамид |
цистеин |
F |
|
(CH3)2CH P CH(CH3)2 + HO
O
диизопропилфторфосфат серин
агенты и т.д.
|
O |
S CH2 C |
+ HI |
|
NH2 |
O
OP CH(CH3)2 + HF CH(CH3)2
Многие инсектициды действуют по такому механизму.
