
7 семестр / ЦЛК
.pdf225
Лекция. Цикл лимонной кислоты. Микросомальное окисление
1.Последовательность реакций.
2.Связь общего пути катаболизма с митохондриальной цепью переноса электронов.
3.Регуляция общего пути катаболизма.
4.Ксенобиотики. Фазы метаболизма ксенобиотиков.
5.Микросомальное окисление веществ.
Общая характеристика и значение цикла лимонной кислоты
Цикл лимонной кислоты представляет собой замкнутый процесс, состоящий из серии отдельных реакций. Оксалоацетат (щавелевоуксусная кислота) является одним из исходных субстратов и одновременно конечным продуктом этого цикла. Вторым субстратом служит ацетил-КоА. В серии реакций, протекающих в митохондриях, включающих дегидрирование, гидратацию, дегидратацию и окислительное декарбоксилирование осуществляется метаболизм ацетильных групп и высвобождение восстановительных эквивалентов (НАДН Н+ и ФАДН2), которые затем окисляются в цепи переноса электронов и дают энергию на синтез АТФ. В этом заключается энергетическая роль цикла лимонной кислоты.
Ацетильные группы находятся в составе ацетил-КоА. В результате реакций ЦЛК атомы углерода ацетильных групп окисляются до СО2. Таким образом, главная функция ЦЛК состоит в том, что он является общим конечным путем окисления углеводов, липидов и белков. В этом заключается
катаболическая роль ЦЛК.
ЦЛК играет также важную роль в процессах глюконеогенеза, переаминирования, дезаминирования аминокислот, липогенеза. Эти метаболические пути берут начало от метаболитов ЦЛК. Например, исходным соединением в синтезе порфиринов является сукцинил-КоА (промежуточный продукт ЦЛК). Оксалоацетат и -кетоглутарат - предшественники многих аминокислот. Таким образом, ЦЛК играет и
анаболическую роль.
О жизненно важной роли ЦЛК говорит тот факт, что у человека неизвестны генетически обусловленные изменения ферментов ЦЛК; вероятно наличие таких нарушений несовместимо с нормальным развитием.
Реакции цикла лимонной кислоты
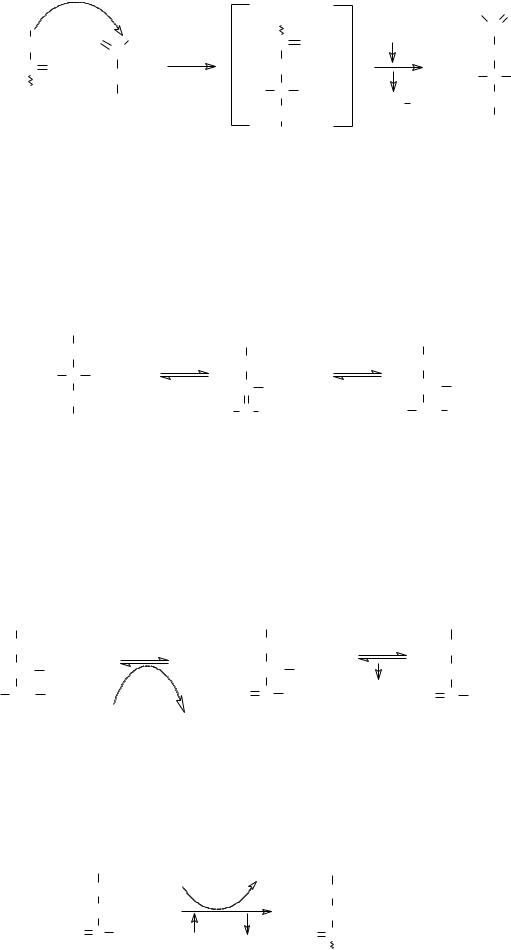
Реакции ЦЛК протекают в матриксе митохондрий.
|
|
|
|
|
|
226 |
|
|
|
|
|
|
H |
|
|
|
|
SKoA |
|
HO |
O |
||
|
|
|
- |
|
|
H O |
C |
||||
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|||
1) |
CH |
|
O |
COO |
E1 |
C |
O |
|
2 |
|
|
|
C |
|
|
CH |
|||||||
|
2 |
|
|
|
|
|
|
|
|||
|
C O |
+ |
|
|
|
CH |
|
|
|
2 |
|
|
|
|
|
|
|
|
- |
||||
|
|
|
CH |
|
|
2 |
|
|
HO C COO |
||
|
|
|
|
|
|
|
|
- |
|||
|
SKoA |
|
|
2 |
|
HO C |
|
|
|
|
|
|
|
|
- |
|
COO |
|
CH |
||||
|
|
|
|
COO |
|
|
|
|
|
KoA SH |
|
|
|
|
|
|
CH |
|
|
2 |
|||
|
|
|
|
|
|
|
|
|
- |
||
|
|
|
|
|
|
|
2 |
- |
|
|
COO |
ацетил-КоА |
|
оксалоацетат |
COO |
|
цитрат |
||||||
|
цитрил-КоА |
|
(лимонная кислота) |
||||||||
|
Е1 - цитратсинтаза, является регуляторным. Цитратсинтазная |
||||||||||
реакция лимитирует скорость всего процесса. |
|
|
|||||||||
|
Превращение |
цитрата |
в |
|
|
изоцитрат |
катализирует |
||||
аконитатгидратаза (Е2), содержащая ионы Fe2+. Эта реакция осуществляется в две стадии: сначала происходит дегидратация с
образованием цис-аконитата, |
а |
затем |
гидратация с образованием |
|||||
2) |
COOH |
|
|
COOH |
|
|
COOH |
|
|
CH |
|
|
|
|
|||
|
E |
|
|
|
E |
|
|
|
|
2 |
2 |
CH |
|
2 |
CH |
||
|
- |
|
|
|
||||
|
|
|
2 |
|
|
2 |
||
|
HO C COO |
|
|
C |
- |
|
|
- |
|
CH |
|
|
COO |
|
|
CH COO |
|
|
|
|
|
- |
|
|
- |
|
|
2 |
|
|
|
|
|
||
|
- |
|
H C COO |
|
|
HO CH COO |
||
|
COO |
|
|
|
|
|
|
|
|
цитрат |
|
цис-аконитат |
|
|
изоцитрат |
||
|
|
|
|
|
|
|
|
|
изоцитрата.
Реакция ингибируется фторацетатом, в результате накапливается
цитрат.
Далее изоцитратдегидрогеназа (Е3) катализирует дегидрирование с образованием оксалосукцината, а затем следует декарбоксилирование под действием того же фермента.
3) COOH |
|
|
COOH |
E3 |
COO- |
CH |
|
E3 |
CH2 |
CH |
|
2 |
|
|
CH COO- |
|
2 |
CH COO- |
|
|
|
CH2 |
|
HO CH COO- |
|
|
O C COO- |
CO2 O C COO- |
|
изоцитрат |
НАД+ |
НАДН Н+ |
оксалосукцинат |
|
2-оксогутарат |
|
|
|
( -кетоглутарат) |
||
|
|
|
|
|
|
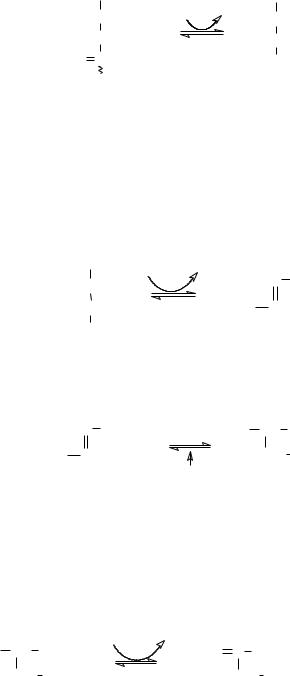
-Кетоглутарат подвергается окислительному декарбоксилированию, сходному с окислительным декарбоксилированием пирувата.
Эта реакция катализируется -кетоглутаратным комплексом (Е4)
4) COO- |
|
E4 |
|
COO- |
НАД |
+ |
НАДН |
||
|
|
|
||
CH2 |
|
|
|
CH |
|
|
|
|
2 |
CH2 |
|
|
|
CH |
O C COO- |
|
|
|
2 |
KoASH |
CO2 |
O C |
||
|
SKoA |
|||
|
|
|
|
|
2-оксогутарат |
сукцинил-КоА |
|
( -кетоглутарат) |
||
|
227
требует такого же набора кофакторов: тиаминдифосфата, липамида, НАД+,
ФАД, КоА-SH. Ферменты комплекса: -кетоглутаратдегидрогеназа,
дигидролипоилсукцинилтрансфераза, дигидролипоилдегидрогеназа.
Первый фермент данного комплекса не имеет такой сложной регуляции как пируватдегидрогеназа. В результате образуется сукцинил-КоА, содержащий макроэргическую связь. Реакция ингибируется арсенатом, что приводит к накоплению -кетоглутарата.
Под действием фермента сукцинаттиокиназы (сукцинил-КоА-
синтетатазы) энергия макроэргической связи сукцинил-КоА расходуется на образование макроэргической связи в молекуле ГТФ (субстратное фосфорилирование).
|
- |
|
|
|
- |
5) |
COO |
|
|
|
|
ГДФ + Ф |
ГТФ |
COO |
|||
|
CH |
|
н |
|
|
|
|
|
|
CH |
|
|
2 |
|
|
|
|
|
|
|
|
|
2 |
|
CH |
|
|
|
CH |
|
2 |
|
|
|
|
|
|
E |
|
|
2 |
O |
C |
5 |
|
- |
|
|
|
COO |
|||
|
SKoA |
|
|
|
сукцинат |
сукцинил-КоА |
|
(янтарная кислота) |
|||
Далее сукцинат под действием сукцинатдегидрогеназы (Е6)
превращается в фумарат. Это единственная реакция ЦЛК, в ходе которой осуществляется прямой перенос атомов водорода с субстрата на флавопротеин ЦПЭ без участия НАД+. Коферментов данного фермента
является ФАД. |
|
|
|
|
Затем к фумарату присоединяется |
молекула H2O под действием |
|||
6) |
- ФАД |
ФАДН |
|
|
|
COO |
|
2 |
- |
|
CH |
|
|
HC COO |
|
2 |
|
|
|
|
CH |
|
- |
CH |
|
E |
OOC |
||
|
2 |
|
|
|
|
- |
6 |
|
|
|
COO |
|
|
|
|
сукцинат |
|
фумарат |
|
(янтарная кислота) |
(фумаровая кислота) |
|||
фумаратгидратазы (Е7) с образованием малата. |
||||
7) |
- |
E7 |
HO |
- |
HC COO |
CH COO |
|||
- |
CH |
|
|
- |
OOC |
|
|
CH COO |
|
|
|
|
|
2 |
фумарат |
H O |
|
L-малат |
|
|
|
2 |
(яблочная кислота) |
|
(фумаровая кислота) |
|
|||
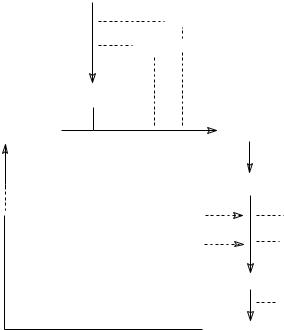
Малатдегидрогеназа (Е8) катализирует превращение малата в оксалоацетат, реакция идет с участием НАД+. Хотя реакция обратима, реально она протекает в направлении образования оксалоацетата, поскольку он вместе с НАДН постоянно потребляется в других реакциях.
8) |
НАД+ |
НАДН Н+ |
|
HO CH COO- |
|
O C COO- |
|
|
|
||
|
CH2 COO- |
E8 |
CH COO- |
|
|
2 |
L-малат |
оксалоацетат |
|
(щавелевоуксусная кислота) |
||
(яблочная кислота) |
||
|
228
Регуляция общего пути катаболизма
Скорость дыхания и фосфорилирования в митохондриях зависит от концентрации АДФ и, в конечном счете, определяется скоростью расходования АТФ (дыхательный контроль - состояние 4). В свою очередь скорость реакций общего пути катаболизма, поставляющего водород в митохондрии, зависит от скорости дыхания митохондрий и окислительного фосфорилирования. Один из механизмов этой зависимости связан с необходимостью регенерации НАД+, которая происходит в результате передачи водорода с НАДН Н+ в дыхательную цепь митохондрий. Кроме того, существует регуляция по принципу отрицательной обратной связи, с участием аллостерических ферментов. НАДН Н+ ингибирует некоторые ферменты общего пути катаболизма.
При снижении дыхания митохондрий расходуется меньше НАДН, его
Пируват
хАТФ
хНАДН 
|
Ацетил-КоА |
|
|
|
Оксалоацетат |
х |
х |
Цитрат |
|
|
|
|
Изоцитрат |
|
|
|
АДФ |
х |
АТФ |
|
|
АМФ |
х |
НАДН |
|
|
|
|
|
|
|
2-Оксоглутарат |
||
|
|
|
х |
НАДН |
|
|
|
Сукцинил-КоА |
|
концентрация увеличивается и приводит к замедлению реакций общего пути катаболизма в результате ингибирования указанных реакций.
Ряд реакций общего пути катаболизма зависит от концентрации адениловых нуклеотидов - АТФ, АДФ и АМФ.
Суммарная концентрация адениловых нуклеотидов в клетке постоянна, но относительные концентрации могут изменяться вследствие их взаимопревращений. Во многих клетках концентрации АТФ, АДФ и АМФ относятся как 100:10:1. Отсюда следует, что небольшие изменения концентрации АТФ могут приводить к значительным изменениям концентрации других нуклеотидов. Например, если 1/10 часть всей АТФ превратится в АДФ, то концентрация АДФ увеличится в 2 раза. Это имеет существенное значение, поскольку изменения активности аллостерических ферментов зависят от величины изменения концентрации модификаторов.

229
Для оценки влияния система адениловых нуклеотидов на метаболические процессы пользуются величиной энергетического заряда
клетки:
[ АТФ] 1 |
2 |
[ АДФ] |
Энергетиче ский заряд |
|
|
|
|
|
[ АТФ] [ АДФ] [ АМФ] |
||
Если весь фонд адениловых нуклеотидов представлен только АТФ, то энергетический заряд равен 1. Если в клетке имеется только АМФ, то энергетический заряд равен 0. В большинстве клеток энергетический заряд равен 0,8 - 0,9. При уменьшении клеточного заряда (уменьшении [АТФ], увеличении [АДФ], [АМФ]) скорость реакций общего пути катаболизма увеличивается. В скелетных мышцах энергетический заряд равен 0,94 как в покое, так и при интенсивной мышечной работе.
Кроме нуклеотидных коферментов на активность регуляторных ферментов общего пути катаболизма влияют некоторые метаболиты, действующие как аллостерические модификаторы. Чаще всего встречается регуляция по принципу обратной связи продуктами реакции. В таблице приведены некоторые ингибиторы и активаторы этих ферментов.
Таблица. Регуляторные ферменты общего пути катаболизма.
№ |
Регуляторные ферменты |
Ингибиторы |
Активаторы |
|
1. |
Пируватдегидрогеназный |
АТФ, |
НАДН, |
|
|
комплекс |
ацетил-КоА |
|
|
2. |
Цитратсинтаза |
АТФ, |
НАДН, |
|
|
|
сукцинил-КоА, |
|
|
|
|
ацил-КоА, |
|
|
|
|
цитрат |
|
|
3. |
Изоцитратдегидрогеназа |
АТФ, НАДН |
АДФ, АМФ |
|
4. |
- |
НАДН, |
|
|
|
Кетоглутаратдегидрогеназн |
сукцинил-КоА |
|
|
|
ый комплекс |
|
|
|
Механизмы обезвреживания ксенобиотиков в организме
Ксенобиотики – это чужеродные соединения, попадающие в организм.
Микросомальное окисление
R H + O2 + НАДФН Н+  R OH + H2O + НАДФ+
R OH + H2O + НАДФ+
В мембранах гладкого эндоплазматического ретикулума и митохонлриальной мембране некоторых органов (печени, коры надпочечников) функционирует система, которая катализирует гидроксилирование большого числа субстратов (биологически активных соединений, ксенобиотиков). В этих реакциях используется молекулярный кислород. Один атом кислорода встраивается в субстрат, другой, восстанавливается с помощью НАДФH с образованием молекулы воды. Такие процессы называются
230
монооксигенированием, а ферментные комплексы, катализирующие их –
монооксигеназами.
Эта окислительная система включает два белковых компонента: цитохром Р-450 и НАДФН-цитохром Р-450-редуктазу. Цитохром Р-450 является гемопротеином и присоединяет кислород к субстрату, а редуктаза переносит на этот комплекс электроны и ионы H+, восстанавливая его. Цитохром Р-450 катализирует гидроксилирование жирных кислот, стероидных гормонов и большинства ксенобиотиков. Гидроксилирование ксенобиотиков протекает в печени.
Обезвреживание ксенобиотиков в организме
Катаболизм ксенобиотиков можно разделить на две фазы:
Химическая модификация – ферментативный процесс изменения структуры ксенобиотиков, при котором происходит разрыв связив молекуле или встраивание дополнительных функциональных групп. В результате такой модификации повышается растворимость ксенобиотиков.
Фаза коньюгации – образование связей между модифицированными ксенобиотиками и специальными молекулами организма. Образовавшийся комплекс легче выводится из организма.
Ксенобиотики моут подвергаться целому ряду модификаций: окислению, циклизации, гидролизу и т.д.). Например, ароматические соединения гидроксилируются в печени под действием монооксигеназ, коньюгируют с гликуроновой кислотой, после чего выводятся из организма.
Другие антибиотики накапливаются в организме. К ним относятся вещества, способные прочно связываться с макромолекулами клеток (белками, липидными структурами). Например, хлорорганические соединения (хлороформ) хорошо растворимы в липидах, и плохо подвергаются модификации. В результате они накапливаются в тканях, богатых липидами. Ионы тяжелых металлов связываются с сульфгидрильными группами белков и также накапливаются в организме.
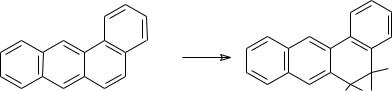
Некоторые антибиотики в результате модификации превращаются в боле токсичные вещества по сравнению с исходными. Например, при окислении бензопирена (компонента угольной пыли и асфальта) образуются канцерогены.
Другим примером ксенобиотиков является ДДТ (дуст). В организме он может медленно
|
H |
|
H O |
бензопирен |
окисленный бензопирен - |
|
очень реакционно способное |
|
соединение |
превращаться в различные производные, которые очень токсичны. В частности, они ингибируют синтез гормонов коры надпочечников и приводят к атрофии надпочечников. Выделение ДДТ и его производным происходит очень медленно, т.к. эти вещества накапливаются в липидных тканях
