
7 семестр / Обмен углеводлв-лекция 1
.pdf
231
Лекция № 27. Обмен углеводов. Катаболизм. Пентозофосфатный путь
1.Анаэробный и аэробный гликолиз. Энергетика гликолиза.
2.Спиртовое и молочнокислое брожение. Глиоксилатный цикл.
3.Пентозофосфатный путь. Синтез НАДФН и рибозы. Значение процесса в жировой ткани, печени, эритроцитах.
Основные функции углеводов в организме:
1.Энергетическая. За счет окисления углеводов удовлетворяется более половины (55%) всей потребности человека в энергии, Глюкоза служит единственным или основным источником энергии для нервной ткани (в том числе мозга), почек, семенников, эритроцитов и всех тканей эмбриона.
2.Входят в состав структурно-функциональных компонентов клеток и межклеточного вещества. В виде гликозаминогликанов углеводы входят в состав межклеточного вещества. Пентозы используются для синтеза нуклеотидов и нуклеиновых кислот. Большое число белков являются гликопротеинами и т.д.
3.Из углеводов в организме могут синтезироваться соединения других классов, в частности липиды и заменимые аминокислоты.
Наиболее распространенный углевод млекопитающих – глюкоза. Она играет роль связующего звена между энергетическими и пластическими функциями углеводов, поскольку из глюкозы могут образоваться все другие моносахариды, и наоборот – разные моносахариды могут превращаться в глюкозу.
Общая схема метаболизма глюкозы
Углеводы пищи |
|
Аминокислоты, |
|
|
|
|
глицерин |
|
|
глюконео- |
|
|
|
генез |
|
Гликоген |
Глюкоза |
CO2 + H2O + энергия |
|
Пентозы |
Другие |
Аминокислоты Липиды |
|
|
моноса- (заменимые) |
||
|
хариды |
|
|
Нуклеотиды Гетерополисахариды
Источником углеводов организма служат углеводы пищи – главным образом крахмал (хлеб и хлебобулочные изделия, макароны и макаронные
232
изделия, картофель, крупы и т.д.), а также сахароза (сахар, варенья и т.д.) и лактоза (в составе молока). Кроме того, глюкоза может образовываться в организме из аминокислот, а также глицерина, входящего в состав жиров.
Переваривание углеводов
Углеводы пищи в пищеварительном тракте распадаются на мономеры при действии гликозидаз – ферментов, катализирующих гидролиз гликозидных связей.
Переваривание крахмала начинается уже в ротовой полости: в слюне содержится фермент α-амилаза, расщепляющий α-1,4-гликозидные связи. Поскольку пища в ротовой полости находится недолго, то крахмал здесь переваривается лишь частично.
Основным местом переваривания крахмала служит тонкий кишечник, куда поступает панкреатическая амилаза. Амилаза не гидролизует гликозидную связь в дисахаридах, поэтому основным продуктом действия панкреатической амилазы является дисахарид мальтоза. Из глюкозных остатков, которые в молекуле крахмала соединены α-1,6-гликозидной связью, образуется дисахарид изомальтоза. Помимо этого, с пищей в организм поступают дисахариды сахароза и лактоза.
Мальтоза, изомальтоза, сахароза и лактоза гидролизуются специфическими гликозидазами – соответственно, мальтазой, изомальтазой, сахаразой и лактазой:
Мальтоза + Н2О → глюкоза + глюкоза Изомальтоза + Н2О → глюкоза + глюкоза Сахароза + Н2О → глюкоза + фруктоза Лактоза + Н2О → глюкоза + галактоза
Дисахаридазы синтезируются в клетках кишечника, однако в просвет кишечника не выделяются, а катализируют реакции гидролитического расщепления субстратов на поверхности клеток, т.е. имеет место пристеночное пищеварение.
Продукты полного переваривания углеводов – глюкоза, фруктоза и галактоза – через клетки кишечника поступают в кровь.
Трансмембранный перенос глюкозы
Поступление глюкозы из крови в клетки происходит путем облегченной диффузии при участии специальных белков-переносчиков. Следовательно, скорость трансмембранного переноса глюкозы зависит только от градиента ее концентрации и количества белков-транспортеров. Исключением являются клетки мышц и жировой ткани, в которых белкитранспортеры (ГЛЮТ-4) являются инсулин-зависимыми. В отсутствие
233
инсулина плазматическая мембрана этих клеток становится непроницаемой для глюкозы.
Катаболизм глюкозы. Аэробный и анаэробный гликолиз.
Термин “гликолиз” происходит от греческих слов glykys – сладкий и lysis – распад, разложение. Гликолиз – процесс окисления глюкозы, в результате которого происходит расщепление глюкозы с образованием 2 молекул пирувата (аэробный гликолиз) или 2 молекул лактата (анаэробный гликолиз).
Химизм процесса
Гликолиз условно можно разделить на две стадии. Первые пять реакций составляют подготовительную стадию гликолиза.
И аэробный, и анаэробный гликолиз начинаются с фосфорилирования глюкозы.
В большинстве тканей реакцию фосфорилирования глюкозы катализируют изоферменты гексокиназы (ГК), в паренхиматозных клетках печени эту реакцию катализирует глюкокиназа (ГлК).
I этап гликолиза: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
6 |
|
|
|
|
|
|
|
|
|
|
|
|
- |
|
|
|
|
|
|
CH OH |
|
|
|
|
|
|
|
CH OPO |
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
2 |
|
|
|
|
|
|
|
|
|
2 |
|
3 |
|
|
|
|
|
|
|
|
|
O |
|
|
|
E1 |
|
|
|
|
|
O |
|
|
|
E |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
OH |
|
|
|
|
|
|
|
|
|
OH |
|
|
|
OH |
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
HO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
АДФ + Ф |
АТФ |
|
|
|
OH |
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
6 |
глюкоза |
|
|
|
|
|
|
глюкозо-6-фосфат |
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
- |
|
|
|
|
|
|
|
CH OPO |
- |
|
1 |
|
|
|
|
|
CH OPO |
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
2 |
3 |
|
|
|
|
|
|
|
2 |
3 |
|
|
|
|
|
|
|||
|
O |
|
CH OH |
|
E |
|
|
|
O |
|
|
|
CH OPO |
- |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
2 |
|
|
3 |
|
|
|
|
|
|
2 |
|
3 |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
OH |
|
|
АТФ |
АДФ + Ф |
|
|
OH |
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
фруктозо-6-фосфат |
|
|
|
|
|
|
фруктозо-1,6-дифосфат |
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
E |
|
|
|
|
|
|
|
|
|
|
O |
|
E |
|
|
|
|
|
|
4 |
|
|
O |
|
|
|
|
|
|
C |
|
5 |
|
CH |
OPO |
- |
|
|
|
C |
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
H |
|
|
|
|
2 |
3 |
|
|
|
H |
|
|
||||
|
HO C |
|
|
|
|
C O |
|
|
|
|
HO C |
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
CH OPO |
- |
|
|
CH OH |
|
|
|
|
CH OPO |
- |
||||||
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|||||||
|
|
|
|
2 |
3 |
|
дигидроксиацетон- |
|
|
|
|
2 |
|
3 |
|||||
глицеральдегид-3-фосфат |
|
|
глицеральдегид-3-фосфат |
||||||||||||||||
|
|
|
|
|
|
|
|
фосфат |
|
|
|
|
|
|
|
|
|
|
|
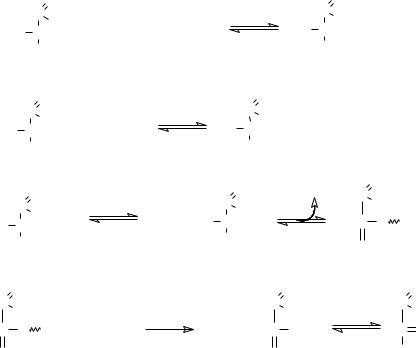
Е1 - гексокиназа или глюкокиназа. Особенности ГК: 1) обладает групповой специфичностью, т.к. катализирует фосфорилирование не только глюкозы, но и других гексоз (фруктозы, маннозы), 2) имеет высокое сродство к глюкозе (Км < 0,1 мМ), поэтому катализирует реакцию с максимальной скоростью при низкой концентрации глюкозы в крови, 3) резко ингибируется глюкозо-6-фосфатом. Особенности ГлК: 1) обладает стереохимической специфичностью, т.к. катализирует фосфорилирование только глюкозы, 2)
234
имеет низкое сродство к глюкозе (Км ≈ 10 мМ), поэтому катализирует реакцию только при высокой концентрации глюкозы в крови, 3) не ингибируется глюкозо-6-фосфатом.
Образовавшийся в результате 1-ой реакции глюкозо-6-фосфат в отличие от глюкозы не способен проходить через клеточные мембраны (они не проницаемы для заряженных молекул). Таким образом, в результате фосфорилирования глюкоза “запирается” в клетке.
Е2 - глюкозофосфатизомераза Е3 - фосфофруктокиназа
Е4 - фруктозодифосфатальдолаза Е5 – триозофосфатизомераза
Этой реакцией завершается подготовительная стадия гликолиза. В ходе этой стадии на активацию молекулы глюкозы и подготовку к расщеплению на два трехуглеродных фрагмента затрачивается 2 молекулы АТФ:
Глюкоза + 2 АТФ → 2 глицеральдегид-3-фосфат + 2 АДФ
На второй стадии гликолиза (стадии извлечения энергии), также включающей 5 реакций, происходит превращение глицеральдегид-3-фосфата в пируват с запасанием выделяющейся энергии в форме АТФ.
|
O |
|
|
|
|
|
|
|
C |
O |
|
C |
|
|
|
|
E6 |
|
|
- |
|
||
|
|
|
|
|
|
|
|
||||
HO C H |
|
+ |
НАД+ |
+ H3PO4 |
|
|
|
HO C |
OPO3 |
+ НАДH + 2 H+ |
|
CH OPO |
- |
|
|
|
|
|
CH2OPO3- |
|
|||
|
2 |
3 |
|
|
|
|
|
1,3-дифосфолицерат |
|||
глицеральдегид-3-фосфат |
|
|
|
|
|
||||||
|
O |
|
|
|
|
|
O |
|
|
|
|
C |
|
- |
|
|
E7 |
C |
|
- |
|
|
|
|
|
|
|
|
|
|
|
||||
HO C |
OPO3 |
+ |
АДФ |
HO C |
O |
+ |
АТФ |
|
|||
|
|
|
|
|
|||||||
CH OPO - |
|
|
|
CH2OPO3- |
|
|
|||||
|
2 |
3 |
|
|
|
|
|
|
|
|
|
1,3-дифосфолицерат |
3-фосфолицерат |
|
|
||||||||
O |
|
|
|
|
O |
|
|
H2O |
O |
|
|
|
E |
|
C |
|
|
C O- |
|||||
C |
|
|
8 |
- |
|
|
|
||||
HO C O- |
|
|
-O3PO C |
O |
|
|
E9 |
C O PO3- |
|||
|
|
- |
|
|
CH2OH |
|
CH2 |
|
|||
CH2OPO3 |
|
|
|
|
|
|
|
|
|||
3-фосфолицерат |
|
|
2-фосфолицерат |
|
фосфоенолпируват |
||||||
O |
|
|
|
|
|
|
|
|
O |
|
O |
C O- |
|
|
|
|
E10 |
|
|
C O- |
|
C O- |
|
C O PO - |
+ |
АДФ |
АТФ + |
|
C OH |
|
C O |
||||
|
3 |
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
CH2 |
|
CH3 |
|
фосфоенолпируват |
|
|
|
фосфоенолпируват |
пируват |
||||||
Е6 - глицеральдегид-3-фосфатдегидрогеназа Е7 - фосфоглицераткиназа Е8 - фосфоглицератфосфомутаза Е9 - енолгидратаза
235
Е10 - пируваткиназа
Таким образом, суммарное уравнение 2 этапа гликолиза выглядит следующим образом:
Глицеральдегид-3-фосфат + НАД+ + 2 АДФ + 2 Н3РО4 → пируват + НАДН·Н+ + 2 АТФ
Суммируя уравнения обоих этапов, получаем:
Глюкоза + 2 НАД+ + 2 АДФ + 2 Н3РО4 → 2 пируват + 2 НАДН·Н+ + 2 АТФ
Для непрерывного протекания гликолиза необходимо реокисление НАДН·Н+, образовавшегося в ходе глицеральдегид-3- фосфатдегидрогеназной реакции, до НАД+. В аэробных условиях продуктом гликолиза в животных тканях является пируват, а НАДН·Н+ снова окисляется до НАД+, отдавая свои электроны в дыхательную цепь.
Челночные механизмы
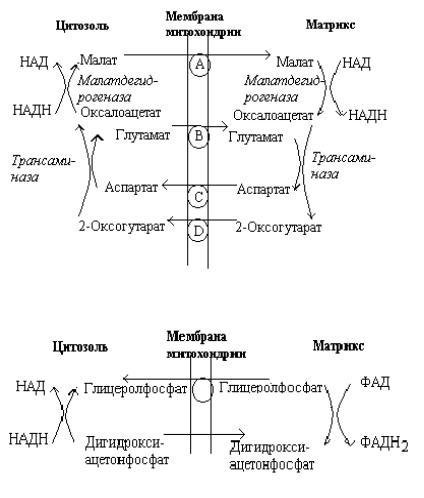
Поскольку ферменты гликолиза локализованы в цитоплазме, то и НАДН·Н+, образовавшийся в ходе глицеральдегид-3-фосфатдегидрогеназной реакции, находится в цитоплазме. Для переноса водорода с цитоплазматического НАДН·Н+ в дыхательную цепь существуют специальные механизмы, называемые челночными: 1) малат-аспартатный – дает на выходе 3 молекулы АТФ, и 2) α-глицеролфосфатный (глицерол-3- фосфатный) – дает на выходе 2 молекулы АТФ.
Рис. Малат-аспартатный челнок
236
Рис. Глицеролфосфатный челнок
Выход АТФ при аэробном распаде глюкозы
Аэробный распад глюкозы не следует путать с аэробным гликолизом. Аэробный распад глюкозы это процесс полного распада глюкозы до СО2 и Н2О. И в этом процессе аэробный гликолиз представляет собой лишь первый этап:
Глюкоза
Глицеральдегид-3-фосфат
Пируват
Ацетил-КоА
СО2 и Н2О
Поскольку в результате подготовительной стадии гликолиза глюкоза окисляется с образованием 2 молекул глицеральдегид-3-фосфата, начиная с глицеральдегид-3-фосфата вводим коэффициент 2.
При окислении 1 мол. ацетил-КоА до СО2 и Н2О (ЦЛК) образуется 3 молекулы НАДН·Н+, молекула ФАДН2 и молекула ГТФ.
При окислении 1 мол. пирувата до ацетил-КоА образуется 1 мол. НАДН·Н+.
При окислении глицеральдегид-3-фосфата до пирувата образуется 2 молекулы АТФ (путем субстратного фосфорилирования) и молекула НАДН·Н+. Наконец, при окислении глюкозы в глицеральдегид-3-фосфат затрачивается 2 молекулы АТФ.
Итого, 38(40) – 2 = 36(38) молекул АТФ в расчете на 1 молекулу глюкозы.
Аэробный распад глюкозы может происходить во всех органах и тканях. В наибольшей зависимости от аэробного распада глюкозы находится мозг. Он расходует около 100 г глюкозы в сутки. В состоянии основного обмена около 20% всего поступающего в организм кислорода потребляется мозгом (при том, что на долю мозга приходится лишь 2% массы тела). Поэтому как недостаток глюкозы, так и недостаток кислорода проявляют себя прежде всего симптомами со стороны ЦНС – головокружением, потерей сознания, судорогами.
Анаэробный гликолиз
237
В анаэробных условиях образовавшийся при гликолизе НАДН·Н+ реокисляется не за счет кислорода (который отсутствует), а за счет пирувата, восстанавливающегося в лактат:
|
|
лактатдегидрогеназа |
|
|
|
|
CH |
|
|
CH |
|
|
|
3 |
|
|
3 |
|
|
|
C O |
+ |
+ |
CH OH |
+ |
НАД |
+ |
НАДН + H |
|
|||||
- |
|
|
- |
|
|
|
COO |
|
|
COO |
|
|
|
пируват |
|
|
лактат |
|
|
|
Лактатдегидрогеназа представляет собой тетрамер, содержащий протомеры двух типов - М (muscle) и Н (heart). Известно 5 изоферментов, различающихся набором протомеров.
Изомерные формы ЛДГ1 и ЛДГ2 обнаруживаются в мозге, сердце, корковом веществе почек, т.е. в тканях с интенсивным снабжением кислородом. Форма ЛДГ3 - в поджелудочной железе, ЛДГ4 и ЛДГ5 в скелетных мышцах, печени, мозговом веществе почек, т.е. в тканях с менее интенсивным снабжением кислородом. Все эти формы ферментов значительно различаются максимальной скоростью реакции и константами Михаэлиса для лактата и пирувата. ЛДГ5 быстро катализирует восстановление пирувата в лактат при низких концентрациях лактата. ЛДГ1 катализирует быстрое окисление лактата в пируват в сердечной мышце.
H |
M |
H |
H M |
H M |
HM |
M |
|
3 |
4 |
||||
4 |
3 |
2 |
2 |
|
|
ЛДГ1 |
ЛДГ2 |
ЛДГ3 |
ЛДГ4 |
ЛДГ5 |
|
Суммарное уравнение анаэробного гликолиза выглядит следующим образом:
Глюкоза + 2 АДФ + 2 H3PO4 2 Лактат + 2 АТФ + 2 Н2О
Т.о. десять ферментов, превращающих глюкозу в пируват, совместно с ЛДГ способны обеспечить синтез АТФ в отсутствие кислорода. В анаэробных условиях АТФ образуется только за счет двух реакций субстратного фосфорилирования. В этих реакциях в расчете на 1 моль глюкозы образуется 4 моль АТФ. После вычитания 2 моль АТФ, потребляемых в подготовительной стадии, получаем чистый выход АТФ при гликолизе – 2 моль АТФ на 1 моль глюкозы.
238
Гликолиз у животных и человека протекает во многих типах клеток, но его значение для разных органов различно. В интенсивно работающих скелетных мышцах аэробный процесс не может обеспечить потребности мышц в энергии. В этих условиях резко усиливается анаэробный путь синтеза АТФ и в мышцах накапливается молочная кислота. Если после ночного сна концентрация лактата в крови составляет 1-2 ммоль/л, то после тяжелой мышечной работы может достигать 20 ммоль/л. Особенно большое значение анаэробный гликолиз имеет при кратковременной интенсивной работе продолжительностью от 30 секунд до 2,5 минут. При более продолжительной интенсивной мышечной работе скорость анаэробного гликолиза довольно быстро уменьшается, а аэробного процесса – возрастает. Через 4-5 минут бега (дистанция 1,5 км) энергия поставляется поровну аэробным и анаэробным процессами, а через 30 минут (10 км) – почти целиком аэробным процессом. В продолжение первой минуты работы благодаря анаэробному процессу достигается гораздо большая мощность, чем при дальнейшей работе. Следует отметить, что при длительной работе в аэробном процессе все в большей мере используется не глюкоза, а жирные кислоты.
Эритроциты вообще не имеют митохондрий, и их потребность в АТФ целиком удовлетворяется за счет анаэробного гликолиза. Интенсивный гликолиз характерен также для клеток злокачественных опухолей.
Пентозофосфатный путь превращений глюкозы
ПФП является альтернативным путем окисления глюкозы. Он не приводит к синтезу АТФ, но поставляет клеткам кофермент НАДФН·Н+, а также обеспечивает клетки рибозой. НАДФН·Н+, использующийся как донор водорода в реакциях восстановления, участвует в реакциях биосинтеза жирных кислот и холестерина, а также в реакциях гидроксилирования, играющих важную роль в функционировании микросомальной цепи обезвреживания чужеродных веществ. Рибоза участвует в синтезе нуклеотидов и нуклеиновых кислот, а также аминокислоты гистидина.
ПФП может функционировать в печени, жировой ткани, молочной железе, коре надпочечников, эритроцитах и органах, где активно протекают восстановительные синтезы, например синтез жирных кислот. Все ферменты ПФП локализованы в цитозоле.
Реакции ПФП
1 реакция: дегидрирование глюкозо-6-фосфата Реакцию катализирует глюкозо-6-фосфатдегидрогеназа, ключевой
фермент пентозофосфатного цикла. Образовавшийся в ходе реакции 6- фосфоглюконолактон - соединение нестабильное, которое спонтанно, либо под действием специфической лактоназы гидролизуется.
2 реакция: гидролиз 6-фосфоглюконолактона с образованием 6- фосфоглюконата. Равновесие суммарной реакции сильно смещено в сторону образования НАДФ·Н+.
239
3 реакция: дегидрирование и декарбоксилирование 6-фосфоглюконата с образованием рибулозо-5-фосфата.
CH OPO |
- |
|
|
|
|
|
CH OPO |
- |
|
||||
|
|
|
|
|
|
|
|
||||||
|
2 |
3 |
|
|
|
|
|
2 |
3 |
|
|||
|
|
|
O |
|
|
|
E1 |
|
|
|
O |
|
E2 |
|
|
|
|
|
|
|
|
|
|
|
O |
||
OH |
|
|
|
|
|
|
|
OH |
|
H O |
|||
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|
|
2 |
|
|
|
|
|
|
НАДФ |
НАДФН |
|
|
|
|
|||
|
|
|
OH |
|
|
OH |
|
||||||
|
|
|
|
|
|
|
|
|
|
||||
глюкозо-6-фосфат |
|
|
|
6-фосфоглюконолактон |
|
||||||||
|
|
|
|
|
|
|
|
|
|
||||
|
E |
|
|
|
|
CH OH |
|
|
|
|
|
||
|
3 |
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C O |
|
+ |
CO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
H |
C OH |
|
2 |
|
|
|
||
|
+ |
|
|
|
|
|
|
|
|
||||
НАДФ |
|
НАДФН |
H C OH |
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
CH OPO H |
|
|
|
|
|||
|
|
|
|
|
|
|
2 |
3 |
2 |
|
|
|
|
|
|
|
|
|
рибулозо-5-фосфат |
|
|
|
|||||
- |
|
|
COO |
|
|
H C OH |
|
|
HO C H |
|
|
H C OH |
|
|
H C OH |
|
|
CH OPO H |
||
2 |
3 |
2 |
6-фосфоглюконат |
||
Превращение глюкозо-6-фосфата до рибулозо-5-фосфата принято называть окислительной фазой пентозофосфатного цикла. Фаза от рибулозо- 5-фосфата до образования вновь глюкозо-6-фосфата называется неокислительной или анаэробной фазой этого цикла.
4 реакция: изомеризация пентозофосфатов. Рибулозо-5-фосфат под действием ферментов рибозофосфатизомеразы и рибулозо-5-фосфат-3- эпимеразы может обратимо изомеризоваться в другие пентозы: рибозо-5- фосфат, ксилулозо-5-фосфат.
|
O |
|
|
|
|
|
|
|
|
|
|
C H |
|
|
CH OH |
|
|
|
CH OH |
|
|
H |
C OH |
|
|
2 |
|
|
|
2 |
|
|
|
|
C O |
|
|
|
C O |
|
|
||
|
|
|
|
|
|
|
|
|
||
H |
C OH |
|
H |
C OH |
|
|
HO |
C H |
|
|
|
|
|
|
|
|
|
||||
H C OH |
|
H C OH |
|
|
H C OH |
|
|
|||
|
|
|
|
|
|
|
||||
|
CH OPO H |
|
CH OPO H |
|
CH OPO H |
|||||
|
2 |
3 2 |
|
|
||||||
|
|
|
|
2 |
3 |
2 |
|
2 |
3 |
2 |
рибозо-5-фосфат |
рибулозо-5-фосфат |
ксилулозо-5-фосфат |
||||||||
В некоторых случаях ПФП на этом заканчивается. И тогда суммарное уравнение реакции выглядит так:
глюкозо-6-фосфат + Н2О + 2НАДФ+ рибозо-5-фосфат + 2НАДФН·Н+ +СО2
Однако многие клетки нуждаются в большем количестве НАДФН·Н+ (для восстановительных синтезов), чем требуется рибозо-5-фосфата (для включения в нуклеотиды). В таких случаях рибозо-5-фосфат превращается в глицеральдегид-3-фосфат и фруктозо-6-фосфат под действием двух ферментов: транскетолазы и трансальдолазы. Эти ферменты создают обратимую связь между ПФП и гликолизом, катализируя следующие реакции:
240
5) ксилулозо-5-фосфат + рибозо-5-фосфат седогептулозо-7-фосфат + глицеральдегид-3-фосфат
6) седогептулозо-7-фосфат + глицеральдегид-3-фосфат эритрозо-4- фосфат + фруктозо-6-фосфат* 7) ксилулозо-5-фосфат + эритрозо-4-фосфат фруктозо-6-фосфат* + глицеральдегид-3-фосфат*
Суммируя эти реакции, получаем: 2 ксилулозо-5-фосфат + рибозо-5-фосфат2 фруктозо-6-фосфат + глицеральдегид-3-фосфат
Итак, избыток рибозо-5-фосфата, образованный в ПФП, может превращаться в метаболиты гликолиза.
