
7 семестр / Л5_ХОБП
.pdf35
Лекция № 5. Структура и свойства моносахаридов, олигосахаридов и полисахаридов
1.Биологические функции углеводов.
2.Важнейшие семейства моносахаридов. Стереохимия. D- и L-ряды. Открытые и циклические (пиранозные и фуранозные) формы.
3.Гликозиды. Биологически важные производные моносахаридов. Олигосахариды.
4.Полисахариды. Структура, классификация, свойства. Биологическое значение. Резервные, структурные и водорастворимые полисахариды.
Биологические функции углеводов
Углеводы можно считать основой существования большинства организмов. В таких углеводах, как сахара и крахмал, заключено основное количество калорий, поступающих с пищей человеком, почти всеми животными и многими бактериями. Центральное место углеводы занимают и в метаболизме зеленых растений и других фотосинтезирующих организмов, утилизирующих солнечную энергию для синтеза углеводов из CO2 и H2O. Образующиеся в результате фотосинтеза огромные количества крахмала и других углеводов играют роль главных источников энергии и углерода для неспособных к фотосинтезу клеток животных, растений и моносахаридов.
Углеводам присущи также и другие важные биологические функции. Крахмал и гликоген используются как временные депо глюкозы. Нерастворимые полимеры углеводов выполняют функции структурных и опорных элементов в клеточных стенках бактерий и растений, а также в соединительной ткани и оболочках животных клеток. Углеводы других типов служат в качестве смазки в суставах, обеспечивающих слипание клеток и придают биологическую специфичность поверхности животных клеток.
Общая характеристика и классификация
Углеводы – это природные соединения, имеющие в подавляющем большинстве состав Cn(H2O)m. Их подразделяют на низкомолекулярные углеводы и продукты их поликонденсации.
Моносахариды – мономеры, из остатков которых состоят углеводы более сложного строения (глюкоза, фруктоза, рибоза, галактоза, манноза и их функциональные производные – аминосахара, дезоксисахара ит.д.).
Олигосахариды – олигомеры, содержащие от 2 до 10 моносахаридных остатков (дисахариды – манноза, целлобиоза, лактоза, сахароза).
Полисахариды – полимеры, включающие до нескольких тысяч моносахаридных звеньев (крахмал, гликоген, целлюлоза, хитин, гиалуроновая кислота).

36
Моносахариды
Химическое строение и классификация
Моносахариды – это полигидроксикарбонильные соединения, в которых каждый атом углерода (кроме карбонильного) связан с группой ОН. Общая формула моносахаридов – Сn(H2O)n, где n =3-9.
По химическому строению различают:
-альдозы – моносахариды, содержащие альдегидную группу;
-кетозы – моносахариды, содержащие кетонную группу (как
правило, в положении 2).
В зависимости от длины углеродной цепи моносахариды делятся на
триозы, тетрозы, пентозы, гексозы и т.д. Обычно моносахариды
|
|
* * |
|
|
|
O |
* * |
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
CH2 |
|
CH |
|
CH |
|
C |
H |
CH2 |
|
CH |
|
CH |
|
C |
|
CH2 |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
OH OH |
|
OH OH OH O OH |
|||||||||||||||||||||
|
альдотетроза |
|
|
|
|
кетопентоза |
|||||||||||||||||||
классифицируют с учетом сразу двух этих признаков:
В природе встречаются производные моносахаридов, содержащие аминогруппу (аминосахара), карбоксильную группу (сиаловые кислоты, аскорбиновая кислота), а также атом Н вместо одной или нескольких групп ОН (дезоксисахара). Наиболее важными производными моносахаридов являются амино- и дезоксисахара.
Все моносахариды (кроме дигидроксиацетона) содержат хиральные атомы углерода и имеют стереоизомеры. Простейшая альдоза , глицериновый альдегид, содержит один хиральный атом С и существует в виде двух
|
|
CHO |
|
|
CHO |
||||||
H |
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
OH |
HO |
|
C |
|
H |
|||
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
||||
|
|
CH2OH |
|
|
CH2OH |
||||||
D-глицеральдегид |
L-глицеральдегид |
||||||||||
оптических изомеров – D и L:
По мере увеличения длины цепи количество стереоизомеров у альдогексоз растет. В соответствии с числом хиральных центров существует 4 стереоизомерных альдотетрозы, 8 альдопентоз, 16 альдогексоз и т.д. В зависимости от конфигурации наиболее удаленного от карбонильной группы хирального атома С все моносахариды делят на два стереохимических ряда –
|
|
CHO |
|
|
|
CHO |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(CHOH) |
|
|
(CHOH)n |
||||||
|
|
|
|
|
n |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
C |
|
OH |
HO |
|
C |
|
H |
||
|
|
|
|
||||||||
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
||
|
|
CH OH |
|
|
CH2OH |
||||||
2 |
|
|
|
|
|
|
|||||
|
|
D-альдоза |
L-альдоза |
||||||||
D-моносахариды и L-моносахариды:

37
Подавляющее большинство природных моносахаридов принадлежит к D-ряду.
Родоначальником ряда D-альдоз является D-глицериновый альдегид. Остальные D-альдозы могут быть построены на основе D-глицеральдегида путем последовательной вставки фрагмента СНОН сразу после карбонильной группы. Стереоизомерные альдозы имеют тривиальные названия.
Уточним стереоизомерные отношения в ряду D-альдоз. Между собой D-альдозы с одинаковым числом атомов углерода (D-альдотетрозы, D- альдопентозы, D-альдогексозы и т.д.) являются диастереомерами. Среди них
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Семейство D -альдоз |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CHO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CHO |
|
|
|
|
|
|
D-глицеральдегид |
|
|
|
|
|
|
CHO |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH OH |
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
D-эритроза |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
D-треоза |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
CHO |
|
|
|
|
|
|
|
|
|
|
|
|
CHO |
|
|
|
|
|
|
|
|
|
|
|
|
CHO |
|
|
|
|
|
|
|
|
|
|
|
CHO |
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
OH |
|
|
|
|
|
|
|
|
|
HO |
|
|
H |
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
H |
|
OH |
|
|
|
|
|
|
|
|
|
|
HO |
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
|
H |
|
|
|
|
|
|
|
|
|
HO |
|
H |
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
H |
|
OH |
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
OH |
|
|
|
|
|
|
|
|
|
|
H |
|
OH |
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
H |
|
OH |
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2OH |
|
|
|
|
|
|
|
|
|
|
|
CH2OH |
|
|
|
|
|||||||
|
|
|
|
|
|
CH2OH |
|
|
|
|
|
|
|
|
|
|
|
|
CH OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
D-рибоза |
|
|
|
|
|
|
|
|
|
|
D-арабиноза |
|
|
|
D-ксилоза |
|
|
|
|
|
|
|
|
|
D-ликсоза |
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
CHO |
|
|
|
|
|
CHO |
|
|
|
|
CHO |
|
|
|
CHO |
|
|
CHO |
|
|
|
|
CHO |
|
|
|
|
CHO |
|
|
|
CHO |
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
HO |
|
|
|
H |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
H |
|
|
OH |
|
HO |
|
|
H |
H |
|
|
OH |
HO |
|
|
|
|
|
H |
H |
|
|
|
|
OH |
HO |
|
|
H |
H |
|
|
HO |
|
|
|
H |
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
H |
|
|
OH |
|
H |
|
|
OH |
HO |
|
|
H |
HO |
|
|
|
|
|
H |
H |
|
|
|
|
OH |
H |
|
|
OH |
HO |
|
|
H |
|
|
|
|
|
|
|||||||||||||||||||||||||
H |
|
|
|
OH |
|
H |
|
|
|
OH |
H |
|
|
|
OH |
H |
|
|
|
|
OH |
HO |
|
|
|
H |
HO |
|
|
|
H |
HO |
|
|
|
H |
HO |
|
|
|
H |
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||
H |
|
|
|
OH |
|
H |
|
|
|
OH |
H |
|
|
|
OH |
H |
|
|
|
|
OH |
H |
|
|
|
OH |
H |
|
|
|
OH |
H |
|
|
|
OH |
H |
|
|
|
|
OH |
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||
|
|
|
CH OH |
|
|
|
|
CH OH |
|
|
|
CH OH |
|
|
|
CH OH |
|
|
CH OH |
|
|
|
CH2OH |
|
|
|
CH2OH |
|
|
CH2OH |
||||||||||||||||||||||||||||||||||
|
|
|
2 |
|
|
|
|
|
2 |
|
|
|
|
|
2 |
|
|
|
|
|
|
2 |
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
D-аллоза |
|
D-альтроза D-глюкоза |
D-манноза |
D-гулоза |
D-иодоза D-галактоза D-талоза |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
выделяют особый тип диастереомеров, который называют эпимерами. Эпимеры – это диастереомеры, которые отличаются по конфигурации
только одного хирального центра.
Например, D-рибоза и D-арабиноза являются эпимерами, так как отличаются конфигурацией только хирального атома углерода в положении 2. D-глюкоза имеет несколько эпимеров: D- маннозу по С2, D- аллозу по С3, D-галактозу по С4, L-иодозу по С5.
Каждая из D-альдоз имеет энантиомер, относящийся к L-ряду, который может быть построен аналогично D-ряду на основе L-глицеральдегида. Энантиомером D-глюкозы является L-глюкоза, D-маннозы – L-манноза и т.д.

38
|
|
|
CHO |
|
|
|
CHO |
||||||
H |
|
|
|
|
|
OH |
|
HO |
|
|
|
|
H |
|
|
|
|
|
|
|
|
||||||
HO |
|
|
|
|
|
H |
|
H |
|
|
|
|
OH |
|
|
|
|
|
|
|
|
||||||
H |
|
|
|
|
OH |
|
HO |
|
|
|
H |
||
|
|
|
|
|
|
|
|||||||
H |
|
|
|
|
OH |
|
HO |
|
|
|
H |
||
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
CH2OH |
|
|
|
CH2OH |
||||||
D-глюкоза |
|
L-глюкоза |
|||||||||||
Таким образом, на приведенной выше схеме представлена ровно половина из возможных стереоизомерных альдоз. Другая половина относится к L- ряду.
Ряд D-кетоз может быть построен на основе простейшей кетозы – дигидроксиацетона. Названия кетоз образуются из названий соответствующих альдоз путем введения суффикса «ул». Для некоторых
Семейство D-кетоз
CH2OH
C=O
CH2OH
|
|
|
|
|
|
|
|
|
|
дигидроксиацетон |
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2OH |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
C=O |
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
CH2OH |
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
D-эритрулоза |
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
CH2OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2OH |
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
C=O |
|
|
|
|
|
|
|
|
|
|
|
|
C=O |
|
|
|
|||||
|
|
|
H |
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
HO |
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
H |
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
CH2OH |
|
|
|
|
|
|
|
|
|
|
|
|
CH2OH |
|
|
|
|||||
|
|
|
D-рибулоза |
|
|
|
|
|
|
|
|
|
|
|
D-ксилулоза |
|
|
|
|||||||
|
CH OH |
|
|
|
|
CH OH |
|
|
|
|
|
CH2OH |
|
|
|
|
|
CH2OH |
|||||||
|
|
2 |
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
C=O |
|
|
|
|
C=O |
|
|
|
|
C=O |
|
|
|
|
C=O |
|||||||||
H |
|
|
OH |
|
|
|
HO |
|
|
H |
|
|
H |
|
|
|
OH |
|
|
HO |
|
|
|
H |
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
H |
|
|
OH |
|
|
|
H |
|
|
OH |
|
|
HO |
|
|
|
H |
|
|
HO |
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
H |
|
|
OH |
|
|
|
H |
|
|
OH |
|
|
H |
|
|
|
OH |
|
|
H |
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
CH OH |
|
|
|
|
CH OH |
|
|
|
|
CH2OH |
|
|
|
|
CH2OH |
|||||||||
|
2 |
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
D-псикоза |
|
|
|
D-фруктоза |
|
|
D-сорбоза |
|
|
D-тагатоза |
|||||||||||||||
кетоз утвердились тривиальные названия.
Дигидроксиацетон не содержит хирального атома С и не имеет стереоизомеров. Остальные кетозы являются хиральными соединениями.
В природе широко распространены гексозы (D-глюкоза, D-галактоза, D-манноза, D-фруктоза) и пентозы (D-рибоза, D-ксилоза, D-арабиноза). Среди производных моносахаридов наиболее распространенными являются аминосахара D-глюкозамин и D-галактозамин и дезоксисахар 2-дезокси-D- рибоза.

39
|
|
|
CHO |
|
|
|
CHO |
|
CHO |
|||||||||
H |
|
|
|
|
|
NH2 |
H |
|
|
|
|
|
NH2 |
|
CH2 |
|||
|
|
|
|
|
|
|
|
|
||||||||||
HO |
|
|
|
|
|
H |
HO |
|
|
|
|
|
H |
H |
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
H |
|
|
|
OH |
HO |
|
|
|
H |
|||||||||
|
|
|
|
|
|
H |
|
|
|
OH |
||||||||
H |
|
|
|
|
OH |
H |
|
|
|
|
OH |
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
CH2OH |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
CH2OH |
|
|
|
CH2OH |
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||
D-глюкозамин |
D-галактозамин |
2-дезокси-D-рибоза |
||||||||||||||||
Цикло-оксо-таутомерия
Известно, что альдегиды способны присоединять спирты с образованием полуацеталей:
R |
|
|
|
R |
C |
OH |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
||
H |
C O + R`OH |
H |
OR` |
||||
|
|||||||
полуацеталь
Карбонильная и гидроксильная группы моносахаридов взаимодействуют внутримолекулярно с образованием циклического полуацеталя:
H |
O |
H * |
OH |
полуацетальный (гликозидный) гидроксил |
|
|
|
|
|
|
C |
C |
|
|
|
|
O |
аномерный атом углерода |
|
|
|
|
|
|
OH
циклический полуацеталь
При этом возникает новый хиральный центр – бывший карбонильный, а теперь аномерный атом углерода. Наиболее устойчивы циклические полуацетали, содержащие шестичленный (пиранозный) или пятичленный (фуранозный) циклы. Они образуются при взаимодействии альдегидной группы с гидроксильной группой в положении 5 или 4 моносахарида
1 |
|
|
|
|
|
|
|
|
|
|
|
|
H 1 |
|
|
O |
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
HO |
|
|
|
C |
|
|
|
|
H |
|
|
|
|
|
|
C |
|
|
|
|
|
|
H |
|
|
C |
|
|
|
|
OH |
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
OH |
|
|
|
|
2 |
|
|
|
|
OH |
|
|
|
|
||||||||||||
H |
|
|
|
|
|
|
OH |
O |
|
H |
|
|
H |
|
|
|
|
|
O |
||||||||||||||||||||||||||||
3 |
|
|
|
3 |
|
|
|
|
|||||||||||||||||||||||||||||||||||||||
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
HO |
|
|
|
|
|
|
H |
|
|
|
|
|
HO |
|
|
H |
|
|
|
|
HO |
|
|
|
|
|
H |
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
|
|
|
|
4 |
|
|
|
4 |
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||
H |
|
|
|
|
|
|
OH |
|
|
|
|
|
H |
|
|
OH |
|
|
|
|
H |
|
|
|
|
|
OH |
|
|
|
|
||||||||||||||||
|
|
|
|
5 |
|
|
|
5 |
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
OH |
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
6 |
|
|
|
6 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
6 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
CH OH |
|
|
|
|
|
|
CH2OH |
|
|
|
|
CH2OH |
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
D-глюкопираноза |
D-глюкоза (линейная форма) |
|
D-глюкопираноза |
||||||||||||||||||||||||||||||||||||||||||||
1 |
|
|
|
|
|
|
|
|
|
|
|
H 1 |
|
O |
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
HO |
|
C |
|
|
|
H |
|
|
|
|
|
|
|
C |
H |
|
|
C |
|
|
OH |
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
O |
|||||||||||||||||||||||||||||||||||
|
|
|
|
O |
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||
H |
2 |
|
|
|
OH |
|
H |
2 |
|
|
OH |
|
H |
|
2 |
|
|
|
|
|
OH |
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
HO |
|
|
|
H |
|
|
|
|
|
HO |
|
|
H |
|
HO |
|
|
|
|
|
|
H |
|
|
|
|
|||||||||||||||||||||
|
|
|
|
4 |
|
|
|
4 |
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||
H |
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
OH |
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
5 |
|
|
|
|
5 |
|
|
|
|
|
OH |
|
|
|
|
||||||||||||||||||
H |
|
|
|
OH |
|
|
|
|
|
H |
|
|
OH |
|
H |
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
6 |
|
|
|
|
6 |
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
6 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
CH OH |
|
|
|
|
|
|
|
CH2OH |
|
|
|
|
|
|
|
CH2OH |
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
D-глюкофураноза |
|
D-глюкоза (линейная форма) |
|
|
|
|
D-глюкофураноза |
||||||||||||||||||||||||||||||||||||||||
соответственно. На рисунке представлена схема образования циклических форм D-глюкозы:

40
Возникновение нового хирального центра приводит к появлению 2-х стереоизомеров для каждой из циклической форм: - и -аномеров.
Аномеры – это эпимеры, которые различаются по конфигурации
|
|
CH2OH |
|
|
|
|
|
|
|
|
|
|
6 CH OH |
|
|
|
|||||||||||||
HO |
|
H O |
|
|
|
|
|
|
|
|
|
|
5 |
|
|
|
2 |
O |
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
OH |
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
HO |
|
|
3 |
|
|
|
2 OH |
|
|||||||
|
|
|
|
|
OH |
H 1 |
|
O |
|
|
|
|
|
|
|
OH |
|
|
|
||||||||||
D-глюкофураноза |
|
|
C |
|
D-глюкопираноза |
|
|||||||||||||||||||||||
|
|
(следы) |
|
|
|
H |
2 |
|
OH |
|
|
|
|
|
|
~32% |
|
|
|
||||||||||
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
HO |
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
H |
|
4 |
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
5 |
|
|
|
|
|
6 |
|
|
|
|
|
|
|
|
||||
|
|
CH OH |
|
|
|
H |
|
OH |
|
|
|
|
CH2OH |
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
2 |
|
|
|
|
|
6 |
|
|
|
|
|
|
|
5 |
|
|
|
O |
OH |
|
||||||
HO |
|
|
H O |
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
CH2OH |
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
4 |
|
|
OH |
|
|
||||||||||||||||
|
|
|
|
OH |
|
|
1 |
D-глюкоза |
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
линейная форма |
|
HO |
|
|
3 |
|
|
|
2 |
|
|
|||||||
|
|
|
|
|
|
OH |
|
|
|
(следы) |
|
|
|
|
|
|
|
|
|
OH |
|
||||||||
|
D-глюкофураноза |
|
|
|
|
|
|
|
|
D-глюкопираноза |
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
~68% |
|
|
|||||||||||||||
|
|
|
(следы) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
аномерного атома углерода. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
У |
|
-аномера |
конфигурация аномерного |
|
центра |
|
совпадает |
с |
||||||||||||||||
конфигурацией концевого |
хирального |
атома |
С, у |
-аномера |
она |
||||||||||||||||||||||||
противоположна. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
Циклические формы моносахаридов изображают с помощью формул |
||||||||||||||||||||||||
Хеуорса. Молекулу представляют в виде плоского цикла, перпендикулярного плоскости рисунка. Заместители, находившиеся в формуле Фишера слева, располагают над плоскостью цикла, справа – под плоскостью. Для определения положения группы СН2ОН в формуле Фишера предварительно делают две перестановки.
В кристаллическом состоянии моносахариды находятся в одной из циклических форм. При растворении образуется равновесная смесь линейной и циклических форм. Их содержание определяется термодинамической стабильностью. Циклические, особенно пиранозные формы, энергетически более выгодны для большинства моносахаридов. Например, в растворе D- глюкозы преобладает -D-глюкопираноза:

41
|
1 |
|
|
|
|
|
1 |
|
|
6CH OH |
|
||
H |
C |
OH |
|
|
H |
C |
OH |
5 |
2 |
O |
|
||
H 32 |
|
OH O |
|
H 32 |
OH |
O |
4 OH |
1 |
|
||||
HO |
|
|
H |
|
HO |
4 |
H |
|
HO |
|
2 OH |
гликозидный |
|
4 |
|
|
OH |
|
|
||||||||
H |
|
|
OH |
|
6 |
H |
5 |
|
|
3 |
|
гидроксил |
|
H |
5 |
|
|
|
HOCH2 |
H |
|
|
|
OH |
|
||
|
6CH2OH |
|
|
D-глюкопираноза |
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
||||
|
|
1 |
|
|
|
|
6CH2OH |
|
|
|
|
||
HO |
|
C H |
|
|
|
гликозидный |
|
||||||
H |
2 |
OH |
O |
|
|
5 |
O OH |
|
|||||
|
|
|
|
|
|
|
|
||||||
3 |
|
|
|
OH |
|
гидроксил |
|
||||||
HO |
|
H |
|
|
4 |
|
1 |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
||
6 H 54 |
|
|
|
|
|
|
|
|
|
|
|||
OH |
|
|
HO |
3 |
2 |
|
|
|
|
||||
HOCH2 |
|
H |
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
OH |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
D-глюкопираноза
Существование равновесия между линейной и циклическими формами моносахаридов получило название цикло-оксо-таутомерии.
Растворение кристаллического моносахарида сопровождается постепенным таутомерным превращением, которое заканчивается установлением таутомерного равновесия. Каждая таутомерная форма оптически активна и имеет свою величину удельного вращения. Поэтому за таутомерным превращением можно следить по изменению удельного вращения раствора, которое заканчивается с установлением равновесия. Явление изменения удельного вращения свежеприготовленного раствора моносахарида называют мутаротацией. Явление мутаротации – одно из доказательств существования цикло-оксо-таутомерии у моносахаридов.
Гликозиды
Циклические формы моносахаридов содержат несколько групп ОН, одна из которых – гликозидный (полуацетальный) гидроксил, обладает особыми свойствами.
Известно, что в присутствии кислотных катализаторов полуацетали реагируют со спиртами. При этом происходит нуклеофильное замещение
R |
|
OH |
H+ |
R |
|
OR` + H O |
|
H |
C |
OR` + R`OH |
|
H |
C |
OR` |
2 |
|
|||||||
|
|
||||||
полуацеталь |
|
ацеталь |
|
||||
полуацетального гидроксила и образуются полные ацетали.
В аналогичных условиях в альдозах и кетозах происходит замещение гликозидного (полуацетального) гидроксила с образованием ацеталя. Спиртовые ОН группы при этом не затрагиваются. Продукты замещения гликозидного гидроксила в моносахаридах называют гликозидами. В

42
зависимости от размера цикла их называют гликопиранозидами или
гликофуранозидами.
CH2OH |
|
CH OH |
|
|
CH2OH |
|
|
2 |
O OCH |
|
|
O |
|
O |
|
+ |
|
|
||
|
|
CH3OH, H |
3 |
|
|
|
|
|
|
|
|
OH |
|
OH |
OH |
OH |
|
+ |
|
|
HO |
|
HO |
|
|
HO |
OCH3 |
OH |
|
|
OH |
|
|
OH |
D-глюкопираноза |
метил- |
D-глюко- |
|
метил- D-глюко- |
||
и аномеры |
|
|||||
пиранозид |
|
пиранозид |
||||
|
|
|
||||
Гликозиды существуют только в циклической форме. Для них не характерна цикло-оксо-таутомерия и - и -аномеры гликозидов не могут переходить друг в друга в результате таутомерных превращений. Гликозиды не имеют свободной альдегидной группы и поэтому являются невосстанавливающими сахарами. Как полные ацетали они гидролизуются под действием кислот, но не щелочей.
|
CH2OH |
|
|
CH OH |
|
|
O |
|
H+ |
2 |
O |
|
OH |
+ |
H2O |
OH |
OH + CH3OH |
|
|
|
|
|
|
HO |
OCH3 |
|
|
HO |
|
|
OH |
|
|
|
OH |
Расщепление гликозидной связи важно с биологической точки зрения, поскольку многие природные соединения являются гликозидами. Молекулу гликозида рассматривают как состоящую из двух частей – сахарной части и
агликона:
O X
X 
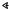



 агликон
агликон
В качестве агликона в природных гликозидах могут выступать спирты, фенолы, стероиды, сами моносахариды. Перечисленные агликоны связаны с сахарной частью через атом кислорода, поэтому такие гликозиды называют О-гликозидами. В природе широко распространены N-гликозиды, в которых агликонами являются азотистые основания. К ним относятся нуклеозиды – структурные единицы нуклеиновых кислот.
Дисахариды
Дисахариды состоят из двух моносахаридных остатков, связанных гликозидной связью. Их можно рассматривать как О-гликозиды, в которых агликоном является остаток моносахарида.
Возможно два варианта образования гликозидной связи:
1)за счет гликозидного гидроксила одного моносахарида и спиртового гидроксила другого моносахарида;
2)за счет гликозидных гидроксилов обоих моносахаридов.

43
Дисахарид, образованный первым способом, содержит свободный гликозидный гидроксил, сохраняет способность к цикло-оксо-таутомерии и обладает восстанавливающими свойствами.
Вдисахариде, образованном вторым способом, нет свободного гликозидного гидроксила. Такой дисахарид не способен к цикло-оксо- таутомерии и является невосстанавливающим.
Вприроде в свободном виде встречается незначительное число дисахаридов. Важнейшими из них являются мальтоза, целлобиоза, лактоза и сахароза.
Мальтоза
Мальтоза содержится в солоде и образуется при неполном гидролизе крахмала. Молекула мальтозы состоит из двух остатков D-глюкозы. Гликозидная связь между ними образована за счет гидроксильной группы в
CH2OH |
|
CH2OH |
|
|
||
|
O |
|
O |
|
|
|
OH |
1 |
4 |
OH |
OH |
свободный гликозидный |
|
O |
||||||
HO |
|
|
|
гидроксил |
||
|
|
|
|
|||
|
OH |
|
OH |
|
|
|
|
гликозидная связь |
|
|
|||
D-глюкопиранозил -1,4- |
или D-глюкопираноза ( или мальтоза) |
|||||
положении 4 одного моносахарида |
и гликозидного гидроксила в - |
|||||
конфигурации другого моносахарида.
Таким образом, мальтоза – это восстанавливающий дисахарид. Она
|
|
|
|
CH2OH |
|
CH2OH |
|
|
|
|
|
|
|
|
|
|
|
O |
|
OH |
|
|
|
|
|
|
|
|
|
OH |
1 |
4 |
OH |
CHO |
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
||
|
|
|
HO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
OH |
|
|
|
|
|
|
|
|
|
|
открытая форма |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
CH OH |
|
CH OH |
||
CH2OH |
|
CH2OH |
|
|
|
|
2 |
O |
|
2 |
O OH |
|
|
O |
|
O |
|
|
|
|
OH |
1 |
4 |
OH |
|
OH |
1 |
|
4 OH |
|
|
|
|
|
||||
O |
|
|
|
|
HO |
|
O |
|
|
|||
HO |
|
OH |
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
OH |
||||
|
|
|
|
|
|
OH |
|
|
||||
|
OH |
|
OH |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
||
|
мальтоза |
|
|
|
|
|
|
мальтоза |
|
|||
способна к таутомерии и имеет - и |
-аномеры. |
|
|
|
|
|||||||
Целлобиоза
Целлобиоза – продукт неполного гидролиза целлюлозы. Молекула
CH2OH |
|
CH2OH |
|
|
|
|
O |
|
O |
|
|
OH |
1 O |
4 |
OH |
OH |
свободный гликозидный |
|
|||||
HO |
|
|
|
|
гидроксил |
|
OH |
|
OH |
|
|
|
гликозидная связь |
|
|
||
D-глюкопиранозил -1,4- |
или |
D-глюкопираноза ( или целлобиоза) |
|||

44
целлобиозы состоит из двух остатков D-глюкозы, связанных -1,4- гликозидной связью.
Целлобиоза – восстанавливающий дисахарид. Она способна к таутомерии и имеет - и -аномеры.
Дисахариды вступают в большинство реакций, характерных для моносахаридов: образуют простые и сложные эфиры, гликозиды. Восстанавливающие дисахариды окисляются до соответствующих кислот.
Гликозидная связь в дисахаридах расщепляется под действием кислот (но не щелочей) и ферментов.
Ферменты действуют селективно и расщепляют только - или - гликозидную связь. Последовательность реакций – метилирование, а затем гидролиз, позволяет определить положение гликозидной связи в дисахариде.
Конфигурация гликозидной связи ( |
или ) |
может быть определена с |
||||||||||||
помощью ферментативного гидролиза. |
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
Лактоза |
|
|
|
|
|
CH2OH |
|
|
|
CH2OH |
|
|
|
|||||
HO |
|
O |
|
|
|
|
O |
|
|
|
||||
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
1 O |
4 |
|
|
|
|
|
OH |
свободный гликозидный |
|
|
OH |
|
|
|
|
OH |
||||||||
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
гидроксил |
|
|
|
|
OH |
|
|
|
|
OH |
|
|
|
|||
|
|
|
|
гликозидная связь |
|
|
|
|||||||
D-галакопиранозил -1,4- |
|
или |
D-глюкопираноза ( |
или лактоза) |
||||||||||
Лактоза содержится в молоке (4-5%). Молекула лактозы состоит из остатков D-галактозы и D-глюкозы, связанных -1,4-гликозидной связью.
Лактоза – восстанавливающий дисахарид. В растворе лактозы устанавливается таутомерное равновесие между открытой формой и двумя циклическими - -лактозой и -лактозой.
Сахароза
Сахароза содержится в сахарном тростнике, сахарной свекле, соках растений и плодах. Она состоит из остатков D-глюкозы и D-фруктозы, которые связаны за счет гликозидных гидроксилов. Таким образом, сахароза
– невосстанавливающий дисахарид. В составе сахарозы D-глюкоза находится в пиранозной, а D-фруктоза – в фуранозной форме.
