
7 семестр / Биоэнергетика
.pdf208
Лекция. Введение в обмен веществ. Биоэнергетика
Понятие о метаболизме и метаболических путях. Метаболизм как совокупность процессов катаболизма и анаболизма
Биоэнергетика. Элементы термодинамики открытых систем. Сопряжение экзергонических и эндергонических процессов. Макроэргические соединения. АТФ - основной источник и аккумулятор энергии в организме.
Фазы катаболизма основных питательных веществ в организме. Окислительные реакции катаболических процессов. Субстратное и окислительное фосфорилирование. Клеточное дыхание.
Организация дыхательной цепи в митохондриях. Направление движения электронов по дыхательной цепи. Электрохимический потенциал. Роль АТФсинтазы в сопряжении окислительного фосфорилирования с цепью переноса электронов. Коэффициент фосфорилирования при переносе восстановительных эквивалентов на кислород от различных субстратов.
Биоэнергетика. Основные понятия и определения
Особенности живых организмов как объектов для термодинамических исследований
Химическая термодинамика является теоретической основой биоэнергетики. Биоэнергетика занимается изучением энергетических превращений, сопровождающих биохимические реакции. Все эти превращения осуществляются в полном соответствии с первым и вторым началами термодинамики. Тем не менее, живой организм, как объект для термодинамических исследований, отличается целым рядом специфических особенностей в сравнении с системами, которые служат объектами изучения в технической и химической термодинамики. Из этих особенностей наибольшего внимания заслуживают следующие.
Живой организм представляет собой типично открытую систему, непрерывно обменивающуюся с окружающей средой веществом и энергией. В то же время для биологических систем применимо понятие стационарного состояния. В этом состоянии параметры в системе остаются постоянными, а скорость притока веществ и энергии равна скорости удаления их из системы. Такие системы не изменяют своих свойств во времени и сходны с системами, находящимися в равновесии.
Характер изменения энтропии, имеющий решающее значение при оценке процессов в неживых системах, в случае биологических систем имеет лишь подчиненное значение. Ведь все живые организмы высоко организованы и постоянно поддерживают свой уровень организации, поэтому для биологических систем справедливо неравенство Sокр. + Sсист.
> 0 , а не Sсист > 0.
209
Все биохимические процессы, происходящие в клетках в условиях постоянства температуры и давления, при отсутствии значительных перепадов концентраций, резких изменений объема.
Небиологические системы могут совершать работу за счет тепловой энергии, биологические функционируют в изотермическом режиме и для осуществления процессов жизнедеятельности используют химическую энергию.
Стандартное состояние для биологических объектов отличается от стандартного состояния технических и химических систем. Вспомним, что стандартным состоянием химической системы является состояние, при котором концентрации всех веществ равны 1 моль/л ( или для газов, входящих в систему, парциальные давления равны 1 атм). Для биологических систем это определение остается в силе за исключением концентрации ионов Н+, которая для стандартного состояния принимается равной 10-7 моль/л. Это соответствует нейтральной среде (рН 7), характерной для биологических объектов.
G0 - стандартная энергия Гиббса для химических систем;G0 - стандартная энергия Гиббса для биологических систем.
Сопряжение экзергонических процессов с эндергоническими
Человек получает энергию за счет разложения органических веществ пищи. Органические вещества являются термодинамически нестабильными. Катаболические превращения этих веществ (распад или окисление) протекают с уменьшением свободной энергии. Такие процессы являются самопроизвольными (экзергоническими - G<0) и могут служить источником энергии для функционирования живой клетки. Все процессы, которые идут с увеличением свободной энергии (эндергонические - G>0), несамопроизвольные и должны быть сопряжены с экзергоническими процессами.
Жизненно важные процессы - реакции синтеза (т.е. анаболические процессы), мышечное сокращение, активный транспорт - являются эндергоническими процессами. Эндергонический процесс не может протекать изолированно. Такие процессы получают энергию путем химического сопряжения с реакциями окисления молекул пищевых веществ (катаболическими процессами), которые являются экзергоническими реакциями. Совокупность метаболических и анаболических процессов есть метаболизм.

210
Схематически такое сопряжение можно проиллюстрировать следующим образом. Пусть превращение метаболита (промежуточного соединения в цепи реакций) А в метаболит В сопровождается выделением свободной энергии. Оно сопряжено с другой реакцией - превращением метаболита С в метаболит D, которое может происходить лишь при поступлении свободной энергии.
Каким же образом осуществляется это сопряжение?
Одним из возможных механизмов состоит в образовании промежуточного соединения - общего для обеих реакций.
A + C I B + D
Здесь заложен механизм регуляции скорости окислительных процессов, т.к. скорость потребления D определяет скорость окисления А. Этим путем осуществляется дыхательный контроль - процесс, позволяющий организму избежать неконтролируемого самоокисления.
Другим примером сопряжения являются дегидрогеназные реакции (реакции отщепления атомов водорода), промежуточным соединением, в которых является промежуточный переносчик атомов водорода.
Еще один |
пример |
сопряжения состоит в синтезе в ходе |
|||
A-H2 |
переносчик |
|
B-H2 |
|
|
|
|
|
|
||
A |
переносчик-H 2 |
B |
|
||
экзергонических |
реакций высокоэнергетического соединения, общего для |
||||
|
|
|
|
|
NH2 |
|
|
|
|
N |
N |
|
|
|
|
|
|
|
- |
O |
- |
N |
N |
|
O |
O |
|
||
|
O- P |
O P O P OH2C |
|
|
|
|
O |
O- |
O |
|
|
OH OH

211
многих процессов, и последующего включения этого соединения в эндергонические реакции, что обеспечивает передачу энергии. Таким общим для многих реакций соединением - энергетической валютой клетки - является аденозинтрифосфат (АТР).
Это позволяет сопрягать большее число экзергонических реакций с большим числом эндергонических. В молекуле АТР две макроэргические связи, т.е. связи, при гидролизе которых высвобождается энергия.
Макроэргические соединения
Энергия, освобождающаяся при реакциях гидролиза разных веществ, обычно невелика. Если она превышает 30 кДж/моль, то такую связь называют высокоэнергетической. Энергия гидролиза некоторых субстратов приведена в таблице.
Макроэргические соединения можно разделить на две группы: 1)Соединения, образующиеся в ходе процессов катаболизма и
служащие для превращения энергии в качестве передаточного звена (1,3- дифосфоглицерат, фосфоенолпируват - промежуточные метаболиты катаболизма углеводов).
2) Соединения, которые могут быть использованы тканями в качестве "аварийного" источника энергии (креатинфосфат локализован в основном в мышцах и служит дополнительным источником энергии при стремительных кратковременных нагрузках).
Соединение |
|
- G', |
|
|
|
|
кДж/моль |
Фосфоенолпируват |
|
|
67,9 |
1,3-Дифосфоглицерат |
(продукт: |
3- |
49,3 |
фосфоглицерат) |
|
|
|
Креатинфосфат |
|
|
43,1 |
АТФ АДФ + Ф |
|
|
30,5 |
АДФ АМФ + Ф |
|
|
27,6 |
Пирофосфат |
|
|
27,6 |
Глюкоза-1-фосфат |
|
|
20,9 |
АМФ |
|
|
14,2 |
Фазы освобождения энергии из питательных веществ
Характер метаболизма в тканях во многом определяется питанием. У человека метаболическим превращениям подвергаются, главным образом, глюкоза, жиры и аминокислоты. Глюкоза и аминокислоты - структурные компоненты белков и углеводов. Таким образом, необходимыми компонентами пищи являются белки углеводы и жиры.
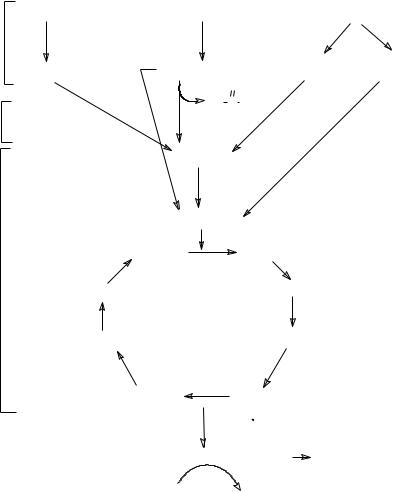
В ходе извлечения энергии из различных субстратов можно условно выделить три фазы катаболизма питательных веществ.
212
Углеводы |
Белки |
|
Жиры |
|
I |
|
|
|
|
Глюкоза |
Аминокислоты |
Глицерин |
Жирные кислоты |
|
|
|
O |
|
|
|
H2N C NH 2 |
|
|
|
II |
|
|
|
|
|
Пируват |
|
|
|
|
Ацетил-КоА |
|
|
|
III |
Оксалоацетат |
Цитрат |
|
|
|
|
|
||
|
|
|
|
|
|
Малат |
Изоцитрат |
|
|
|
|
|
|
|
|
Цикл Кребса |
|
|
|
Фумарат |
2-Оксоглутарат |
|||
|
Сукцинат |
Сукцинил-КоА |
|
|
|
|
+ |
|
|
|
|
НАДН Н |
|
|
|
|
ФАДН |
|
|
|
|
2 |
|
|
|
Цепь переноса электронов |
АТФ |
|
|
|
|
|
|
|
|
+ |
H O |
|
|
|
1/2 O + 2 H |
2 |
|
|
|
2 |
|
|
|
Первая фаза - подготовительная. Она необходима для превращения полимеров, поступающих с пищей или находящихся внутри клетки, в удобную для извлечения энергии форму - мономеры. На этом этапе освобождается около 1% всей энергии, запасенной в питательных веществах. Эта энергия рассеивается в форме теплоты.
Вторая фаза - частичный распад мономеров до ключевых промежуточных продуктов: пирувата, ацетил-КоА и некоторых метаболитов цикла Кребса. На этом этапе освобождается около 20% энергии. Эта стадия называется промежуточный обмен. Реакции промежуточного обмена протекают в цитоплазме.
Третья фаза - окончательный распад всех веществ до CO2 и H2O. Этот этап включает реакции общего пути катаболизма (окислительное декарбоксилирование пирувата, цикл Кребса) и цепь переноса электронов.
Примерно 80% всей энергии химических связей освобождается в данной фазе. Все реакции этой фазы локализуются в митохондриях.
Роль высокоэнергетических фосфатов в улавливании энергии. Клеточное дыхание
213
Главный путь синтеза АТФ из АДФ - окислительное фосфорилирование. При этом АДФ фосфорилируется неорганическим фосфатом:
АДФ + H3PO4 + энергия АТФ + H2O
Реакция энергетически сопряжена с переносом водорода с восстановительных эквивалентов на кислород. Восстановительные эквиваленты образуются при окислении органических молекул. Последовательность реакций, с помощью которых организм использует энергию связей органических молекул для синтеза АТФ, и при этом углерод органических молекул превращается в углекислый газ, а водород (Н+ и е-) переносится на молекулярный кислород с образованием молекулы воды,
называется клеточным дыханием.
Другой путь синтеза АТФ из АДФ - субстратное фосфорилирование.
В этом случае макроэргическая связь в молекуле АТФ может образоваться за счет энергии макроэргической связи в другом субстрате (например, креатинфосфате).
Таким образом, энергия пищевых веществ в клетке трансформируется сначала в энергию АТФ, а затем АТФ служит непосредственным источником энергии для совершения работы в биохимических и физиологических процессах.
ЦЕПЬ ПЕРЕНОСА ЭЛЕКТРОНОВ И ОКИСЛИТЕЛЬНОЕ ФОСФОРИЛИРОВАНИЕ
Большая часть энергии, высвобождаемой при окислении жирных кислот, аминокислот и углеводов запасается в виде восстановительных эквивалентов никотинамидадениндинуклеотида (НАДН Н+) и флавинадениндинуклеотида (ФАДН2), которые поставляются в дыхательную цепь для преобразования энергии химических связей в энергию электрохимического потенциала при прохождении восстановительных эквивалентов (Н+ и е-) по цепи переноса электронов. Энергия электрохимического потенциала затем вновь преобразуется в химическую энергию макроэргических связей АТФ в процессе окислительного фосфорилирования.
Организация дыхательной цепи в митохондриях. Движущая сила процесса переноса электронов
В состав внутренней мембраны митохондрий входит кардиолипин (менее полярный липид, чем другие мембранные липиды), поэтому мембрана проницаема только для малых незаряженных молекул, непроницаема для заряженных молекул (особенно для ионов Н+) и содержит специальные переносчики для неорганического фосфата, АДФ, АТФ, аминокислот, жирных кислот, ди- и трикарбоновых кислот и их производных.

214
Компоненты цепи переноса электронов и ферменты окислительного фосфорилирования АДФ также локализованы во внутренней мембране митохондрий ( 20-25 % всех белков внутренней мембраны митохондрий).
Компоненты дыхательной цепи в основном являются сложными интегральными белками, коферменты которых могут участвовать в обратимых окислительно-восстановительных реакциях. Они располагаются последовательно в порядке возрастания восстановительных потенциалов. Атомы водорода или электроны перемещаются по цепи от более электроотрицательных компонентов к более электроположительному кислороду. Главная дыхательная цепь в митохондриях начинается от НАДзависимых дегидрогеназ, проходит через флавопротеины и цитохромы и заканчивается молекулярным кислородом. Не все субстраты связаны с цепью переноса электронов через НАД-зависимые дегидрогеназы, некоторые связаны с флавопротеиновыми дегидрогеназами, которые в свою очередь связаны с цитохромами дыхательной цепи.
Белки, участвующие в транспорте электронов ассоциированы в комплексы I, II, III и IV.

|
|
|
215 |
|
A |
|
AH |
|
|
|
|
2 |
|
|
ФАДН |
|
ФАД |
комплекс II |
|
2 |
(сукцинатдегидрогеназа) |
|||
|
|
S S-H2
|
|
|
+ |
|
|
2 Fe |
+3 |
|
+2 |
|
+3 |
|
+ |
+ |
|
НАДНН |
ФМН-Fe-S |
Ко-QH2 |
|
|
2Fe |
|
|
||||||||
|
|
2Fe |
2Cu |
1/2O +2H |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
флавопротеин и |
|
2 цит b и |
цит c |
|
цит c |
|
цит aa |
|
|
||
|
|
|
|
Fe-S-белки |
|
Fe-S-белок |
1 |
|
3 |
|
|||||
|
|
|
|
|
|
|
|
|
|
||||||
НАД |
+ |
ФМН Н -Fe-S |
Ко-Q |
2 Fe |
+2 |
+3 |
+2 |
+2 |
|
||||||
|
H O |
||||||||||||||
|
2 |
|
|
|
|
2Fe |
|
2Fe |
|
2Cu |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
-0,32 В |
-0,25 В |
+0,02 В |
+0,03 В |
+0,22 В |
+0,24 В |
+0,39 В |
+0,82 В |
||||||||
|
|
|
|
комплекс I |
|
комплекс III |
|
|
|
комплекс IV |
|||||
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
(НАДН-дегидрогеназа) |
(убихинолдегидрогеназа) |
(цитохромоксидаза) |
||||||||||
S-H |
2 |
: пируват, 2-оксоглутарат, 3-гидроксибутират, глутамат, изоцитрат, малат, |
|||||||||||||
|
|
глутамат, 3-гидроксиацил-КоА, пролин |
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
||||||
AH |
|
|
: сукцинат, ацил-КоА, глицерол-3-фосфат, холин |
|
|
|
|
|
|
||||||
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Рис. |
Компоненты дыхательной цепи митохондрий. |
|
|
|
|
|
|||||||||
|
ФМН - флавинмононуклеотид, Ко-Q - убихинон, цит - цитохромы, |
||||||||||||||
|
Fe-S - железо-серный белок. |
|
|
|
|
|
|
|
|
|
|
||||
Комплекс I (НАДН:КоQ-оксидоредуктаза) представляет собой НАДНдегидрогеназу с кофактором ФМН и негемовые белки, в состав которых входят железо-серные центры. Комплекс I способен катализировать перенос атомов водорода (Н+ и е-) от НАДН на убихинон. Е0` 0,35 В для этого переноса, соответственно G0` 67 кДж/моль. Этого вполне достаточно для синтеза АТФ.
Комплекс II (сукцинат:КоQ-оксидоредуктаза с коферментом ФАД) известен как сукцинатдегидрогеназа. Е0` 0,05 В для этого переноса, соответственно G0` 9.6 кДж/моль. Этого недостаточно для синтеза АТФ.
Кофермент Q - (убихинон) малый мобильный переносчик атомов водорода. КоQ гидрофобен в окисленном и восстановленном состоянии и легко диффундирует в липидном слое мембраны, передавая только электроны комплексу III.
В комплекс III (убихинолдегидрогеназу) входят цитохромы b, цитохром с1 и железо-серный белок Риске. При переносе электронов через комплекс III наблюдается второй скачок потенциала.
Электронным переносчиком от комплекса III на комплекс IV является самый маленький цитохром - цитохром с.
Комплекс IV (цитохромоксидаза) содержит цитохромы а, а3 и медьсвязывающие белки, в которых ион меди меняет степень окисления (Cu+ Cu2+), передавая электроны на молекулярный кислород О2. На этом этапе - третий скачок потенциала. Цитохромоксидаза имеет очень высокое сродство к О2 и функционирует с максимальной скоростью пока есть хоть небольшое количество кислорода в ткани. Эта реакция необратима и определяет направление переноса электронов на кислород. О2 - конечный акцептор электронов, превращается в Н2О - конечный продукт восстановления.

216
O |
+ |
+ e |
- |
OH |
+ |
|
- |
OH |
|
H |
|
|
+ e |
|
|||
|
|
|
|
|
H |
|
|
|
O |
+ |
+ e |
- |
O |
+ |
|
- |
OH |
H |
|
H + e |
|
|||||
хинон |
|
|
|
семихинон |
|
|
|
хинол |
(убихинон) |
|
|
|
|
|
|
|
(убихинол) |
Нормальное окисление НАДН и сукцината всегда двух электронная реакция с переносом двух атомов водорода (Н+ и е-) на флавин. В отличие от НАДН и сукцината флавины и КоQ могут участвовать в одно- и двух электронных реакциях, приводящих к образованию восстановленного хинола, окисленного хинона и промежуточной формы - семихинона.
Способность флавинов и КоQ образовывать семихиноновые промежуточные соединения является ключевым моментом в электронном транспорте в митохондриях, т.к. эти кофакторы связывают обязательные двух электронные реакции НАДН и сукцината с обязательными одноэлектронными реакциями в цитохромах.
Цитохромы - это сложные белки, содержащие в качестве простетической группы гем. В отличие от гемоглобина и миоглобина гемовое железо цитохромов обратимо меняет степень окисления (Fe2+ Fe3+).
Окислительное фосфорилирование
Свободная энергия, доступная в результате переноса двух электронов от НАДН и сукцината соответственно составляет 238 и 150 кДж/моль соответственно. На синтез одного моль АТФ расходуется 31 кДж/моль энергии. Синтез АТФ из АДФ сопряженный с процессом переноса электронов по дыхательной цепи и катализируемый интегральным белком - АТФ-синтазой, называется окислительным фосфорилированием. Суммарный процесс можно представить в следующем виде:
АДФ + Фн + энергия АТФ + Н2О Сопряжение происходит при участии внутренней мембраны
митохондрий.

217
