
1318
.pdf
181
Рис. 4.27. Изменение теплопроводности стали в зависимости от содержания добавок к ней
Стр. 181 |
ЭБ ПНИПУ (elib.pstu.ru) |

182 4. По номограмме (см. рис. 4.19) определим:
С1 = 12, |
С2 = 13,2. |
|||||
Отсюда по формуле (4.4) λ |
2 |
= λ |
1 |
C2 |
= 0,09913,2 = 0,109 Вт/(м·К). |
|
C |
||||||
|
|
12 |
||||
|
|
|
|
1 |
|
|
Ответ. Теплопроводность жидкого н-пентана равна 0,109 Вт/(м·К). |
||||||
Пример 4.3. Вычислить теплопроводность 32%-ного раствора NaNO3 |
||||||
при 393 К, если его плотность 1243 |
кг/м3, плотность воды 998 кг/м3, |
|||||
теплопроводность воды 0,599 Вт/(м·К).
Решение.
1. Определим объемную долю соли в растворе по уравнению (4.9):
x =1 − (100 −32) 1243 = 0,153, или 15,3 об.%. 100 998
Потабл. 4.6 значение теплопроводности100%-ногораствора NaNO3 λр = 0,69. По номограмме (см. рис. 4.22) определим:
λр = 0,937 .
λводы
Отсюда λр = 0,937·0,599 = 0,561 Вт/(м·К).
Ответ. Теплопроводность 32%-ного раствора NaNO3 равна 0,561 Вт/(м·К).
4.24. Задачи для самостоятельного решения
Задача 4.1. Вычислить теплопроводность заданного газа при давлении P и температуре t. Варианты заданий представлены в табл. 4.7.
Задача 4.2. Вычислить теплопроводность заданной жидкости при давлении P и температуре t. Варианты заданий представлены в табл. 4.8.
Стр. 182 |
ЭБ ПНИПУ (elib.pstu.ru) |
183
|
Варианты заданий к задаче 4.1 |
Таблица 4.7 |
|
|
|
||
|
|
|
|
Номер варианта |
Наименование |
t |
P, МПа |
|
газа |
|
|
1 |
Метан |
53 |
8,0 |
2 |
Этан |
60 |
9,0 |
3 |
Кислород |
81 |
10,0 |
4 |
Этилен |
94 |
10,7 |
5 |
Азот |
52 |
12,0 |
6 |
Аммиак |
53 |
20 |
7 |
Диоксид |
60 |
5 |
|
углерода |
|
|
8 |
Водород |
81 |
50 |
9 |
Метан |
52 |
8,0 |
10 |
Этан |
53 |
9,0 |
11 |
Кислород |
60 |
10,0 |
12 |
Этилен |
81 |
20 |
13 |
Азот |
53 |
5 |
14 |
Аммиак |
60 |
50 |
15 |
Диоксид |
81 |
10,0 |
|
углерода |
|
|
16 |
Водород |
94 |
10,7 |
17 |
Метан |
52 |
12,0 |
18 |
Этан |
53 |
20 |
19 |
Кислород |
60 |
9,0 |
20 |
Этилен |
53 |
10,0 |
21 |
Азот |
60 |
20 |
22 |
Аммиак |
81 |
5 |
23 |
Диоксид |
53 |
50 |
|
углерода |
|
|
24 |
Водород |
60 |
10,0 |
25 |
Аммиак |
81 |
5 |
Стр. 183 |
ЭБ ПНИПУ (elib.pstu.ru) |
184
|
Варианты заданий к задаче 4.2 |
|
Таблица 4.8 |
|
|
|
|
|
|
|
|
|
|
|
Номер варианта |
Наименование вещества |
t |
|
P, МПа |
|
|
|
|
|
1 |
Гексан |
53 |
|
8,0 |
2 |
2-Метилпентан |
60 |
|
9,0 |
3 |
3-Метилпентан |
81 |
|
10,0 |
4 |
2,2-Диметилбутан |
94 |
|
10,7 |
5 |
2,3-Диметилбутан |
52 |
|
12,0 |
6 |
Гептан |
53 |
|
20 |
7 |
2-Метилгексан |
60 |
|
5 |
8 |
3-Метилгексан |
81 |
|
50 |
9 |
3-Этилпентан |
52 |
|
8,0 |
10 |
2,2-Диметилпентан |
53 |
|
9,0 |
11 |
Октан |
60 |
|
10,0 |
12 |
2,2,3-Триметилпентан |
81 |
|
20 |
13 |
2,2,4-Триметилпентан (изооктан) |
53 |
|
5 |
14 |
2,2,3,3-Тетраметилбутан |
60 |
|
50 |
15 |
Нонан |
81 |
|
10,0 |
16 |
н-Пропиловый спирт |
94 |
|
10,7 |
17 |
изо-Пропиловый спирт |
52 |
|
12,0 |
18 |
Тетракрезиолоксисилан |
53 |
|
20 |
19 |
Трихлорэтилен |
60 |
|
9,0 |
20 |
Триэтиламин |
53 |
|
10,0 |
21 |
Хлорбензол |
60 |
|
20 |
22 |
Хлористый этилен |
81 |
|
5 |
23 |
Циклогексан |
53 |
|
50 |
24 |
Четыреххлористый углерод |
60 |
|
10,0 |
25 |
Этилбензол |
81 |
|
5 |
Стр. 184 |
ЭБ ПНИПУ (elib.pstu.ru) |
185
5. ТЕПЛОТА СГОРАНИЯ
Количество тепла, выделяющегося при полном сгорании единицы массы или объема вещества или топлива, называют теплотой сгорания. Эта важнейшая величина характеризует потенциальный запас энергии в топливе и определяет во многом мощность двигателей (или других устройств), в которых используется топливо.
Различают высшую и низшую теплоты сгорания топлив. Высшая теплота сгорания отличается от низшей на величину теплоты полной конденсации водяных паров, образующихся при сгорании углеводородов. В технологических расчетах обычно пользуются низшей теплотой сгорания:
Qн =Qв −2500(9H +W ) , |
(5.1) |
где Qн и Qв – соответственно низшая и высшая теплоты сгорания, кДж/кг; H и W – содержание водорода и растворенной воды в топливе, мас.%.
Если известен элементный химический состав топлива, то его высшую теплоту сгорания легко подсчитать по формуле Д.И. Менделеева:
Qв = 33913C +102995H −10885(S −O) , |
(5.2) |
где Qв – высшая теплота сгорания, кДж/кг,
С, H, S и O – массовые доли в топливе углерода, водорода, серы и кислорода. Существуют также эмпирические формулы, по которым можно приближенно подсчитать теплоту сгорания топлива, если известна его
плотность: |
|
Qв =12400 −2100(ρ1515 )2 , |
(5.3) |
Qн = Qв −5045H , |
(5.4) |
H = 26 −15ρ1515 , |
(5.5) |
100 |
|
где Qн и Qв – соответственно низшая и высшая теплоты сгорания, ккал/кг; ρ1515 – относительная плотность топлива.
Теплота сгорания – величина аддитивная, поэтому если известен углеводородный состав (например, природного или попутного газа), теплоту сгорания можно найти как сумму теплот сгорания этих углеводородов, умноженных на их объемные доли в смеси.
5.1.Теплота сгорания различных видов топлив
Втабл. 5.1 [3, табл. 6.3] приведены значения теплот сгорания различных видов топлив.
Стр. 185 |
ЭБ ПНИПУ (elib.pstu.ru) |
186
Теплота сгорания различных топлив |
Таблица 5.1 |
||
|
|||
|
|
|
|
Топливо |
Низшая теплота сгорания топлива |
||
ккал/кг |
|
ккал/м3 |
|
Дрова |
2800–2980 |
|
- |
Торф |
2150–3760 |
|
- |
Бурый уголь |
2740–3440 |
|
- |
подмосковный |
|
||
|
|
|
|
Каменный уголь |
5450–6950 |
|
- |
Антрацит донецкий |
7350 |
|
- |
Мазут топочный |
9820–10600 |
|
- |
Бензин |
10500–11000 |
|
- |
Керосин |
11000 |
|
- |
Нефть |
10590 |
|
- |
Природный газ с |
11660 |
|
8470 |
содержанием CH4 98 % |
|
||
|
|
|
|
Окись углерода |
2416 |
|
3020 |
Газы заводов СК |
9750 |
|
3760 |
с содержанием H2 74 % |
|
||
|
|
|
|
Водород |
27700 |
|
2570 |
5.2. Теплота сгорания органических соединений
Теплоты сгорания ряда органических соединений приведены в табл. 5.2 [4, табл.18].
|
|
Таблица 5.2 |
Теплоты сгорания органических соединений при 18 оС и P = 1 атм. |
||
Конечные продукты CO2 (газ), H2O (ж), SO2 (газ), N2(газ) |
||
|
|
|
Соединение |
Состояние |
Теплота сгорания, |
|
|
ккал/кмоль |
1 |
2 |
3 |
Углерод |
Графит |
94400 |
Углерод |
Кокс |
97000 |
Окись углерода |
г |
67620 |
Водород |
г |
68310 |
|
Углеводороды |
|
Метан |
г |
212790 |
Этан |
г |
372810 |
Пропан |
г |
530570 |
Бутан |
г |
687940 |
Стр. 186 |
ЭБ ПНИПУ (elib.pstu.ru) |
187
|
|
Продолжение табл. 5.2 |
|
|
|
|
|
1 |
2 |
3 |
|
изо-Бутан |
г |
686310 |
|
Пентан |
г |
845370 |
|
изо-Пентан |
г |
838300 |
|
изо-Пентан |
ж |
844700 |
|
Гексан |
ж |
990600 |
|
Гептан |
ж |
1149000 |
|
Октан |
ж |
1305000 |
|
Этилен |
г |
332000 |
|
Пропилен |
г |
490200 |
|
изо-Бутилен |
г |
647200 |
|
Амилен |
ж |
803400 |
|
Гексилен |
ж |
952600 |
|
Ацетилен |
г |
312000 |
|
Аллилен |
г |
464600 |
|
Триметилен |
г |
496800 |
|
(циклопропан) |
|||
|
|
||
Циклопентан |
ж |
783600 |
|
Циклогексан |
ж |
939000 |
|
Циклогептан |
ж |
1087300 |
|
Бензол |
г |
787200 |
|
Бензол |
ж |
783400 |
|
Толуол |
ж |
936000 |
|
o-Ксилол |
ж |
1093000 |
|
m-Ксилол |
ж |
1089600 |
|
p-Ксилол |
ж |
1089100 |
|
Мезитилен |
ж |
1243,600 |
|
Нафталин |
тв |
1231800 |
|
Дифенил |
тв |
1493600 |
|
Антрацен |
тв |
1605000 |
|
Фенантрен |
тв |
1693000 |
|
Камфен |
тв |
1468000 |
|
|
Спирты |
|
|
Метиловый |
ж |
170900 |
|
Этиловый |
ж |
328000 |
|
Пропиловый |
ж |
428000 |
|
изо-Пропиловый |
ж |
474800 |
|
Бутиловый |
ж |
639000 |
|
Амиловый |
ж |
787000 |
|
Этиленгликоль |
ж |
281000 |
|
Глицерин |
ж |
379000 |
|
Аллиловый |
ж |
442400 |
Стр. 187 |
ЭБ ПНИПУ (elib.pstu.ru) |
188
|
|
|
|
Продолжение табл. 5.2 |
|
|
|
|
|
1 |
|
2 |
|
3 |
|
|
Кислоты |
|
|
Муравьиная |
|
ж |
|
62800 |
Уксусная |
|
ж |
|
208000 |
Пропионовая |
|
ж |
|
365000 |
Масляная |
|
ж |
|
520000 |
Щавелевая |
|
тв |
|
60150 |
Пальмитиновая |
|
тв |
|
2380000 |
Олеиновая |
|
тв |
|
2669000 |
Стеариновая |
|
ж |
|
2698000 |
Гликолевая |
|
тв |
|
166600 |
Молочная |
|
тв |
|
325000 |
Винная (d) |
|
тв |
|
275100 |
Лимонная |
|
тв |
|
474500 |
Бензойная |
|
тв |
|
771840 |
o-Фталевая |
|
тв |
|
771000 |
o-Толуидиновая |
|
тв |
|
928900 |
|
|
Углеводы |
|
|
Глюкоза (декстроза) |
|
тв |
|
673000 |
l-Фруктоза |
|
тв |
|
675000 |
Лактоза |
|
тв |
|
1350800 |
Сахароза |
|
тв |
|
1349600 |
Ацетилцеллюлоза |
|
тв |
|
4496 |
Декстрин |
|
тв |
|
4110 |
Крахмал |
|
тв |
|
4179 |
Целлюлоза |
|
тв |
|
4181 |
|
Другие кислородные соединения |
|
||
Формальдегид |
|
г |
|
134000 |
Ацетальдегид |
|
г |
|
280000 |
Ацетон |
|
ж |
|
427000 |
Метилацетан |
|
г |
|
397700 |
Этилацетат |
|
г |
|
544400 |
Этилацетат |
|
ж |
|
538500 |
Серный эфир |
|
ж |
|
651700 |
Фенол |
|
тв |
|
732000 |
Пирогаллол |
|
тв |
|
639000 |
Амилацетат |
|
ж |
|
1040000 |
Камфора |
|
тв |
|
1411000 |
Стр. 188 |
ЭБ ПНИПУ (elib.pstu.ru) |
189
|
|
|
|
Окончание табл. 5.2 |
|
|
|
|
|
1 |
|
2 |
|
3 |
|
|
Соединения, содержащие азот |
|
|
Мочевина |
|
тв |
|
152000 |
Триметиламин |
|
ж |
|
578600 |
Пиридин |
|
ж |
|
660000 |
1,3,5-Тринитробензол |
|
тв |
|
664000 |
1,4,6-Тринитробензол |
|
тв |
|
620000 |
Нитробензол |
|
ж |
|
739000 |
o-Нитрофенол |
|
тв |
|
689000 |
o-Динитробензол |
|
тв |
|
703200 |
Анилин |
|
ж |
|
812000 |
2,4,6-Тринитротолуол |
|
тв |
|
821000 |
Никотин |
|
ж |
|
1428000 |
|
|
Соединения, содержащие серу |
|
|
Сероводород |
|
г |
|
138380 |
Сероокись углерода |
|
г |
|
130500 |
Сероуглерод |
|
ж |
|
246600 |
Метилмеркаптан |
|
г |
|
297000 |
Диметилсульфид |
|
г |
|
455600 |
Этилмеркаптан |
|
г |
|
452000 |
|
|
Галогенпроизводные |
|
|
Четыреххлористый |
|
г |
|
44500 |
углерод |
|
|
||
|
|
|
|
|
Четыреххлористый |
|
ж |
|
37300 |
углерод |
|
|
||
|
|
|
|
|
Хлороформ |
|
г |
|
96250 |
Хлороформ |
|
ж |
|
89200 |
Хлористый метил |
|
ж |
|
164000 |
Хлористый Этил |
|
г |
|
381800 |
Хлоруксусная кислота |
|
тв |
|
171000 |
5.3. Теплота сгорания реактивных топлив
Для некоторых видов топлив (например, реактивных) теплота сгорания строго нормируется. Поэтому для оперативного определения теплоты сгорания топлив для реактивных двигателей существует расчетный стандартный метод (ГОСТ 10065–75), по которому низшую теплоту сгорания определяют по формуле
Qн = [9940 + (ta + 17,8)K ] 4,1868, |
(5.6) |
Стр. 189 |
ЭБ ПНИПУ (elib.pstu.ru) |
|
190 |
|
где Qн – низшая теплота сгорания, кДж/кг; |
|
|
ta – анилиновая точка топлива, оС; |
|
|
K – коэффициент. |
|
|
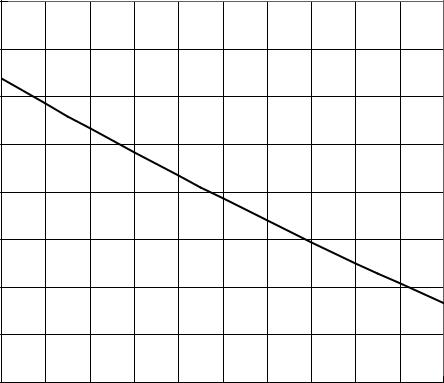
Значения коэффициента K в уравнении (5.6) определяют по прилагаемой |
||
к ГОСТу таблице или графически (рис. 5.1) [8, рис. 3.35]. |
|
|
K |
|
|
7 |
|
|
6 |
|
|
5 |
|
|
4 |
|
|
3 |
|
|
0,75 |
0,8 |
0,85 |
|
|
ρ20 |
|
|
4 |
Рис. 5.1. График для определения коэффициента K к формуле расчета |
||
|
теплоты сгорания |
|
5.4. Теплота сгорания нефтепродуктов
На рис. 5.2 [5, рис. 31; 2, рис. X-7в] представлена зависимость между высшей теплотой сгорания, относительной плотностью ρ1515 и характеристическим фактором K длянефтепродуктовиотдельныхсоставляющихихуглеводородов.
Стр. 190 |
ЭБ ПНИПУ (elib.pstu.ru) |
