
Биомеханика - 2014. Материалы XI Всероссийской конференции с международн
.pdfВсероссийская конференция «БИОМЕХАНИКА – 2014» |
231 |
Действие монафрама на прочность эритроцитарных агрегатов
В норме монафрам не оказывал значимого влияния на прочность эритроцитарных агрегатов – в контрольных и содержащих монафрам образцах крови β составила, соответственно, 23,3 ± 7,9 с–1 и 26,3 ± 9,2 с–1 (н.д.) в случае Нн, а также 43,1 ± 9,0 с–1 и 34,2 ± 9,8 с–1 (н.д.) в случае Нг. Исходное увеличение прочности агрегатов в группе Нг по сравнению с Нн (43,1±9,0 с–1 vs. 23,3 ± 7,9 с–1; p < 0,0004) проявилось лишь при наличии тромбоцитов – в суспензиях эритроцитов группы Нг β достигла 40,6 ± 8,3 с–1 и 41,2 ± 15,3 с–1 в случаях нормального и увеличенного содержания тромбоцитов, но достигала лишь 23,1 ± 7,1 с–1 (p < 0,0004) в плазме без тромбоцитов. Аналогичная нормализация прочности соединения эритроцитов наблюдалась и на уровне парных агрегатов: данные табл. 2 показывают, что и в группе Нн, и в группе Нг пары эритроцитов разъединялись с одинаковой легкостью.
Таблица 2
Действие монафрама на максимально возможную степень разъединения пары эритроцитов оптическими пинцетами (L/D) в норме (Н) и при системной красной волчанке (СКВ) в случае среднестатистически нормальных показателей эритроцитарной агрегации (н) и при гиперагрегации (г)*
L/D |
Нн |
Нг |
СКВн |
СКВг |
Контроль |
0,96 [0,88, 0,99] |
0,97 [0,91, 0,98] |
1,00 [0,88, 1,00] |
0,33 [0,16, 0,97] v & |
Монафрам |
0,98 [0,96, 1,00] |
0,95 [0,81, 0,97] |
0,99 [0,98, 1,00] |
1,00 [0,97, 1,00] ^ |
* СКВг vs. СКВн: vp < 0,004, СКВн vs. Нн: &p < 0,042, «монафрам» vs. «контроль»: ^p < 0,003.
При заболевании даже на уровне отдельных пар клеток, при практическом отсутствии влияния тромбоцитов, эритроцитарные агрегаты пациентов с гиперагрегацией (СКВг) разъединялись хуже, чем в группе СКВн, и это различие нивелировалось в присутствии монафрама (см. табл. 2).
Обсуждение
В наших экспериментах, в отсутствие активации тромбоцитов, ингибитор специфического связывания фибриногена монафрам действовал на соответствующие эритроцитарные рецепторы [6], что подтверждается схожестью его влияния на кинетику (дез)агрегации эритроцитов в крови и эритроцитарных суспензиях с разным содержанием тромбоцитов. Использование не только модельных суспензий, но и цельной крови позволило оценить реальную значимость специфического механизма для эритроцитарной агрегации.
Результаты опытов показывают, что в норме наличие специфического связывания фибриногена может значимым образом ускорять агрегацию эрит-
232 |
Всероссийская конференция «БИОМЕХАНИКА – 2014» |
роцитов без существенного влияния на прочность образующихся агрегатов. Эти данные согласуются с литературными свидетельствами слабости рецепторного связывания фибриногена эритроцитами [6] и позволяют предполагать, скорее, позитивные, чем патологические последствия активации специфического механизма нормальной эритроцитарной агрегации. Аномальному возрастанию прочности эритроцитарных агрегатов у клинически здоровых лиц могут способствовать тромбоциты, хотя механизмы их влияния остаются неясными.
При системной красной волчанке усиление прочности соединения эритроцитов наблюдалось даже в плазме без тромбоцитов, причем прочность агрегатов нормализовалась под действием монафрама, т.е. именно патологическая активация специфического связывания фибриногена эритроцитами приводила к гиперагрегации, которая, как известно, может способствовать развитию самых разных патологических процессов [1].
Таким образом, аномальное возрастание прочности эритроцитарных агрегатов при заболевании и в норме может реализоваться принципиально различным образом – благодаря специфическому компоненту в первом случае и за счет неспецифических процессов – во втором.
Благодарности
Авторы благодарят проф. А.В. Мазурова (ФГУ, Российский Кардиологический научно-производственный комплекс, г. Москва) за предоставление монафрама.
Список литературы
1.Baskurt O.K., Meiselman H.J. Erythrocyte aggregation: Basic aspects and clinical importance // Clin. Hemorheol. Microcirc. – 2013. – Vol. 53. – P. 23–37.
2.Chien S., Jan K. Ultrastructural basis of the mechanism of rouleaux formation // Microvasc. Res. – 1973. – Vol. 5. – P. 155–166.
3.Lominadze D., Dean W. Involvement of fibrinogen specific binding in erythrocyte aggregation // FEBS Lett. – 2002. – Vol. 517. – P. 41–44.
4.Korotaeva V., Firsov N.N. [et al.]. Erythrocytes aggregation in healthy donors at native and standard hematocrit: the influence of sex, age, immunoglobulins and fibrinogen concentrations. Standardization of parameters // Clin. Hemorheol. Microcirc. – 2007. – Vol. 36. – P. 335–343.
5.Khokhlova M.D., Lyubin E.V. [et al.]. Normal and system lupus erythematosus red blood cell interactions studied by double trap optical tweezers: direct measurements of aggregation forces // J. Bio-
med. Opt. – 2012. – Vol. 17. – 025001.
6. Carvalho F.A., Connell S. [et al.]. Atomic force microscopy-based molecular recognition of a fibrinogen receptor on human erythrocytes // ACS Nano. – 2010. – Vol. 4. – P. 4609–4620.
Всероссийская конференция «БИОМЕХАНИКА – 2014» |
233 |
УДК 616:617.58(075.8)
МАТЕМАТИЧЕСКОЕ МОДЕЛИРОВАНИЕ ГЕМОДИНАМИЧЕСКИХ ЭФФЕКТОВ НАРУЖНОЙ КОНТРПУЛЬСАЦИИ
И КАРДИОСИНХРОНИЗИРОВАННОЙ ПОСЛЕДОВАТЕЛЬНОЙ АНТЕГРАДНОЙ ПНЕВМОКОМПРЕССИИ
А.М. Сударев1, 2, 3, Л.Б. Платонова2
1«КОНСТЭЛ»,
Россия, 107076, г. Москва, ул. Стромынка, 19, корп. 2, alexeysudarev@gmail.com
2Московский государственный университет приборостроения и информатики, Россия, 107076, г. Москва, ул. Стромынка, 20 3ИРЭ им. В.А. Котельникова РАН,
Россия,125009, г. Москва, ул. Моховая, д. 11, корп. 7, (495)629-3590.
Ключевые слова: кардиосинхронизированная пневмокомпрессия, облитерирующие заболевания нижних конечностей.
Введение
Целью работы является построение модели усиленной наружной контрпульсации (УНКП) [1] и кардиосинхронизированной последовательной антеградной пневмокомпрессии (КПАПК) [2]. Данные методы эффективны при лечении сердечно-сосудистых заболеваний, в том числе кардиологических и заболеваний артерий нижних конечностей. В УНКП воздействие создается компрессией нижних конечностей с помощью пневматических манжет. Манжеты голеней, бедер и ягодиц последовательно надуваются, создавая ретроградную волну давления крови в артериях, синхронизированную с кардиоциклом так, что ретроградная волна доходит до устья аорты в диастолу, увеличивая коронарный кровоток. Одновременный сдув манжет происходит перед началом систолы, что уменьшает механическую работу сердца. В методе КПАПК последовательность обжатия обратная, создает антеградную волну давления, которая оказывает гемодинамические эффекты в сосудах конечностей, аналогичные влиянию УНКП на коронарные сосуды.
Материалы и методы
Использована 0D-модель сосудистой системы. Для модели использован подход [3], когда гидродинамические параметры сосудов (компартментов) заменяются их электрическими аналогами. По известным параметрам сосудов оценивались гидродинамические параметры сосудов. Так, напрмер: сопротивление R = 8lπµ/A2, инерционность крови (индуктивность) L = 9lρ/4A, комплайнс сосуда (емкость) С = 3lπr3/2Eh, где l – длина сосуда; A – площадь поперечного сечения; µ – вязкость крови; E – модуль Юнга стенки; r – радиус; h – толщина стенки сосуда; ρ – плотность крови.

234Всероссийская конференция «БИОМЕХАНИКА – 2014»
Втаблице приведены эквивалентные единицы измерения. Эквивалентные единицы измерения
Параметр |
Гидродинамическое |
Электрическое |
|
Сопротивление |
10–3 Па с мл–1 |
1 |
Ом |
Комплайнс (емкость) |
103 мл Па–1 |
1 |
Ф |
Инерционность (индуктивность) |
10–3 Па с2 мл–1 |
1 |
Гн |
Масса (заряд) |
133,416 л |
1 |
Кл |
Давление (напряжение) |
1 мм рт. ст. |
1 |
В |
В качестве модели артериального дерева использованы как подробная (30 компартментов) [4], так и упрощенная незамкнутая схема (рис. 1), в которой представлены основные ветви большого круга кровообращения.
Рис. 1. Упрощенная схема артериального дерева
Моделирование воздействия осуществляется с помощью источников внешнего давления (V2 – V4). Левый желудочек представлен в виде конденсатора (С12) с зависящей от времени емкостью аналогично [5]. Для численного моделирования использован программный пакет Microcap 9.
Результаты и их обсуждение
Приведем оценки параметров модели. Основное периферическое сопротивление Rобщ определяется в первую очередь резистивными сосудами
и составляет порядка 160 кОм. Если систолическое и диастолическое давление составляют в норме 120 и 80 мм рт. ст., соответственно, а длительность диастолы τдиаст порядка 0,6 с, то оценка характерного времени релаксации
давления в диастолу τ = Rобщ Собщ составляет порядка 1,5 с, что дает для
Всероссийская конференция «БИОМЕХАНИКА – 2014» |
235 |
||
Собщ |
(емкость |
магистральных артерий) величину порядка |
10 мкФ |
(1,3 |
мл/мм рт. |
ст.). Ударный выброс 70–100 мл (500–700 мкКл) создаст |
|
в системе артерий систолическое увеличение давления порядка 40 мм рт. ст. Для увеличения диастолического давления в аорте при УНКП (на десятки мм рт. ст.) требуется масса крови, поступающая в аорту из артерий ног по порядку величины, близкая к ударному выбросу. Однако значение емкости артерий ног в линейном приближении дает для заряда (объема крови) недостаточные значения. Поэтому, как в работе [6], мы использовали тот факт, что при приближении трансмурального значения давления к нулю сосуды претерпевают коллапс и из них можно «выжать» объем крови, сопоставимый с объемом в расправленном состоянии. Для этого в модели использовали нелинейную зависимость объем (заряд) – трансмуральное давление. В нашей модели не имеет принципиального значения точная форма зависимости, поэтому мы использовали формулу, качественно описывающую эффект кол-
лапса: Q = |
Q0 |
tanh |
U |
|
+1 |
+C U . Заряд сосуда |
Q0 при малых значениях |
|
|
|
|||||||
2 |
|
U0 |
|
|
|
|
||
|
|
|
|
|||||
давлений оценивали из объема сосуда в расправленном состоянии [4]. Сосуды бедер и голени представлены симметричными схемами из двух сопротивлений, зависящих от трансмурального давления для описания эффекта пережатия манжетами.
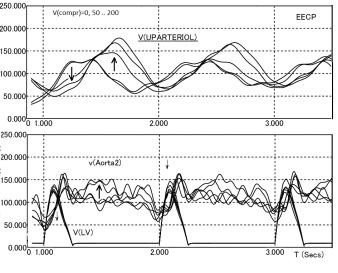
Рис. 2. Гемодинамические эффекты при УНКП

236 |
Всероссийская конференция «БИОМЕХАНИКА – 2014» |
|
Использована модель R = R0 (1+k (Q(C) <Qпорог )), где Q(C) – заряд |
емкости С, Qпорог – заряд сосуда, соответствующий коллапсу; k – коэффици-
ент увеличения сопротивления.
На рис 2 показаны зависимости давления при УНКП в артериолах верхней половины тела (UPARTERIOL) (этот сигнал доступен в измерениях, так как обычно воздействие оценивают по фотоплетизмограмме пальца руки), в аорте (Aorta2) и левом желудочке (LV) при разных значениях давления компрессии (стрелками показаны изменения кривых при изменении давления от 0 до 200 мм рт. ст.). Видно, что эффект диастолического усиления является пороговым. Существенный эффект (усиление в 1,5–2 раза) наступает при давлениях компрессии порядка артериального давления, что соответствует экспериментальным данным. Систолическая разгрузка происходит из-за зарядки емкостей конечностей после сдува манжет.
Исследован эффект усиления кровотока дистальных отделов нижних конечностей (давление в артериолах) (legarter2) в режиме КПАПК (последовательное сжатие бедра–голени) (рис. 3). Как и при УНКП, продемонстрирована нелинейная зависимость эффекта от давления компрессии. Кроме того, сравнивался эффект усиления кровотока в дистальном отделе в режимах КПАПК и УНКП. При КПАПК увеличение давления выше примерно в 1,5 раза, что близко к экспериментальным данным [2]. При КПАПК также исследована зависимость давления крови в аорте и верхней половине тела. В этом случае также наблюдаются положительные эффекты (диастолическое усиление и систолическая разгрузка), однако они меньше, чем при УНКП.
Рис. 3. Гемодинамические эффекты при КПАПК
Предложенная модель качественно описывает основные экспериментально гемодинамические эффекты УНКП и КПАПК, в том числе временные диаграммы, пороговую зависимость усиления кровотока от давления компрессии, зависимость эффекта от последовательности обжатия.
Благодарности
Благодарим д.т.н. А.И. Дьяченко за полезные дискуссии. Работа поддержана грантом РФФИ 13-07-00621.
Всероссийская конференция «БИОМЕХАНИКА – 2014» |
237 |
Список литературы
1.Conti C.R. EECP-Enhanced External Counterpulsation // Journal of the American College of Cardiology. – 1999. – Vol. 33(7). – P. 1841–1842.
2.Сударев А.М. Лечение облитерирующих заболеваний артерий нижних конечностей. Ангиология и сосудистая хирургия. – М.: Ангиология инфо, 2013. – Т. 19(1). – C. 26–32.
3.Noordergraaf A., Jager G.N., Westerhof N. Circulatory Analogy Computer, North-Holland Publishing Co. – Amsterdam, 1963.
4.Avolio A.P. Multi-branched model of the human arterial system // Med. Biol. Eng. Comput. – 1980. – Vol. 18. – P. 709–718 (Модель дерева и параметры артерий).
5.Sagawa K., Suga H., Nakayama K. Instantaneous pressure–volume ratio of the left ventricle versus instantaneous force–length relation of papillary muscle // Cardiovascular System Dynamics. eds. J. Baan, A. Noordergraaf, J. Raines. – Cambridge, MA: M.I.T. Press 1978. – P. 99–105.
6.Ozawa E.T., Bottom K.E., Xiao X., Kamm R.D. Numerical Simulation of Enhanced External Counterpulsation // Annals of Biomedical Engineering. – 2001. – Vol. 29. – P. 284–297.
238 |
Всероссийская конференция «БИОМЕХАНИКА – 2014» |
УДК 616:617.58(075.8)
МЕТОД И АППАРАТУРА КАРДИОСИНХРОНИЗИРОВАННОЙ ПОСЛЕДОВАТЕЛЬНОЙ АНТЕГРАДНОЙ ПНЕВМОКОМПРЕССИИ НИЖНИХ КОНЕЧНОСТЕЙ
А.М. Сударев1, 2, 3, Е.В. Коротич1, 2, 3, П.С. Кантор1, 2, 3, О.И. Усс1, О.Ю. Атьков4, А.М. Зудин4, М.А. Орлова4
1«КОНСТЭЛ»,
Россия, 107076, г. Москва, ул. Стромынка, 19, корп. 2, alexeysudarev@gmail.com
2Московский государственный университет приборостроения и информатики, Россия, 107076, г. Москва, ул. Стромынка, 20 3ИРЭ им. В.А. Котельникова РАН, Россия, 125009, г. Москва, ул. Моховая, д. 11, корп. 7
4Департамент здравоохранения ОАО «РЖД», Россия,107174, г. Москва, ул. Новая Басманная, 2
Ключевые слова: кардиосинхронизированная пневмокомпрессия, облитерирующие заболевания нижних конечностей.
Введение
Целью работы является разработка эффективного метода терапии хронических облитерирующих заболеваний артерий сосудов нижних конечностей (ХОЗАНК). ХОЗАНК встречаются у 2–3 % населения, составляя более 20 % среди сердечно-сосудистых заболеваний. Широко применяемые хирургические и медикаментозные методы не всегда эффективны [1]. Не удивителен сохраняющийся интерес к разработке немедикаментозных методов.
В последнее десятилетие для улучшения коронарного кровотока широко применяется метод усиленной наружной контрпульсации (УНКП) [2]. В этом методе воздействие создается компрессией нижних конечностей с помощью пневматических манжет. Манжеты голеней, бедер и ягодиц последовательно надуваются, создавая ретроградную волну давления крови в артериях, синхронизированную с кардиоциклом так, что ретроградная волна доходит до устья аорты в диастолу, увеличивая коронарный кровоток. Одновременное опорожнение (сдув) всех манжет происходит перед началом систолы, что приводит к уменьшению механической работы сердца. Исследования показали, что гемодинамическое воздействие УНКП производит в организме целую цепочку благоприятных физиологических изменений. Увеличение перфузионного давления, скорости кровотока и напряжения сдвига в коронарных артериях приводит к выбросу вазодилататоров и высвобождению факторов ангиогенеза.
Накопленный опыт в создании аппаратуры и применении УНКП [3] позволил предложить новый метод воздействия для лечения ХОЗАНК – кар-

Всероссийская конференция «БИОМЕХАНИКА – 2014» |
239 |
диосинхронизированную последовательную антеградную пневмокомпрессию (КПАПК) [4]. Он разработан для получения в конечностях гемодинамических эффектов, аналогичных тем, которые создает УНКП в коронарных сосудах.
Материалы и методы
В методе КПАПК с помощью кардиосинхронизированного импульсного компрессионного воздействия создается усиленная антеградная периферическая волна давления крови. Для этого компрессия осуществляется последовательно в проксимальной и затем с задержкой в дистальной зоне. Волна давления способствует усилению скорости кровотока в дистальных областях, увеличению гидростатического давления и напряжения сдвига в сосудах в участках ниже зон воздействия, увеличению перфузии тканей (рис. 1). Уровень давления
вимпульсах компрессии в КПАПК превышает систолическое артериальное давление для полного пережатия подлежащих артерий.
Синхронизация с кардиоритмом эффективно решает одновременно две задачи: усиление кровотока в конечностях и усиление кровотока в миокарде с одновременным уменьшением механической работы сердца. Для этого, аналогично УНКП, сброс давления
вманжетах производится перед систолой, что снижает механическую работу сердца.
В отличие от традиционной ритмической пневмокомпрессии при КПАПК для эффек-
тивного создания волны давления в артериолярном и капиллярном отделах принципиально важна высокая скорость нарастания давления в импульсах компрессии. При длительном времени нарастания рост давления вне зоны сдавливания шунтируется существующими коллатералями и не достигает максимальных значений. Для максимального усиления волны, распространяющейся в антеградном направлении, момент начала обжатия конечности должен быть близок к моменту прохождения естественной пульсовой волны через зону обжатия. В этом случае суперпозиция двух этих волн максимальна. Задержка импульса в дистальной манжете относительно проксимальной должна быть порядка времени распространения пульсовой волны между манжетами.
Оптимальное время начала импульса в проксимальной манжете оцени-
вается следующим образом: tprox = tsys + tprop1, где tsys – момент в промежутке от начала анакроты до систолического максимума давления в районе устья
аорты, а tprop1 – время распространения пульсовой волны от устья аорты до

240 |
Всероссийская конференция «БИОМЕХАНИКА – 2014» |
места наложения проксимальной манжеты. В среднем tsys отстоит от R-пика
ЭКГ на время порядка 0,15–0,2 с. При этом tprop1 = L1/v, где v – скорость пульсовой волны в крупных артериях (4–7 м/с), а L1 – расстояние от устья аорты
до места наложения проксимальной манжеты. Это дает для tprop1 (задержка начала компрессии в манжете бедра относительно R-пика ЭКГ) величину порядка 0,2–0,3 с. Задержка между импульсами давления в проксимальной
и дистальной манжетах составляет tprop2 = L2/v, где L2 – расстояние между манжетами, что для tprop2 дает значение порядка 0,03–0,06 с.
При обжатии проксимальной манжетой образуется и ретроградная волна давления, распространяющаяся в сторону аорты. Для усиления коронарного кровотока (как в УНКП) необходимо, чтобы она достигала устья аорты во
время диастолы. Таким образом, tprox ≥ tdias – tprop1, где tdias – начало диастолы, (порядка 0,3 с), что дает для tprox ограничение не менее 0,15–0,25 с.
Метод реализован на базе комплекса УНКП «КАРДИОПУЛЬСАР» (КОНСТЭЛ, Россия) [3]. Для синхронизации импульсов давления использован сигнал ЭКГ. Для мониторинга изменений кровотока дистальных отделов использован датчик ФПГ, размещенный на пальце ноги. Проведено экспериментальное исследование воздействия нового метода пневмокомпрессии (КПАПК) на систему кровообращения с тем, чтобы оценить открывающиеся перспективы лечения больных ХОЗАНК.
Результаты и их обсуждение
В ходе исследований было отмечено, что во время воздействия происходит увеличение пульсовой волны. Характерное увеличение амплитуды ФПГ по сравнению с исходным уровнем составляет от 2 до 4 раз.
Форма и амплитуда ФПГ в дистальных отделах конечности (рис. 2, 3) может служить сигналом обратной связи для более точной подстройки временной диаграммы воздействия, так как время возникновения и степень фактического сдавливания тканей конечностей манжетами зависит от
Рис. 2. Сигналы ЭКГ и ФПГ до воздействия |
Рис. 3. Сигналы ЭКГ и ФПГ во время |
|
воздействия |
