
- •Для выполнения лабораторных работ
- •Задание 3. Определение триптофана в зерне сельскохозяйственных растений
- •Задание4. Определение аминокислот методом тонкослойной хроматографии (тсх)
- •Задание 7. Определение изоэлектрической точки белков
- •Задание 8. Специфичность действия ферментов
- •Задание 9. Определение оптимальных значений pH для различных ферментов
- •Задание 11. Обнаружение каталазы и пероксидазы в растительных объектах
- •Обнаружение пероксидазы
- •Задание 12. Определение активности тирозиназы
- •Углеводы
- •Задание 16. Свойства моносахаридов и дисахаридов. Ферментативный гидролиз сахарозы
- •Задание 18. Определение сахарозы в сахарной свекле на поляриметре
- •Задание 20. Определение констант жиров
- •Витамины
- •Задание 23. Определение содержания аскорбиновой кислоты в растениях
- •Органические кислоты Задание 24. Определение общей кислотности
- •Задание 25. Определение свободных органических кислот
- •Небелковые азотистые соединения Задание 26. Определение нитратного азота потенциометрическим методом
Задание 7. Определение изоэлектрической точки белков
Оборудование и реактивы: сухие препараты растительных белков; пипетки на 1 мл и 10 мл градуированные; мерные цилиндры на 100 мл; колбы на 100 мл; пробирки в штативах; водяная баня; 0,1 Н р-р CH3COOH; 0,01 Н р-р CH3COOH; 0,5 Н р-р CH3COONa.
В состав белков входят аминокислоты- моноаминодикарбоновые (аспарагиновая, глутаминовая) и диаминомонокарбоновые (аргинин, лизин, гистидин). Первые придают молекулам белков отрицательный заряд, а вторые – положительный. В большинстве белков преобладают остатки аспарагиновой и глутаминовой кислот, поэтому в нейтральной среде молекулы белков заряжены отрицательно.
При подкислении раствора белка постепенно подавляется диссоциация карбоксильных групп, и в определенный момент число положительных и отрицательных зарядов в молекуле оказывается равным. При дальнейшем подкислении раствора число отрицательных зарядов еще больше уменьшается, молекула белка приобретает положительный заряд.
pH раствора, при котором в молекуле белка число положительных зарядов равно числу отрицательных, называется изоэлектрической точкой (ИЭТ). У большинства белков ИЭТ лежит в области 5,5-5,6. Некоторые белки (протамины, гистоны), в составе которых преобладают лизин и аргинин имеют ИЭТ равную 8-9. По величине ИЭТ можно составить некоторое представление об аминокислотном составе данного белка.
Раствор, pH которого равно ИЭТ данного белка, молекулы белка электронейтральны и поэтому легко слипаются и выпадают в осадок. В растворах со значением pH больше или меньше ИЭТ белки имеют соответственно отрицательный или положительный заряд, что препятствует их осаждению.
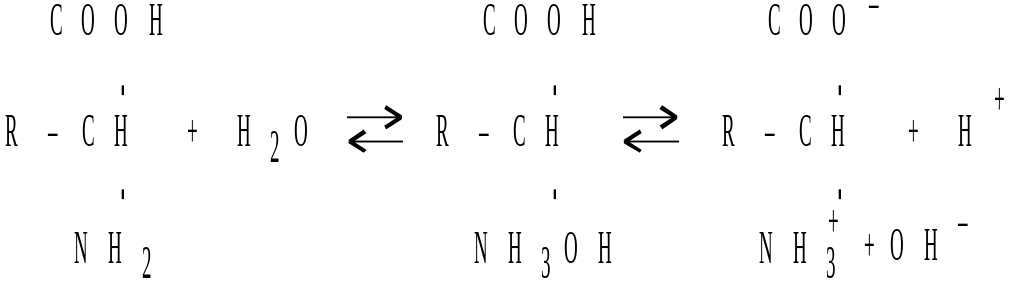

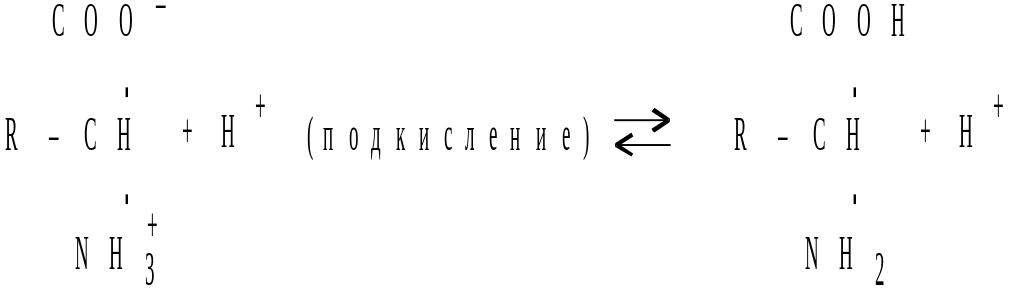
Для определения ИЭТ необходимо найти pH того раствора, в котором белок легко выпадает в осадок.
Ход работы
Отвешивают по 0,1-0,2 г различных белков (лучше использовать подготовленные заранее сухие препараты альбуминов, глобулинов и проламинов). Навески растворяют при слабом нагревании на водяной бане в 5 мл 0,5 н CH3COONa. Раствор доводят водой до 25 мл, тщательно перемешивают и берут по 1 мл его в 8 сухих пробирок. В каждую из этих пробирок вносят соответствующее количество воды и уксусной кислоты, которые указаны в таблице:
Наименование реактива |
№ пробирок и количество реактива, мл |
|||||||
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
Вода |
8.4 |
7.75 |
8.75 |
8.5 |
8.0 |
7.0 |
5.0 |
1.0 |
0,01 Н CH3COOH |
0.6 |
1.25 |
|
|
|
|
|
|
0,1 Н CH3COOH |
- |
- |
0.25 |
0.5 |
1.0 |
2.0 |
4.0 |
8.0 |
Р-р белка |
1.0 |
1.0 |
1.0 |
1.0 |
1.0 |
1.0 |
1.0 |
1.0 |
Величина pH в пробирке |
5.9 |
5.6 |
5.3 |
5.0 |
4.7 |
4.4 |
4.1 |
3.8 |
В растворе, pH которого равен или почти равен ИЭТ данного белка, происходит его осаждение, что легко наблюдать по появлению мути в соответствующей пробирке. Для ускорения осаждения белка можно все пробирки подогреть на водяной бане при 70-800С. Результаты определения записать в таблицу:
Вид белка |
№ пробирки с осадком |
ИЭТ белка |
Альбумины |
|
|
Глобулины |
|
|
Проламины |
|
|
