
- •Общие требования к выполнению и оформлению лабораторных работ
- •Использованные сокращения, термины и понятия
- •Понятия о погрешностях измерений
- •Задание
- •Основные понятия
- •Экспериментальная установка
- •Порядок выполнения работы
- •Протокол наблюдений
- •Обработка экспериментальных данных
- •Результаты обработки экспериментальных данных
- •Вопросы и задания для самоконтроля
- •З адание
- •Основные понятия
- •Экспериментальная установка
- •Порядок выполнения работы
- •Протокол наблюдений
- •Обработка экспериментальных данных
- •Вопросы и задания для самоконтроля
- •Задание
- •Основные понятия
- •Экспериментальная установка
- •Порядок выполнения работы
- •Протокол наблюдений
- •Обработка экспериментальных данных
- •Результаты обработки экспериментальных данных
- •Вопросы и задания для самоконтроля
- •Задание
- •Основные понятия
- •Экспериментальная установка
- •Порядок выполнения работы
- •Протокол наблюдений
- •Обработка экспериментальных данных
- •Результаты обработки экспериментальных данных
- •Вопросы и задания для самоконтроля
- •Задание
- •Основные понятия
- •Экспериментальная установка
- •Порядок выполнения работы
- •Протокол наблюдений
- •Обработка экспериментальных данных
- •Вопросы и задания для самоконтроля
- •Задание
- •Основные понятия
- •Экспериментальная установка
- •Порядок выполнения работы
- •Протокол наблюдений
- •Обработка экспериментальных данных
- •Вопросы и задания для самоконтроля
- •Задание:
- •Основные понятия
- •Экспериментальная установка
- •Порядок выполнения работы
- •Обработка экспериментальных данных
- •Результаты обработки экспериментальных данных
- •Вопросы и задания для самоконтроля
- •Основные понятия
- •Экспериментальная установка
- •Порядок выполнения работы
- •Протокол наблюдений
- •Обработка экспериментальных данных
- •Вопросы и задания для самоконтроля
- •Задание
- •Основные понятия
- •Экспериментальная установка
- •Порядок выполнения работы
- •Протокол наблюдений
- •Обработка экспериментальных данных
- •Вопросы и задания для самоконтроля
- •Отопления
- •Задание
- •Основные понятия
- •Экспериментальная установка
- •Порядок выполнения работы
- •Протокол наблюдений
- •Обработка экспериментальных данных
- •Вопросы и задания для самоконтроля
- •Приложение
- •Библиографический список
- •Оглавление
Задание
Экспериментально определить среднюю объемную изобарную теплоемкость воздуха методом проточного калориметрирования.
По экспериментальным данным вычислить средние массовую, объемную и молярную изобарные теплоемкости воздуха; средние массовую, объемную и молярную изохорные теплоемкости воздуха.
Определить показатель адиабаты воздуха.
Вычислить энтальпию и внутреннюю энергию воздуха при его температуре на выходе из калориметра.
Сравнить полученные данные со справочными.
Составить отчет о выполненной работе.
Основные понятия
Для определения количества теплоты, участвующей в любом процессе, используется понятие теплоемкости, представляющее собой количество теплоты, необходимое для изменения температуры единицы количества вещества в каком-либо термодинамическом процессе на один кельвин.
Теплоемкость
единицы количества вещества называется
удельной. Различают массовую c,
кДж/(кгК),
объемную
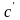 ,
кДж/(м3К)
и молярную μc,
кДж/(кмольК)
теплоемкости. Связь между ними выражается
соотношениями
,
кДж/(м3К)
и молярную μc,
кДж/(кмольК)
теплоемкости. Связь между ними выражается
соотношениями
|
|
(3.1) |
Здесь
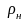 –
плотность газа при нормальных физических
условиях (НФУ), кг/м3,
–
плотность газа при нормальных физических
условиях (НФУ), кг/м3,
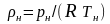 ,
,
где
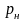 ,
,
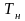 –
давление и температура газа при НФУ
(
–
давление и температура газа при НФУ
(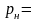 101332
Па,
101332
Па,
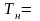 273,15
К); R
– его газовая постоянная, Дж/(кгК);
μ – молекулярная масса, кг/кмоль; 22,416
м3/кмоль
– объем киломоля идеального газа при
НФУ. Для воздуха
273,15
К); R
– его газовая постоянная, Дж/(кгК);
μ – молекулярная масса, кг/кмоль; 22,416
м3/кмоль
– объем киломоля идеального газа при
НФУ. Для воздуха
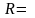 287
Дж/(кгК),
287
Дж/(кгК),
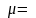 28,97
кг/кмоль и
28,97
кг/кмоль и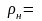 1,293
кг/м3.
1,293
кг/м3.
Теплоемкость
зависит от характера термодинамического
процесса, в котором теплота подводится
к газу или отводится от него. При
экспериментальном определении ее
значения обычно используют два
термодинамических процесса, протекающих
при постоянных объеме (
const)
или давлении (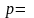 const),
a
теплоемкости этих процессов называют
изохорной
и изобарной
const),
a
теплоемкости этих процессов называют
изохорной
и изобарной
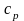 .
Подведенная к газу в изохорном процессе
теплота расходуется только на изменение
внутренней энергии, так как работа
внешняя
.
Подведенная к газу в изохорном процессе
теплота расходуется только на изменение
внутренней энергии, так как работа
внешняя
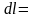 0.
Под внутренней энергией понимают
кинетическую энергию хаотического
движения молекул и атомов, а также
потенциальную энергию сил взаимодействия
между молекулами.
0.
Под внутренней энергией понимают
кинетическую энергию хаотического
движения молекул и атомов, а также
потенциальную энергию сил взаимодействия
между молекулами.
В
изобарном процессе, в отличие от
изохорного, теплота расходуется как на
изменение удельной внутренней энергии,
так и на совершение внешней работы,
поэтому для изменения температуры тела
на 1 К при
const
требуется большее количество теплоты,
чем при
const
и, следовательно,
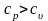 .
Под энтальпией понимают термодинамическую
функцию h
=
.
Под энтальпией понимают термодинамическую
функцию h
=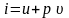 ,
физический смысл которой состоит в том,
что это есть полная энергия расширенной
термодинамической системы.
,
физический смысл которой состоит в том,
что это есть полная энергия расширенной
термодинамической системы.
Внутренняя энергия и энтальпия идеального газа зависят только от температуры и вычисляются по формулам:
|
|
(3.2) |
|
|
|
|
|
(3.3) |
Внутренняя
энергия и энтальпия идеальных газов
принимаются равными нулю при
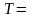 273,15
К. Связь между изобарной и изохорной
теплоемкостями устанавливается
уравнением Майера:
273,15
К. Связь между изобарной и изохорной
теплоемкостями устанавливается
уравнением Майера:
|
|
(3.4) |
Для нормальных физических условий
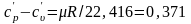 кДж/(м3К),
кДж/(м3К),
где
μR
– универсальная
газовая постоянная,
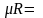 8314,2
Дж/(кмольК).
8314,2
Дж/(кмольК).
Отношение изобарной теплоемкости к изохорной называют показателем адиабаты
|
|
(3.5) |
Используя соотношения (3.4), (3,5) и зная величину k, можно определить:
|
|
|
Теплоемкость газа зависит от температуры. В зависимости от интервала температур различают истинную с и среднюю cm удельные теплоемкости.
Истинной называют теплоемкость, соответствующую бесконечно малому изменению температуры:
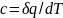
Количество теплоты, необходимое для нагревания единицы количества вещества на один кельвин в некотором интервале температур, называют средней теплоемкостью в этом температурном интервале:
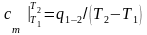 .
.
Для
многих теплотехнических расчетов
зависимость теплоемкости от температуры
принимают линейной
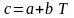 ,
либо выражают степенным полиномом вида
,
либо выражают степенным полиномом вида
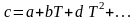 ,
где a,
b,
d
– постоянные, зависящие от природы
газа.
,
где a,
b,
d
– постоянные, зависящие от природы
газа.
Поскольку
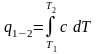 ,
то
,
то
|
|
(3.6) |
где
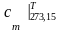 – средняя теплоемкость в интервале
температур от 273,15 К до T
К;
и
– средняя теплоемкость в интервале
температур от 273,15 К до T
К;
и
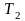 –
граничные температуры интервала, для
которого определяется cm,
К.
–
граничные температуры интервала, для
которого определяется cm,
К.
Теплоемкость идеальных газов зависит от температуры. Величина теплоемкости реальных газов зависит также и от давления, влияние которого при высоких температурах (t > 1000 С) незначительно. У водяного пара при давлениях ниже критического с повышением давления при низких температурах теплоемкость растет медленно, а при высоких быстро увеличивается, достигая
при критической температуре бесконечности. При увеличении давления выше критического с ростом температуры теплоемкость постоянно уменьшается.
Таблицы средней теплоемкости и термодинамических функций воздуха в зависимости от температуры приведены в приложении (табл. 1 и 2).

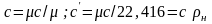 .
.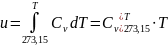
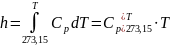
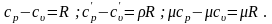
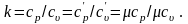
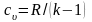 и
и 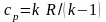 .
.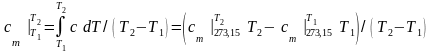 ,
,