
Tomchuk_POSІB_VET_BІOHІMІJa
.pdfзначна частина енергії випромінюється і у видимій та УФ-області оптичного спектра (до 300 нм). Водневі лампи мають спектральну область випромінювання в діапазоні 165–500 нм (з найбільшою енергією випромінювання при довжи-нах хвиль менше 300 нм). Недоліком цих ламп є їх мала потужність. Тому більш ефективними є дейтерієві лампи, особливо в області спектру 250–290 нм. Газорозрядні лампи надвисокого тиску заповнені інертним газом (як правило ксеноном) при електричному розряді дають майже рівномірний спектр.
До оптичних елементів спектральних приладів, зокрема спектрофотометрів, відносяться світофільтри або монохроматори. Світофільтри – це оптичні пристрої, які змінюють спектральний склад світла або енергію світлових хвиль.
Типи світлофільтрів:
адсорбційні – послаблюють світло за рахунок поглинання світлового потоку речовиною фільтра;
дисперсійні – послаблюють світло за рахунок зміни показника заломлення речовини фільтра;
інтерференційні – дія яких заснована на явищі інтерференції паралельного променя, котрий відбивається двома дзеркалами, які розміщені на відстані довжини хвилі.
Монохроматори – оптичні системи, які виділяють вузькі ділянки частот чи довжин хвиль оптичного спектра. Монохроматори характеризує: ширина смуги – діапазон довжин хвиль, в якому інтенсивність світла, яке пройшло через монохроматор, більше половини інтенсивності світла при довжині хвилі максимального піка; ширина щілини – діапазон довжин хвиль, які потрапляють на монохроматор (вхідна щілина) і які виходять з нього і попадають на зразок (вихідна щілина).
Потрібно проводити дослідження при мінімально вузьких щілинах. В серійних спектрофотометрах використовують призматичні монохроматори та з дифракційною граткою або їх комбінацію. Для підвищення роздільної здатності спектрофотометра звичайно в монохроматорах спочатку виділяють певний діапазон спектра за допомогою призми, а потім його розкладають дифракційною граткою, що дозволяє отримати монохроматичне світло.
Роздільна здатність спектрофотометра суттєво підвищується при використанні подвійного монохроматора: тобто якщо в одному приладі розміщують два послідовно з’єднаних монохроматора, у
41
яких вихідна щілина першого служить вхідною щілиною другого. Це дає змогу суттєво послабити розсіяне світло.
Кювети – посудини, які виготовляють з оптично прозорого матеріалу, і в які заливають розчин речовини. Для роботи у видимій ділянці спектра використовують скляні кювети, у ближній УФ-об- ласті – кварцові. Для безперервного аналізу розчинів використовують проточні кювети. Як правило, для роботи використовуються кювети з оптичним шляхом 1 см (поперечний переріз являє собою квадрат з довжиною боку 1 см). Існують і інші кювети з оптичним шляхом 100 мм, 20, 5, 2 і 1 мм.
Приймач випромінювання (детектор) – пристрій, який пере-
творює світлову енергію в електричні сигнали. Для подальшого перетворення та підсилення сигналу використовують помножувачі постійного та змінного струму. Після підсилення сигнал потрапляє на реєструючий пристрій.
У двопроменевих спектрофотометрах (рис. 1.7) промінь від джерела випромінювання за допомогою системи дзеркал спрямовується або у кювету із зразком, або у кювету порівняння. Різниця в світлових потоках розраховується автоматично і відповідає значенню поглинання досліджуваної речовини. Багатопроменеві реєструючи спектрофотометри фіксують зміни поглинання одночас-но при двох (чи більше) довжинах хвиль.
При проведенні вимірювань необхідно враховувати, що найменша похибка вимірювання оптичної густини спостерігається при числовому значенні оптичної густини близько 0,4. При оптичній густині більше 0,8 необхідно використовувати кювети з меншою довжиною поглинаючого шару або розводити досліджуваний розчин. При оптичній густині менше 0,1 – необхідно використовувати кювети з більшою довжиною.
При обчисленні в спектрофотометрії використовують метод градуювального графіка. Готують серію розведень стандартного розчину (Сст), вимірюють їх оптичну густину (Аст), будують графік в координатах Аст – Сст. Потім вимірюють оптичну густину аналізованого розчину і по графіку визначають його концентрацію.
42
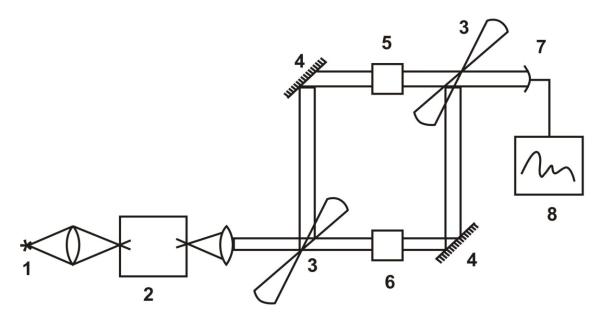
Рис. 1.7. Схема двопроменевого спектрофотометра П р и м і т к а: світло від джерела випромінювання (1)
проходить через монохроматор (2) і розділяється на два пучки обертовим секторним дзеркалом (3); отримані світлові пучки повертаються нерухомими дзеркалами (4), проходять через еталонний і робочий зразки (5 і 6) і, знову, об’єднавшись в один пучок іншим обертовим дзеркалом, потрапляють на фотоприймач (7). Струм фотоелемента підсилюється і отриманий електричний сигнал надходить на реєструючий пристрій (8), який реєструє залежність пропускання або оптичної густини від хвильового числа.
1.3.2. Атомна спектроскопія
Атомно-спектроскопічні методи – це методи аналізу, які засновані на вимірюванні енергетичного стану атомів речовин. Вони відрізняються за способом отримання та реєстрації сигналу, а загальним є необхідність попередньої атомізації проб. Атоми речовин, які випаровуються в полум’ї, випромінюють чи поглинають світло певної довжини хвилі. За інтенсивності смуг у спектрі можна визначити кількість окремих хімічних елементів у зразку.
Атомно-абсорбційна спектроскопія заснована на поглинанні атомами випромінювання від зовнішнього джерела.
Атомно-емісійна спектроскопія заснована на випусканні ви-
промінювання атомами, збудженими за використання різних зовнішніх джерел (дуга, іскра, полум’я, плазма).
43
Атомно-флуоресцентна спектроскопія метод кількісного еле-
ментного аналізу по атомних спектрах флуоресценції. Пробу аналізованої речовини перетворюють на атомну пару і опромінюють для збудження флуоресценції таким випромінюванням, яку поглинає атоми лише елементу, що визначається (довжина хвилі випромінювання відповідає енергії електронних переходів цих атомів). Частина збуджених атомів випромінює світло (аналітичний сигнал), що реєструється спектрофотометрами. Зазвичай використовують резонансну флуоресценцію (довжини хвиль поглиненого і випромінюючого світла однакові). Для атомізації розчинів застосовують полум’я, індуктивно-зв’язану плазму або електротермічні атомізатори (графітові трубки, нитки, стрижні, що нагріваються електричним струмом).
Атомно-абсорбційна (полум’яна) спектрометрія. Метод кількісного елементного аналізу по атомних спектрах поглинання (абсорбції) в полум’ї. Атомні пари проби опромінюють в діапазоні 190–850 нм. У результаті поглинання квантів світла атоми переходять у збуджені енергетичні стани. Цим переходам в атомних спектрах відповідають резонансні лінії, які характерні для даного елемента.
Відповідно до закону Бугера-Ламберта-Бера, мірою концентрації елемента служить оптична густина
A = lg (I0 / I),
де I0 і I – інтенсивності випромінювання від джерела відповідно до і після проходження через поглинаючий шар.
Випромінювання потрапляє на вхідну щілину монохроматора, встановленого таким чином, що виділяється із спектру лише резонансна лінія визначуваного елементу, інтенсивність якої вимірюється фотоелектричним способом. Переведення аналізованого об’єкта в атомізований стан і формування поглинаючого шару пару зазвичай здійснюється в полум’ї. Найбільш часто використовують полум’я сумішей ацетилену з повітрям (2000 °С) і ацетилену з N2O (2700 °С).
Блок-схема атомно-абсорбційного спектрометра представлена на рис. 1.8.
44
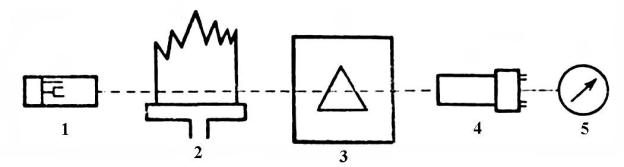
Рис. 1.8. Принципова схема полум’яного атомно-абсорбцій- ного спектрометра. 1 – джерело випромінювання; 2 – полум’я; 3 – монохроматор; 4 – фотопомножувач; 5 – реєструючий прилад
Атомно-емісійна спектроскопія
Атомно-емісійний спектральний аналіз (АЕСА) – це метод елементного аналізу речовини, заснований на вивченні спектрів випускання вільний атомів та іонів у газовій фазі в області довжин хвиль 150–800 нм. Перехід у газову фазу здійснюється за використання різних джерел (дуга, іскра, полум’я, плазма).
Пробу досліджуваної речовини вводять в джерело випромінювання, де відбуваються її випаровування, дисоціація молекул і збудження атомів (іонів). Останні випускають характерне випромінювання, яке надходить в реєструючий пристрій спектрального приладу.
При якісному АЕСА спектри проб порівнюють зі спектрами відомих елементів, наведених у відповідних атласах і таблицях спектральних ліній, і таким чином встановлюють елементний склад аналізованого речовини. При кількісному аналізі визначають кількість (концентрацію) елементу в аналізованій речовині за залежністю величини аналітичного сигналу (щільність почорніння або оптичний щільність аналітичної лінії на фотопластинці; світловий потік на фотоелектричний приймач) цього елементу від його вмісту в пробі.
Збудження атомів відбувається при переході одного або кількох електронів на більш віддалений енергетичний рівень. У не збудженому стані атом має найменшу енергію E0. У збудженому (нестійкому) стані атом може перебувати дуже короткий час (≈10-7– 10-8 с) і завжди прагне зайняти нормальний стан. При цьому атом віддає надлишкову енергію у вигляді випромінювання фотона.
45
Спектральна лінія – випромінювання якоюсь однієї довжини хвилі, що відповідає певному енергетичному переходу збудженого атома. Загальне число атомів прямо пропорційне концентрації (с)
елемента в пробі. Таким чином, інтенсивність емісійної спектраль-
ної лінії може бути використана як аналітичний сигнал для визначення концентрації елемента:
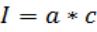 ,
,
де a – коефіцієнт, що залежить від умов процесу.
Чутливість і точність АЕСА залежать головним чином від фізичних характеристик джерел збудження спектрів – температури, концентрації електронів, часу перебування атомів в зоні збудження спектрів, стабільності режиму джерела і т. д.
Атомно-емісійна спектроскопія з індуктивно-зв’язаною плазмою. Суть такого методу полягає в тому, що при збудженні та іонізації з подальшим переходом в стабільний стан елементи випускають квант світла з певною довжиною хвилі. Відповідно, визначаючи довжину хвилі, можна провести якісний аналіз, а визначаючи інтенсивність випускання – кількісний.
Основними вузлами приладу для проведення даного аналізу є: система подачі проби, розпилювач, вузол атомізації проби (кварцовий плазмовий пальник), оптична камера та детектор. Джерелом атомізації і збудження в цьому методі служить індуктивно-зв’язана плазма.
Плазмовий пальник (рис. 1.9) складається з трьох концентричних кварцових трубок, які безперервно продуваються аргоном. Верхня частина пальники поміщена всередину котушки індуктивності високочастотного генератора (зазвичай 27,12 або 40,68 МГц). Високочастотна аргонова плазма ініціюється з допомогою іскрового розряду. При цьому аргон частково іонізується, в ньому виникають вільні носії заряду. Потім в газі ініціюється високочастотний струм, що викликає подальшу лавиноподібнуіонізацію газу. Зважаючи на малий опір плазми вона швидко нагрівається. У центральний канал пальники у вигляді аерозолю надходить розчин проби. У плазмі відбувається висушування проби, дисоціація на атоми, іонізація і термічне збудження.
46
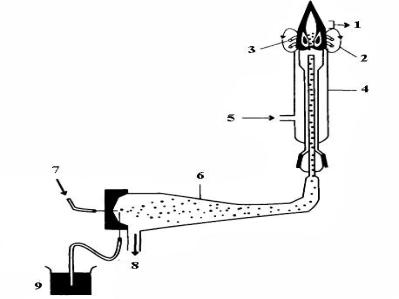
Рис. 1.9. Пристрій плазмового пальника П р и м і т к а:: 1 – зона спостере-ження плазми; 2 – магнітне
поле; 3 – високочастотна котушка; 4 – плазмовий пальник; 5 – плазмоутворюючий газ (Ar); 6 – розпи-лювач; 7 – розпилюючий газ (Ar); 8 – конденсат; 9 – розчин проби.
Перевагою методу є можливість плавно регулювати умови атомізації і збудження, тобто можливо підібрати умови, що забезпечують одночасне визначення безлічі елементів. Недоліком методу є дуже велика витрата аргону. Також потрібно аргон чистотою не менше
99,99 %.
Подальша обробка пучка світла полягає в наступному: через вхідну щілину він надходить в оптичну камеру, де проходить фокусуючі дзеркала, потрапляє на монохроматор. Світло, потрапляючи на монохроматор, розкладається на монохроматичні пучки, які далі проходячи через спеціальну систему лінз потрапляють на детектор. Робочий діапазон − 170–800 нм.
Пробопідготовка та аналіз проб. Всі проби повинні бути пе-
реведені в розчин. Для цього наважку проби масою 0,1–0,5 г (в залежності від природи проби, цільових елементів і їх передбачуваного змісту навішування може відрізнятися) розкладають азотною кислотою при нагріванні або в мікрохвильовій печі. Одержаний розчин при необхідності фільтрується, щоб видалити зважені частки, наявність яких негативно позначиться як на якості аналізу, так і на стані механізмів і деталей приладу.
47
Після описаних процедур проба розбавляється, щоб знизити концентрацію солей і залишки кислоти. По-перше, це необхідно для того, щоб не було зашкалювання, а також для того, щоб уникнути перекривання спектрів випромінювання елементів. По-друге – для того щоб не так швидко руйнувати систему подачі проби і пальник, оскільки нітратна кислота це досить агресивне середовище. Найчастіше рекомендується аналізувати розчини з концентрацією HNO3 (10 -2 М) і нижче.
Аналіз однієї проби зазвичай займає трохи більше хвилини, після чого аналітик отримує спектри всіх виявлених елементів. Витрата − 5–6 см3 проби на один аналіз.
Мас-спектрометрія. Мас-спектрометрія – метод визначення хімічного складу і молекулярної структури речовини, що базується на реєстрації у спектру мас іонів, утворених внаслідок іонізації атомів і (або) молекул проби. Іонізацію здійснюють пучком електронів або іонів, лазерним випромінюванням тощо. Іони розділяють після прискорення в магнітному полі за величиною відношення маси до заряду (m/е). Число хімічних елементів, що одночасно визначаються у природних об’єктах – до 40; одночасно з елементним складом (з точ-
ністю до 1 % при наявності стандартних зразків). Абсолютна границя виявлення: 10-10–10-19 г.
Істотна відмінність мас-спектрометрії від інших аналітичних фізико-хімічних методів полягає в тому, що оптичні чи деякі інші методи детектують випромінювання (поглинання) енергії молекулами або атомами, а мас-спектрометрія безпосередньо детектує самі частки речовини. Мас-спектрометрія належить до найінформативніших методів і відрізняється високими аналітичними характеристиками, дозволяє провести аналіз твердих, рідких і газоподібних речовин.
Іони бувають однозарядні та багатозарядні. Більшість невеликих молекул при іонізації набувають лише один позитивного або негативного заряду. Атоми здатні набувати більш за один позитивний заряд і лише один негативний. Білки, нуклеїнові кислоти і інші полімери здатні набувати множинних позитивних і негативних зарядів.
Перше, що треба зробити для того, щоб отримати маси-спектр
– перетворити нейтральні молекули і атоми, складові будь-якої органічної або неорганічної речовини, в заряджені частки – іони. Цей процес називається іонізацією і по-різному здійснюється для
48
органічних і неорганічних речовин. Другою необхідною умовою є переведення іонів в газову фазу у вакуумній частині мас-спектро- метра. Глибокий вакуум забезпечує безперешкодний рух іонів усередині мас-спектрометра, а при його відсутності іони розсіються і рекомбінують (перетворяться назад в незаряджені частки). Отримані при іонізації іони за допомогою електричного поля перено - сяться в мас-аналізатор. Там починається другий етап мас-спектро- метричного аналізу – сортування іонів по масах (точніше у відношенні маси до заряду або m/е).
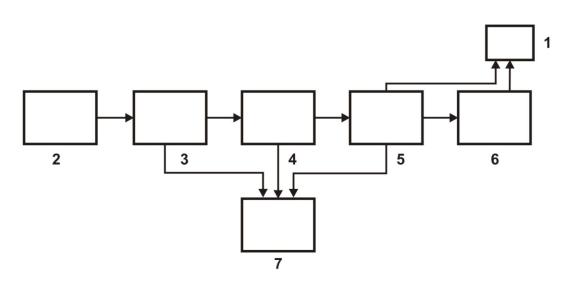
Мас-спектрометр – це вакуумний прилад, що використовує фізичні закони руху заряджених часток в електро-магнітних полях та необхідний для розділення іонів досліджуваної речовини по величинам m/е. Мас-спектральні прилади складаються з системи введення проби (система напуску), іонного джерела, розділюючого пристрою (мас-аналізатора), детектора (приймача іонів), вакуумних насосів, що забезпечують глибокий вакуум у всій вакуумній системі приладу, та системи управління і обробки даних (рис. 1.10).
Рис. 1.10. Блок-схема мас-спектрометра П р и м і т к а: 1 – система управ-ління; 2 – введення проби; 3 –
іонне джерело; 4 – мас-аналізатор; 5 – детектор; 6 – система обробки даних; 7 – система відкачки.
Інтенсивність (амплітуду піків) у мас-спектрі, яка відповідає кількості відповідного іону, виражають, як правило, у відсотках до інтенсивності основного піка (вісь ординат на мас-спектрі). При кількісному визначенні проводять відповідні перерахунки. Мас-
49
спектри різних сполук зібрані в каталоги. Сучасні мас-спектрометри налічують у своїх каталогах 5·105 і більше сполук. Мас-спектр досліджуваної речовини порівнюється з даними каталогу і таким чином встановлюється її структура.
1.3.3. Рефрактометричний метод аналізу
Рефрактометрія – оптичний метод аналізу, заснований на вимірюванні показника заломлення світла (n) речовиною, яку визначають.
Середовище, в якому швидкість розповсюдження світла менша, є оптично щільнішим. При переході променя світла з середовища оптично менш щільного в середовище з більшою оптичною щільністю кут падіння променя більший за кут заломлення.
Абсолютний показник заломлення – відношення швидкості проходження світла у вакуумі до швидкості проходження світла в речовині, що досліджується.
Відносний показник заломлення – відношення швидкості про-
ходження світла в повітрі до швидкості проходження світла в речовині або відношення синуса кута падіння до синуса кута заломлення:
n = v1/v2 = sin α/sin β,
де v1 – швидкість проходження світла в повітрі; v2 – швидкість проходження світла в речовині; α – кут падіння; β – кут заломлення.
Показник заломлення залежить від довжини хвилі світла, температури, агрегатного стану, а також від концентрації речовини і природи розчинника.
Прилади, що використовують для визначення показника заломлення, називають рефрактометрами. Зазвичай вимірювання показника заломлення виконують на рефрактометрах типу Аббе (рис. 1.11, а), дія яких ґрунтується на визначенні кута повного внутрішнього відбиття при проходженні світлом межі між двома середовищами з різними показниками заломлення. Діапазон вимірювання від 1,3 до 1,7, а точність визначення ±2·10–4.
Менш поширені на практиці рефрактометри типу Пульфриха (рис. 1.11, б), дія яких побудована на вимірюванні кута заломлення монохроматичного світла, що забезпечує високу точність визна-
50
