
- •Неорганическая химия теория
- •1. Основные понятия химии: атом, хим. Элемент, молекула, эквивалент, молярная масса эквивалента, относительная атомная масса, моль, молярная масса.
- •2, Основные стехиометрические законы: закон сохранения массы и энергии, закон постоянства состава, закон кратных отношений, закон эквивалентов.
- •3. Основные газовые законы: закон объемных отношений, закон Гей-Люссака, объединенный газовый закон, уравнение Менделеева-Клапейрона.
- •4. Основные классы и номенклатура неорганических веществ: оксиды (солеобразующие и несолеобразующие, основные, кислотные, амфотерные), гидроксиды.
- •5. Основные классы и номенклатура неорганических веществ: кислоты и соли.
- •6. Диссоциация воды, константа диссоциации, pH, ионное произведение воды.
- •7. Развитие учения о строении атома (Модель Томсона, опыты Резерфорда, постулаты Бора), квантово- механическая теория.
- •8. Характеристика основных квантовых чисел: n, m, l, s; строение электронных оболочек атомов.
- •9. Периодическая система элементов, как форма отражения периодического закона.
- •10. Ковалентная химическая связь, способы образования ковалентной связи.
- •11. Геометрия структур с ковалентным типом связей (sp1-, sp2-, sp3- гибридизация).
- •12. Ионная и металлическая связь.
- •13. Водородная связь. Межмолекулярные взаимодействия (Ориентационное взаимодействие, индукционное взаимодействие, дисперсионное взаимодействие).
- •14. Метод валентных связей и метод молекулярных орбиталей.
- •15. Кристаллическое состояние веществ атомные и молекулярные кристаллические решетки. Примеры.
- •16. Химические реакции, скорость химических реакций.
- •17. Влияние температуры на скорость химической реакции, правило Вант-Гоффа.
- •18. Катализ, влияние катализатора на скорость химической реакции.
- •19. Химическое равновесие, принцип Ле-Шателье.
- •20. Внутренняя энергия, энтальпия, энтропия.
- •21. Законы Генри, законы Рауля, закон Дальтона.
- •22. Осмотическое давление, закон Вант-Гоффа.
- •23. Особенности растворов электролитов. Основные положения теории электролитической диссоциации.
- •24. Произведение растворимости, реакция обмена в растворах электролитов.
- •25. Теория овр, важнейшие окислители и восстановители, метод электронного баланса, метод полуреакции.
- •26. Электролиз. Электродный потенциал, водородный электрод.
- •27. Гидролиз солей. Количественные характеристики гидролиза.
- •28. Гальванический элемент и его э. Д. С. Влияние условий на протекание овр.
- •29. Номенклатура и классификация комплексных соединений.
- •30. Характеристика комплексных соединений, константа стойкости и константа неустойчивости.
- •31. Общая характеристика водорода. Физические и химические свойства. Окислительно-восстановительные свойства пероксида водорода.
- •32. Галогены, общая характеристика, свойства простых веществ.
- •33. Галогеноводороды, плавиковая и соляная кислоты.
- •34. Кислородсодержащие соединения галогенов. Оксиды и фторид оксигена.
- •35. Кислородсодержащие соединения галогенов. Гидроксиды и соли.
- •36. Общая характеристика халькогенов. Свойства простых веществ.
- •37. Гидриды халькогенов. Биологическое действие халькогеноводородов.
- •38. Оксиды халькогенов, диоксиды и триоксиды.
- •39. Сернистая, селенистая и теллуристая кислоты.
- •40. Серная, селеновая и теллуровые кислоты.
- •41. Промышленные способы получения серной кислоты.
- •42. Общая характеристика элементов vа группы. Соединения азота, фосфора, сурьмы и висмута в природе.
- •43. Химические свойства элементов vа группы, взаимодействие с простыми веществами. Взаимодействие с водой кислотами и щелочами.
- •44. Оксиды азота (n2o, no, n2o3, n2o5).
- •45. Азотистая кислота и ее соли.
- •46. Бинарные соединения элементов vа группы. Соединения с водородом.
- •47. Гидразин и гидроксиламин. Окислительно -восстановительные свойства.
- •48. Аммиак его получение и свойства. Соли аммония. Нашатырь.
- •49. Азотная кислота. Физические и химические свойства концентрированной и разбавленной азотной кислоты.
- •50. Промышленные способы получения азотной кислоты. Нитраты, разложение нитратов.
- •51. Кислородсодержащие соединения фосфора. Оксиды фосфора (lll и V).
- •52. Кислородсодержащие соединения мышьяка, сурьмы и висмута (lll и V).
- •53. Фосфорная, фосфористая и фосфорноватистые кислоты.
- •54. Гидролиз фосфатов. Показатель кислотности среды.
- •55. Гидроксиды мышьяка, сурьмы и висмута.
- •56. Общая характеристика элементов четвертой а группы. Аллотропные модификации углерода. Строение и свойства кремния.
- •57. Германий, олово, свинец, химические свойства.
- •58. Углерод и кремний, химические свойства.
- •59. Гидриды элементов четвертой а группы. Оксиды углерода.
- •60. Угольная кислота и ее соли. Жесткость воды и способы ее устранения. Карбонатное равновесие в природе.
- •61. Кислородсодержащие соединения кремния. Диоксид кремния.
- •62. Щелочные металлы. Общая характеристика оксидов, гидроксидов и солей. Калийные удобрения.
- •63. Щелочноземельные металлы. Общая характеристика оксидов, гидроксидов и солей. Известь и ее применение.
- •64. Характеристика vib подгруппы. Химические и физические свойства простых веществ. Способы получения хрома, молибдена и вольфрама.
- •65. Соединения трехвалентного хрома. Оксиды и гидроксиды. Применение.
- •66. Соединения шестивалентного хрома. Оксиды и гидроксиды. Применение.
- •67. Подгруппа марганца. Физические и химические свойства простых веществ.
- •68. Окислительно-восстановительные свойства соединений марганца.
28. Гальванический элемент и его э. Д. С. Влияние условий на протекание овр.
Ответ. Гальванический элемент – это устройство, в котором на основе ОВР получают электрический ток. Гальванический элемент состоит из электродов, внешней цепи и электролитического ключа. С физической точки зрения разность электродных потенциалов это - электродвижущая сила гальванического элемента (ЭДС). Поскольку в гальваническом элементе протекает самопроизвольная реакция, т.е. ток вырабатывается, то: E > 0. При этом потенциал катода больше потенциала анода (EК > EА), и в процессе работы гальванического элемента электроны перемещаются от отрицательно заряженного анода к положительно заряженному катоду. Поэтому ЭДС можно рассчитать по формуле:
E = EК - EА |
|
При расчете ЭДС гальванического элемента, составленного из стандартных электродов в формулу необходимо подставлять стандартные значения электродных потенциалов:
E = EК - EА |
|
где E - стандартная ЭДС гальванического элемента. Если же условия работы гальванического элемента отличаются от стандартных, то в формулу необходимо подставлять уравнения Нернста для соответствующих полуреакций. Поэтому в общем виде, для химической реакции: aA + bB = cC + dD. ЭДС (E) можно рассчитать по формуле:
|
|
где E - стандартная ЭДС; [A], [B] и [C], [D] - молярные концентрации исходных веществ и продуктов реакции соответственно; R - универсальная газовая постоянная; F - постоянная Фарадея, T - абсолютная температура, n - число электронов, принимающих участие в элементарной электрохимической реакции. Для более точных расчетов вместо молярной концентрации следует использовать значения активности ионов, принимающих участие в реакции. При экспериментальном измерении ЭДС гальванических элементов применяются специальные методики (например, компенсационный метод) или используют измерительное оборудование, имеющее высокое внутренне сопротивление (например, высокоомные вольтметры). Чем большим сопротивлением будет обладать измерительный прибор, тем меньший ток будет протекать в цепи, тем меньшее влияние будет оказывать поляризация и тем ближе к искомой ЭДС будет показание измерительного прибора. Реальное напряжение (U) гальванического элемента всегда меньше ЭДС из-за поляризации и омических потерь: U = Е - IR - , где I - сила тока; R - омическое сопротивление; - поляризация элемента, равная сумме поляризаций анода и катода. Таким образом, напряжение при разряде зависит от ЭДС элемента т.е. в основном обусловлено: типом и свойствами активных материалов электродов; составом и концентрацией электролита и деполяризатора; поляризацией; омическими потерями и температурой гальванического элемента. По мере работы элемента (разряда) уменьшается концентрация исходных реагентов и увеличивается концентрация продуктов реакции, поэтому в соответствии с уравнением ЭДС элемента уменьшается. Вследствие этого при разряде элемента напряжение его постепенно падает. С ростом же температуры напряжение гальванического элемента, как правило, немного возрастает. Описание работы гальванического элемента. При замыкании цепи под влиянием разности потенциалов в цепи начинает течь электрический ток. Так, катион цинка покидает кристаллическую фазу и переходит в раствор (цинковая пластинка начинает растворяться), а электроны движутся по проводнику по внешней цепи к медной пластинке. При этом электроны могут совершить работу. Обратите внимание: электроны в нашей системе двигаются от цинка к меди, т.е. справа налево, а электрический ток течет наоборот, слева направо, так как за направление электрического тока принято направление движения положительных зарядов. В тот момент, когда ион цинка переходит из пластинки в раствор, в растворе оказывается больше положительных ионов, чем отрицательных (нарушается уравнение электронейтральности), вследствие чего часть анионов соли электролитического ключ мигрирует из геля в раствор соли цинка. Тогда в растворе соли меди также возникает избыток катионов, в результате чего катион меди осаждается на медную пластинку (масса медной пластинки увеличивается), принимая два электрона из внешней цепи.
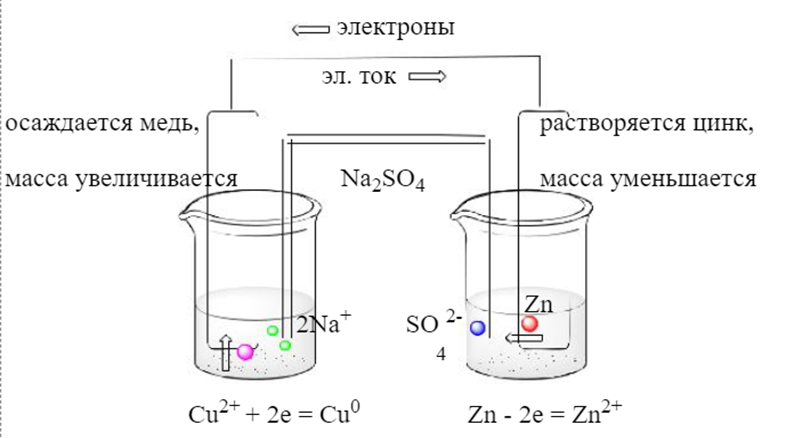 Таким
образом, измерив изменение массы
металлической пластинки, можно сделать
вывод о том, какое количество вещества
израсходовалось (образовалось), а также
определить, какой из электродов был
катодом, а какой – анодом.
Таким
образом, измерив изменение массы
металлической пластинки, можно сделать
вывод о том, какое количество вещества
израсходовалось (образовалось), а также
определить, какой из электродов был
катодом, а какой – анодом.

