
5. Гормоны поджелудочной железы..
Исключительно важное значение имеют инсулин и глюкагон.
Мономерный инсулин состоит из 51 аминокислотного остатка и имеет 2 цепи: одну – короткую ( 21 ам.кисл.остаток) и длинную – 30 аминокитслотных остатка. Эти две цепи соединены двумя дисульфидными мостиками. Инсулин влияет на синтез и распад гликогена в печени и мышцах, синтез жиров в печени и тканях. При дефиците инсулина развивается сахарный диабет.
Глюкагон состоит из 29 остатков аминокислот. Он стимулирует мобилизацию гликогена и жиров в организме, увеличивает концентрацию глюкозы в крови. Таким образом, инсулин и глюкагон – гормоны-антагонисты.
(структуры данных гормонов см. в учебнике «Химия» С.А.Пузаков Стр. 473, 486).
5.Гормоны желудочно-кишечного тракта.
Основная функция этих гормонов – стисуляция работы желудочно-кишечного тракта (ЖКГ).К ним относят – секретин, гастрин,мотилин, энтероглюкагон и др.
Гастрин синтезируется клетками слизистой желудка и представляет собой смесь 3-х молекулярных форм, отличающихся числом аминокислотных остатков в полипептидной цепи. Первичная структура гастрина имеет следующий вид: Глицин-Глицин-Пролин-Триптофан-Метионин- Глутамат- Глутамат- Глутамат- Глутамат- Глутамат- Аланин-Тирозин- Глицин-Тирозин-Метионин-Аспарагин-Фенилаланин.( 17 аминокисл. остатка) Биохимическая роль заключается в стимуляции выделения соляной кислоты из эпителиальных клеток желудка, кроме этого гастрин активирует секрецию пептидаз( ферментов гидролиза белков).
Секретин – пептид, содержащий 27 аминокислотных остатков, синтезируется в двенадцатиперстной кишке и тоже служит активатором секреции пептидаз.
Мотилин – состоит из 22 аминокислотных остатков, синтезируется в слизистой кишечника, выполняет сходные с секретином функции.
Лекция № 13
« Биополимеры важнейших биохимических процессов».
Биополимеры играют огромную роль в жизнедеятельности организма.
Множество физиологических процессов ,происходящих в организме не обходятся без участия биополимеров. Остановимся на некоторых из них.
Порфирины – класс тетрапиррольных макероциклических лигандов, в основе которых лежит молекула порфина :








NH N 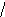
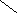

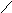

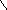


N
HN 

Ярким представителем порфиринов является гемоглобин ( от греч.-
- haimatos –кровь; от лат.-globus-шар). Гемоглобин по строению представляет собой тетрамерный белок, состоящий из 4-х субъединиц, каждая из которых состоит из гема и белковой части глобина, которая содержит около 574 остатков аминокислот. По химической структуре гемм представляет собой макроциклический комплекс железа ( II) с протопорфирином.
(Строение гемоглобина и его производных см. в учебниках«Химия» С.А.Пузаков стр. 286 – 293; «Общая химия» Ю.А.Ерщов, В.А.Попков стр. 280-28, 199, 356). Молярная масса гемоглобина человека приблизительно равна 64500 г/моль. Гемоглобин составляет около 95% сухой массы эритроцитов. Концентрация гемоглобина у мужчин составляет от 13 до 18% от общей массы, а у женщин – от 12 до 16% от общей массы.
Миоглобин – мышечный белок, также является гемпротеином. Он содержит полипептидные цепи глобина, в состав которых входят 153 остатка аминокислот. Важная функция гемоглобина – перенос кислорода из легких к тканям и углекислого газа из тканей к легким:
Hb
+ O2
Hb(O2
)n
n=
1-4

оксигемоглобин
Mb
+ O2
MbO2
оксимиоглобин
Из-за низкой диэлектрической проницаемости среды внутри гемма при взаимодействии с mvjktrekzhysv кислородом степень окисления не меняется, наблюдается ,так называемый ,эффект « белковой защиты», т.е. глобин предохраняет железо со степенью окисления +2 от окисления.
Метгемоглобин- производное гемоглобина, где центр. Атомом является железо (+3). (структуру см. в учебнике «Химия» С.А.Пузаков стр. 331).
Карбоксигемоглобин прочнее оксигемоглобина, блокирует дыхательный центр. Образуется более прочный комплекс гемоглобина с СО по сравнению с комплексом гемоглобин-кислород, т.к. константа нестойкости карбоксигемоглобина в 300 раз меньше, чем константа нестойкости оксигемоглобина.
Схематично гем можно представить так :
Z

N N


Fe(2+)


Z может быть - O2 или СО
N N
N
HC
C
C
H
N
N CH2 - глобин
Цитохромы – дыхательные ферменты белковой природы, простетической группой которых является гем. Они катализируют реакции переноса електронов в дыхательной цепи.(см. в учебниках «Химия» С.А.Пузаков стр. 217; «Общая химия» Ю.А.Ерщов, В.А.Попков стр. 280).
Важным физиологическим аспектом организма является иммунитет.
Иммунитет- обеспечение организмом собственной целостности при химическом воздействии на него.
Антитела( иммуноглобулины-Ig)- группа белков, синтезированных организмом в ответ на попадание в его внутреннюю среду чужеродного вещества.
