
- •Содержание предыдущей лекции
- •Контрольный вопрос
- •Cодержание сегодняшней лекции
- •Принцип исключительности и периодическая таблица
- •Принцип исключительности
- •Принцип исключительности
- •Многоэлектронные атомы
- •Многоэлектронные атомы
- •Принцип исключительности и периодическая таблица
- •Принцип исключительности и периодическая таблица
- •Принцип исключительности и периодическая таблица
- •Принцип исключительности и периодическая таблица
- •Периодическая таблица элементов
- •Периодическая таблица элементов
- •Электронные конфигурации элементов
- •Электронные конфигурации элементов
- •Электронные конфигурации элементов
- •Электронные конфигурации элементов
- •Электронные конфигурации элементов
- •Электронные конфигурации элементов
- •Электронные конфигурации элементов
- •Оптические и рентгеновские атомные спектры
- •Оптические и рентгеновские атомные спектры
- •Оптические и рентгеновские атомные спектры
- •Оптические и рентгеновские атомные спектры
- •Рентгеновские атомные спектры
- •Рентгеновские атомные спектры
- •Рентгеновские атомные спектры
- •Интенсивность
- •Рентгеновские атомные спектры
- •Рентгеновские атомные спектры
- •Спонтанное (самопроизвольное) и вынужденное (индуцированное)
- •Спонтанные переходы
- •Спонтанные переходы
- •Спонтанные переходы
- •Вынужденные переходы
- •Вынужденные переходы
- •Вынужденные переходы
- •Лазеры
- •Лазеры
- •Лазеры
- •Лазеры
- •Лазеры
- •Лазеры
- •Лазеры
- •Применение лазеров
- •Применение лазеров
- •Применение лазеров
- •Применение лазеров
- •Применение лазеров
- •Применение лазеров
- •Применение лазеров
- •Вопрос
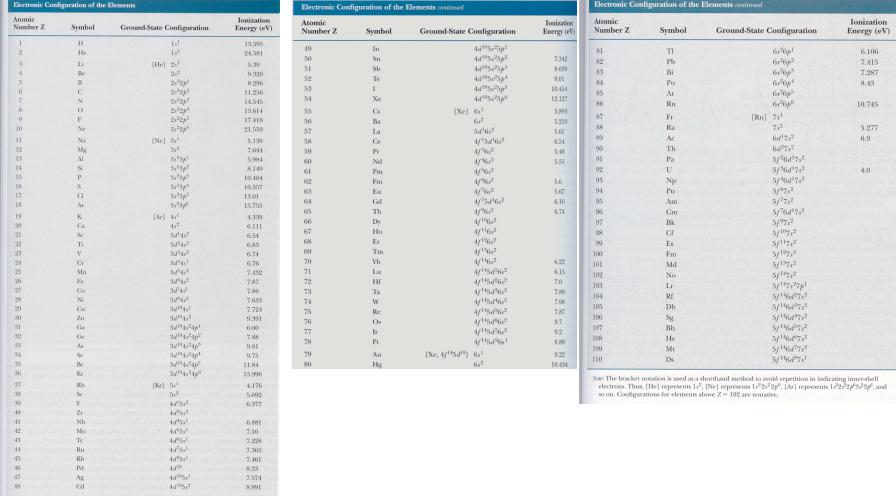
Электронные конфигурации элементов
Возможность объяснения свойств в результате анализа электронных конфигураций химических элементов.
21
Оптические и рентгеновские атомные спектры
22
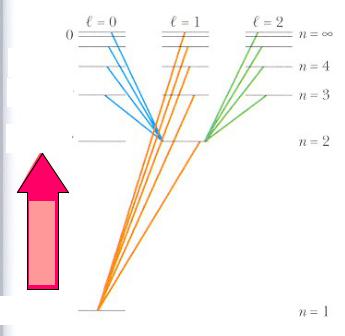
Оптические и рентгеновские атомные спектры
Спектральные линии – результат переходов атома с одних квантовых энергетических уровней на
другие.
-0,8 эВ -1,5 эВ
-3,4 эВ
ЭНЕРГИЯ
-13,6 эВ
Цветные линии - некоторые из разрешенных переходов электронов в атоме водорода.
Разнесение по горизонтали уровней с разными l для каждого слоя.
Запрещенные переходы: l не изменяется.
Диагональные линии - разрешенные переходы между стационарными состояниями.
Правила отбора для разрешенных переходов: l 1 и ml 0, 1.
23
Оптические и рентгеновские атомные спектры
Испускание или поглощение фотона при переходе атома из одного состояния в другое.
Частота фотона f = E/h, E – разница в энергиях между двумя состояниями.
Изменение орбитального момента |
Сохранение орбитального |
атома в результате перехода. |
момента системы «атом-фотон». |
 Обладание фотоном, вовлеченным в процесс перехода, моментом импульса.
Обладание фотоном, вовлеченным в процесс перехода, моментом импульса.
Эквивалентность момента импульса фотона моменту импульса частицы со спином, равным 1.
Обладание фотоном энергией и импульсом.
24
Оптические и рентгеновские атомные спектры
Разрешенные энергии для одноэлектронных атомов и ионов (водород, He+)
E |
k |
e2 |
Z 2 |
|
|
13, 6Z 2 |
эВ. |
|
e |
|
|
n2 |
|
n2 |
|||
n |
2a |
|
|
|||||
|
|
0 |
|
|
|
|
|
|
Многоэлектронные атомы:
экранирование в большой степени положительного заряда ядра Ze
отрицательным зарядом электронов внутренних слоев.
Взаимодействие внешних электронов с эффективным зарядом, меньшим, чем заряд ядра.
|
13,6Z 2 |
|
|
Разрешенные энергии для многоэлектронных атомов En |
эфф |
эВ, |
|
n2 |
|||
|
|
Zэфф – эффективное атомное число.
25
Рентгеновские атомные спектры
Испускание рентгеновских лучей при бомбардировке металлической мишени высокоэнергетическими электронами или любыми другими заряженными частицами.
Интенсивность
, пм
Типичный рентгеновский спектр - широкая непрерывная полоса c наложенными на нее сериями острых максимумов.
Широкая непрерывная полоса - сплошной спектр.
Серии острых максимумов – характеристический рентгеновский спектр.
26
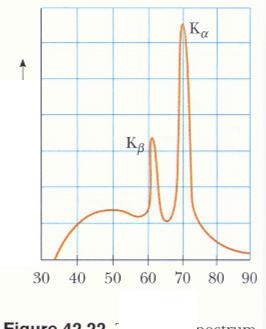
Рентгеновские атомные спектры
Сплошной спектр
Сплошной спектр – результат излучения ускоренным электрическим зарядом.
Интенсивность
Рентгеновские лучи – результат торможения высокоэнергетических электронов при бомбардировке мишени.
|
Потеря кинетической энергии электроном |
|
при взаимодействии с атомами мишени – |
|
от нуля до всего значения. |
|
Непрерывный диапазон длин волн излучения |
|
- от некоторого минимального значения до |
|
бесконечности. |
|
Зависимость минимального значения длины |
, пм |
волны от кинетической энергии электронов. |
|
27
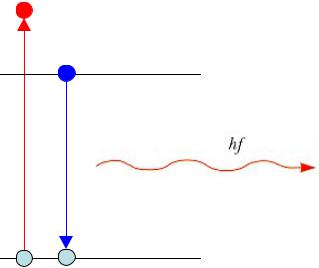
Рентгеновские атомные спектры
Характеристическое излучение
Отсутствие понимания природы характеристических рентгеновских лучей вплоть открытия строения атомов (1908).
Появление характеристического излучения:
результат удаления электрона с внутренних слоев атома мишени электроном, обладающим достаточной энергией.
Заполнение вакансии, появившейся в слое, при переходе электрона с более высокого уровня.
Чрезвычайная малость временного интервала перехода (менее 10-9 сек).
Сопровождение перехода испусканием фотона с энергией, равной разности энергий двух уровней.
Типичная энергия, высвобождаемая при таких переходах, > 1000 эВ.
Длины волн испущенных рентгеновских фотонов - от 0,01 нм до 1 нм. 28
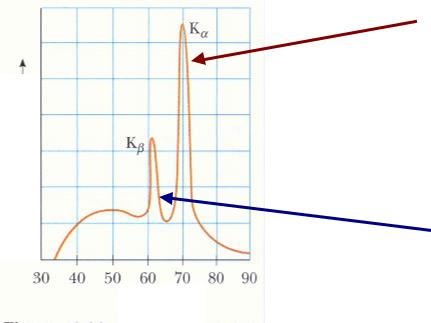
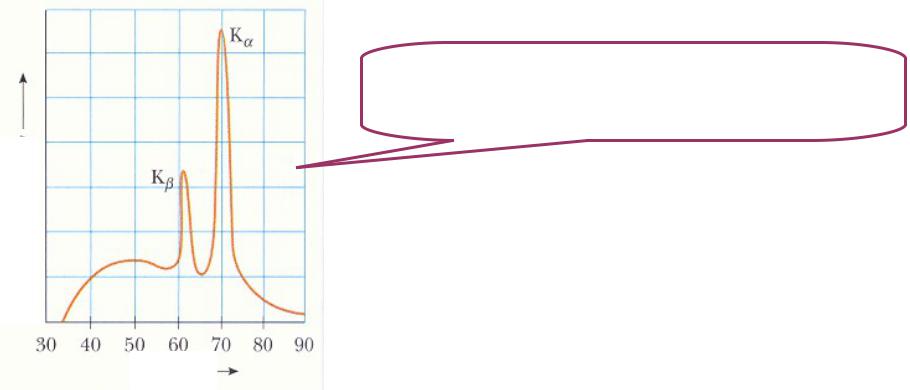
Интенсивность
Рентгеновские атомные спектры
|
Характеристическое излучение |
|
K -линия: испускание фотона при |
|
переходе электрона из слоя |
|
L в слой K. |
|
K - конечный уровень электрона, |
|
- начальный уровень L (первый из уровней, |
|
располагающихся выше конечного). |
|
K -линия: испускание фотона при |
|
переходе электрона из слоя |
, пм |
M в слой K. |
|
Появление характеристических линий L-серии благодаря переходу электрона с более высоких уровней на вакантные места нижележащих уровней в слоях, отличных от слоя K:
L -линия – со слоя M на слой L;
L -линия – со слоя N на слой L.
29

Рентгеновские атомные спектры
График Мозли
1914: Генри Дж. Mозли (1887-1915) - график зависимости зарядового числа Z от 
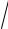 1/
1/
для ряда элементов,
- длина волны K -линии каждого из элементов.
График - прямая линия.
Соответствие результатов расчетов уровням энергии
EK Z 1 213,6 эВ.
30
