
Расследование пожаров / Cheshko - Analiz versiy vozniknoveniya pozhara. Kniga 2 2012
.pdf
Глава 14. Поджоги
порошкообразном или растворенном состояниях, а также нанесенных на поверхности и осажденных на фильтры.
В качестве примера на рис.14.15 представлен спектр остатков после сгорания пирофорного сос-
тава: «KMnO4 + K2Cr2O7 + глицерин».
Рентгенофазовый анализ
Разновидностью рентгеновского анализа является рентгеновский анализ фазового состава вещества. Он также может применяться для обнаружения остатков ЗС.
Рис.14.15. Рентгенофлуоресцентный спектр остатков сгорания состава «K2Cr2O7 + KMnO4 + глицерин» (объект-носитель – древесина)
В основе метода рентгенофазового анализа используется явление дифракции рентгеновских лучей на кристаллической решетке. По полученной дифрактограмме определяют межплоскостные расстояния(d) иотносительныеинтенсивностидлякаждойлинии(I). Дляидентификациивещества сравнивают полученный набор d и I со справочными данными. В программное обеспечение современных рентгеновских дифрактометров входит база данных рентгенофазовых стандартов (эталонных спектров чистых фаз), которая содержит данные о рентгеновских характеристиках большого количества веществ и дает возможность быстро (за несколько минут) определять вещество или группу веществ с соответствующими характеристиками. У разных веществ могут быть совпадающие в пределах точности эксперимента межплоскостные расстояния, но набор межплоскостных расстояний является уникальным, т.е. является «паспортом» вещества.
К достоинству метода относится его «неразрушающий» характер – пробы при анализе сохраняются; к недостаткам – относительно большое количества требуемого для анализа вещества и сложности в расшифровке состава, особенно многокомпонентных смесей. В последнем случае часто требуется сочетание рентгенофазового и элементного анализов.
При рентгенофазовом анализе необходима тщательная пробоподготовка (размер частиц анализируемого вещества должен быть порядка 1-10 мкм). В случае, когда остатки ЗС, привезенные с места пожара, находятся в смеси с частицами объекта-носителя (волокна древесины, кусочки линолеума и т.п.), требуется их разделение, поскольку последние могут существенно исказить дифракционную картину.
На рисунке 14.16 представлена в качестве примера дифрактограмма остатков сгоревшего состава «KClO3 + Mg», снятая на приборе СУР-01 «Реном».
161

И.Д. Чешко, В.Г. Плотников. Анализ экспертных версий возникновения пожара
Идентификация фаз по базе данных позволила установить, что сгорание пирофорного состава прошло полностью – обнаружены фазы, соответствующие исключительно конечным продуктам реакции (хлорид калия, оксид магния):
KClO3 + 3Mg → KCl + 3MgO
О возможностях применения различных рентгеновских методов в исследовании остатков зажигательных средств более подробно рассказано в методическом пособии [64].
Рис.14.16. Фазовый состав остатков сгорания смеси «KClO3 + Mg»
Применение реактивных индикаторных средств в лабораторных условиях
Реактивные средства бывают нескольких видов: рассмотренные выше индикаторные бумаги (РИБ), индикаторные растворы, индикаторные порошки и трубки, таблетки и др.
В качестве реактивных индикаторных средств могут применяться и реактивные индикаторные комплекты (РИК), всоставкоторыхвходяткакбуферныерастворы, такиразличныехимические реагенты. Применение РИК в полевых условиях сопряжено с определенными трудностями, по этой причине целесообразнее их использование в лаборатории.
При помощи РИС возможно обнаружение NO3-, NO2-, Cr2O72-, CrO42-, NH4+, Mn2+, Al3+, H2PO4-, HPO42-, PO43-, Cl-, SO42- и других ионов.
Анализ проводится как с помощью РИС отечественного производства (ЗАО «Крисмас+», г. Санкт-Петербург и др.), так и выпускаемыми зарубежными производителями (фирма «Merсk», Германия и др.).
Обнаружение остатков ЗС при помощи РИС в лаборатории проводится по следующей схеме: часть исследуемого образца растворяется в горячей дистиллированной воде, раствор фильтруется и проверяется при помощи РИБ и РИК на наличие водорастворимых ионов NO3ˉ, NO2ˉ, CrO42-, Cr2O72-, Mn2+, Al3+, NH4+, SO42-. Нерастворившийся в воде остаток растворяется в разбавленной соляной кислоте, после чего раствор исследуется на наличие следов марганца, хрома, меди, железа.
Недостатком метода является применение «мокрой химии» – растворение, фильтрация и т.д. Несомненным достоинством – простота, отсутствие необходимости использования сложных приборов.
Молекулярная спектроскопия в видимой и УФ-области спектра
Методы молекулярной спектроскопии являются при исследовании остатков ЗС менее информативными, нежели методы элементного, фазового, химического анализа. Однако, учитывая наличие в СЭУ ФПС ИПЛ ИК-спектрометров и спектрофлуориметров (с помощью последних можно снимать УФ-спектры), необходимо рассмотреть возможность их использования для решения данных задач.
162

Глава 14. Поджоги
Всостав ЗС входят вещества, имеющие спектры пропускания в видимой и ультрафиолетовой
области. К ним относятся нитраты NO3-, хроматы CrO42-, бихроматы Cr2O72-, перманганаты MnO4-, соединения Fe3+ (Fe2О3). Спектры пропускания в видимой и ультрафиолетовой области имеют и вещества, образующиеся в ходе термического разложения ЗС: нитриты NO2ˉ, соединения Cr3+ (Cr2О3), иодиды Iˉ и др.
Втаблице 14.3. представлены характеристические полосы пропускания перечисленных выше неорганических соединений в водных растворах [58-60].
Исследование остатков ЗС может проводиться на любом современном спектрофлуориметре, обеспечивающим изучение фотометрических характеристик. К таким приборам можно отнести
испектрофлуориметр «Флюорат-02-Панорама», имеющийся в наличии в СЭУ ФПС и экспертных организациях других ведомств.
|
|
|
Таблица 14.3. |
|
|
Характеристические полосы пропускания неорганических соединений, |
|||
|
входящих в состав ЗС и продуктов их химических реакций |
|||
|
|
|
|
|
№ |
Ион |
Положение полосы |
Молярный коэффициент |
|
пропускания, нм |
экстинции, ε |
|||
|
|
|||
|
|
|
|
|
1 |
NO3ˉ |
303 |
7 |
|
194 |
8800 |
|||
|
|
|||
|
|
|
|
|
|
|
354 |
23 |
|
2 |
NO2ˉ |
210 |
5380 |
|
|
|
287 |
9 |
|
|
|
|
|
|
3 |
Cr3+ |
588 |
14 |
|
416 |
15 |
|||
|
|
|||
|
|
|
|
|
4 |
Iˉ |
226 |
12600 |
|
194 |
12600 |
|||
|
|
|||
|
|
|
|
|
5 |
Fe3+ |
714 |
14000 |
|
|
|
|
|
|
6 |
MnO4- |
528 |
240 |
|
|
|
|
|
|
7 |
CrO42- |
370 |
1400 |
|
|
|
|
|
|
8 |
Cr2O72- |
350 (0,9 н. раствор Н2SO4) |
750 |
|
|
|
|
|
|
Вслучае, если поджигающий состав состоит из смеси веществ, имеющих спектры с близко находящимисядругкдругуполосамипропускания, носразнымизначениямимолярныхкоэффициентовэкстинкции, товспектрепропусканияисследуемогосоставаслабыеполосымогутмаскироваться более интенсивными (с наибольшим молярным коэффициентом экстинкции). Это существенно усложняет расшифровку результатов анализа остатков ЗС данным методом.
Впринципе, метод УФ-спектроскопии применим для обнаружения остатков ЗС в случае сохранения в этих остатках даже незначительных количеств водорастворимых ионов, имеющих спектр пропускания в области 200-700 нм, таких как NO3-, NO2-, CrO42-, I-, MnO4-. Но лучше применять его
вкомплексе с другими инструментальными методами (см. ниже)
ИК-спектроскопия
Какизвестно, ИК-спектрвеществасодержитполосыпоглощения, соответствующиеколебаниям определенныхгруппатомов, функциональныхгруппимолекул, входящихвсоставданноговещества и служит его характеристикой. Поэтому спектроскопические данные позволяют идентифицироватьнеизвестныехимическиесоединения. Однакоданныйметодимеетисвоиограничения, связанные со свойством аддитивности, в силу которого спектр смеси нескольких веществ представляет собой наложение спектров входящих в ее состав индивидуальных соединений. Это существенно
163
И.Д. Чешко, В.Г. Плотников. Анализ экспертных версий возникновения пожара
снижает возможность использования спектральных данных для установления природы неизвестных веществ [61].
Обнаружение и исследование остатков ЗС проводят на инфракрасном спектрофотометре с Фурье-преобразованием (например, ФСМ 1201), используя методику приготовления образцов в таблетке с бромидом калия (KBr) [46].
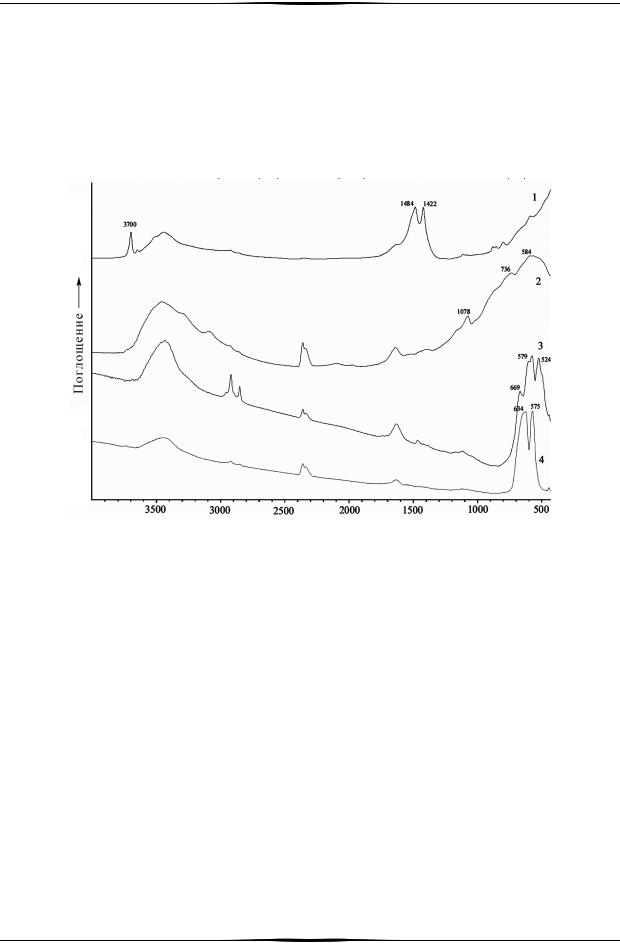
На рисунке 14.17 приведены спектры ряда оксидов металлов, как одних из наиболее вероятных соединений, способных остаться на месте пожара.
ν, см-1
1 – MgO; 2 – Al2O3; 3 – MnO2; 4 – Cr2O3.
Рис.14.17. ИК-спектры некоторых оксидов металлов – продуктов сгорания ЗС
Большинство оксидов имеют широкие полосы поглощения сложной структуры в области ниже 1000 см-1, за исключением MgO, имеющего полосы поглощения при 1422 и 1484 см-1. Все исследованные оксиды имеют широкие полосы поглощения при 3300-3600 см-1, отвечающих валентным колебаниям связей О−Н ассоциированных гидроксильных групп, что может указывать на содержащуюся в соединениях влагу. MgO, помимо этого, имеет полосу поглощения валентных колебаний неассоциированных гидроксильных групп. Это может служить косвенным признаком содержания ввеществепримесигидрооксидамагнияMg(OH)2, иобъясняетсянаибольшейреакционнойспособностью MgO по отношению к воде.
Исходя из приведенного примера, можно полагать, что, если в спектре неизвестного вещества присутствует широкая полоса в области длин волн 900-400 см-1, это может указывать на присутствие в пробе исследуемого вещества соединений класса оксидов.
Наличие в спектре узкой полосы поглощения при 3650-3750 см-1 может указывать на присутствие в пробе гидрооксидов, также являющихся одними из возможных остатков ЗС.
Помимо оксидов, методом ИК-спектроскопии возможно обнаружение и некоторых других компонентов пирофорных составов или их остатков, в частности, солей [56].
Вблагоприятныхслучаях, когданаместепожараудаетсяобнаружитьисходные, неразложившиеся компоненты ЗС, ИК-спектроскопия также может оказать помощь в установлении природы неизвестного вещества. Однако, как правило, в результате пожара исходные окислители и горючее остаются довольноредко, асгоревшиенаместепожараматериалы(древесина, полимерныесоединения, бумага и т.д.), находясь в смеси с остатками ЗС, существенно затрудняют расшифровку ИК-спектров.
164

Глава 14. Поджоги
Ионная хроматография
Для обнаружения ионов ЗС в водных растворах может использоваться ионная хроматография. Современные ионные хроматографы позволяют проводить качественный и количественный анализ неорганических (Cl-, NO3-, NO2-, Br-, SO42-, PO43-, Na+, NH4+, K+, Mg2+, Ca2+, Sr2+, Ba2+ и др.) и органи-
ческих ионов в водных растворах, водах различного происхождения (природных, сточных), а также в водных экстрактах.
Нижнийпределобнаружениянеорганическихионовнаходитсявдиапазоне0,1-1,0 мг/л. Существуютстандартныеметодикикачественногоиколичественногоанализаразличныхкатионовианионов.
Ниже приведены хроматограммы анализа анионов и катионов 2 группы (рис. 14.18, 14.19) в стандартных условиях (концентрация ионов в смесях – 100 мг/л).
Рис.14.18. Хроматограмма смеси анионов
Рис.14.19. Хроматограмма смеси катионов 2 группы
165

И.Д. Чешко, В.Г. Плотников. Анализ экспертных версий возникновения пожара
Методионнойхроматографииприменяют, восновном, дляанализанаиболеераспространенных
вминеральных и сточных водах катионов и анионов. Однако, анализ других ионов, составляющих
основу компонентов ЗС, таких, как CrO42-, Cr2O72-, ClO3-, катионы тяжелых металлов: Mn2+, Cr3+, Pb2+ и др., также возможен.
Метод ионной хроматографии, из всех перечисленных выше методов, наиболее трудоёмок, требует больших затрат времени на подготовку прибора к работе и поддержание его в рабочем состоянии. Поэтому очевидно, что применяется и будет применяться для данных целей он редко, только
влабораториях с соответствующим оборудованием.
Аналитические схемы исследования объектов, содержащих остатки ЗС
Рассмотренные выше химические и инструментальные методы исследования ЗС имеют свои, отмеченныевыше, достоинства, недостаткииопределенныеаналитическиевозможности. Конечно, вэтойсвя- зинаиболееполнуюинформациюопредполагаемомхимическомсредствеподжогапожарно-технический эксперт может получить лишь в случае комплексного использования указанных физико-химических методов. ОднакоредкаялабораторияСЭУФПСимеетполныйкомплексуказанногооборудования. Поэтому разработаныразличныевариантыаналитическихсхем, которыерекомендуетсяприменятьвзависимос- тиотналичиявэкспертныхподразделенияхтехилииныхприборовфизико-химическогоанализа[56].
Наиболее простой вариант предусматривает использование исключительно реактивных индикаторныхсредств(РИС). ЕёреализациявозможнавлюбомСЭУ. ИметькомплектРИС, чтобыпри подозрении в применении ЗС была возможность провести соответствующие исследования, желательно в большинстве СЭУ ФПС.
Более сложные варианты предусматривают применение РИС совместно с элементным анализом; применение РИС совместно с ИК- и УФспектроскопией; исследование методами химического анализа и ионной хроматографии.
Наиболее полная аналитическая схема (рис.14.20) включает сочетание методов химического анализа (РИС), рентгеновского анализа, а также методов молекулярной спектроскопии (ИК-, УФ-спектроскопии) и ионной хроматографии. Применение данных методов в комплексе позволяет обнаруживать широкий спектр пирофорных составов, включающих нитраты, перманганаты, хроматы, бихроматы, минеральные кислоты-окислители, фосфор, серу, соединения тяжелых металлов и т.д.
Уженаначальнойстадииисследования, безспециальнойпробоподготовки, неизвестноевещество, изъятое с места пожара, может в короткие сроки быть проанализировано методами рентгенофлуоресцентной и ИК-спектроскопии на наличие в своем составе элементов, составляющих основу ЗС(К, Ca, Sr, Ba, Zn, Fe, Cu, Mn, Cr, Br, I), атакжеоксидовигидроокисидов. Этопозволяетэксперту определитьстратегиюдальнейшихэкспериментовсиспользованиемметодовхимическогоанализа, УФ-спектроскопии и ионной хроматографии.
Так, имея в распоряжении метод элементного анализа, в частности рентгенофлуоресцентного, можно значительно упростить исследование остатков ЗС. Можно вовсе обойтись без привлечения метода УФ-спектроскопии или применять его в случае неоднозначных результатов химического анализа и ИК-спектроскопии. Метод с использованием РИС также упрощается, отпадает необходимость в окислительном спекании образцов.
Поскольку в некоторых зажигательных составах используются легковоспламеняющиеся и горючие жидкости, целесообразно также привлечение существующих методик по обнаружению на месте пожара остатков ЛВЖ и ГЖ методами флуоресцентной спектроскопии и газо-жидкостной хроматографии [28].
В этой связи перед проведением водной экстракции неизвестного образца проводят его гексановую экстракцию. Водная экстракция же проводится путем растворения пробы в горячей дистиллированной воде. Нерастворимый осадок затем обрабатывается 20% раствором соляной кислоты, определяется наличие ионов Cr3+, Mn2+, Fe3+, Fe2+. Водный экстракт отделяется в делительной
166

Глава 14. Поджоги
воронке от остатков гексанового слоя, проводится определение с помощью РИС присутствия ионов NO3-, NO2-, SO42-, PO43-, Cl-, CrO42-, Cr2O72-, NH4+ и др. На следующей стадии проводится фильтрация водного экстракта и анализ ионного состава инструментальными методами [56].
Рис.14.20. Полная аналитическая схема обнаружения остатков ЗС и установления их природы
167

И.Д. Чешко, В.Г. Плотников. Анализ экспертных версий возникновения пожара
14.10.Компоненты специальных устройств для поджогов
•Остатки емкостей, содержащих ЛВЖ (ГЖ)
•Огнепроводные шнуры (фитили)
•Свечи
•Тлеющие табачные изделия
•Проволочные нагревательные элементы
•Устройства, изготовленные из ламп накаливания
•Остатки радиоуправляемых и программируемых игрушек
Крометрадиционногоразливагорючейжидкостиипримененияспецсоставов, поджигателимогут использовать и более сложные способы поджога и поджигающие устройства. На месте пожара могут оставаться их отдельные фрагменты, следы. Некоторые устройства достаточно технически сложны, некоторые примитивны и, тем не менее, свои функции выполняют. Главная задача таких устройств – задержка времени возникновения горения и обеспечение алиби поджигателю.
На месте пожара целиком устройства для поджога сохраняются редко. Чаще, если и находят, то только отдельные их компоненты. Некоторые из них рассмотрены ниже.
Остатки емкостей, содержащих ЛВЖ (ГЖ)
Стеклянные емкости
Из всех известных средств поджога, содержащих емкости с ЛВЖ (ГЖ), самыми известными во всем мире и распространенными являются бутылки с так называемым «коктейлем Молотова». Он представляет собой разбивающийся стеклянный контейнер с легковоспламеняющейся жидкостью. Зажигание происходит при контакте с горящим фитилем или химическим поджигающим устройством. Максимальный эффект достигается, когда этот контейнер ударяют о твердую поверхность (камень, бетон и т.п.), он при этом разбивается и бензин превращается в паровое и аэрозольное облако. Одновременно это облако поджигается, образуя огненный шар, который очень быстро перемещается (до 10 м/с). Хотя «коктейль Молотова» обычно зажигается от собственного фитиля, достаточно часто поджигатели используют и самовоспламеняющиеся смеси. Например, пакет с сахаром и хлоратом натрия привязывается или приклеивается к бутылке, а серная кислота добавляется в бензин. Когда бутылка разбивается, кислота реагирует с сахаром и хлоратом и в результате происходит вспышка пламени, которая зажигает бензино-воздушную смесь.
Иногда в подобных рецептурах бензин заменяют на описанный выше сгущенный «напалм». Факт применения подобных средств поджога устанавливается относительно легко. Во-первых, остаются осколки от разбитой бутылки, часто обнаруживается разбитое окно, если
бутылкузабрасываличерезнего. Разбитаябутылкаобычнооказываетсянаполу, гдеонаподвергается минимальному воздействию тепла, поэтому и повреждения от огня у нее минимальны.
Вовторых, методами рассмотренными выше, в подразделах 14.5, 14.7, вполне могут быть обнаружены остатки бензина и других светлых нефтепродуктов.
В-третьих, очень уж специфическим является в этом случае возникновение горения (удар, хлопок, огненный шар, мгновенное интенсивное развитие горения), что непременно отметят свидетели, если таковые имелись.
Пластиковые бутылки (контейнеры), наполненныегорючимижидкостями, такжеприменяются при поджогах. Их могут разместить над какими-либо нагревателями, чтобы они расплавились, жидкостьвытеклаивоспламенилась. Ночащетакиебутылкиобкладываютбумагойимусором, которыеподжигаютсядлятого, чтобыемкостьрасплавиласьизагорелосьеесодержимое. Иногдапластиковую емкость, как и стеклянную бутылку, просто забрасывают в разбитое дома или автомобиля.
Конечно, эти контейнеры могут сгореть до такой степени, что идентификация их будет невозможной. Но обычно от них остается какой-то остаток в виде оплавленного и обожженого
168

Глава 14. Поджоги
агломерата. Особенно, если емкость упала на пол. Сам факт наличия такого агломерата в очаговой зоне, например, на полу салона автомобиля, там, где не было ничего подобного до пожара, свидетельствует в пользу версии о поджоге.
Хорошо бы в подтверждение этого обнаружить еще и остатки ЛВЖ; для этого по месту обнаружения остатков емкости и вокруг него целесообразно отобрать пробы хорошо впитывающих жидкости объектов-носителей, например, коврового покрытия пола. Реально, как показывает практика, и сохранение остатков (следовых количеств) бензина внутри полимерного агломерата.
Тонкостенные резиновые и пластиковые емкости.
Один из вариантов применения такого рода «тары» для ЛВЖ (Ж) – использование воздушного шарика или пластикового пакета, содержащего бензин и завязанного бечевкой. Шарик подвешивается над свечкой и раскачивается. Когда колебания прекращаются, шарик останавливается над свечкой, в результате чего в шарике появляется дырка; вылившееся топливо загорается и пожар распространяется на лежащий рядом мусор.
Тут неумелый поджигатель тоже может перестараться. Дж. ДеХаан пишет, что «...Хотя неболь-
шое количество топлива достаточно эффективно, любители часто берут большой мешок для мусора с большим количеством топлива, который, скорее всего, потушит свечу, а не загорится» [2].
Отечественный опыт показывает, что можно обойтись и без раскачивания – тонкая резина, из которой сделан презерватив или воздушный шарик, если их наполнить бензином, через какое-то время неминуемо набухнет, растворится и бензин выльется наружу. Если внизу будет источник зажигания (например, свечка), произойдет загорание.
Аналогичным образом могут быть использованы применяемые в медицине напальчники, тонкие резиновые и пластиковые перчатки.
Известны устройства для поджогов, в которых зажигаемыми материалами являются упомянутые выше «конфетки», спичечные головки, порошковый алюминий, а веществом, инициирующим загорание, концентрированная серная кислота. В этом случае в воздушные шарики или презервативы заливаетсякислота. Принципдействияэтогоустройствасостоитвтом, чтокислотаразъедаетмембрану (тонкую резину) через определенный промежуток времени. Аналогичный принцип реализуется в случае, когдана стеклянную или пластиковую бутылку с кислотой надевают пластиковую перчатку.
Использованиепрезервативапозволяетотсрочитьзажиганиена15-20 минут, апластиковойперчатки обычно от 30 до 40 минут [20].
Вслучаях подобных поджогов, кроме поисков остатков горючей жидкости, имеет смысл иметь
ввидувозможностьобнаружения, вчастности, толстыхколечекотупомянутыхрезинотехнических изделий. Как это ни странно, в относительно «холодных» зонах, на полу, их находили в достаточно жесткихусловияхпожара, чтосвидетельствуетореальнойвозможностисохранениятакихостатков простейших поджигательных устройств.
Огнепроводные шнуры (фитили)
Огнепроводный шнур может применяться при поджогах как средство замедленного действия (как фитиль), как устройство, соединяющее несколько очагов пожара или как средство перемещения пламени в отдаленные места. Есть два основных типа шнуров: пиротехнический, который представляет собой «нитку» из воспламеняемого порошка, обвитую вокруг шнура из бечевки и так называемый «безопасный», в котором «нитка» дымного пороха находится внутри упаковки из бечевки и залита (покрыта) смолой, либо в трубке из водостойкой пластмассы.
Пиротехнический шнур горит открытым пламенем на всем своем протяжении и обугливает и даже зажигает все горючие материалы, с которыми он находится в контакте. «Безопасный» шнур горитоткрытымпламенемтольконаконцах. Хотясмоляноепокрытиебудетплавитьсяитлеть, оболочка останется на месте и повреждения соседним предметам будут минимальны.
Судя по [2], в западных странах пиротехнический шнур, также называемый «хобби-шнуром» или «ракетным шнуром», легко можно купить в магазинах, в то время, как безопасный шнур почти
169

И.Д. Чешко, В.Г. Плотников. Анализ экспертных версий возникновения пожара
всегда продается только организациям, занимающимся взрывными работами. Существует также так называемый «воспламенительный» шнур, у которого сердцевина содержит пиротехнический порошоквоболочкеизпроволоки. «Воспламенительный» шнуриспользуетсятолькоприспециальных взрывных работах, при которых нужна большая скорость и высокая температура горения.
Пиротехнические шнуры имеют разные скорости горения, от 1 см/с до 3 см/с. Безопасные шнуры горят со скоростью от 0,75 до 1 см/с [2],
Иногда, вместообычныхпиротехническихшнуров, поджигателииспользуютшнуротигрушечнойракеты. Обычноэтотшнуримееттемно-зеленыйцветиупакованвпластиковуюилицеллофановуюобертку.
Один метр этого шнура горит от 100 до 150 секунд.
При горении пиротехнического шнура на покрытии пола, лестничных маршей, на горючих предметах может остаться «трейлер» (см. выше раздел 14.4).
От «воспламенительного» шнура остается спираль из проволоки.
Самодельные шнуры. Иногда поджигатели изготавливают огнепроводные шнуры самостоятельно. Наиболее распространенные самодельные шнуры – это веревки (бечевки), пропитанные горючей жидкостью или раствором сильного окислителя.
В последнем случае используют, например, нитрат натрия или калия, а также бечевку или тонкую веревку, сделанную из хлопка, льна, джута, конопли или других растительных волокон.
Свечи
Свечи часто используются как зажигательное устройство замедленного действия. Зажигательные устройства, сочетающие свечи и контейнеры из тонкой резины, описаны выше. Из практики расследования отечественных пожаров известны случаи. когда массовые поджоги
совершалисьспомощьюбутылкисбензином, вкоторуювкачествепробкибылавставленагорящая свеча. Свеча прогорала через определенное время, бензин выливался наружу и загорался.
Еще одно устройство описывается в литературе следующим образом:
«...Сначала разливается топливо, имеющее низкую летучесть, такое как топочный мазут или керосин.
Вмаленькийконтейнерпомещаетсясвечатакимобразом, чтобыонанеупала. Послетого, каксвеча надежно закреплена, вокруг нее и напротив нее размещается ветошь при помощи «дорожек», отходящих от контейнера на расстояние в несколько дюймов. Эти «дорожки» также намочены в горючей жидкостиилежатповерхсмоченногогорючейжидкостьюпола. (Свечуможнонасадитьнагвоздь).
Нельзя использовать жидкости с высокой степенью летучести, такие как бензин, так как его пары могут воспламениться раньше расчетного времени» [20].
Но иногда поджигатель не мудрствует, а просто ставит и зажигает свечку, обложив ее ватой, бумагой и другими легкогорючими материалами.
Свечи обычно не применяются в ситуациях, когда задержка зажигания должна быть менее одного часа. В общем, свечи применяют, когда задержка зажигания должна составлять от одного до восьми часов. Время задержки зажигания зависит от размера и вида свечи.
Свеча – не очень надежное зажигательное устройство. Она может упасть и погаснуть, ее может задутьсквозняком. Поэтомунаместепожарамогутбытьобнаружены«несработавшие» попричине затухания свечи устройства. Поджигатели для надежности иногда устанавливают на месте поджога несколько таких устройств и были случаи, когда на месте пожара находили потухшие, обложенные горючими материалами свечи (см. выше).
На месте пожара могут быть обнаружены и остатки расплавленного парафина или воска. В 90-х годах прошлого века были публикации [62], свидетельствующие о возможности сохранения тяжелых парафиновых углеводородов даже на обугленной древесине, чего не бывает с более легкими, светлыми нефтепродуктами.
Более подробно о свече как источнике зажигания и экспертном исследовании ее остатков – см. выше, главу 4 книги 1.
170
