
- •1. Уровни организации белковых молекул. Структуры белка и их краткая характеристика Ам-к состав белков, пептидная связь и ее физико-химическая характеристика.
- •2. Четвертичная структура белков. Особенности строения и функционирования олигомерных белков на примере гемсодержащих белков - гемоглобина и миоглобина.
- •3. Физико-химические свойства белков и их классификация. Потребность в белках. Азотистый баланс. Белковая недостаточность. Квашиокор.
- •5. Основные свойства белковых фракций крови и значение их определения для диагностики. Методы исследования. Эмбриоспецифические белки и их значение. Энзимо-диагностика.
- •8. Строение нуклеиновых кислот. Азотистые основания и сахара, входящие в состав днк и рнк. Нуклеозиды и нуклеотиды. Адениловые динуклеотиды (над, надф, фад). Денатурация и ренатурация днк(см.10в)
- •9. Вторичная структура днк и рнк. Комплементарность азотистыx оснований.
- •11. Общая характеристика витаминов, классификации, биологическое значение, источники, потребность, а- и гипервитаминозы. Кофакторы и коферменты.
- •12. Витамины и коферменты. Роль флавиновых коферментов.
- •13. Витамин b1(тиамин), его строение и медико-биологическое значение.
- •14. Тиаминпирофосфат, его строение и биологическая роль.
- •15. Биотин и витамин в12(кобаламин, антианемический). Роль этих витаминов в биосинтезах.
- •25. Роль биотина и витамина b12 в клеточном метаболизме.
- •17. Строение фад и его роль в клеточном метаболизме.
- •2 9. Витамины в2 и рр их химическое строение и роль в клеточном метаболизме.
- •30. Витамин а(ретинол, антисерофтальмический), его химическое строение и роль в обмене веществ клеток. Основные пищевые источники витамина а.
- •31. Витамины группы d, их строение и физиологическая роль.
- •3 2.Аскорбиновая кислота. Строение и физиологические функции.
- •34. Витамины е и к, их химическое строение и медико-биологическое значение. Витамин е см.33.
- •35. История открытия и изучения ферментов. Особенности ферментативного катализа.
- •36. Особенности ферментативного катализа. Специфичность действия ферментов. Основные представления о механизме ферментативного катализа.
- •37. Современные представления о механизмах действия ферментов. Мультиферментные комплексы на примере структуры синтазы жирных кислот.
- •42. Регуляция активности ферментов. Различные способы активации и ингибирования ферментов.
- •44. Классификация и номенклатура ферментов. (см.39в) Виды энзимопатологий. Наследственные энзимопатии.
- •45. Строение окисленного и восстановленного над. Важнейшие субстраты над-зависимых дегидрогеназ. Представление о надн-дегидрогеназах и других переносчиках электронов внутренней мембраны митохондрий.
- •47. Различия ферментного состава тканей. Изменения активности ферментов в процессе развития. Изоферменты и энзимодиагностика.
- •48. Различия ферментного состава органов и тканей. Органоспецифичные ферменты. Изменения активности ферментов в процессе развития. Изоферменты и энзимодиагностика.
- •56. Амфиболические функции цикла трикарбоновых кислот.
- •57. Анаболические функции цикла лимонной кислоты. Реакции, пополняющие цитратный цикл.
- •54. Представление о процессах окислительного фосфорилирования. Надн-дегидрогеназа как компонент дыхательной цепи.
- •57. Дыхательная цепь митохондрий, ее строение и основные принципы функционирования. Теории сопряжения окисления и фосфорилирования
- •64. Иерархия регуляторных систем. Место гормонов в системе регуляции метаболизма. Механизмы передачи гормонального сигнала в клетку.
- •67 Гормоны задней доли гипофиза
- •73. Прогестерон, его физико-химическая характеристика и биологические функции
- •80 Краткая характеристика гомо- и гетерополисахаридов. Их биологическое и физиологическое значение.
- •84 Наследственные нарушения обмена моносахаридов и дисахаридов: галактоземия, непереносимость фруктозы, непереносимость дисахаридов.
- •86. Глюкозо-6-фосфат, схема путей его образования и использования в организме.
- •87 Синтез гликогена и гликогенолиз-распад
- •90. Гликогенолиз и его биологическое значение.
- •88. Пути синтеза полисахаридов. Роль утф в синтезе полисахаридов. Регуляция синтеза и распада полисахаридов. Гликогенозы и биохимические механизмы их возникновения.
- •89. Свойства и строение гликогена. Биосинтез гликогена. Мобилизация гликогена и его гормональная регуляция.
- •90, 91 Гликолиз, биологическое значание.
- •93. Анаэробный гликолиз. Гликолитическая оксидоредукция, субстратное фосфорилирование.
- •94. Молочнокислое брожение –
- •95 Метаболические превращения пвк.
- •96. Окислительное декарбоксилирование пвк(см.58-59)
- •99.Глюконеогенез.См.Выше и в метаболизме*
- •112.Классификация липидов. Роль в жизнедеят-ти клетки. Метаболизм липопротеинов, транспорт липидов между органами и тканями. Нарушение обмена липидов при сердечно-сосудистых.
- •124. Окисление ненасыщенных жирных кислот, метаболические особенности этого процесса.
- •129.Фосфолипиды, разновидности, структура, роль в построении биомембран и в формировании их функциональных особенностей(см.121,119).
- •130. Желчные кислоты и их роль в переваривании липидов. Связь с обменом холестерина.
- •133. Биосинтез кефалина и лецитина и их биологическая роль(см.135)
- •134. Биосинтез фосфолипидов и их биологическая роль.
- •135. Биосинтез лецитина и его биологическое значение. Липотропные факторы.
- •136. Строение холестерина и его биологическое значение. Представление о биосинтезе холестерина.
- •138. Представление о биологическом значении и метаболизме холестерина.
- •140. Ресинтез триацилглицеринов в стенке кишечника. Образование хиломикронов и транспорт жиров. Роль аполипопротеинов в составе хиломикронов. Липопротеинлипаза.
- •141. Краткая характеристика липопротеидов крови. Роль апопротеинов в функционировании липопротеидов. Диагностическое значение определения липопротеинов в клинике.
- •142. Хиломикроны, их физико-химическая характеристика и физиологическое значение.
- •144. Кетоновые тела, структура, механизмы образования и окисления. Кетогенез при голодании и сахарном диабете. Резистентность и склонность к кетозу у детей.(см.143).
- •145. Образование кетоновых тел, химизм реакции, биологическое значение. Основные причины их избыточного образования(см.Выше)
- •146. Роль печени в липидном обмене.
- •151. Рекции переаминирования и трансдезаминирования и их значение в метаболизме клеток.
- •164. Метионин и его роль в обмене веществ. S-аденозилметионин, как липотропный фактор.
- •165. Роль лизина и аргинина в клеточном метаболизме.
- •167. Строение днк эукариотических клеток и механизмы, лежащие в основе ее пространственной упаковки. Многообразие азотистых оснований. Функции нуклеиновых кислот в живых организмах.
- •168. Генетический код и его характеристика. Молекулярные механизмы возникновения наследственных болезней. Краткое описание процесса трансляции.
- •170. Синтез белка на рибосомах. Условия необходимые для реализации этого процесса.
- •172. Распад пуриновых оснований. Химизм процесса и его медико-биологическое значение. Подагра.
- •173. Распад пуриновых оснований. Химизм процесса и его медико-биологическое значение. Подагра.(см.172)
- •175. Распад гема. Образование и пути выделение билирубина. Желтухи, диагностика. Характеристика распада гемоглобина в неонатальном периоде. Физиологическая желтуха новорожденных.
- •176. Биосинтез гема и его регуляция. Химизм реакций до порфобилиногена, представление о дальнейших путях синтеза гема. Порфирии.
- •178. Незаменимые факторы питания и их медико-биологическое значение. Необходимость оптимального обеспечения детского организма незаменимыми факторами питания.
- •179. Основные пищевые вещества: углеводы, жиры, белки; суточная потребность, переваривание; частичная взаимозаменяемость при питании.
- •180. Обмен веществ: питание, метаболизм и выделение продуктов метаболизма. Состав пищи человека. Органические и минеральные компоненты. Основные и минорные компоненты.
34. Витамины е и к, их химическое строение и медико-биологическое значение. Витамин е см.33.

Витамин К (нафтохиноны, антигеморрагический).
Ист. Капуста, рябина, шпинат, печень. Синтез.микрофлорой. 3 формы витамина- К1-филлохинон, К2-менахинон, и К3-менадион. Витамин явл.коферментом микросомальных ферментов печени, осущ.гамма карбоксилирование глутаминовой к-ты в составе белковой цепи. Ф-ции: синтез факторов свертывания крови, синтез белков костной ткани.
35. История открытия и изучения ферментов. Особенности ферментативного катализа.
Экспериментальное изучение ферментативных процессов началось в XYIIIв, когда французский естествоиспытатель Р. Реомюр поставил опыты, чтобы выяснить механизм переваривания пищи в желудке хищных птиц. Т. Шванн открыл в желудочном соке фермент пепсин. Эти работы послужили началом изучения так называемых протеолитических ферментов.
Особенности ферментативного катализа.
Ферм. ускоряют хим. р-ции во многие миллионы раз. В ходе р-ции не расход., после р-ции ост. в неизм. виде. сниж. энергию активации катализ. ими р-ции. Энергия акт-ции - эн-я, необх. для перевода всех молекул моля вещ-ва в активированное состояние при данной температуре. т.е. для запуска данной р-ции.
36. Особенности ферментативного катализа. Специфичность действия ферментов. Основные представления о механизме ферментативного катализа.
Этапы катализа:
![]()
1. Присоединение субстрата (S) к ферменту (E) с образованием фермент-субстратного
комплекса (E-S).
2. Преобразование фермент-субстратного комплекса в один или несколько переходных
комплексов (E-X) за одну или несколько стадий.
3. Превращение переходного комплекса в комплекс фермент-продукт (E-P).
4. Отделение конечных продуктов от фермента.
Специфичность, т.е. высокая избирательность действия ферментов, основана на
комплементарности структуры субстрата и активного центра фермента. Бывает стереоспецифичность – катализ только одного из стереоизомеров, Абсолютная специфичность – фермент производит катализ только одного вещества. Например,расщепление мочевины уреазой. Групповая специфичность – катализ субстратов с общими структурными
особенностями, т.е. при наличии определенной связи или химической группы
Механизмы катализа: 1. Кислотно-основной– в активном центре фермента находятся группы специфичных аминокислотных остатков, которые являются хорошими донорами или акцепторами протонов.Такие группы представляют собой мощные катализаторы многих органических реакций.
2. Ковалентный – ферменты реагируют со своими субстратами, образуя при помощи ковалентных связей очень нестабильные
фермент-субстратные комплексы, из которых в ходе внутримолекулярных перестроек
образуются продукты реакции.
37. Современные представления о механизмах действия ферментов. Мультиферментные комплексы на примере структуры синтазы жирных кислот.
Р азличают три стадии в механизме ферментативного катализа:
1.образование фермент-субстратного комплекса;2.образование комплекса «фермент-продукт реакции»;3.отщепление продуктов реакции от фермента.
1. фермент отличается от субстрата наличием АЦ . В АЦ имеются якорные участки, за счет которых субстрат закрепляется и каталитический участок АЦ, ответственен за тип ускоряемой реакции.
2. – функционально-активные группы АЦ фермента действуют на субстрат, дестабилизируя связи в нем, вызывая изменение конфигурации субстрата, поляризацию его молекулы. Это приводит к химическому преобразованию субстрата и образованию продуктов реакции, которые некоторое время находятся в связи с ферментом
3.от этого времени и зависит скорость реакции. Происходит отделение фермента от продуктов реакции.
Мультиферментные комплексы
В мультиферментном комплексе несколько ферментов прочно связаны между собой в единый комплекс и осуществляют ряд последовательных реакций, где продукт реакции непосредственно передается на следующий фермент и является только его субстратом. Благодаря таким комплексам значительно ускоряется скорость превращения
молекул. Напр.: пируватдегидрогеназный комплекс превращающий пируват в ацетил-SКоА,
α-кетоглутаратдегидрогеназный комплекс (в ЦТК превращающий α-кетоглутарат в сукцинил-SКоА
38. Зависимость скорости ферментативных реакций от факторов окружающей среды.
От t: с увелич.ее увелич.скорость ферменат.р-ции. Но не выше t при кот.происх.денатурация.
От pH, от конц.субстрата, от конц.фермента.
39. Специфичность действия ферментов. Классификация и номенклатура ферментов. Специфичность, т.е. высокая избирательность действия ферментов, основана на
комплементарности структуры субстрата и активного центра фермента. Бывает стереоспецифичность – катализ только одного из стереоизомеров, Абсолютная специфичность – фермент производит катализ только одного вещества. Например, расщепление мочевины уреазой. Групповая специфичность – катализ субстратов с общими структурными
особенностями, т.е. при наличии определенной связи или химической группы.
В 1961 г в Москве приняли современную
классификацию
ферментов.
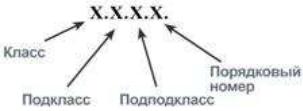
Выделяют 6 классов ферментов: оксидоредуктазы, трансферазы,гидролазы, лиазы, изомеразы, лиазы.
