
Мачула А.А. Сборник задач по курсу Общая и неорганическая химия
.pdf
↑↓ |
↑↓ |
↑↓ |
↑↓ |
↑ |
↑ |
↑↓
В символьном виде
КL3s23p63d24s2 .
Электронное строение атомов и таблица химических элементов
s-Элементами называются элементы, в атомах которых последний электрон поступает на s-подуровень. Аналогично определяются p-
элементы, d-элементы и f-элементы.
Начало каждого периода соответствует открытию нового электронного слоя. Номер периода равен номеру открываемого электронного слоя. Каждый период, кроме первого, заканчивается заполнением р-подуровня слоя, открытого в начале этого периода. В первом периоде содержатся только s-элементы (два). В четвертом и пятом периодах между s-(два) и р-элементами (шесть) расположены d-элементы (десять). В шестом и седьмом за парой s-элементов расположен (в нарушение правил Клечковского) один d-элемент, затем четырнадцать f-элементов (они помещены отдельными строками в нижней части таблицы - лантаноиды и актиноиды), затем девять d-элементов и, как всегда, периоды заканчиваются шестью р- элементами.
По вертикали таблица делится на 8 групп, каждая группа - на главную и побочную подгруппы. В главных подгруппах находятся s- и р-элементы, в побочных - d-элементы. Главную подгруппу определить легко- в ней находятся элементы 1-3 периодов. Строго под ними расположены остальные элементы главной подгруппы. Элементы побочной подгруппы располагаются в стороне (слева или справа).
Валентность атомов
121
В классическом представлении валентность определяется числом неспаренных электронов в основном или возбужденном состоянии атомов. Основное состояние - электронное состояние атома, в котором его энергия минимальна. Возбужденное состояние - электронное состояние атома, соответствующее переходу одного или нескольких электронов с орбитали с меньшей энергией на свободную орбиталь с большей энергией. Для s- и р-элементов возможен переход электронов только в пределах внешнего электронного слоя. Для d-элементов возможны переходы в пределах d-подуровня предвнешнего слоя и s- и р-подуровней внешнего слоя. Для f-элементов возможны переходы в пределах (n-2)f-, (n-1)d-, ns- и np-подуровней, где n- номер внешнего электронного слоя. Валентными электронами называются электроны, определяющие валентность атома в его основном или возбужденном состоянии.
Валентный электронный слой - слой, на котором расположены валентные электроны.
Пример 2 Описать с помощью квантовых чисел электроны внешнего слоя
атома серы и валентные электроны железа (основное состояние). Указать возможные валентности и степени окисления атомов этих элементов.
Решение 1). Атом серы.
Сера имеет порядковый номер 16. Она находится в третьем периоде, шестой группе, главной подгруппе. Следовательно, это р-элемент, внешний электронный слой - третий, он и является валентным. На нем шесть электронов. Электронное строение валентного слоя имеет вид
no pq r s
122

↑↓ |
|
↑↓ |
↑ |
↑ |
|
|
|
|
|
Для всех электронов n=3, т. к. они расположены на третьем слое. Рассмотрим их по порядку:
n n=3, L=0 (электрон расположен на s-орбитали), ml=0 (для s- орбитали возможно только такое значение магнитного квантового числа), ms=+1/2 (вращение вокруг собственной оси происходит по часовой стрелке);
o n=3, L=0, ml=0 (эти три квантовых числа такие же, как и у первого электрона, т. к. оба электрона находятся на одной орбитали), ms= - 1/2 (только здесь проявляется различие, требуемое по принципу Паули);
p n=3, L=1 (это р-электрон), ml=+1 (из трех возможных значений ml= ±1, 0 для первой р-орбитали выбираем максимальное, это рх-
орбиталь), ms= +1/2;
q n=3, L=1, ml= +1, ms=-1/2;
r n=3, L=1, ml= 0 (это ру-орбиталь), ms= +1/2; s n=3, L=1, ml= -1 (это рz-орбиталь), ms= +1/2.
Рассмотрим валентности и степени окисления серы. На валентном слое в основном состоянии атома имеются две электронные пары, два неспаренных электрона и пять свободных орбиталей. Следовательно, валентность серы в этом состоянии II. Сера - неметалл. До завершения слоя ей не хватает двух электронов, поэтому в соединениях с атомами менее электроотрицательных элементов, например, с металлами, она может проявлять минимальную степень окисления -2. Распаривание электронных пар возможно, т. к. на этом слое есть свободные орбитали. Следовательно, в первом возбужденном состоянии (S* )
↑↓ |
|
↑ |
↑ |
↑ |
|
↑ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
атом серы может иметь валентность IV, а во втором (S**) VI:
↑ |
|
↑ |
↑ |
↑ |
|
↑ |
↑ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
123
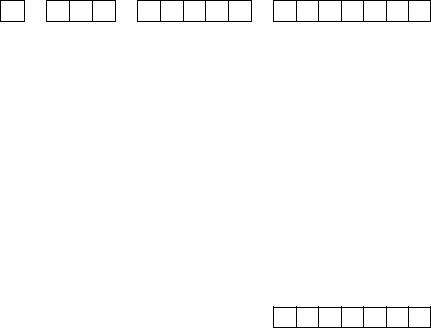
В соединениях с атомами более электроотрицательных элементов, например, кислородом, все шесть валентных электронов могут быть смещены от атомов серы, поэтому ее максимальная степень окисления +6.
2). Железо.
Порядковый номер железа 26. Оно расположено в четвертом периоде, в восьмой группе, побочной подгруппе. Это d-элемент, шестой в ряду d-элементов четвертого периода. Валентные электроны железа (восемь) расположены на 3d-подуровне (шесть, в соответствии с положением в ряду d-элементов) и на 4s-подуровне
(два):
no p q r s
↑↓ |
|
↑↓ |
↑↓ |
↑↓ |
|
↑↓ |
↑ |
↑ |
↑ |
↑ |
|
|
|
|
|
|
|
|
|
|
|
tu
↑↓
Рассмотрим их по порядку:
n n=3, L=2, ml= +2, ms= +1/2; o n=3, L=2, ml= +2, ms= -1/2; p n=3, L=2, ml= +1, ms= +1/2; q n=3, L=2, ml= 0, ms= +1/2; r n=3, L=2, ml= -1, ms= +1/2; s n=3, L=2, ml= -2, ms= +1/2; t n=4, L=0, ml= 0, ms= +1/2; u n=4, L=0, ml= 0, ms= -1/2.
Валентность На внешнем слое нет неспаренных электронов, поэтому
минимальная валентность железа (II) проявляется в возбужденном состоянии атома:
↑↓ |
|
↑↓ |
↑↓ |
↑↓ |
|
↑↓ |
↑ |
↑ |
↑ |
↑ |
|
|
|
|
|
|
|
|
|
|
|
↑ |
|
↑ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
124
После того, как будут использованы электроны внешнего слоя, в образование химических связей могут быть задействованы 4 неспаренных электрона 3d-подуровня. Следовательно, максимальная валентность железа VI.
Степень окисления Железо – металл, поэтому для него характерны положительные
степени окисления от +2 (задействованы электроны 4s-подуровня) до +6 (задействованы 4s- и все неспаренные 3d-электроны).
Задания для самостоятельной работы
Индивидуальные задания
1.А. Какие значения квантовых чисел ml и ms возможны для 2рсостояния электрона?
Б. Охарактеризовать квантовыми числами электроны атома натрия (основное состояние).
В. Чем отличаются 1s- и 2s-орбитали?
2.А. Указать максимально возможное число электронов в s- и d- оболочках атома. Ответ обосновать.
Б. Описать квантовыми числами d-электроны атома цинка (основное состояние).
В. Изобразить s- и f-орбитали.
3.А. Какие значения квантовых чисел ml и ms возможны для 3рсостояния электрона?
Б. Описать квантовыми числами d-электроны атома кобальта (основное состояние).
В. Изобразить p- и d-орбитали.
4.А. Сколько орбиталей в атоме могут быть описаны значением квантового числа l=3 при фиксированном значении главного квантового числа?
125
Б. Описать квантовыми числами d-электроны атома хрома (основное состояние).
В. Изобразить d-орбитали.
5.А. Каков физический смысл побочного квантового числа? Б. Описать квантовыми числами f-электроны атома гольмия
(основное состояние).
В. Изобразить р-орбитали.
6.А. Сколько электронов в атоме стронция (основное состояние) имеют значение l=0?
Б. Описать квантовыми числами электроны внешнего слоя атома селена (основное состояние).
В. Чем отличаются 2р- и 3р-орбитали?
7.А. Какую составляющую движения электрона определяет спиновое квантовое число?
Б. Описать квантовыми числами электроны атома кремния (основное состояние)?
В. Изобразить 2рx – и 3s-орбитали.
8.А. Сколько электронов атома теллура (основное состояние) имеют значение квантового числа l=1?
Б. Описать квантовыми числами электроны внешнего слоя атома сурьмы (основное состояние).
В. Изобразить рy – и dxy –орбитали.
9.А. Сколько электронов атома марганца (основное состояние) имеют значение квантового числа l=1?
Б. Описать квантовыми числами электроны внешнего слоя атома полония (основное состояние).
В. Изобразить pz – и dxz –орбитали.
10.А. Какое квантовое число обозначается буквами s, p, d, f ? Какие его значения соответствуют этим числам?
Б. Описать квантовыми числами d-электроны атома осмия (основное состояние).
126
В. Изобразить 4dyz – и 3s-орбитали.
11.А. Каковы значения орбитального квантового числа для следующих состояний электрона: 3p, 3d, 4s, 5f, 2p, 4f, 5d?
Б. Описать квантовыми числами электроны атома кислорода (основное сотояние).
В. Изобразить 2рх – и 3рх –орбитали.
12.А. Какие значения магнитного квантового числа возможны для 4f-состояния электрона?
Б. Описать квантовыми числами d-электроны атома молибдена (основное состояние).
В. Изобразить 2ру- и 3ру-орбитали.
13.А. Какие значения магнитного квантового числа возможны для 4d-состояния электрона?
Б. Описать квантовыми числами электроны атома фтора (основное состояние).
В. Изобразить 2рz- и 3pz-орбитали.
14.А. Сколько орбиталей в атоме могут характеризоваться значением главного квантового числа 3?
Б. Описать квантовыми числами электроны атома магния (основное состояние).
В. Изобразить 3dxy- и 4dxy-орбитали.
15.А. Каков физический смысл побочного квантового числа? Б. Описать квантовыми числами d-электроны атома ниобия
(основное состояние).
В. Изобразить 3dxz- и 4dxz-орбитали.
16.А. Каков физический смысл главного квантового числа?
Б. Описать квантовыми числами электроны внешнего слоя атома сурьмы (основное состояние).
В. Изобразить 3dyz- и 4dyz-орбитали.
17.А. Указать максимальное число электронов в атоме, обладающих определенным значением главного квантового числа.
127
Б. Описать квантовыми числами электроны внешнего слоя атома свинца (основное состояние).
В. Изобразить d(x2)- и d(x2-y2)-орбитали.
18.А. В приведенном ряду указать невозможные обозначения состояния электронов: 1s, 3d, 2d, 4f, 5f, 1p, 3p, 3f. Ответ обосновать.
Б. Описать квантовыми числами электроны внешнего слоя атома ксенона (основное состояние).
В. Изобразить 3d(x2)- и 4d(x2)-орбитали.
19.А. Сформулировать правило Хунда и приведите иллюстрирующий его пример.
Б. Описать квантовыми числами электроны атома алюминия (основное состояние).
В. Изобразить 3d(x2-y2)- и 4d(x2-y2)-орбитали.
20.А. Каковы значения квантового числа l для следующих состояний электрона: 3p, 3d, 5f, 2s, 4d,4f?
Б. Описать квантовыми числами электроны внешнего слоя атома германия (основное состояние).
В. В каком случае размеры орбитали прямо пропорциональны квадрату главного квантового числа?
21.А. Указать максимально возможное число электронов в р- и f- оболочках атома. Ответ обосновать.
Б. Описать квантовыми числами d-электроны атома никеля (основное состояние).
В. Какой физический смысл магнитного квантового числа? Привести иллюстрирующие примеры.
22.А. Перечислить квантовые числа электронов в атоме и указать диапазон их изменений.
Б. Описать квантовыми числами d-электроны атома кобальта (основное состояние).
В. Изобразить 1s- и 2s-орбитали.
128
23.А. Каковы значения квантового числа l для следующих состояний электрона: 1s, 3s, 4s, 4f, 4p,3d, 4f ?
Б. Описать квантовыми числами f-электроны атома самария (основное состояние).
В. В каких правилах заключен принцип минимума энергии электронов в атоме? Привести примеры исключений.
24. А. Расположить орбитали атома водорода в порядке увеличения их энергии: 3d, 1s, 5p, 2s, 4f.
Б. Описать квантовыми числами d-электроны атома железа (основное состояние).
В. Изобразить 2р и 3р орбитали.
25.А. В приведенном ряду выделите обозначения состояния электронов, которые невозможны: 2s, 2p, 3p, 3f, 2d, 5f, 6p. Ответ обосновать.
Б. Описать квантовыми числами d-электроны атома марганца (основное состояние).
В. В каком случае больше разница в энергиях электронных состояний: 1s и 2s, 2s и 3s? Ответ обосновать.
Многовариантное задание 1). Написать электронные формулы атомов с зарядами ядер А, Б, В.
2). К какому типу элементов (s, p, d, f) они относятся?
3). Описать их положение в периодической системе элементов. 4). Какие валентности и степени окисления для них возможны? 5). Привести примеры электронных аналогов этих элементов.
129
№ |
А |
Б |
В |
1 |
30 |
35 |
81 |
2 |
13 |
44 |
83 |
3 |
7 |
59 |
73 |
4 |
17 |
63 |
24 |
5 |
43 |
56 |
75 |
6 |
10 |
93 |
35 |
7 |
47 |
65 |
52 |
8 |
8 |
69 |
74 |
9 |
38 |
57 |
33 |
10 |
14 |
20 |
41 |
11 |
48 |
60 |
50 |
12 |
92 |
46 |
34 |
13 |
71 |
12 |
21 |
14 |
80 |
61 |
32 |
15 |
87 |
95 |
26 |
16 |
64 |
79 |
53 |
17 |
54 |
11 |
28 |
18 |
94 |
15 |
72 |
19 |
9 |
67 |
82 |
20 |
19 |
58 |
39 |
21 |
66 |
77 |
31 |
22 |
88 |
68 |
27 |
23 |
45 |
90 |
51 |
24 |
62 |
86 |
29 |
25 |
78 |
70 |
49 |
26 |
36 |
91 |
25 |
27 |
96 |
18 |
42 |
28 |
16 |
89 |
22 |
29 |
85 |
37 |
23 |
30 |
76 |
84 |
40 |
130
