
- •Раздел 2. Кинетика простой необратимой реакции
- •Раздел 3. Кинетика реакции n-го порядка
- •Лекция 3. Кинетика обратимой реакции
- •Раздел 1. Кинетическая модель обратимой реакции в общем виде
- •Раздел 2. Кинетика обратимой реакции а r
- •Лекция 4. Кинетика параллельной реакции
- •Раздел 1. Кинетическая модель параллельной реакции в общем виде
- •Раздел 2. Кинетика параллельной реакции а s
- •Раздел 3. Селективность параллельной реакции а
Раздел 2. Кинетика простой необратимой реакции
Рассмотрим простую необратимую реакцию типа:
A → R
протекающую при постоянном объеме реакционной смеси и постоянной температуре. Примем, что в начальный момент времени в исходной реакционной смеси присутствует только реагент и, значит, начальная концентрация продукта равна нулю. Эти условия запишем в виде:
T,V = const;
С А
= САо
при τ
= 0
А
= САо
при τ
= 0
СR = СRо =0
Если объем реакционной смеси постоянный V = const, то скорость реакции это изменение концентрации в единицу времени:
![]() (2.5)
(2.5)
![]() (2.6)
(2.6)
Теперь согласно уравнениям (2.2–2.4) составим кинетическую модель рассматриваемой реакции:

Сопоставим выражения (2.5) и (2.7), (2.6) и (2.8):

Определим изменение концентрации реагента А в ходе реакции. Для этого рассмотрим выражение (2.9). Разделим переменные, интегрируем его в пределах изменения концентрации от САо до СА и по времени от 0 до τ :
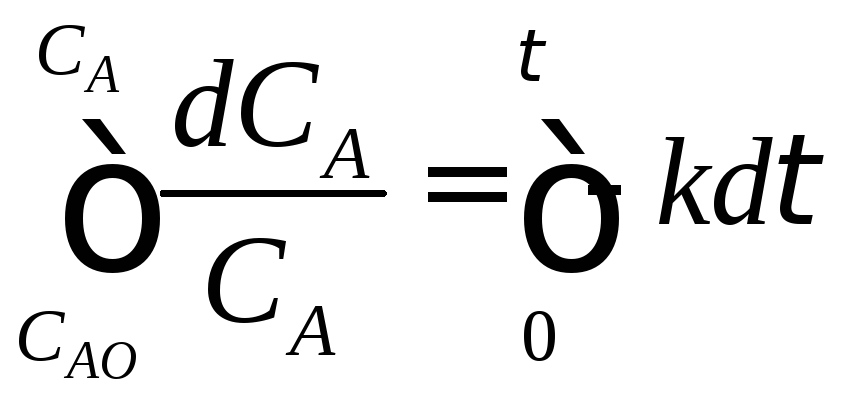
![]()
![]()
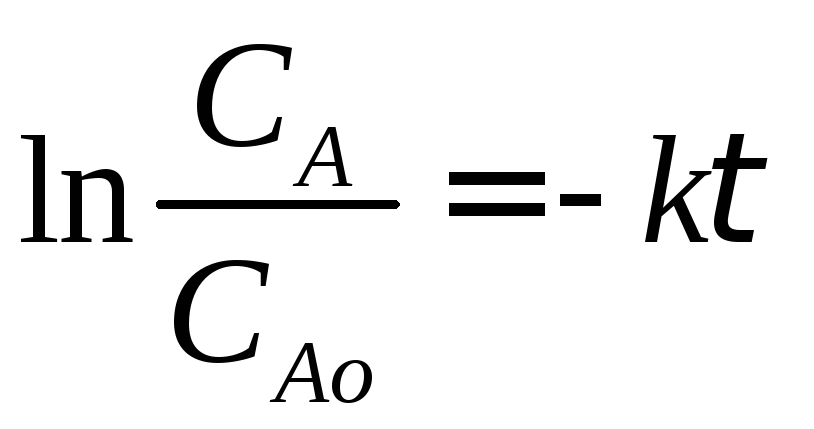
СА = САо е –кτ (2.11)
Выражение (2.11) представляет искомую зависимость изменения концентрации реагента А в ходе реакции или определяет вид кинетической зависимости СА = f(τ). Кинетическую зависимость СR = f(τ) найдем из материального баланса рассматриваемой реакции. Так как для нашей реакции νА = νR = 1, то САо =СА + СR. Тогда:
СR = САо - СА = САо - САо е–кτ = САо (1 – е–кτ ) (2.12)
Выражение (2.12) представляет искомую зависимость СR = f(τ).
Найдем зависимость степени превращения от времени для рассматриваемой реакции:

хА=1 – е–кτ (2.13)
Выражение (2.13) представляет искомую зависимость xА = f(τ).
Изобразим графически зависимости СА, СR, хА = f(τ).

Из представленного следует, что для простой необратимой реакции, протекающей по схеме A→R, концентрация реагента А уменьшается в ходе реакции по экспоненциальной зависимости и стремится к нулю к концу реакции. Концентрация продукта R экспоненциально возрастает. Степень превращения реагента экспоненциально возрастает и стремится к единице.
Раздел 3. Кинетика реакции n-го порядка
Рассмотрим реакцию n–го порядка, протекающую по схеме:
n A→R (2.14)
Порядок реакции это сумма показателей степеней при концентрации реагирующих веществ в кинетическом уравнении реакции. Чаще всего порядок реакции не совпадает с ее молекулярностью так как суммарное стехиометрическое уравнении реакции, как правило, не может показать действительный механизм реакции, которая протекает через рад последовательных стадий. Реакции бывают первого, второго, третьего и дробного порядка.
Рассмотрим реакцию (2.14). Пусть начальные условия будут те же, что и для простой необратимой реакции:
T,V = const;
С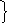 А
= САо
при τ
= 0
А
= САо
при τ
= 0
СR = СRо =0
Если объем реакционной смеси постоянный V = const, то скорость реакции это изменение концентрации в единицу времени:
![]() (2.15)
(2.15)
![]() (2.16)
(2.16)
Составим кинетическую модель рассматриваемой реакции:

Сопоставим выражения (2.15) и (2.17 ), (2.16) и (2.18):
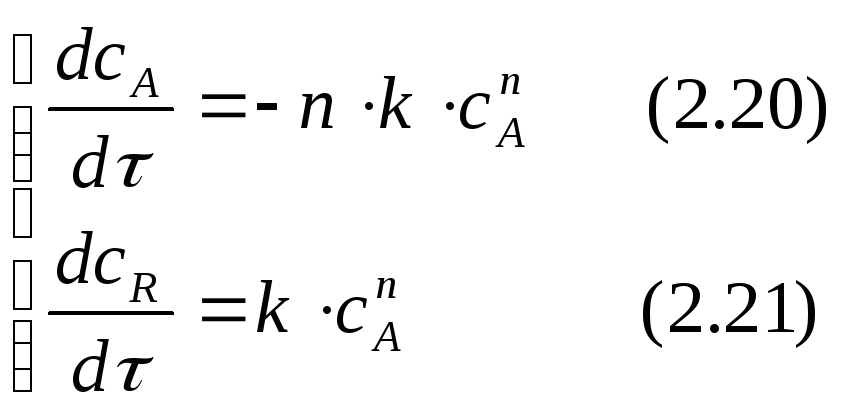
Определим изменение концентрации реагента А в ходе реакции. Для этого рассмотрим выражение (2.20). Разделим переменные, интегрируем его от САо до СА и от 0 до τ :
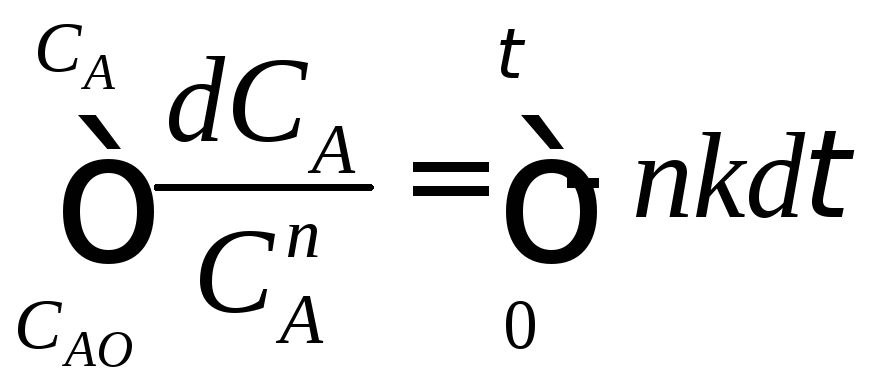

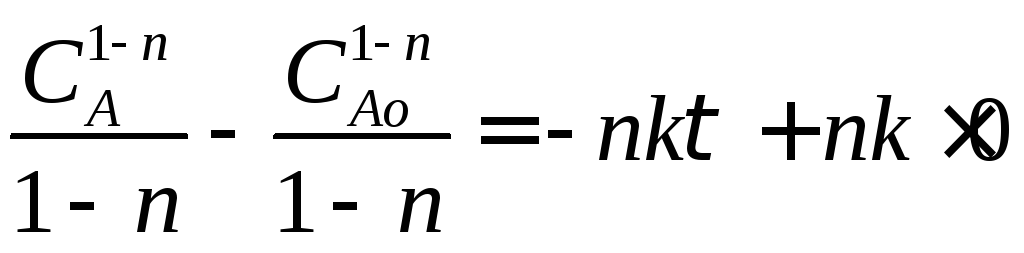
![]() (2.22)
(2.22)
![]() (2.23)
(2.23)
Выражение (2.23) представляет искомую зависимость СА = f(τ).
Найдем зависимость степени превращения от времени для рассматриваемой реакции. Вспомним, что СА=САо(1-хА). Подставим это выражение в (2.22):
![]()
Разделим полученное выражение на САо1-n

![]()
![]() (2.24)
(2.24)
Выражение (2.24) представляет искомую зависимость хА = f(τ).
