
- •Введение
- •1 Технико–экономическое обоснование проекта
- •2 Выбор и расчет основного технологического оборудования
- •2.1 Расчет необходимого количества печей
- •2.2 Описания конструкции печи
- •2.3 Электрическое оборудование печи
- •3 Технология производства низкоуглеродистого феррохрома
- •3.1 Годовая продукция проектируемого цеха
- •3.2 Основные требования к исходным материалам
- •3.3 Технология производства низкоуглеродистого феррохрома
- •3.3.1 Физико-химические основы производства
- •3.3.2 Технология ведения плавки
- •3.3.3 Расчет материального и теплового балансов выплавки низкоуглеродистого феррохрома силикотермическим печным способом
- •4 Структура и оборудование цеха
- •4.1 Схема расположения отделений цеха
- •4.2 Склад шихты
- •4.3 Плавильный корпус цеха
- •4.4 Склад готовой продукции
- •5 Автоматизация производства
- •6 Специальная часть
- •6.1 Краткое описание
- •6.2 Наименование
- •6.3 Цель и назначение
- •6.4 Технические требования для изготовления магнитного сепаратора
- •6.4.1 Состояние вопроса
- •6.4.2 Состав магнитного сепаратора и требования к конструктивному устройству
- •6.4.3 Общие требования к элементам конструкции магнитного сепаратора
- •6.5 Управление магнитным сепаратором
- •6.6 Обслуживание магнитного сепаратора
- •6.7 Требования безопасности и охраны природы
- •6.8 Выводы
- •7 Экономическая часть
- •7.1 Краткая характеристика проектируемого цеха
- •7.2 Расчет производственной программы проектируемого цеха
- •7.3 Организация и управления цехом
- •7.4 Организация труда рабочих
- •7.5 Штаты рабочих
- •7.6 Организация заработной платы
- •7.7 Расчет заработной платы итр, специалистов и служащих
- •7.8 Капитальные вложения
- •7.9 Калькуляция себестоимости
- •7.10 Рентабельность и прибыль предприятия
- •8 Охрана труда и техника безопасности
- •8.1 Выбор территории цеха
- •8.2 Защита от источников тепловых выделений
- •8.3 Пожарная и взрывобезопасность
- •8.4 Защита от загрязнения воздуха
- •8.5 Защита от электрического тока
- •8.6 Защита от шума и вибрации
- •8.7 Безопасность при чрезвычайных ситуациях и меры защиты
- •Заключение
- •Список использованных источников
3.3.3 Расчет материального и теплового балансов выплавки низкоуглеродистого феррохрома силикотермическим печным способом
l.l Исходные данные
Расчет состава шихты выполняем на 100 кг хромовой руды. В соответствии с заданием на выполнение дипломной работы задаемся видами шихтовых материалов, их составом (табл.1-2) и условиями проведения плавки. Сумма компонентов в шихтовых материалах должна быть равна 100 %.
Таблица 3.6- Химический состав материалов
Материал |
Cr2O3 |
FeO |
SiO2 |
Al2O3 |
CaO |
MgO |
P2O5 |
S |
ППП |
∑ |
Хром.ру |
52,44 |
12,42 |
6,08 |
7,72 |
0,465 |
18,25 |
0,0046 |
0,013 |
2,61 |
100 |
Известь |
- |
0,06 |
1,64 |
0,49 |
91 |
0,46 |
0,008 |
0,006 |
6,334 |
100 |
Таблица 3.7 - Химический состав ферросиликохрома
Материал |
Cr |
Si |
C |
P |
S |
Fe |
∑ |
ФСХ 48 |
29,68 |
49,72 |
0,025 |
0,026 |
0,020 |
20,529 |
100 |
Для проведения расчета необходимо знать распределение основных элементов между продуктами плавки: металл, шлак и газы, которые принимаются на основании практических данных (табл. 3). Для упрощения расчетов считаем, что электроды состоят только из углерода и полностью переходят в сплав. Также принимаем, что все элементы ферросиликохрома (кроме кремния) переходят полностью в металл.
Таблица 3.8 - Распределение элементов
Продукты плавки |
Элементы |
|||||
Сr(руда) |
Fe(руда) |
C,Cr,Fe (ФСХ) |
Si |
S |
P |
|
Сплав |
85 |
95 |
100 |
3 |
50 |
15 |
Шлак |
15 |
5 |
0 |
97 |
45 |
15 |
Улет |
0 |
0 |
0 |
0 |
5 |
70 |
B условия расчёта включены также дополнительные требования к составу получаемого металла и шлака, расход электродов на расчетное количество шихты, угар восстановителя, доля различных восстановителей в смеси и др.
Дополнительные условия:
Доля концентрата в смеси, % 40
Основность шлака СаО/SіO2 2
Окислится кремния кислородом воздуха, % 10,0
Соотношение руда/концентрат 50/50
С0держание углерода в сплаве, не более % 0,1
Расход электродной массы, кг 0,05
Расчет состава шихты
Расчет ведем на 100 кг хромовой руды. Для этого определяем ее средний химический состав. По условиям расчета задается соотношением хромовой руды и хромового концентрата. 50/50. Расчитываем средний состав руды:
Cr203 (51,7 50 + 52,44 50)/100 = 52,07
S102 (7,25 50 + 6,08 50)/ 100 = 6,665
A1203 (7,68 50 + 7,82 50)/ 100 = 7,70
FeO (12,1 50 + 12,42 50)/100 = 12,26
СаО (0,37 50 + 0,465 50)/100 = 0,417
MgO (18,76 50 + 18,25 50)/100 = 18,505
P205 (0,0053 50 + 0,0046 50)/100 = 0,0049
S (0,019 50 +0,013 50 )/100 = 0,016
ППП (2,12 50 +2,61 50)/100 = 2,365
Расчет количества восстановителя
На восстановление 100 кг концентрата потребуется кремния, кг:
2Cr2O3 3Si→4Сr + 3SiO2 52,07 0,85 84/304 = 12,229
2FeO + Si→2Fe + SiO2 12,26 0,95 28/144 = 2,264
2P205+ 5Si→4P + 5SiO2 0,0049 (0,15+0,70)140/284= 0,002
Итого 14,495
С учетом окисления 10% кремния кислородом воздуха и перехода его в металл 3% необходимо кремния:
14,495(1-0,10-0,03) = 16,661
Для восстановления 100 кг рунной смеси потребуется ферросиликохрома ФСХ48.
16,661 / 0,4972 = 33,509 кг.
На окисление кремния ферросиликохрома воздухом потребуется кислорода
33,509 0,4972 0,14 32 / 28 = 2,665 кг.
Расчет количества извести
В шлак перейдет кремнезема, кг: от окисления кремния силикохрома
33,509 0,4972 0,97 60/28 = 34,630
из пустой породы руды 100 0,06665 = 6,665
Итого в шлак перейдет кремнезема 34,630 + 6,665 = 41,295 кг. При заданной основности шлака, равной 2,00 потребуется извести:

 =
93,676
=
93,676
Расчет количества и состава металла
Из хромовой руды в состав металла перейдет, кг:
Cr 52,07 0,85 104/152 = 30,282
Fе 12,26 0,95 112/144 = 9,058
S 0,016 0,52= 0,008
P 0,0049 0,5 62/142 = 0,001
Итого 39,349
Из ферросиликохрома в состав металла перейдет, кг:
Cr 33,509 0,2968 = 9,945
Ре 33,509 0,20529 = 6,879
Si 33,509 0,4972 = 0,499
C 33,509 0,00025 = 0,008
S 33,509 0,006 = 0,006
P 33,509 0,00026 = 0,008
Итого 17,345
Из электродов в металл перейдет 0,05 кг углерода. Результаты проведенных расчетов сводятся в таблицу 4, и находится состав количество металла.
Таблица 3.9 _- Состав и количество металла
Элемент |
Источник поступление |
Итого |
|||
Хром.руда |
ФСХ |
кг |
% |
||
Si |
0 |
0,499 |
0,499 |
0,879 |
|
Fe |
9,058 |
6,879 |
15,937 |
28,085 |
|
Cr |
30,282 |
9,945 |
40,227 |
70,892 |
|
S |
0,008 |
0,006 |
0,014 |
0,024 |
|
P |
0,001 |
0,008 |
0,009 |
0,015 |
|
C |
0,05 |
0,008 |
0,058 |
0,102 |
|
Всего |
39,399 |
17,345 |
56,744 |
100,00 |
|
⃰ электрод
Расчёт состава и количества шлака
Из состава руды в шлак перейдут следующие оксиды, кг:
SiO2 = 6,665
A1203 = 7,70
Fe2O3 12,25 0,05 = 0,613
СаО = 0,417
MgO = 18,505
Cr203 52,07 0,15 = 7,810
S 0,016 0,45 = 0,0072
P205 0,005 0,15 = 0,000
Итого 41,7172 кг
В результате окисления кремния из состава ФСХ в шлак перейдет кремнезем:
SіO2 33,509 ∙ 0,4972 ∙ 0,97 ∙ 60 / 28 = 34,630 кг
Для упрощения расчета условно принимается, что все оксицы в составе извести полностью перейдут в шлак:
SіO2 93,676 0,0164 = 1,536
А12O3 93,676 0,0049 = 0,459
Fe2O3 93,676 0,0006 = 0,056
СаО 93,676 0,91 = 85,245
MgO 93,676 0,0046 = 0,431
Р2О5 93,676 0,00008 = 0,007
S 93,676 0,00006 = 0,005
Итого 87,739
Результаты проведенных расчетов сводится втаблицу 5,и находится состав и количество шлака.
Таблица 3.10- Состав и количества шлака.
Оксид |
Источник поступления |
Итого |
||||
Руда |
Известь |
ФСХ |
кг |
% |
||
SіO2 |
6,665 |
1,536 |
34,630 |
42,831 |
26,102 |
|
А12O3 |
7,70 |
0,459 |
0 |
8,159 |
4,972 |
|
Fe2O3 |
0,613 |
0,056 |
0 |
0,669 |
0,407 |
|
СаО |
0,417 |
85,245 |
0 |
85,662 |
52,205 |
|
MgO |
18,505 |
0,431 |
0 |
18,936 |
11,540 |
|
Cr2О3 |
7,810 |
0,000 |
0 |
7,810 |
4,759 |
|
S |
0,0072 |
0,005 |
0 |
0,012 |
0,007 |
|
Р2О5 |
0,000 |
0,007 |
0 |
0,007 |
0,004 |
|
Всего |
41,7172 |
87,739 |
34,630 |
164,086 |
100 |
|
Кратность шлака 164,086 / 56,744 = 2,891
Основность шлака СаО / SіO2 = 85,662 / 42,831 = 2,00
Расчет количество газов и пыли и улета.
S 0,016 0,05 = 0,0008
P 0,005 0,70 62/142 = 0,001
ППП 2,365
Итого 2,366
Газы и пыли выделяющеся из состава извести ,кг.
ППП 93,676 0,06334 = 5,933
Таблица 3.11 – Состав и количество газов и пыли и улета.
Газы |
Виды шихты |
Всего |
||
руда |
известь |
кг |
% |
|
P |
0,001 |
- |
0,001 |
0,012 |
S |
0,0008 |
- |
0,000 |
0 |
ППП |
2,365 |
5,933 |
8,298 |
99,988 |
Итого |
2,366 |
5,933 |
8,299 |
100 |
Расчет материального баланса
Таблица 3.12 – Материальный баланс
Приход |
Расход |
||||
Материал |
кг |
% |
Продукт |
кг |
% |
Руда |
100 |
43,497 |
Металл |
56,744 |
24,765 |
Известь |
93,676 |
40,746 |
Шлак |
164,086 |
71,613 |
ФСХ48 |
33,509 |
14,575 |
Газы |
8,299 |
3,622 |
Электроды |
0,05 |
0,021 |
Невязка |
0,771 |
0,336 |
Кислород |
2,665 |
1,159 |
|
|
|
Всего |
229,900 |
100 |
|
|
|
B материальном балансе разность между статьями расхода и прихода равна:
229,9 – 229,129 = 0,771 кг
Расчет удельного расхода материалов
Удельный расход шихтовых материалов на тонну сплава составит, кг:
Хромовая руда (50% Cr203) 1000 100 / 56,744 (52,07 / 50) = 1835
Известь (90% СаО) 1000 93,676 / 56,744 (91 / 91) = 1650
ФСХ (48% Si) 1000 33,509 / 56,744 (49,72 / 48) = 611
Достоверность данных, полученных в результате расчета состава шихты и составления материального баланса, подтверждается минимальным расхождением между приходной и расходной частями баланса (не более 0,5%), а также совпадением расчетных удельных расходов материалов с практическими данными, приведенными в литературе для заданного сплава.
Расчет теплового баланса
Тепловой баланс процесса получения ферросплавов определяется равенством, кДж.
Qcпл + Qшл + Qгаз + Qэнд + Qпот =Qфиз + Qэкз + Qэл.эн
Qcпл + Qшл + Qгаз - теплосодержание продуктов;
Qэнд - тепловые затраты на эндотермические процессы;
Qпот - тепловые потери процесса;
Qфиз - физическое тепло нагретой шихты;
Qэкз - экзотермическое тепло реакции окисления и шлакообразования;
Qэл.эн - тепло, вводимое электроэнергией, которое определяется как разность между расходнои и приходной частями баланса.
Приход тепла
Физическое тепло шихты
В расчетах, как правило, за нулевую отметку по температуре принимают температуру окружзющей среды. Шихта внесет дополнительное тепло,если ее температура превышает температуру среды:

Так как в нашем случае по условиям расчета не предусмотрен предварительный нагрев шихты, то шихта не будет вносить дополнительное количество тепла Qфиз = 0.
Экзотермическое тепло реакций
Статья включает тепло реакций окисления Qэкз.ок ,тепло реакций восстановления Qэкз.восст тепло металлообразования Qэкз.восст и тепло шлакообразования Qэкз.шл .Тепло от окисления силиковосстановителей на колошнпке, растворения кремния в сплаве, образования силикатов и шпинетидов в шлаке рассчитывают по количеству окислившегося элемента или образовавшегося соединения gi и соответствующему тепловому эффекту.

Qэкз=Qэкз.ok + Qэкз.восст +Qэкз.мет + Qэкз.шл
1. Тепло реакций окисления Qэкз.ok выделяется при окислении кремния кислородом воздуха по реакции:
Si
+ O2 = SiO2
 H=
-911,55 кДж/моль.
H=
-911,55 кДж/моль.
Qэкз.ok = (33,509 0,4972 0,10 ) 911,55 / 0,028 = 54239 кДж/моль:
2. Тепло реакций восстановления Qэкз.восст выделяется при восстановлении хрома. железа и фосфора по реакциям:
1. 2Cr2O3+3Si=4Cr+3SiO2, Н=-2734,65 + 2 1141,32 = 452,01 кДж/моль
Q1 =30,282 452,01 / (4 0,052 )= 65802 кДж.
2. 2FeO+Si=2Fe+SiO2, H = -911.55+ 2 265.44= -380,67 кДж/моль
Q2 = 9,058 380,67 / (2 0.056) = 30785 кДж.
3. 2P2O5+5Si = 4P+5SiO2 , Н =4557.75+2 1530.5 = -1496,75 кДж/моль
Q3 = 0,001 1496,75 / (4 0,031) = 9 кДж.
Qэкз.восст = 65802 + 30785 + 9 = 96596 кДж.
3.Тепло металлообразование Qэкз.мет складывается в основном из реакций образования в сплаве карбидов и силицидов (остальным пренебрегаем). Принимаем что весь углерод в феррохроме связан только с хромом и присутствует в виде Cr23C6 .Образование карбида хрома происходить по реакции.
23Cr + 6C = Cr23C6 H = - 411,480 кДж/моль:
Также принимаем, что весь кремний в феррохроме связан только железом и присутствует в виде FeSi .Образование силицида железа происходить по реакции.
Fe + Si = FeSi H = - 80.38 кДж/моль:
При растворении 0,065кг углерода в феррохроме выделится тепла
Q1 =0.058 411.480 / (6 0.012 )= 331,47 кДж.
При растворение 0,499 кг кремния в феррохроме выделится тепла
Q2 =0,499 80.32 / 0.028 = 1432 кДж.
Таким образом, Qэкз.мет = 1432+331,47= 1763 кДж.
4.Тепло шлакообразование Qэкз.мет складывается в основном из реакций образование в шлаке двухкальциевого силиката и шпинели (остальным пренебрегаем).Принимаем, что весь оксид алюминия в шлаке связан только с оксида магния и присутствует в шпинели MgO Al2O3. Образование шпинели из оксидов происходить по реакции.
MgO + Al2O3 = MgO Al2O3
Н = - 2302,32 + 601,89 + 1676,81 = - 23,62 кДж/моль.
Также принимаем, что весь кремнезем связан с оксидом кальция и примутствует в шлаке в виде ларнита 2CaO SiO2 .Образование ларнита происходить по реакций.
2CaO + SiO2=2CaO SiO2
Н = - 2308,98 + 2 635,6 + 911,55 = - 126,23 кДж/моль.
При образовании шпинели из 8,265 кг оксида алюминия выделится тепла.
Q1 = 8,159 23,62 / (0,102) = 1889 кДж.
44,078 кг кремнезема связывается в ларнит, при этом выделится тепла.
Q2 = 42,231 126,23 / 0,060 = 90109 кДж.
Таким оброзом,при шлакообразование выделится тепла
Qэкз.шл = 1889 + 90109 = 91998 кДж.
Qэкз = 54239 +96596 +1763 +91998 =244596 кДж.
Расход тепла.
Теплосодержание сплава при температуре выпуска
Теплосодержание сплава определяется теплоемкостью,температурой и массой сплава (на основе материального баланса)при нагрева сплава до температурой плавление и перегрева жидкого сплава до температуры выпуска из печи.
Для стандартных сплавов величину теплосодержание сплава следует читать до экспериментально определенным постоянным теплофизическим величинам согласно нижепроведенной формуле.
Qспл=
Gспл
 ,
кДж.
,
кДж.
Таблица 3.13 –Теплофизические свойства феррохромма марки ФХ010.
Температура
плавление
|
Энтальпия
при Тпл кДж/кг. |
Теплота
плавление
|
Теплоемкость жидкого Сж , кДж/кг. |
Температура сплава на выпуске С |
1630 |
950 |
309,8 |
0,707 |
1700-1720 |
Используя данные приведенные в таблице 8 рассчитаем теплосодержание феррохрома марки ФХ010 при температуре выпуска 1720С.
Qспл=56,744
 кДж.
кДж.
Теплосодержание при температуре выпуска
Температура
плавления шлаков выплавки нискоуглеродистого
феррохрома, как и любых других, находится
на
 100С
выше температуры плавление сплава, т.е.
на уровне 1730С.Температура
шлака на выпуске прывышает анологичные
для сплавов на 50-80С,
т.е. находится на уровне 1790С.
100С
выше температуры плавление сплава, т.е.
на уровне 1730С.Температура
шлака на выпуске прывышает анологичные
для сплавов на 50-80С,
т.е. находится на уровне 1790С.
Теплосодержание шлака при отсутствии экспериментальных данных можно оценить аддитовно, но основным (трем-четырем) составляющим компониентам по справочным данным согласно нижеприведенной формуле:
 кДж/моль.
кДж/моль.
Qшл=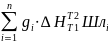
Однако температуры плавление большинства оксидов, составляющих шлак, намного выше температуры плавление самого шлака.Поэтому, сторого говоря, оксиды не плавятся, образуя шлак, а растворяются. Однако однотипность физических процессов лежащих в осове плавление и растворения,позволяет уровнять изменения энтальпии в этих процессах
LраствMeO
= LплMeO
Таким образом, задаваясь нижеприведенным справочными данным, рассчитаем теплосодержание шлака при температуре 1790С для основных составлющих шлака (MgO,SiO2,Al2O3,Cr2O3,CaO), сумма которых превышает 99% от общей массы.
Таблица 3.14 – Теплофизические величины основных компониентов шлака и газа.
Элемент |
Ср=а+ bT+cT2 , кДж/мольК |
Энтальпия плавления кДж/моль. |
Температура плавления , К |
Теплоемкость в жидком состоянии кДж/мольК |
|||||
a |
b103 |
c105 |
|||||||
Al2O3 |
114,84 |
12,81 |
-35,46 |
113,04 |
2326 |
144,96 |
|||
SiO2 |
46,98 |
34,33 |
-11,3 |
0,63 |
0-848 |
- |
|||
60,33 |
8,12 |
0 |
7,70 |
848-1996 |
85,82 |
||||
MgO |
42,62 |
7,28 |
-6,2 |
77,46 |
3098 |
84,0 |
|||
Cr2O3 |
113,04 |
9,21 |
-15,66 |
125,0 |
2705 |
156,9 |
|||
CaO |
105,37 |
11,953 |
-18,979 |
80,0 |
3172 |
84,0 |
|||
CO |
28,43 |
4,1 |
-0,46 |
- |
- |
- |
|||
CO2 |
44,17 |
9,04 |
-8,54 |
- |
- |
- |
|||
 dt
dt
+113,04=(111,84(2063-298)+0,012810,5(2063-298)2+3546000/(2063-298) ) / 1000+113,042063/2326 = 319,62 кДж/моль.
 =121,78
кДж/моль.
=121,78
кДж/моль.
 138,50
кДж/моль.
138,50
кДж/моль.
 310.08
кДж/моль.
310.08
кДж/моль.
 257,70
кДж/моль.
257,70
кДж/моль.
Qшл = 319,62
= 319,62 8,159/0.102+121,78
42,831/0,060+138,50
18,936/0,040+310,08+7,810/0,152+257,70+85,662/0,056 = 588194 кДж.
8,159/0.102+121,78
42,831/0,060+138,50
18,936/0,040+310,08+7,810/0,152+257,70+85,662/0,056 = 588194 кДж.
Теплосодержание газообразных продуктов
Доступим,что газы покидают печи при средней температуре 450С. Для упрощения расчетов принимаем теплоемкости всех газообразных продуктов равными теплоемкости окиси углерода СО2 основной составляющей газообразной фазы, образующуюся при разложении карбоната кальция в извести.
Qгаз
= Gгаз Т2)dT
= 8,299
Т2)dT
= 8,299
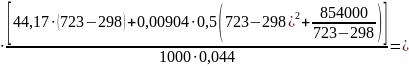
 кДж.
кДж.
Тепло эндотермических реакций
Тепло диссоциацию карбонатов, испарение влаги и т.д. подсчитывают по энтальпии реакции и их массе.
Qшл
CaCO3 = CaO + CO2 , H= - 635.6 – 393,51 + 1207,0 = 177,89 кДж/моль.
Qэнд= 5,933 177,89 / 0,044 = 23986 кДж
Потери тепла
По экспериментальным данным тепловые потери через футеровку, излучением колошника теплопроводностью через электроды, охлаждающей водой и т.д. при выплавке низкоуглеродистого феррохрома составляют 22,4%(табл.10) от общего расхода тепла. Величина тепловых потерь в электропечной силикотермической плавке может быть оценена по выражению.
Qпот=
(1-1)
 = (1-0,776)
= (1-0,776)  = 199564 кДж.
= 199564 кДж.
Общий расход тепла будет равен:
Q1-4= 75096+588194+4073+23986+199564 = 890913 кДж.
Определение расхода электроэнергии
Разность между статьями расхода и прихода тепла равна:
Qэл.эн = 890913 – 244596 = 646317 кДж.
Недостающее количества тепла покрывается подводимой электроэнергией. Учитывая, что электрический КПД современных трехфазных электропечей составляет приблизительно 90% можно определить общий расход электроэнергии.
646317 / (0,90 3600) = 199,480кВтчас.
Учитывая массу полученного сплава 56,744 кг можно определить удельный расход электроэнергии на тонну сплава.
W = 199.480 1000/56,744 = 3515 кВтчас/т.
Как видим, полученные данные по удельному расходу электроэнергии практически совпадают с литературными данными, приведенными в таблице 10,что показывает правильность расчетов.
Таблица 3.15 – Удельный расход электроэнергии и тепловой КПД при выплавке низкоуглеродистого феррохрома печным силикотермическим методом.
Тепловой КПД , 1 |
Потери тепла , % |
Удельный расход электроэнергии, кВтчас/т |
0,776 |
22,4 |
3515 |
2.4 Тепловой баланс
По результатам расчета прихода и расхода тепла составляется тепловой баланс выплавки низкоуглеродистого феррохрома, которая приводится в таблица 3.16.
Приход |
Расход |
||||
Статья |
кДж |
% |
Статья |
кДж |
% |
Физическое тепло шихты |
0 |
0 |
Теплосодержание сплава |
75096 |
8,430 |
Экзотермические реакции |
244596 |
27,454 |
Теплосодержание шлака |
588194 |
66,021 |
Электроэнергия |
646317 |
72,546 |
Теплосодержание газообразных продуктов |
4073 |
0,457 |
|
|
|
Эндотермические реакции |
23986 |
2,692 |
|
|
|
Потери тепла |
199564 |
22,400 |
Итого |
890913 |
100 |
Итого |
890913 |
100 |

 С
С
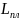 ,
кДж/кг.
,
кДж/кг.